
5 курс / Госпитальная педиатрия / 2 том Респираторная медицина
.pdf
Раздел 10
либо клетками с признаками атипии, выражающимися в полиморфизме размеров и формы клеток и ядер, появлением сосочковых, слоистых структур с наслаиванием клеток — в случае пролиферации клеток с признаками атипии. При иммуногистохимическом исследовании в очагах, содержащих овальные и щелевидные структуры, обнаруживаются митозы и продукция Ki-67 и PCNA, увеличивающаяся при нарастании признаков клеточной атипии [14, 18].
Изучались также овальные структуры с признаками атрофии клеток, когда клетки, выстилающие овальные и щелевидные полости, были уменьшены в размерах, уплощены и похожи на базальные клетки. В этих участках отмечалось накопление продуктов экспрессии PCNА, Ki-67, c-myc, b-TGF и в небольших количествах — р53. Сравнивая цитогенетические варианты дисрегенераторных изменений легочного эпителия в бронхиолах и альвеолах, следует отметить наличие более широкого спектра дисрегенераторных изменений на периферии легкого, что говорит о большей пластичности и разнообразии прогениторных клеток в этой области. Не исключено также, что эта пластичность связана с особым микроокружением периферических отделов легкого, особенно
вусловиях хронического воспаления, накопления эмбриональных типов коллагена.
Всвете последних данных о возможности имплантации мезенхимальной костномозговой клет- ки-предшественницы и ее дифференцировки в клетки легочного эпителия именно на периферии легкого имеются наиболее благоприятные условия для ее выживания: обилие капиллярного кровотока и особенности экстрацеллюлярного матрикса.
Диффузная идиопатическая гиперплазия нейроэндокринных клеток легкого. Синдром диффузной идиопатической гиперплазии нейроэндокринных клеток выделен в 2004 г., вероятно, обусловлен генетической предрасположенностью в связи с аллельным дисбалансом в регионе 11q13. В классификации ВОЗ он отмечается как предопухолевый процесс, который может привести к развитию карциноидов и нейроэндокринных карцином легкого. Характеризуется развитием различных вариантов гиперплазии легочного нейроэпителия
ввиде диффузной пролиферации в бронхах, в строме с формированием так называемых нейроэндокринных телец, опухолей и карциноидов. Часто сочетается с легочным фиброзом, но других патологических процессов, которые могли бы привести к вторичной гиперплазии нейроэндокринных клеток, не выявляется. Нейроэндокринная гиперплазия на светооптическом уровне с трудом отличается от базально-клеточной гиперплазии и плоскоклеточной метаплазии (рис. 10.34, 10.35). Отличительным признаком является наличие в эпителиальном пласте клеток округлой и овальной формы со светлой цитоплазмой и крупными овальными ядрами, при этом в клетках иммуно-
гистохимически выявляются маркеры нейроэндокринной дифференцировки — хромогранин-А, синаптофизин, нейрон специфическая енолаза и др. Ki-67-положительные клетки располагаются в базальных и парабазальных зонах, то есть цитогенетически, вероятнее всего, связаны с клетками Кульчицкого бронхиальной стенки [18].
Рис. 10.34. Гиперплазия нейроэндокринных клеток. Хромогранин А в нейроэндокринных клетках в пласте бронхиального эпителия. Иммунопероксидазная реакция. ×200
Рис. 10.35. Гиперплазия нейроэндокринных клеток. Нейроэпителий с нейроэндокринными гранулами в цитоплазме. Электронограмма. ×10 000
200

Неопластические заболевания легких
Молекулярная патология РЛ изучает совокупность морфологических и молекулярно-генети- ческих особенностей данной опухоли. При этом наиболее важными аспектами проблемы является определение биомолекулярных и гистогенетических маркеров рака, а также патология апоптоза при раке легкого.
Клеточная биология рака легких и роль раковой стволовой клетки
Фундаментальными вопросами клеточной биологии РЛ являются факторы, влияющие на темпы роста неоплазм, а также РСК, что определяет клинические проявления и ответ на терапию. Темпы роста опухолей определяются тремя факторами: временем удвоения опухолевых клеток, фракцией опухолевых клеток, составляющих репликативный пул, и скоростью выхода клеток из митотического цикла или их смерти. В легочной ткани тканевые стволовые клетки локализуются в зоне ниш на разных уровнях респираторного дерева и участвуют не только в регенерации ткани, но и в развитии ряда патологических состояний, проявляющихся фиброзированием, оссификацией и дисрегенераторными изменениями легочных эпителиев [3–5], гиперпластическими изменениями.
Раковая стволовая клетка
Тканевый гомеостаз в организме поддерживается с помощью иерархии стволовых клеток — резидентной популяции костномозговых и тканевых стволовых долгоживущих клеток, способных к самообновлению. Тканевые стволовые клетки малочисленны и располагаются в так называемых нишах, образованных клетками, которые их обслуживают и продуцируют паракринные факторы, поддерживающие жизнедеятельность стволовых клеток [17, 98]. Стволовые клетки делятся асимметрично, в результате чего образуются два типа дочерних клеток — первые с ограниченным пролиферативным потенциалом, вступающие в терминальную дифференцировку и погибающие, вторые — сохраняющие способности стволовых клеток.
Злокачественные опухоли обладают бессмертием своих клеток и неограниченными пролиферативными возможностями, указывающими на то, что в них так же как в нормальных тканях должны содержаться клетки со свойствами подобными стволовым клеткам [75, 141].
Агрессивность поведения РЛ во многом определяется клеточной субпопуляцией [108, 153].
РСК впервые были найдены в опухолях гемопоэтической системы и впоследствии в солидных опухолях, таких как рак молочной железы [110], поджелудочной железы [86], злокачественных опухолях головного мозга [155], раке толстой кишки [29]. Полагают, что они играют ключевую
роль в канцерогенезе, включая развитие опухолей, прогрессии и метастазировании [99, 109, 122].
Происхождение может быть двояким: из нормальных стволовых клеток (тканевых?) и в результате трансформации опухолевых клеток в так называемые подобные [106, 124]. Поэтому уничтожение должно быть во главе стратегии лечения рака. Биология РСК во многом схожа с нормальными стволовыми клетками. Идентифицируются РСК по поверхностным маркерам. РСК могут происходить или из нормальных тканевых стволовых клеток, или из более дифференцированных раковых, которые в ходе процесса трансформации приобрели способность к самообновлению. Злокачественные опухоли могут иметь небольшое количество РСК, которые в основном подвергаются «дифференцировке», формируя основную массу опухоли, в то время как другие могут быть построены в основном из РСК.
Методы верификации стволовости раковых клеток включают несколько этапов:
•выделение РСК из тканей или культур раковых клеток в клеточном сортере на основе экспрессии поверхностных маркеров — СD166 (33), EpCAM, CD90 и CD44(56, 58); в зависимости от происхождения рака маркеры могут меняться. Например, в раке легкого используют ALDH, СD133(89), СD166(33), EpCAM, CD90 и CD44(56, 58);
•индукция дифференцировки РСК in vitro в адипоциты, хондроциты и остеобласты, используя специфические дифференцировочные среды; идентификация адипоцитов, хондроцитов и остеоцитов морфологическими методами;
•колониеообразование в культурах;
•формирование сфероидов в культуре клеток; экспрессия транскрипционных факторов РСК методом ПЦР в реальном времени (Sox2, Klf4, c-Myc, Nanog, Oct3/4, GAPDH);
•оценка туморогенности in vivo путем введения РСК подкожно безтимусным мышам; выделе-
ние РНК с последующим синтезом, амплификацией и гибридизацией с ДНК.
РСК в РЛ были обнаружены более 30 лет тому назад, когда D.N. Carney и соавт. [142] в 1982 г. обнаружили в МРЛ и атипичном карциноиде легкого человека раковые клетки, способные образовывать колонии в мягком агаре и при трансплантации безтимусным мышам воссоздавать МРЛ и атипичный карциноид. Это позволило авторам высказаться о наличии среди опухолевых клеток РЛ со свойствами стволовых клеток. Идентифицируются РСК по поверхностным маркерам.
РСК РЛ экспрессируют следующие поверхностные маркеры: ALDH, СD133(90), СD166(33), EpCAM, CD90 и CD44(59, 56). Из перечисленных маркеров РСК наиболее изученными являются АLDH и СD133.
АLDH — ранний маркер стволовых клеток и РСК, переводит ретинол в ретиноловую кислоту
201

Раздел 10
иучаствует в Notch сигнальном пути. АLDH 1 отвечает за пролиферацию, самообновление и туморогенность РСК. Связан с плохим прогнозом НМРЛ [56].
СD133 как маркер РСК обнаружен в глиобластомах [38], раке толстой кишки [87], поджелудочной железы [84]. Установлено, что в образцах НМРЛ и МРЛ СD133+ опухолевые клетки обладают туморогенностью и способностью к самообновлению [89]. Однако показано, что и СD133-опухолевые клетки РЛ могут обладать туморогенностью с образованием ксенографта при их пересадке мышам, а также способностью к самообновлению [143]. Кроме того, экспрессия опухолевыми клетками СD133 не коррелирует с прогнозом [60, 95, 116]. Nоrashikin Zakaria и соавт. [98] исследовали РСК в культурах НМРЛА 549
иН2170 и обнаружили два типа РСК: CD166+/ CD44+ и CD166+/EpCAM+ (табл. 10.5).
Авторы обнаружили активацию и дисрегуляцию сигнальных путей. Во-первых, это ключевые пути, связанные с биологией самих РСК, во-вто-
рых, сигнальный путь, определяющий нарушение образования ламинина и интегринов экстрацеллюлярного матрикса, являющихся компонентами ниши стволовых клеток [52, 85, 116, 149]. В РСК РЛ были активированы Wnt и Hedghog сигнальные пути, характерные для неопухолевых стволовых клеток и связанные с множественной лекарственной устойчивостью РЛ [35, 105].
Эмбриональные сигнальные пути в раковой стволовой клетке рака легкого
Эмбриональные сигнальные пути являются основой органогенеза.
Ктаким путям относятся:
1)Hedgehog;
2)Notch;
3)Wnt;
4)b lymphoma MLV insertion region;
5)в РСКРЛ имеются нарушения этих путей [129]. Имеются агенты, способные блокировать эти пути, что уже включено в терапевтическую стратегию лечения рака (табл. 10.6).
Таблица 10.5. Экспериментальное исследование раковой стволовой клетки при раке легкого [28, 98]
Исследование |
|
|
Материал |
|
Маркер |
|
|
|
|
Результаты |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Ho et al. [61] |
|
|
Клеточные линии РЛ |
|
SP (side |
|
Высокая инвазивность, резистентность к |
||||||||
|
|
|
|
|
|
|
population) |
|
химиотерапии, высокая туморогенность in vivo |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Levina et al. [83] |
|
|
Клеточные линии РЛ |
|
SP |
|
Увеличение количества клеток SP и CD133 после |
||||||||
|
|
|
|
|
|
|
|
|
|
химиотерапии |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Chen et al. [39] |
|
|
Клеточные линии РЛ |
|
CD133 |
|
CD133+ клетки обладают способностью к |
||||||||
|
|
|
Ткань РЛ |
|
|
|
|
самообновлению и резистентны к химио- и лучевой |
|||||||
|
|
|
|
|
|
|
|
|
|
терапии |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Eramo et al. [56] |
|
|
Ткань РЛ |
|
CD133 |
|
CD133+ клетки экспрессируют Oct-4, NANOG, EPCAM, |
||||||||
|
|
|
|
|
|
|
|
|
|
NCAM, α-6 integrin и CXCR4 |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Bertolini et al. [32] |
|
Клеточные линии РЛ. |
|
CD133 |
|
CD133+ клетки резистентны к цисплатину и имеют |
|||||||||
|
|
|
Ткань РЛ |
|
|
|
|
плохой прогноз |
|
|
|
||||
Jiang et al. [74] |
|
|
Клеточные линии РЛ. |
|
ALDH |
|
ALDH+ клетки способны к дифференцировке и инвазии |
||||||||
|
|
|
Ткань РЛ |
|
|
|
|
и коррелируют с плохим прогнозом. |
|||||||
|
|
|
|
|
|
|
|
|
|
Обладают CD133+ |
|
|
|
||
Таблица 10.6. Клиническо еисследование раковой стволовой клетки при раке легкого [28, 98] |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Исследо- |
|
|
|
|
|
|
|
|
Стадия, |
|
Коли- |
% пози- |
|
Результаты |
|
|
Маркер |
|
Метод |
|
|
|
чество |
|
|||||||
вание |
|
|
|
|
гистотип |
|
тивных |
|
|||||||
|
|
|
|
|
|
|
|
|
пациентов |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Jiang et al. |
ALDH |
|
Иммуногистохимический |
|
НМРЛ |
|
148 |
29% |
|
Плохой прогноз |
|||||
[74] |
|
|
|
|
|
|
|
|
I стадия |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Sullivan et al. |
ALDH 1А |
|
Иммуногистохимический |
|
НМРЛ |
|
200 |
– |
|
Плохой прогноз |
|||||
[127] |
CD133 |
|
|
|
|
|
I стадия |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|||||
Woo et al. |
CD133 |
|
Иммуногистохимический |
|
НМРЛ |
|
177 |
45% |
|
Плохой прогноз |
|||||
[147] |
|
|
|
|
|
|
|
|
I стадия |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Salnikov et al. |
CD133 |
|
Иммуногистохимический |
|
НМРЛ |
|
88 |
63% |
|
Плохой прогноз. По |
|||||
[116] |
|
|
|
|
|
|
|
|
Все стадии |
|
|
|
|
CD133 нет |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
различий |
|
|
|
|
|
|
|
|
|
|
|
|||||
Li et al. [85] |
ALDH 1А |
|
Иммуногистохимический |
|
НМРЛ |
|
179 |
45% |
|
ALDH 1А+ — плохой |
|||||
|
|
|
|
|
|
|
|
|
Все стадии |
|
|
|
|
прогноз |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Dimou et al. |
ALDH |
|
Иммунофлюоресцентный |
|
НМРЛ |
|
430 |
– |
|
ALDH + — благопри- |
|||||
[52] |
|
|
|
|
|
|
|
|
Все стадии |
|
|
|
|
ятный прогноз |
|
202

Неопластические заболевания легких
Hedgehog сигнальный путь участвует в регуляции пролиферации, миграции и дифференцировки прогениторных клеток [118] и не работает в большинстве нормальных тканей. Активирован в РЛ [150]. В МРЛ был впервые продемонстрирован
в2003 г. [144] и считается характерным для РСК с нейроэндокринной дифференцировкой.
Блокирование Hedgehog сигнального пути лекарственными препаратами (Veratrumal kaloid cyclopamine, LDE-225) снимает туморогенность [144] МРЛ и предотвращает рецидивы [102].
Notch сигнальный путь — консервативный путь, определяющий судьбу клетки и способность стволовых клеток к асимметричному делению [31]. Участвует в эмбриогенезе легкого, образовании проксимальных и дистальных отделов легкого. На мышах показано, что его блокирование усиливает нейроэндокринную дифференцировку [43, 71], а также приводит к концентрации стволовых клеток
вдистальных отделах легкого [48].
Вкультурах НМРЛ повышена активность пути [37, 100]. Поддерживает про-апоптотические сигналы и ингибирует антиапоптотические сигналы
спомощью сурвинина [37, 78]. Активирован в ALDH+ клетках НМРЛ [127].
Таргетная терапия на стадии разработки. Блокирование пути путем ингибирования гамма-секре- тазы приводит к остановке роста и активизации апоптоза клеток РЛ как in vivo, так и in vitro [78]. Особенно интересно, что дисрегуляции Notch сиг-
нального пути обнаруживается в Ras-ассоциирован- ном РЛ [145]. Блокада вызывает антиангиогенное действие и воздействует на иммунную резистентность [103, 106].
МРЛ не поддается лечению, вероятно, с редкой экспрессией в его клетках Notch рецепторов.
Wnt/betta-catenin сигнальный путь:
•участвует в туморогенезе РЛ [139];
•таргетная терапия с моноклональными антителами индуцирует апоптоз в клеточных линиях РЛ, продуцирующих Wnt-2 протеин [151].
Концепция РСК имеет несколько важных приложений. Наиболее важным является то, что если РСК обеспечивают персистирование опухоли, то именно эти клетки должны быть элиминированы при лечении онкологического больного. Выдвигается гипотеза: так же как и нормальные стволовые клетки, РСК обладают высокой внутренней резистентностью к стандартной терапии, поскольку отличаются низкой митотической активностью и содержат фактор множественной лекарственной устойчивости-1, препятствующий действию химиотерапевтических препаратов [6, 76].
Следовательно, ограниченный успех современных методов терапии можно связать с невозможностью уничтожить РСК, которые являются источником опухоли.
Однако в настоящее время имеются подходы к возможности воздействия на: полагают о возможности ее созревания и дифференцировки в зрелые клетки, уничтожения или уничтожения через блокирование ее сигнальных путей. Первые попытки такого воздействия через ингибирование эмбриональных сигнальных путей в РЛ приведены в табл. 10.7.
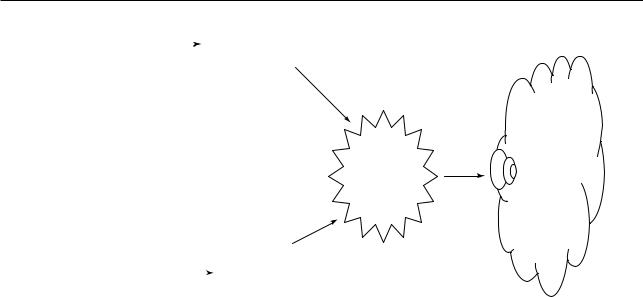
Концепция развития РЛ заключается в том, что первоначально предраковые изменения и РЛ возникают в области ниш тканевых стволовых клеток, где имеется воздействие канцерогенных агентов, с накоплением мутаций с последующей пролиферацией прогениторных клеток и их злокачественной трансформацией и развитием рака. Не исключается также и такая последовательность событий, когда трансформированные пролиферирующие клетки претерпевают перепрограммирование и из них образуется РКС (рис. 10.36).
Таблица 10.7. Маркеры эмбриональных стволовых клеток в таргетной терапии рака легкого [28, 98]
Путь |
Агент |
Объект |
Результаты |
Стадия |
Литература |
|
исследования |
испытаний |
|||||
|
|
|
|
|||
|
|
|
|
|
|
|
Hedgehog |
GDC-0449 |
Клеточная |
Ингибирование |
II фаза |
Tian et al. [134] |
|
(SMO) |
|
линия |
|
|
|
|
Notch |
RO4929097 |
РЛ поздней |
Безопасность |
II фаза |
Richter et al. [110] |
|
(γ-secretase) |
|
стадии |
|
|
(ASCO abstract) |
|
|
|
|
|
|
|
|
Hedgehog |
LDE225 |
Клеточная |
Стабилизация болезни, |
II фаза |
Tawbi et al. [133] |
|
(SMO) |
|
линия |
ингибирование зависит |
|
(ASCO abstract) |
|
|
|
|
от GLI-1 |
|
|
|
Notch |
DAPTa |
Клеточная |
Редукция в ALDH+ кар- |
Доклиническая |
Sullivan et al. [129] |
|
|
|
линия |
циномах |
|
|
|
Notch |
MRK-003 |
Клеточная |
Редукция |
– |
Konishi et al. [80] |
|
|
|
линия |
Оп, снижение проли- |
|
|
|
|
|
|
ферациии усиление |
|
|
|
|
|
|
апоптоза |
|
|
|
WNT 1 |
Моноклональные |
Клеточная |
Снижение пролифера- |
– |
He et al. [62] |
|
|
антитела и RNAi |
линия |
ции и усиление апоп- |
|
|
|
|
|
|
тоза |
|
|
|
|
|
|
|
|
|
203
Раздел 10
Предраковые |
|
|
|
Перепрограммирование |
|
|
|
трансформированных клеток |
|
процессы |
|
|
|
|
|
|
|
|
|
с пролиферацией |
|
|
|
|
|
|
|
|
|
и накоплением |
|
|
|
|
мутацией |
|
|
|
|
и эпигенетических |
|
|
|
|
изменений |
|
|
|
|
|
|
|
|
|
РСК |
РАК |
Костномозговая |
|
|
|
Тканевая |
мезенхимальная |
|
|
|
|
|
|
|
стволовая клетка |
|
стволовая клетка |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 10.36. Гипотеза участия раковой стволовой клетки в канцерогенезе рака легкого
Молекулярные механизмы канцерогенеза рака легких (геномика, протеомика и эпигенетика)
Молекулярные механизмы канцерогенеза рака легких связаны с перестройками генома, протеома, метаболома трансформированных клеток, а также с эпигенетическими нарушениями, которыми занимаются геномика, протеомика, метаболомика и эпигенетика.
Геномные перестройки при раке легкого
Молекулярные основы канцерогенеза базируются на открытии того факта, что развитие опухолей является результатом возникновения множественных мутаций в стволовых клетках, происходящих при повреждении молекул ДНК, которые, в свою очередь, могут быть следствием генетической нестабильности и хромосомных аберраций, а также возникать вследствие эпигенетических изменений.
В большинстве случаев РЛ такие мутации развиваются в тканевых стволовых клетках, однако при наследственных и семейных формах рака определенные мутации могут передаваться и через герминативные клетки. Это заключение подтверждается четырьмя группами фактов:
1)наличием корреляций определенных хромосомных мутаций с некоторыми типами опухолей;
2)развитием опухолевого фенотипа в клетках при трансфекции в них онкогеннных вирусов;
3)обнаружением мутагенных свойств у большинства известных канцерогенных агентов;
4)эпигенетическими перестройками в опухолевых клетках.
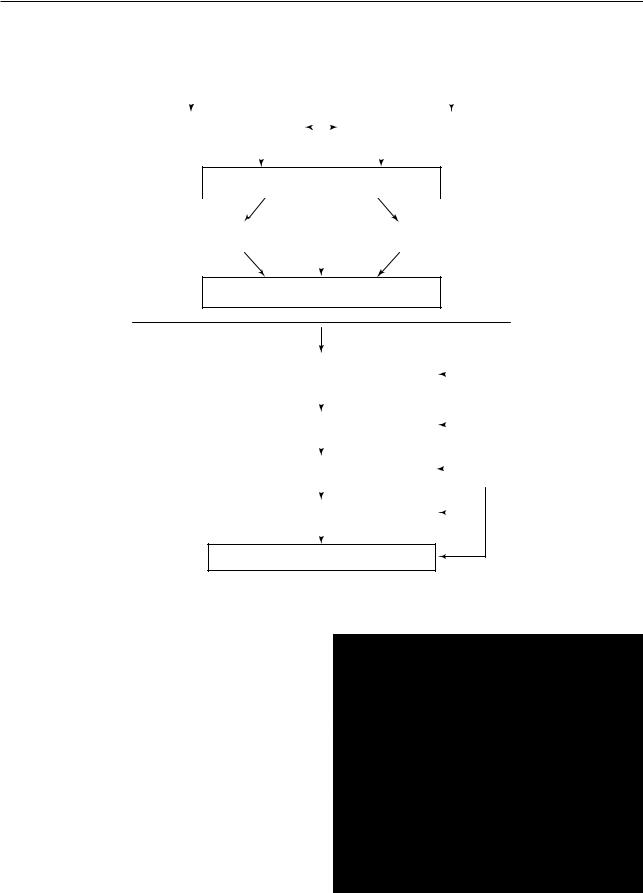
Рассматривая различные теории этиологии опухолей, поражаешься тому факту, что разнообразные канцерогенные агенты, отличающиеся по механизмам своего действия, приводят к одному и тому же результату — развитию опухолей (рис. 10.37).
При этом четыре класса генов являются важнейшими мишенями канцерогенных агентов:
•протоонкогены, регуляторы пролиферации и дифференцировки клеток;
•гены-супрессоры опухолей (антионкогены), ингибирующие пролиферацию клеток;
•гены, участвующие в гибели клеток путем апоптоза;
•гены, отвечающие за репарацию ДНК.
Клеточные онкогены при раке легкого
Доминирующие онкогенов, которые часто участвуют в раке легких, включают С-Мус, KRAS, EGFR, C-MET и С-KIT.
KRAS-мутации в настоящее время считаются одним из ключевых таргетным геном при лечении НМРЛ. Мутации наиболее часто встречаются в РЛ, особенно в аденокарциномах, где они обнаруживаются в 30% случаев [18, 68]. Выдвигается гипотеза о том, что KRAS-мутации являются также маркерами атипической железистой гиперплазии (варианта железистого предрака) и аденокарцином, что подтверждается при исследовании РЛ человека и в эксперименте на трансгенных мышах [18, 97].
Семейство RAS клеточных онкогенов нередко подвергается изменениям при опухолевом росте. Выявляется иммуногистохимическими методами чаще при предраковых аденоматозах (рис. 10.38) и аденокарциномах легкого [18]. Гены кодируют синтез белков р21, обладающих гуанозинтрифосфатазной активностью, связывающихся с гуано-
204
Неопластические заболевания легких
Экзогенные и эндогенные факторы |
|
Наследственные мутации генов репарации |
||||
|
ДНК, регулирующих рост и апоптоз |
|||||
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Повреждение ДНК соматической клетки |
|
|
|
Нарушение репарации ДНК |
||
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Мутации в геноме соматической клетки
|
|
|
|
|
|
Активация онкогенов |
|
|
Потеря (мутации) антионкогенов |
||
|
|
|
|
|
|
|
|
|
|
|
|
Нарушение генов, регулирующих апоптоз
Нарушение процессов пролиферации, |
|
|
|
|
|
|
|
апоптоза и дифференцировки клеток |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Предопухолевая дисплазия |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Множественные |
|
Неинвазивная опухоль |
|
|
|
|
|||
|
|
|
|
|
мутации |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Инвазивная опухоль |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Метастазирующая опухоль
Рис. 10.37. Молекулярные основы канцерогенеза и морфогенез опухолевого роста
зинтрифосфатом и тем самым воздействующих на передачу ростового сигнала в клетке. Описаны мутации, активирующие ras-гены и локализующиеся в 12-м, 13-м и 61-м кодонах.
Наиболее часто в раке легкого обнаруживаются мутации KRAS, присущие только немелкоклеточному РЛ, в отличие от МРЛ [111, 112, 131]. Мутации KRAS могут приводить к активации нескольких сигнальных путей. Ras-онкопротеин активирует сигнальный путь RAF/MEK/extracellular signal-regulated kinase, стимулирующий клеточный рост путем вхождения клеток в митотический цикл через фосфорилирование транскрипционных факторов (например, таких как c-FOS, ELK1, andMYC); фосфорилирование киназ ribosomal protein S6 kinase и mitogen-activated proteinkinase, а также phosphatidyl inositol-3-kinase/proteinkinase B сигнального пути, контролирующих жизнеспособность, рост и метаболизм клетки [107, 119]. Мутантный KRAS может вызвать трансформа-
Рис. 10.38. Экспрессия ras в клетках атипической аденоматозной гиперплазии. Иммунопероксидазная реакция. ×400
205

Раздел 10
цию клетки путем активации extracellular signalregulated kinase-mitogen-activated protein kinase and phosphatidyl inositol-3-kinase/proteinkinase B сигнальных путей [76]. Частота мутаций KRAS в аденокарциномах легкого составляет до 30%, а в плоскоклеточном РЛ только 3%. В двух больших исследованиях 30% случаев аденокарцином имели мутации в кодоне 12 и только 3% в других кодонах. Показана связь KRAS-мутаций с табакокурением [131]. О влиянии на выживаемость больных РЛ данные противоречивы: ранее была показана взаимосвязь мутации в KRAS, не подтвержденная в более поздних работах [107, 117].
KRAS-мутации обнаружены при предраке легкого — атипической гиперплазии альвеолярного эпителия в 40% случаев в окружающей легочной ткани вокруг аденокарцином, в которых мутации соответственно были найдены в 39% полимераз- ноцепной-аллельспецифической гибридизации. В этих же очагах описана экспрессиия р53. Найдены корреляции более высокой экспрессии данного онкопротеина с железистой дифференцировкой РЛ. Высокая экспрессия белковых продуктов ras регистрировалась нами также в очагах аденоматоза легкого и в овальных и щелевидных эпителиальных структурах в рубцах (Коган). Выдвигается гипотеза о том, что KRAS-мутации являются маркерами атипической железистой гиперплазии (варианта железистого предрака) и аденокарцином, что подтверждается при исследовании РЛ не только человека, но и в эксперименте на трансгенных мышах [18].
Поскольку RAS часто мутирует в раковых опухолях человека, естественно, было предпринято множество попыток создать анти-RAS-методы таргетной терапии. К сожалению, эффективность при использовании в клинической практике ни одного из этих методов не была доказана [53, 90, 112].
Семейство myc клеточных онкогенов — c-myc, L-myc, N-myc — немедленно реагирующие гены, кодирующие клеточные регуляторные белки, индуцирующие пролиферацию и подавляющие дифференцировку. Установлено, что в отсутствие факторов роста повышение экспрессии c-myc приводит не к делению клеток, а к апоптозу, который может ингибироваться bcl-2. C-myc амплификация обнаруживается в 10–25% случаев РЛ, в то время как L-myc и N-myc — только в нейроэндокринных опухолях легких (10–30%). Определение повышенной экспрессии myc онкопротенинов регистрируется значительно чаще по матричной. Определение же повышенной экспрессии иммуногистохимически затруднено, поскольку белковые продукты обладают очень коротким периодом жизни. Полупериод распада составляет 10 мин.
Экспрессия L-myc обнаруживалась только в группе нейроэндокринных опухолей легких, а экспрессия с-myc — как в группе мелкоклеточного, так и немелоклеточного РЛ. В группе мелкоклеточного РЛ установлена достоверная корреляция
экспрессии L-myc и c-myc с наличием метастазов и размерами опухоли [18, 97].
Семейство bcl-2, состоящее из bcl-2, bax, bak, bclXL, bclXS, — белковые продукты которых способны образовывать гомо- и гетеродимеры, оказывающие порой диаметрально противоположное действие на пролиферацию и апоптоз опухолевых клеток. Наиболее изученный из данного семейства bcl-2 локализуется на внутренней мембране митохондрий, а также в ядре, стимулирует пролиферацию клеток и ингибирует апоптоз, вероятно, за счет антиоксидантной активности. Напротив, bax-протеины, транскрипция и синтез которых регулируется р53, блокируют пролиферацию и стимулируют апоптоз опухолевых клеток. BclXL ингибирует апоптоз и стимулирует пролиферацию, а bclXS — напротив, индуцирует апоптоз. Таким образом, баланс между белковыми продуктами bcl-2-bax, bclXL-bclXS будут определять сдвиг равновесия в сторону пролиферации или апоптоза в опухоли [18, 97].
Особое внимание следует обратить на ядерную локализацию онкопротеина, так как, по данным литературы, она может соответствовать его неактивной, фосфорилированной форме, не способной блокировать апоптоз. Обнаружена также достоверная корреляция между экспрессией bcl-2 и стадией опухоли. В то же время при исследовании корреляции между экспрессией bcl-2 и выживаемостью больных МРЛ нами была получена положительная корреляция между экспрессией bcl-2 и лучшими показателями выживаемости больных. Полученные противоречия являются, по всей видимости, неслучайными и могут быть связаны с несколькими факторами. Во-первых, не исключено, что bcl-2 положительные мелкоклеточные карциномы более чувствительны к проводимой химиотерапии; во-вторых, выживаемость больных определяется множеством других показателей, например уровнем активности систем, обеспечивающих антибластомную резистентность, общую резистентность организма и др.; и, наконец, известно, что дисбаланс bcl-2 c другими членами семейства bcl-2, прежде всего bax, определяет прогноз при МРЛ.
При НМРЛ остаются сомнительными корреляции экспрессии bcl-2 с выживаемостью больных, данные противоречивы. В целом можно сделать вывод, что иммуногистохимия bcl-2 и bax имеет колоссальное значение в определении прогноза при РЛ.
Гены-супрессоры при раке легкого
Делеции или инактивация генов-супрессоров опухолей охватывают p53, p16, RB1 (Ink4a), а также множество локусов на хромосоме 3p. В этих участках локализуются другие многочисленные гены-супрессоры опухолей, кандидаты для участия в канцерогенезе, такие как FHIT, RASSF1A и др., которые еще предстоит идентифицировать.
206

Неопластические заболевания легких
Роль генов-супрессоров при развитии опухолей сводится в итоге к блокированию апоптоза и снятию их супрессивного влияния на клеточные онкогены, что в итоге заканчивается активацией пролиферации. Для реализации эффекта от повреждений генов-супрессоров изменения должны затрагивать оба аллеля гена, так как мутированный ген-супрессор всегда относится к сохранному как рецессивный к доминантному. Например, мутация или делеция одной из аллелей гена-су- прессора должна сопровождаться потерей или изменениями в другой аллели. Гены-супрессоры
враке легкого изучены относительно хорошо. При РЛ известны наиболее часто встречающиеся делеции хромосом, затрагивающие участки 3p2124, 17p13, 13q14, 9p21-22 и 5q21. 3p21-24 делеция наиболее часто встречается при РЛ — МРЛ в 100% и НМРЛ в 85% случаев. Однако в этой зоне не локализуется ни один ген-супрессор. Другие же сайты соответствуют известным генам-супрессорам. Так, например, р53 локализуется в 17р13, ретинобластомы ген — 13q14, р16 INK4B(MTS1) и р15 INK4B(MTS2) — 9р21-22, МСС (мутированный ген
враке толстой кишки) и АРС (ген аденоматозных полипов толстой кишки) — 5q21. Функции большинства из перечисленных генов хорошо извест-
ны и связаны с контролем G1-фазы митотического цикла и/или апоптоза. Их инактивация вызывает
ускользание из остановки в G1-фазе и развития апоптоза. Потеря гетерозиготности была изучена в очагах метаплазии, дисплазиии рака на месте. При плоскоклеточной метаплазии выявлена потеря гетерозиготности в сайтах 17р13, 5q21 и 9p21. При этом в разных очаагах в пределах одного и того же легкого можно было обнаружить разные мутации. Выявление повреждения генома в области локализации генов-супрессоров на стадии предраковых изменений свидетельствует об участии этих генов на ранних стадиях опухолевого роста. В настоящее время описан ряд новых генов-супрессоров, имеющих, видимо, значение для развития РЛ и локализованных в 1-й и 16-й хромосомах.
TP53-ген и его белковый продукт р53 подвергаются наиболее частым изменениям при опухолевом росте [47, 125, 128, 132]. Выявляется иммуногистохимически по окраске ядер (рис. 10.39–10.41). Мутантный TP53 наиболее часто обнаруживается при МРЛ и периферическом РЛ. В настоящее время известно более 8 изоформ TP53, обладающих, вероятно, различной функциональной активностью. В нетрансформированных клетках существует так называемый, дикий тип TP53, который является транскрипционным фактором с множественными функциями, включающими регулировку перехода
клеток из G1- в S-фазу, репарацию ДНК, апоптоз вслед за повреждением геном. В раковых клетках обнаруживается мутантный TP53, образующийся
восновном за счет делеции одной из аллелей (17р13) в сочетании с точковой мутацией в другом аллеле. Мутированный TP53 фактически действу-
Рис. 10.39. Белковый продукт гена-супрессора рака р53 в ядрах клеток низкодифференцированного плоскоклеточного рака легкого. Иммунопероксидазная реакция. ×400
Рис. 10.40. Белковый пролукт р53 в клетках умереннодифференцированной аденокарциномы. Иммунопероксидазная реакция. ×400
Рис. 10.41. Крупноклеточный рак легкого. Высокая экспрессия гена-супрессора р53. Иммунопероксидазная реакция. ×400
207

Раздел 10
ет как клеточный онкоген, стимулирует пролиферацию опухолевых клеток и вызывает образование антител, которые выявляются в крови больных. Последнее послужило основанием для разработки иммунодиагностики и иммунотерапии РЛ [132].
Мутация вызывает конформационные изменения в протеине р53 и он накапливается в ядрах клеток, что позволяет определять его иммуногистохимическими методами. Напротив, считается, что дикий тип р53 обладает очень коротким полупериодом жизни (20 мин) и поэтому его невозможно определить иммуногистохимически. Накопление мутантного р53 обнаруживается в 70–100% случаев культуры клеток МРЛ, 50–70% МРЛ операционного и секционного материала и 45–75% НМРЛ. р53-аккумуляция в ядрах клеток может достоверно свидетельствовать о появлении мутации в гене, при условии, что имеется не менее 20% позитивных клеток, выявленных не менее чем 2 методами. р53 негативные случаи — это не только случаи с диким типом р53, но и с отсутствием синтеза какого-либо белка р53. Эти случаи могут иметь также и не определяемые и сплайсинговые мутации, которые невозможно выявить иммуногистохимически, составляющие примерно 20% негативных по р53 случаев. В целом инактивация р53 при раке легкого имеется примерно в 70% случаев [18]. Исследования по корреляции экспрессии р53 с выживаемостью противоречивы. В целом если такое действие и есть, то оно очень несущественно. Непонятна и связь р53 со злокачественной трансформацией. В то же время экспериментальные данные показывают, что при активации дикого типа р53 происходит замедление роста и развивается апоптоз, что может привести к реверсии злокачественного фенотипа.
Имеются доказательства о значении мутации р53 на ранних стадиях канцерогенеза легкого. Так, например, мутации Tр53 могут развиваться за счет полициклических углеводородов и обнаруживаться у курильщиков [68]. р53 мутантные формы никогда не выявляются при резервной базально-клеточной гиперплазии или плоскоклеточной метаплазии без признаков дисплазии. При дисплазии р53-мута- ции выявляются в 12–53% случаев, а при раке на месте — в 60–90% случаев в исследованиях ткани, окружающей РЛ [18]. В соответствии с результатами последних исследований ожидаемая частота экспрессии р53 при дисплазиях эпителия легкого составляет до 91%. Взаимосвязь накопления р53 при предраке с последующим развитием опухоли достоверна (р=0,0014). Обнаружение р53 более чем в 20% клеток в очагах дисплазии является маркером необратимых предраковых изменений. Однако следует помнить, что примерно 50% случаев РЛ развивается без р53-мутации. Следовательно, р53-мутация — это необязательный феномен, характерный для РЛ, и поэтому отсутствие р53 не является благоприятным прогностическим фактором. Кроме того, ни накопление р53, ни его мутации
не исчерпывают молекулярные механизмы, через которые р53 может инактивироваться в опухолях. Было установлено, что белковый продукт р53 выявлен в ядрах раковых клеток в 47% наблюдений. При этом частота экспрессии р53 в МРЛ составила 67%, а в НМРЛ — 46%. Найдена достоверная корреляция между уровнем экспрессии р53 и стадией заболевания [47, 125, 132].
В последние годы показано, что нарушение работы р53 происходит при его взаимодействии с другими белками-регуляторами митотического цикла — р21, Мdm2, bax.
Rb-ген локализуется в сайте 13q14, который подвергается делеции в 80% МРЛ (так же часто, как и при ретинобластоме) [18, 97]. Кодирует ядерный фосфопротеин массой 110 кДа и контролирует выход клетки из G1-фазы. Гипофосфорилирование Rb приводит к блокаде клетки на стадии G1 и к апоптозу. Инактивация Rb в опухолях достигается потерей одного из аллелей и мутацией второго аллеля гена. Экспрессия Rb отсутствует в 90% МРЛ и имеет плохое прогностическое значение. В НМРЛ экспрессия отсутствует в 30% случаев и не имеет прогностического значения.
Таким образом, инактивация р53- и Rb-генов- супрессоров имеет значительно большее значение для развития и прогрессии МРЛ, чем НМРЛ, что подтверждает разные пути онкогенеза этих опухолей.
Факторы роста, рецепторы к факторам роста
исвязывающие протеины при раке легкого
Впрогрессии РЛ факторы роста играют важную роль, обеспечивая с помощью аутокринной и паракринной стимуляции рост опухоли.
EGFR-мутации обнаруживаются в 10–40% НМРЛ [97, 149] и наиболее часто выявляются в аденокарциномах у некурящих пациентов. Наиболее хорошо описаны 2 члена семейства EGFR. Нормальная форма EGFBB1, ген EGFR, подвергается гиперэкспрессии в 80% случаев плоскоклеточного РЛ, более чем в 50% глиобластом
ив 80–100% случаев опухолей головы и шеи.
Второй член семейства EGFBB2 (называемый также HER2/NEU) амплифицируется в 25% карцином молочной железы и аденокарцином яичника, легкого, желудка и слюнных желез [65, 113]. На основании того, что в раковых клетках обнаруживатся характерная гиперэкспрессия EGFBB2, разработан новый метод таргетной терапии с помощью антител к EGFBB2, успешно применяемый в клинической практике и являющийся еще одним примером таргетной терапии опухолей [65, 113].
Экспрессиия EGFR обнаруживается в плоскоклеточном раке легкого и реже в других гистологических типах опухоли [18]. Онкоген Her2neu является независимым фактором прогноза, и его экспрессия свидетельствует о высокой степени злокачественности НМРЛ.
Интересные данные были получены по экспрессии инсулиноподобного фактора роста-2
208

Неопластические заболевания легких
(IGF-2) и связывающих его протеинов (IGFBP1-6) при раке легкого [7, 18]. Исследование выполнено на операционном материале и в культурах РЛ с использованием иммуногистохимических методов. Инсулиноподобный фактор роста-2 выявлен в 45% наблюдений РЛ, несколько чаще в плоскоклеточном раке. IGFBP обнаруживались в различных гистологических типах опухоли, IGFBP2,5 — в значительно большем проценте случаев плоскоклеточного РЛ.
Установлены особенности локализации IGFPB3 — не только в цитоплазме, но и в ядрах раковых клеток
Тирозин- и треонинкиназы
ALK является рецептором тирозинкиназы, принимающим участие в развитии целого ряда злокачественных опухолей, включая рак легого [41, 115, 122, 123, 130]. Транслокация ALK описана в анапластических крупноклеточных лимфомах, при дислокации С-терминального киназного домена ALK, располагающегося на хромосоме 2p23, на 5q35 в зону N-терминали нуклеофосмина, в результате чего образуются гибридные белки, которые выявляются во многих опухолях, например в миофибробластической воспалительной опухоли и в НМРЛ [69, 146]. ALK гибридные белки являются высокочувствительными к действию ингибиторов ALK [42]. Подавление активности гибридныех ALK-белков препаратом кризотинибом лежит в основе таргетной терапии соответствующих типов. Полагают также, что кризотиниб может быть активен и против гибридных белков [42].
p16 — ингибитор циклин-зависимой киназы, обладающей опухоль-супрессивной активностью, и являющейся ключевой молекулой, Rb сигнального пути. Инактивация гена обнаруживается более чем в 40% случаев НМРЛ. При этом в 30–50% НМРЛ инактивация р16 возникает в результате точечных мутаций, делеции или потери гетерозиготности 9р21, а также за счет гиперметилирования гена. Особого интереса заслуживает тот факт, что механизмы инактивации гена у курящих и некурящих пациентов различны. Было установлено, что при табакокурении основным механизмом являются точечные мутации и делеция гена, а у некурящих — процессы гиперметилирования [43].
BRAF — серин/треонин киназа, участвующая в работе сигнального пути RAS/RAF/ MEK/extracellularsignal-regulatedkinase/mitogen- activatedproteinkinase, а также играющая важную роль в передаче митогенетического сигнала с клеточной поверхности. BRAF-мутации были обнаружены менее чем в 5% карцином щитовидной железы, толстой кишки, легких и меланомах [81]. В легких BRAF-мутации в основном выявляются в аденокарциномах [43, 97]. В настоящее время разрабатываются методы таргетной терапии таких BRAF-зависимых карцином [47].
PIK3CA — ген, кодирующий каталитическую субъединицу фосфоизонитид-киназы класса-1а, важнейшего антиапоптозного компонента protein kinase B сигнального пути. Мутации данного гена выявлены во многих карциномах. Наиболее часто они обнаруживаются в раке молочной железы, в раке легких — в 5% случаев. Мутации PIK3CA гена приводят к снижению апоптоза [18]. Не так давно было показано, что использование вновь созданных ингибиторов phosphatidylinositol-3-kinase может быть успешным при лечении опухолей с мутациями PIK3CA гена [43].
Обсуждается значение мутаций других киназ, например RET TKIs [43].
Адгезивные молекулы и экстрацеллюлярный матрикс стромы при раке легкого
Адгезивные молекулы, интегриновые рецепторы и экстрацеллюлярный матрикс стромы РЛ оказывают модулирующее действие на опухолевые клетки и обеспечивают рост, инвазию и метастазирование опухоли.
Первая фаза инвазии опухоли характеризуется ослаблением контактов между клетками, о чем свидетельствует уменьшение количества межклеточных контактов, снижение концентрации некоторых адгезивных молекул из семейства CD44
идр. и, наоборот, усиления экспрессии других обеспечивающих мобильность опухолевых клеток
иих контакт с экстрацеллюлярным матриксом. На клеточной поверхности снижается концентрация ионов кальция, что приводит к повышению отрицательного заряда опухолевых клеток. Усиливается экспрессия интегриновых рецепторов, обеспечивающих прикрепление клетки к компонентам экстрацеллюлярного матрикса — ламинину, фибронектину, коллагенам. Во второй фазе опухолевая клетка секретирует протеолитические ферменты
иих активаторы, которые обеспечивают деградацию экстрацеллюлярного матрикса, освобождая тем самым ей путь для инвазии. В то же время продукты деградации фибронектина и ламинина являются хемоаттрактантами для опухолевых клеток, которые мигрируют в зону деградации в ходе третьей фазы инвазии, а затем процесс повторяется снова.
Изучена экспрессия CD44, CD44 variant 5, 6
и7 в 98 случаях РЛ. Исследование проведено на операционном материале с использованием иммуногистохимического определения продуктов в парафиновых срезах. Установлена специфическая экспрессия CD44 variant 6 в плоскоклеточном раке легкого, преимущественно в высококодифференцированных формах и у больных без лимфогенных метастазов. Можно предположить, что различные варианты CD44 и их комбинации могут модулировать поведение опухолевых клеток при раке легкого: CD44 variant 6 обеспечивает, вероятно, сильные межклеточные контакты между опухолевыми клетками и может служить марке-
209
