
- •Тема 1: Предмет органической химии. Классификация,номенклатура, изомерия органических соединений
- •Предметорганическойхимии.Характеристика органических соединений
- •Изомерии;
- •Органическая химия имеет исключительно важное познавательное инароднохозяйственное значение.
- •2. Теорияхимическогостроенияорганических
- •Зная свойства вещества, можно установить его строение, и, наоборот, химическое строение вещества определяет его свойства.
- •Формулы(способыизображенияорганическихсоединений)
- •Классификацияорганическихсоединений
- •Изомерияорганическихсоединений
- •Структурнаяизомерия
- •Пространственнаяизомерия
- •Геометрическаяизомерия
- •Оптическаяизомерия
- •Конформации(поворотнаяизомерия)
- •Тема 2: Электронное строение и реакционная способностьорганических соединений
- •Типысвязейвмолекулахорганическихсоединений
- •Тема3:Алканы
- •1.Общая характеристика: строение, номенклатура, изомерия Предельныеуглеводороды(алканы,парафины,насыщенные
- •Тема3:Алканы
- •1.Общая характеристика: строение, номенклатура, изомерия Предельныеуглеводороды(алканы,парафины,насыщенные
- •Строение.
- •Номенклатураалканов
- •ПорядокпостроенияназванияразветвленногоалканапоИюпак
- •Изомерия
- •Структурнаяизомерия
- •Оптическаяизомерия
- •Радикалыилизаместители.
- •2.Химическиесвойства.Общиепредставленияомеханизмецепныхрадикальных реакций замещения в алканах (на примере реакциигалогенирования).
- •Сульфированиеисульфокисление:
- •Дегидрирования
- •В.Изомеризация
- •3.Способыполученияипрактическоеиспользование
- •2Гидpиpованиенепpедельныхуглеводоpодов:
- •Изсолейкарбоновыхкислот:
- •Разложениекарбидовметаллов(метанидов)водой:
- •Тема4:Циклоалканы
- •Общаяхарактеристика
- •Номенклатура
- •Изомерияциклоалканов
- •Структурнаяизомеpия
- •Пространственнаяизомерия
- •Химическиесвойства
- •Получениециклоалканов
- •Применение
- •Тема5:Алкены
- •1.Общаяхарактеристика:строение,номенклатура,изомерия
- •Строение
- •Номенклатура
- •Физическиесвойства
- •2.Химическиесвойства
- •Механизмыреакции присоединения калкенам:
- •Креакциямэлектрофильногоприсоединения аЕотносятся:
- •ОбъяснениеправилаМарковникова
- •Современная формулировка правила Марковникова:электрофильное присоединение к двойной связи идет черезобразование наиболее устойчивого карбокатиона.
- •Реакциягидратации
- •Реакцииокисленияалкенов:
- •Эпоксидирование (реакция н.А. Прилежаева, 1909г)эпоксидирование (по Прилежаеву)
- •Окислениевприсутствиисолейпалладия:
- •Реакцииозонирования.
- •Гидроборированиеалкеновииспользованиевсинтезеспиртов.
- •Реакцииполимеризации
- •Аллильноехлорированиеалкенов,механизм
- •Реакцииизомеризацииалкенов
- •Способыполученияипрактическоеиспользование
- •Отщепление атома водорода в реакциях дегидрогалогенирования и дегидратации происходитпреимущественно от наименее гидрогенизированного атома углерода.
- •Применениеалкенов
- •Тема6:Алкадиены
- •Общаяхарактеристика:строение,номенклатура,изомерия
- •Общаяформулаалкадиенов:СnН2n-2.Классификация диенов:
- •Кумулированные:
- •Номенклатура
- •Международная
- •Электронноестроение Делокализованныеπ-связи.Сопряжение
- •Химическиесвойства
- •Химические свойства диенов с сопряженными двойнымисвязями
- •Гидрирование
- •Галогенирование
- •Гидрогалогенирование,гидратации
- •Полимеризациясопряженныхдиенов
- •3.Получениеалкадиенов
- •4.Каучуки.Синтетическиекаучуки
- •Тема7:Алкины
- •Общаяхарактеристика:строение,номенклатура,изомерия
- •Номенклатураалкинов
- •Изомерияалкинов
- •Физическиесвойства
- •Химическиесвойства
- •Гидрирование
- •Б)Гомогенноегидрирование
- •Галогенирование
- •Гидрогалогенирование
- •Гидратация(реакцияКучерова)
- •Присоединениекарбоновыхкислот:
- •Реакциинуклеофильногоприсоединения
- •РеакцияФаворского
- •Реакцииполимеризации
- •Образованиеалкинидов
- •Этот метод дает возможность переходить от простых ацетиленовых углеводородов к более сложным.
- •Б)Реакцииокислительногорасщепления
- •Получениеалкинов
- •Применение
- •Тема8:Ароматическиеуглеводороды(арены)
- •Критерииароматичности.ПравилоХюккеля.
- •Теплотагидрированиябензола
- •Ароматическойявляется:
- •Небензоидные ароматические системы: циклопропенилий- и тропилий-катионы, циклопентадиенильный анион, азулен.
- •Арены. Общая характеристика: строение, номенклатура,изомерия
- •Одноядерныеарены:
- •Многоядерныеарены:
- •Гомологическийряд:
- •4.Химическиесвойствааренов
- •Электрофильноезамещениевбензольномкольце.
- •Наиболеетипичнаясхемареакцииароматическогоэлектрофильного замещения:
- •Свободнорадикальноегалогенированиебензола иалкилбензолов
- •АцилированиепоФриделю–Крафтсу
- •Реакция сульфированияпроисходит при нагревании под действием «дымящей» серной кислоты (олеум) с образованием ароматических сульфокислот:
- •Ориентацияприсоединениявмонозамещенныхбензолах
- •6.Конденсированныеароматическиеуглеводороды
- •В общем и целом, полиядерные конденсированные соединенияболее реакционноспособны (и менее ароматичны), чем бензолы.
- •Ориентация замещения в монозамещенных нафталине иантрацене
- •Антрацен
- •Антрахинон
- •Фенантрен
- •Конденсированные полиядерные соединения (нафталин, антрацен, фенантрен) получают, главным образом, при коксованииуглей.
- •Тема9: Галогенпроизводныеуглеводородов
- •1.Общаяхарактеристика
- •Наполярностьсвязивлияют:
- •Химическиесвойства
- •Реакциинуклеофильногозамещения,механизмыSn1 иSn2
- •Протеканиюреакциипомономолекулярномумеханизму(sn1)спо-собствуют:
- •Таким образом, протеканию замещения по бимолекулярномумеханизму (sn2) благоприятствуют:
- •Соединениясповышеннойипониженнойподвижностьюатома галогена
- •Реакционнаяспособностьвинил-иарилгалогенидов
- •Которое гласит, что придегидрогалогенировании алкилгалогенидовводород отщепляется от соседнего наименее гидрогенизированного атома углерода:
- •Получение литий- и магнийорганических соединений и ихиспользование в органическом синтезе
- •3.Способыполучениягалогенпроизводныхуглеводородов
- •4.Биологическое действие галогенпроизводных, их применение в народном хозяйстве
- •Тема 10:Спирты (одноатомные, многоатомные), тиолы, простыеэфиры
- •1 Общая характеристика одноатомных спиртов: строение, номенклатура, изомерия. Физические свойства спиртов, роль водородной связи
- •В зависимости от того, с каким атомом углерода(первичным,вторичным или третичным)связана гидроксогруппа, различаютспирты:
- •Номенклатураспиртов
- •2.Химическиесвойстваодноатомныхспиртов
- •Реакциизамещенияатомаводороданаметалл(кислотныесвойства)
- •Алкоголяты металлов обладают сильными основными инуклеофильными свойствами в отличие от спиртов (см. Ниже).
- •Реакция этерификации - образование сложных эфиров.(нуклеофильные свойства спиртов)
- •Реакциисгалогенидами фосфораисеры
- •Отдельныепредставители.
- •3.Многоатомныеспирты:особенностихимическихсвойств
- •4.Промышленныеилабораторныеметодыполученияспиртов
- •Щелочнойгидролизгалогеноуглеводородов:
- •Гликоли получают окислением алкенов щелочным или нейтральным раствором kMnO4(реакция Вагнера):
- •В технике глицерин получают гидролизом (омылением) природных жиров и масел:
- •Химическиесвойства
- •Простыеэфиры
- •Номенклатураиизомерия
- •Способыполучения
- •Тема11: Фенолы
- •1 Общая характеристика фенолов: классификация, строение, номенклатура, изомерия, физические свойства
- •2.Химическиесвойствафенолов
- •Образованиепростыхалкилариловыхэфиров
- •Образованиепростыхдиариловыхэфиров
- •Образованиесложныхэфиров-реакцияацилирования
- •Галогенирование
- •Нитрование
- •Сульфирование
- •Ацилирование
- •Реакциясформальдегидом
- •Карбоксилирование.РеакцияКольбе
- •Восстановление
- •Окисление
- •Качественнаяреакциянафенолы
- •3Промышленныеилабораторныеметодыполученияфенолов.
- •Гидролизводных растворовароматическихдиазосоединений
- •Тема12: Карбонильныесоединения
- •Общая характеристика карбонильных соединений: строение, классификация, номенклатура, изомерия, электронное строение
- •Изомерияальдегидов:
- •Енолизация,кето-енольнаятаутомерия.
- •Физическиесвойства
- •Электронноестроениекарбонильнойгруппы
- •Химическиесвойствакарбонильныхсоединений
- •Присоединениециановодородной (синильной)кислотыHcn:
- •Присоединениегидросульфитанатрия
- •Присоединениеаммиакаи егопроизводных
- •Первичныхспиртов:
- •Окислительно-восстановительныереакции
- •Альдольнаяикротоноваяконденсации.
- •3 Способыполученияипрактическоеиспользование карбонильных соединений
- •Окислениеспиртов
- •Гидратацияалкинов(реакцияКучерова)
- •Восстановлениехлорангидридовкарбоновыхкислот–реакцияРозенмунда
- •Почислукарбоксильных группкислотыподразделяютсяна:
- •Номенклатура
- •Изомерия
- •Спирта(сложныйэфир), аммиака (амид),
- •Химические свойства одноосновных карбоновых кислот и ихпроизводных
- •Способы получения и практическое использование одноосновных карбоновых кислот
- •5Сложныеэфирыкарбоновыхкислот.Жиры
- •Тема 14: Непредельные,ароматическиеидикарбоновыекарбоновыекислоты
- •Непредельныекарбоновыекислоты
- •Отдельныепредставителинепредельныходноосновныхкислот
- •Высшиенепредельныекислоты
- •A.Двухосновныекарбоновыекислоты
- •Свойствадвухосновныхкислот
- •Способыполучениядвухосновныхкислот
- •Ненасыщенныедикарбоновыекислоты
- •3Ароматическиекарбоновыекислоты
- •Химическиесвойства
- •Важнейшиепредставители
- •Ароматическиедикарбоновыекислоты
- •Важнейшиепредставители
- •Тема15: Амины.Азо-идиазосоединения
- •Амины.Общаяхарактеристика
- •2Химическиесвойстваалифатическихаминов
- •Особенностихимическихсвойствароматическихаминов
- •4Способыполученияаминов
- •Отдельныепредставителиалифатическихаминов
- •Диазосоединения
- •Реакции,идущиесвыделениемазота
- •Образованиегалогенопроизводных(реакцияЗандмейера).
- •Замещение диазогруппы, катализируемое солями одновалентноймеди (реакция Зандмейера)
- •Реакции,идущиебезвыделенияазота
- •В основе всех азокрасителей лежитядроазобензола,ипоэтому все азокрасители можно рассматривать как производныеазобензола.
- •Тема16:Гидрокси-,оксо-иаминокислоты.Пептидыибелки
- •Гидроксикислоты
- •Основныепредставители:
- •Оптическаяизомерияоксикислот
- •Еслигидроксилрасположенсправа–этоD-конфигурацияилиD-ряд. Если гидроксил расположен слева – этоL- конфигурация илиL-ряд.
- •Молочнаякислота
- •Яблочнаякислота
- •2(R),3(s)бутандиол-2,3
- •Винныекислоты
- •Особенностихимическихсвойств
- •Поведениеоксикислотпринагревании
- •2Оксокислоты(альдегидо-икетокислоты)
- •Общаяформула:
- •Особенностихимическихсвойств
- •Специфическиесвойства
- •Глиоксиловаякислота
- •Ацетоуксуснаякислота
- •Аминокислоты.Пептидыибелки
- •Оптическаяизомерияаминокислот
- •Методыполученияаминокислот
- •Особенностихимическихсвойств
- •Реакциясформальдегидом
- •Нингидриннаяреакция(качественная)
- •Этерификация
- •Термическоеповедениеаминокислот
- •Номенклатура
- •Примеры:
- •Тема17: Углеводы:моносахариды,дисахариды,полисахариды
- •Углеводы:общаяхарактеристика,классификация
- •Моносахариды(монозы)
- •2.1.Изомериямоносахаридов
- •МетоOдHыпHолучениямоносахаридов
- •Химическиесвойствамоносахаридов
- •Окислениемоносахаридов
- •Восстановлениемоносахаридов
- •Действиещелочейнамоносахариды
- •Реакциициклическихформмоносахаридов
- •Отдельныепредставителимоносахаридов
- •Дисахариды
- •Отдельныепредставителидисахаридов
- •Высшиеполисахариды
- •Тема18:Гетероциклическиесоединения
- •Пятичленныегетероциклы:фуран,тиофен,пиррол,ихстроениеНоменклатура
- •Реакционнаяспособность
- •Методыполучения
- •Гидрированиепиррола
- •Сульфирование
- •Галоидирование
- •Синтезпиридина
- •Строениепиридина.
- •IiРеакцииэлектрофильногоамещения
- •Реакциинуклеофильногозамещения
- •Восстановление(гидрирование)
- •Реакциинуклеофильногозамещения,snAr Биологическиактивныепроизводныехинолина
Реакции,идущиесвыделениемазота
Образование фенолов.При кипячении солей диазония с водой происходит бурное выделение азота и образование фенолов, например:
Образованиегалогенопроизводных(реакцияЗандмейера).
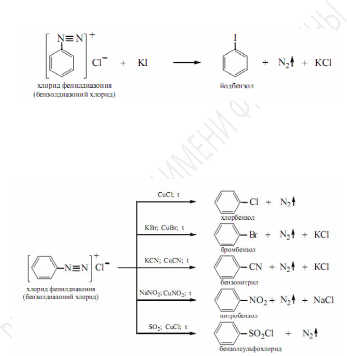 Принагреваниисолей
диазония ссолямигалогеноводородныхкислот
(KJ, КВг, КС1) происходит выделение азота
и замещение диазогруппы —N =N
на атом галогена, например:
Принагреваниисолей
диазония ссолямигалогеноводородныхкислот
(KJ, КВг, КС1) происходит выделение азота
и замещение диазогруппы —N =N
на атом галогена, например:
С достаточным выходом идет образование лишь иодзамещенных. Для получения других галогенозамещенных реакцию проводят в присутствии катализаторов — солей одновалентной меди (CuCl, CuBr) или же мелко раздробленной металлической меди.
Замещение диазогруппы, катализируемое солями одновалентноймеди (реакция Зандмейера)
Замещение диазогруппы на атом водорода.При нагревании солей диазония с некоторыми восстанавливающими агентами (фосфорноватистая кислота, формальдегид, спирты) выделяется азот и диазогруппа замещается на атом водорода, то есть соль арендиазония превращается в ароматический углеводород:
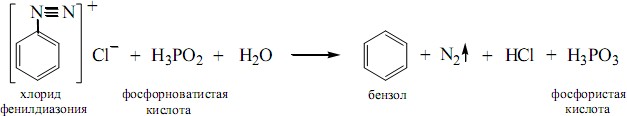
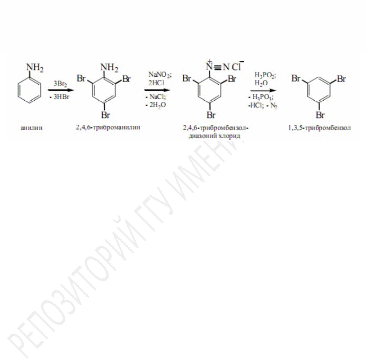 Этот
метод может быть использован для удаления
аминогруппы из ароматического
ядра.Например,1,3,5-трибромбензолне
удаётся получить прямым бромированием
бензола, однако его легко синтезировать
из анилина через 2,4,6-гриброманилин
диазотированием последнего и
восстановлением образовавшейся соли
диазония:
Этот
метод может быть использован для удаления
аминогруппы из ароматического
ядра.Например,1,3,5-трибромбензолне
удаётся получить прямым бромированием
бензола, однако его легко синтезировать
из анилина через 2,4,6-гриброманилин
диазотированием последнего и
восстановлением образовавшейся соли
диазония:
Реакции,идущиебезвыделенияазота
Образование азокрасителей.Из ряда реакций, идущих без выделения азота, наибольшее значение имеют реакции образованияазокрасителей.
Азокрасителиполучаютсяпривзаимодействиисолейдиазония: а) с ароматическими аминами
б)сфенолами.
Реакции образования азокрасителей из солей диазония иароматических аминов или фенолов часто называютреакциямисочетания.Ароматический амин, который превращается в соль диазония, а затем входит в состав азо-красителя, называетсяпервым компонентомкрасителя.Амин, или фенол, который сочетается с солью диазония, называетсявторым компонентом красителя.
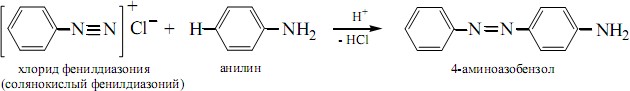 а)Реакция
сочетания солей диазония с ароматическими
аминами.Привзаимодействии
солейдиазониясаминамиатомводородавмолекуле
амина, находящийся в пара-положении по
отношению к замещенной аминогруппе,
являющийся, как мы знаем очень подвижным,
отщепляется вместе с анионом соли
диазония, а бензольные ядра соли диазония
и ароматического амина соединяются так
называемой азогруппой —N=N— с образованием
азокрасителя:
а)Реакция
сочетания солей диазония с ароматическими
аминами.Привзаимодействии
солейдиазониясаминамиатомводородавмолекуле
амина, находящийся в пара-положении по
отношению к замещенной аминогруппе,
являющийся, как мы знаем очень подвижным,
отщепляется вместе с анионом соли
диазония, а бензольные ядра соли диазония
и ароматического амина соединяются так
называемой азогруппой —N=N— с образованием
азокрасителя:
В основе всех азокрасителей лежитядроазобензола,ипоэтому все азокрасители можно рассматривать как производныеазобензола.
 б)
Реакция сочетания солей диазония с
фенолами.В молекулах фенолов атом
водорода, находящийся в пара-положении
по отношению к гидроксилу, отличается
значительной подвижностью. Привзаимодействии
солей диазония с фенолами происходит
образование азокрасителейподобно
тому,каки
вреакциистретичнымиароматически-
ми аминами:
б)
Реакция сочетания солей диазония с
фенолами.В молекулах фенолов атом
водорода, находящийся в пара-положении
по отношению к гидроксилу, отличается
значительной подвижностью. Привзаимодействии
солей диазония с фенолами происходит
образование азокрасителейподобно
тому,каки
вреакциистретичнымиароматически-
ми аминами:
Краситель, полученный из солянокислого фенилдиазония и фенола, можно рассматривать как азобензол, в котором атом водорода замещен гидроксилом, или оксигруппой, а поэтому его называютоксиазобензолом.Окси-азобензол – азокраситель оранжевого цвета.
Применяя различные первые компоненты красителей (т. е. диазотируемые ароматические амины) и различные вторые компоненты красителей (т. е. различные замещенные аминов и фенолов), можно получить самые разнообразные азокрасители, обладающие различными цветами и оттенками. В настоящее время известны многие сотни различных азокрасителей, обладающих всеми цветами спектра; преобладают среди них желтые, оранжевые и красные.
Для повышения растворимости азокрасителей часто в их молекулы вводят сульфогруппы, для чего, например, диазотируют сульфаниловую кислоту, а затем полученную соль диазония сочетают с аминами илифенолами.
Соль диазония в реакции азосочетания называютдиазосоставляющей (диазокомпонентой),а фенол или ароматический амин –азосоставляющей (азокомпонентой). Используя в реакции азосочетания различные диазо- и азосоставляющие можно получить большое число азосоединений.
Согласно хромофорной теории О.Витта (1876г.) структурные фрагменты молекулы, отвечающие за поглощение излучения в видимой области спектра, т. е. заокраскувещества, носят названиехромофоры(от греч. «хромое» – цвет и «форос»–носитель).Хромофорами являются:длинные цени сопряжения, азогруппа -N=N-,хиноидная группа,нитрогруппа–NО2,нигрозоруппа—N=Оидр.Дляпоявления
окраскичасто достаточноодного такоюхромофоравструктуремолекулы. Если молекула содержит несколько хромофоров, включённых в единую цепь сопряжения, интенсивность окраски увеличивается.
Однако окрашенное вещество далеко не всегда является красителем. Чтобы вещество было красителем, в его структуре должныприсутствоватьгруппы,получившиеназваниеауксохромы(отгреч.
«ауксео» – увеличиваю и «хромое» - цвет). Ауксохромами являются группы: ОН, NH2NHR, NR2, OR, SH и др. Эти группировки без хромофоров не способны вызывать окраску, но, находясь с ними в единой сопряженной системе, усиливают окраску и способствуют взаимодействию красителя с окрашиваемым материалом, что повышает устойчивость окраски к действию внешней среды, моющих средств и др.
По химическому составу различают азокрасители, трифенилметановые, антрахиноновые, индигоидные красители и др. Примером азокрасителей являетсяметиловый оранжевый(метилоранж, гелиантин). Причём его окраска изменяется в зависимости от рН среды, что позволяет использовать метилоранж в качестве индикатора.
Метилоранж получают азосочетанием диазотированнойсульфаниловой кислоты с N,N-диметиланилином.Дляэтогосначала сульфаниловую кислоту превращают в её натриевую соль:
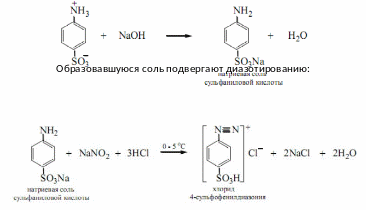
N,N-диметиланилинвкислойсредепереводятвеговодорастворимую
соль:
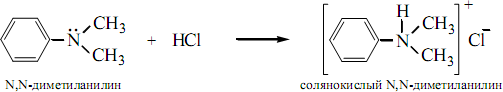 Проводятазосочетаниесолидиазония
ссольюдиметиланилина:
Проводятазосочетаниесолидиазония
ссольюдиметиланилина:
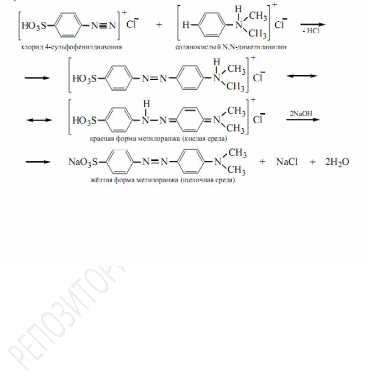 В
щелочной среде метилоранж жёлтого
цвета. Такая окраска обусловлена наличием
в его структуре длинной цепи сопряжения,
включающей хромофор – азогруппу
(-N=N-).Вкислойсредежёлтая
окраскапереходитвкрасную,тоестьпроисходитуглублениецветазасчёт
возникновения двух мезомерных структур
и образования хиноидной группы, более
сильного хромофора.
В
щелочной среде метилоранж жёлтого
цвета. Такая окраска обусловлена наличием
в его структуре длинной цепи сопряжения,
включающей хромофор – азогруппу
(-N=N-).Вкислойсредежёлтая
окраскапереходитвкрасную,тоестьпроисходитуглублениецветазасчёт
возникновения двух мезомерных структур
и образования хиноидной группы, более
сильного хромофора.
Таким образом, при изменении окраски одна хромофорная группа – азогруппа — N == N — исчезает, но появляется другая хромофорная группа – хиноидное ядро. Эта реакция обратима: при прибавлении к красному метилоранжу щелочи опять образуется желтый метилоранж.
При энергичном восстановлении азокрасителей (например, водородом в момент выделения) молекулы их расщепляются по месту двойной связи в азогруппе и образуется смесь аминов или аминов с аминофенолами. Такие реакции применяются для выяснения строения красителей, а также для получения некоторых аминов и диаминов.
Восстановление солей диазония.Эта реакция идет с разрывом тройной связи между атомами азота и приводит к ароматическим гидразинам, например:
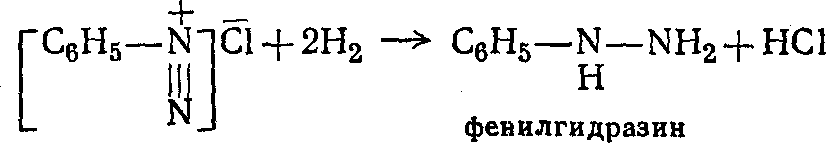 Ароматические
производные гидразинов широко применяются
в химии карбонильных соединений (в
частности, сахаров) для получения
гидразонов, а также при ряде синтезов
в качестве сильных восстановителей.
Фенилгидразин – почти бесцветная
жидкость, быстро темнеющая на воздухе
вследствие окисления. Солянокислая
соль фенилгидразина – кристаллическое
вещество, плавящееся при 243°С.
Ароматические
производные гидразинов широко применяются
в химии карбонильных соединений (в
частности, сахаров) для получения
гидразонов, а также при ряде синтезов
в качестве сильных восстановителей.
Фенилгидразин – почти бесцветная
жидкость, быстро темнеющая на воздухе
вследствие окисления. Солянокислая
соль фенилгидразина – кристаллическое
вещество, плавящееся при 243°С.
Дополнительно:
ОЦВЕТЕИЭЛЕКТРОННОМ СТРОЕНИИ КРАСИТЕЛЕЙ
Изложенная выше хромофорная теория красителей, появившаясяеще в прошлом столетии, лишь формально связывала цветность веществ с наличием определенных групп атомов. В течение последующих десятилетий химики и физики пытались установить реальную, физическую связь между цветом и электронным строением молекул красителей. Как известно из физики, окрашенными являются вещества, поглощающиелучи определенной длины волныиз белого видимого света, и вещество кажется окрашенным в цвет, являющийся дополнительным к поглощенному цвету. Поглощение тех или иных квантов света (видимого или ультрафиолетового) зависит от особенностей электронов. Электроны, участвующие в построении-связей, возбуждаются большими квантами и поэтомувещества с простыми связями поглощают лишь вдалекой ультра- фиолетовой части спектра при длинах волн до 2000 А; квантов видимого света они не поглощают и кажутся бесцветными. Электроны, участвующие в построении-связей, возбуждаются меньшими квантами. Особенно легко возбуждаются электроны, участвующие в построении сопряженныхдвойных связей, причем, чем длиннее система сопряженных связей, тем меньшие кванты нужны для их возбуждения.
Окрашенные вещества содержат хромофоры, например хиноидные ядра, азогруппы, связанные с бензольными ядрами, представляющие собой системы сопряженных конъюгированных) связей. Такие системы возбуждаются небольшими квантами, относящимися к области видимого света, и поэтому соответствующие вещества кажутся окрашенными. Такимобразом,сэлектроннойточкизрения хромофоромявляется система сопряженных связей. Поглощение света, обусловленное наличием хромофоров, обычно невелико, и вещества, содержащие хромофоры, хотя и окрашены, все же не могут служить красителями.
Как упоминалось, в красителях, помимо хромофоров, должны быть ауксохромы. Обычно это кислые или основные группы, способные находитьсявионизированнойформеилисильнополяризованные.Заряды
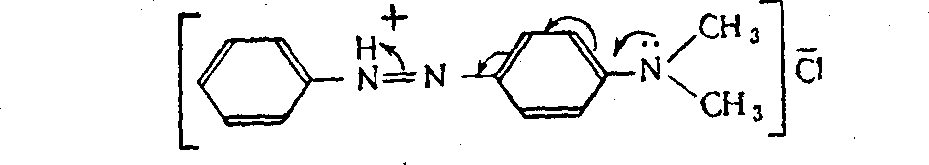 (ионов
или поляризованных групп) более или
менее равномерно распределяются по
всей молекуле. В ионе основного
азокрасителя электроны сдвигаются в
сторону положительного заряда, что
ведет к выравниванию электронной
плотности:
(ионов
или поляризованных групп) более или
менее равномерно распределяются по
всей молекуле. В ионе основного
азокрасителя электроны сдвигаются в
сторону положительного заряда, что
ведет к выравниванию электронной
плотности:
 Например,
в красный цвет окрашены вещества,
поглощающие лучи сине-зеленого цвета,
и наоборот: дополнительные цвета дают
белый цвет.
Например,
в красный цвет окрашены вещества,
поглощающие лучи сине-зеленого цвета,
и наоборот: дополнительные цвета дают
белый цвет.
