
- •Тема 1: Предмет органической химии. Классификация,номенклатура, изомерия органических соединений
- •Предметорганическойхимии.Характеристика органических соединений
- •Изомерии;
- •Органическая химия имеет исключительно важное познавательное инароднохозяйственное значение.
- •2. Теорияхимическогостроенияорганических
- •Зная свойства вещества, можно установить его строение, и, наоборот, химическое строение вещества определяет его свойства.
- •Формулы(способыизображенияорганическихсоединений)
- •Классификацияорганическихсоединений
- •Изомерияорганическихсоединений
- •Структурнаяизомерия
- •Пространственнаяизомерия
- •Геометрическаяизомерия
- •Оптическаяизомерия
- •Конформации(поворотнаяизомерия)
- •Тема 2: Электронное строение и реакционная способностьорганических соединений
- •Типысвязейвмолекулахорганическихсоединений
- •Тема3:Алканы
- •1.Общая характеристика: строение, номенклатура, изомерия Предельныеуглеводороды(алканы,парафины,насыщенные
- •Тема3:Алканы
- •1.Общая характеристика: строение, номенклатура, изомерия Предельныеуглеводороды(алканы,парафины,насыщенные
- •Строение.
- •Номенклатураалканов
- •ПорядокпостроенияназванияразветвленногоалканапоИюпак
- •Изомерия
- •Структурнаяизомерия
- •Оптическаяизомерия
- •Радикалыилизаместители.
- •2.Химическиесвойства.Общиепредставленияомеханизмецепныхрадикальных реакций замещения в алканах (на примере реакциигалогенирования).
- •Сульфированиеисульфокисление:
- •Дегидрирования
- •В.Изомеризация
- •3.Способыполученияипрактическоеиспользование
- •2Гидpиpованиенепpедельныхуглеводоpодов:
- •Изсолейкарбоновыхкислот:
- •Разложениекарбидовметаллов(метанидов)водой:
- •Тема4:Циклоалканы
- •Общаяхарактеристика
- •Номенклатура
- •Изомерияциклоалканов
- •Структурнаяизомеpия
- •Пространственнаяизомерия
- •Химическиесвойства
- •Получениециклоалканов
- •Применение
- •Тема5:Алкены
- •1.Общаяхарактеристика:строение,номенклатура,изомерия
- •Строение
- •Номенклатура
- •Физическиесвойства
- •2.Химическиесвойства
- •Механизмыреакции присоединения калкенам:
- •Креакциямэлектрофильногоприсоединения аЕотносятся:
- •ОбъяснениеправилаМарковникова
- •Современная формулировка правила Марковникова:электрофильное присоединение к двойной связи идет черезобразование наиболее устойчивого карбокатиона.
- •Реакциягидратации
- •Реакцииокисленияалкенов:
- •Эпоксидирование (реакция н.А. Прилежаева, 1909г)эпоксидирование (по Прилежаеву)
- •Окислениевприсутствиисолейпалладия:
- •Реакцииозонирования.
- •Гидроборированиеалкеновииспользованиевсинтезеспиртов.
- •Реакцииполимеризации
- •Аллильноехлорированиеалкенов,механизм
- •Реакцииизомеризацииалкенов
- •Способыполученияипрактическоеиспользование
- •Отщепление атома водорода в реакциях дегидрогалогенирования и дегидратации происходитпреимущественно от наименее гидрогенизированного атома углерода.
- •Применениеалкенов
- •Тема6:Алкадиены
- •Общаяхарактеристика:строение,номенклатура,изомерия
- •Общаяформулаалкадиенов:СnН2n-2.Классификация диенов:
- •Кумулированные:
- •Номенклатура
- •Международная
- •Электронноестроение Делокализованныеπ-связи.Сопряжение
- •Химическиесвойства
- •Химические свойства диенов с сопряженными двойнымисвязями
- •Гидрирование
- •Галогенирование
- •Гидрогалогенирование,гидратации
- •Полимеризациясопряженныхдиенов
- •3.Получениеалкадиенов
- •4.Каучуки.Синтетическиекаучуки
- •Тема7:Алкины
- •Общаяхарактеристика:строение,номенклатура,изомерия
- •Номенклатураалкинов
- •Изомерияалкинов
- •Физическиесвойства
- •Химическиесвойства
- •Гидрирование
- •Б)Гомогенноегидрирование
- •Галогенирование
- •Гидрогалогенирование
- •Гидратация(реакцияКучерова)
- •Присоединениекарбоновыхкислот:
- •Реакциинуклеофильногоприсоединения
- •РеакцияФаворского
- •Реакцииполимеризации
- •Образованиеалкинидов
- •Этот метод дает возможность переходить от простых ацетиленовых углеводородов к более сложным.
- •Б)Реакцииокислительногорасщепления
- •Получениеалкинов
- •Применение
- •Тема8:Ароматическиеуглеводороды(арены)
- •Критерииароматичности.ПравилоХюккеля.
- •Теплотагидрированиябензола
- •Ароматическойявляется:
- •Небензоидные ароматические системы: циклопропенилий- и тропилий-катионы, циклопентадиенильный анион, азулен.
- •Арены. Общая характеристика: строение, номенклатура,изомерия
- •Одноядерныеарены:
- •Многоядерныеарены:
- •Гомологическийряд:
- •4.Химическиесвойствааренов
- •Электрофильноезамещениевбензольномкольце.
- •Наиболеетипичнаясхемареакцииароматическогоэлектрофильного замещения:
- •Свободнорадикальноегалогенированиебензола иалкилбензолов
- •АцилированиепоФриделю–Крафтсу
- •Реакция сульфированияпроисходит при нагревании под действием «дымящей» серной кислоты (олеум) с образованием ароматических сульфокислот:
- •Ориентацияприсоединениявмонозамещенныхбензолах
- •6.Конденсированныеароматическиеуглеводороды
- •В общем и целом, полиядерные конденсированные соединенияболее реакционноспособны (и менее ароматичны), чем бензолы.
- •Ориентация замещения в монозамещенных нафталине иантрацене
- •Антрацен
- •Антрахинон
- •Фенантрен
- •Конденсированные полиядерные соединения (нафталин, антрацен, фенантрен) получают, главным образом, при коксованииуглей.
- •Тема9: Галогенпроизводныеуглеводородов
- •1.Общаяхарактеристика
- •Наполярностьсвязивлияют:
- •Химическиесвойства
- •Реакциинуклеофильногозамещения,механизмыSn1 иSn2
- •Протеканиюреакциипомономолекулярномумеханизму(sn1)спо-собствуют:
- •Таким образом, протеканию замещения по бимолекулярномумеханизму (sn2) благоприятствуют:
- •Соединениясповышеннойипониженнойподвижностьюатома галогена
- •Реакционнаяспособностьвинил-иарилгалогенидов
- •Которое гласит, что придегидрогалогенировании алкилгалогенидовводород отщепляется от соседнего наименее гидрогенизированного атома углерода:
- •Получение литий- и магнийорганических соединений и ихиспользование в органическом синтезе
- •3.Способыполучениягалогенпроизводныхуглеводородов
- •4.Биологическое действие галогенпроизводных, их применение в народном хозяйстве
- •Тема 10:Спирты (одноатомные, многоатомные), тиолы, простыеэфиры
- •1 Общая характеристика одноатомных спиртов: строение, номенклатура, изомерия. Физические свойства спиртов, роль водородной связи
- •В зависимости от того, с каким атомом углерода(первичным,вторичным или третичным)связана гидроксогруппа, различаютспирты:
- •Номенклатураспиртов
- •2.Химическиесвойстваодноатомныхспиртов
- •Реакциизамещенияатомаводороданаметалл(кислотныесвойства)
- •Алкоголяты металлов обладают сильными основными инуклеофильными свойствами в отличие от спиртов (см. Ниже).
- •Реакция этерификации - образование сложных эфиров.(нуклеофильные свойства спиртов)
- •Реакциисгалогенидами фосфораисеры
- •Отдельныепредставители.
- •3.Многоатомныеспирты:особенностихимическихсвойств
- •4.Промышленныеилабораторныеметодыполученияспиртов
- •Щелочнойгидролизгалогеноуглеводородов:
- •Гликоли получают окислением алкенов щелочным или нейтральным раствором kMnO4(реакция Вагнера):
- •В технике глицерин получают гидролизом (омылением) природных жиров и масел:
- •Химическиесвойства
- •Простыеэфиры
- •Номенклатураиизомерия
- •Способыполучения
- •Тема11: Фенолы
- •1 Общая характеристика фенолов: классификация, строение, номенклатура, изомерия, физические свойства
- •2.Химическиесвойствафенолов
- •Образованиепростыхалкилариловыхэфиров
- •Образованиепростыхдиариловыхэфиров
- •Образованиесложныхэфиров-реакцияацилирования
- •Галогенирование
- •Нитрование
- •Сульфирование
- •Ацилирование
- •Реакциясформальдегидом
- •Карбоксилирование.РеакцияКольбе
- •Восстановление
- •Окисление
- •Качественнаяреакциянафенолы
- •3Промышленныеилабораторныеметодыполученияфенолов.
- •Гидролизводных растворовароматическихдиазосоединений
- •Тема12: Карбонильныесоединения
- •Общая характеристика карбонильных соединений: строение, классификация, номенклатура, изомерия, электронное строение
- •Изомерияальдегидов:
- •Енолизация,кето-енольнаятаутомерия.
- •Физическиесвойства
- •Электронноестроениекарбонильнойгруппы
- •Химическиесвойствакарбонильныхсоединений
- •Присоединениециановодородной (синильной)кислотыHcn:
- •Присоединениегидросульфитанатрия
- •Присоединениеаммиакаи егопроизводных
- •Первичныхспиртов:
- •Окислительно-восстановительныереакции
- •Альдольнаяикротоноваяконденсации.
- •3 Способыполученияипрактическоеиспользование карбонильных соединений
- •Окислениеспиртов
- •Гидратацияалкинов(реакцияКучерова)
- •Восстановлениехлорангидридовкарбоновыхкислот–реакцияРозенмунда
- •Почислукарбоксильных группкислотыподразделяютсяна:
- •Номенклатура
- •Изомерия
- •Спирта(сложныйэфир), аммиака (амид),
- •Химические свойства одноосновных карбоновых кислот и ихпроизводных
- •Способы получения и практическое использование одноосновных карбоновых кислот
- •5Сложныеэфирыкарбоновыхкислот.Жиры
- •Тема 14: Непредельные,ароматическиеидикарбоновыекарбоновыекислоты
- •Непредельныекарбоновыекислоты
- •Отдельныепредставителинепредельныходноосновныхкислот
- •Высшиенепредельныекислоты
- •A.Двухосновныекарбоновыекислоты
- •Свойствадвухосновныхкислот
- •Способыполучениядвухосновныхкислот
- •Ненасыщенныедикарбоновыекислоты
- •3Ароматическиекарбоновыекислоты
- •Химическиесвойства
- •Важнейшиепредставители
- •Ароматическиедикарбоновыекислоты
- •Важнейшиепредставители
- •Тема15: Амины.Азо-идиазосоединения
- •Амины.Общаяхарактеристика
- •2Химическиесвойстваалифатическихаминов
- •Особенностихимическихсвойствароматическихаминов
- •4Способыполученияаминов
- •Отдельныепредставителиалифатическихаминов
- •Диазосоединения
- •Реакции,идущиесвыделениемазота
- •Образованиегалогенопроизводных(реакцияЗандмейера).
- •Замещение диазогруппы, катализируемое солями одновалентноймеди (реакция Зандмейера)
- •Реакции,идущиебезвыделенияазота
- •В основе всех азокрасителей лежитядроазобензола,ипоэтому все азокрасители можно рассматривать как производныеазобензола.
- •Тема16:Гидрокси-,оксо-иаминокислоты.Пептидыибелки
- •Гидроксикислоты
- •Основныепредставители:
- •Оптическаяизомерияоксикислот
- •Еслигидроксилрасположенсправа–этоD-конфигурацияилиD-ряд. Если гидроксил расположен слева – этоL- конфигурация илиL-ряд.
- •Молочнаякислота
- •Яблочнаякислота
- •2(R),3(s)бутандиол-2,3
- •Винныекислоты
- •Особенностихимическихсвойств
- •Поведениеоксикислотпринагревании
- •2Оксокислоты(альдегидо-икетокислоты)
- •Общаяформула:
- •Особенностихимическихсвойств
- •Специфическиесвойства
- •Глиоксиловаякислота
- •Ацетоуксуснаякислота
- •Аминокислоты.Пептидыибелки
- •Оптическаяизомерияаминокислот
- •Методыполученияаминокислот
- •Особенностихимическихсвойств
- •Реакциясформальдегидом
- •Нингидриннаяреакция(качественная)
- •Этерификация
- •Термическоеповедениеаминокислот
- •Номенклатура
- •Примеры:
- •Тема17: Углеводы:моносахариды,дисахариды,полисахариды
- •Углеводы:общаяхарактеристика,классификация
- •Моносахариды(монозы)
- •2.1.Изомериямоносахаридов
- •МетоOдHыпHолучениямоносахаридов
- •Химическиесвойствамоносахаридов
- •Окислениемоносахаридов
- •Восстановлениемоносахаридов
- •Действиещелочейнамоносахариды
- •Реакциициклическихформмоносахаридов
- •Отдельныепредставителимоносахаридов
- •Дисахариды
- •Отдельныепредставителидисахаридов
- •Высшиеполисахариды
- •Тема18:Гетероциклическиесоединения
- •Пятичленныегетероциклы:фуран,тиофен,пиррол,ихстроениеНоменклатура
- •Реакционнаяспособность
- •Методыполучения
- •Гидрированиепиррола
- •Сульфирование
- •Галоидирование
- •Синтезпиридина
- •Строениепиридина.
- •IiРеакцииэлектрофильногоамещения
- •Реакциинуклеофильногозамещения
- •Восстановление(гидрирование)
- •Реакциинуклеофильногозамещения,snAr Биологическиактивныепроизводныехинолина
Карбоксилирование.РеакцияКольбе
ОNa
O
+ C t,p
O
ОH
COONa
HCl
ОH
COOH
фенолят салицилат о-гидроксибензой-
натрия натрия ная кислота(салициловая)
Восстановление
ОH ОH
3Н2 H
Ni,t,p
фенол циклогексанол
Приперегонкенад цинковойпыльюфенолдегидроксилируется.
ОH
Окисление
Znпыль
+ZnO
Фенол и многие замещенные фенолы при хранении постепенно окисляются кислородом воздуха, образуя сложную смесь соединений. На первом этапе окисления фенолы превращаются в реакционноспособные феноксильные радикалы. Еслипара-положения бензольного кольца фенолов свободны, то одним из основных превращений феноксильных радикалов является димеризация попара-положению с образованием 4,4'-дигидроксидифенила.
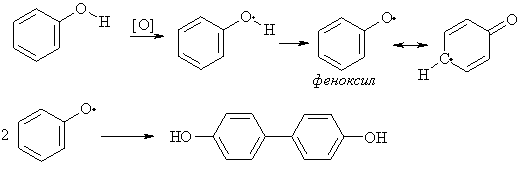
 Феноксильные
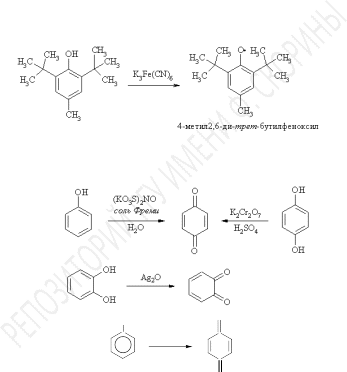
радикалы, имеющие ворто- ипара-положениях
объемные заместители, настолько
стабильны, что могут существовать в
растворе длительное время и даже быть
выделенными в кристаллическомвиде.
Феноксильные
радикалы, имеющие ворто- ипара-положениях
объемные заместители, настолько
стабильны, что могут существовать в
растворе длительное время и даже быть
выделенными в кристаллическомвиде.
Фенол окисляется бихроматом калия или солью Фреми (нитрозодисульфонатом калия) допара-бензохинона. При окислении двухатомных фенолов пирокатехина и гидрохинона, образуютсяорто- ипара-бензохиноны, соответственно.
OH O
CrO3
илиK2Cr2O7/H+
O
п-бензохинон

 OH OH
OH OH
 Н2О2 OH
Н2О2 OH
Fe
пирокатехин
Качественнаяреакциянафенолы
 Для
большинства фенолов характерна
интенсивная цветная реакцияс
FeCl3, обусловленная образованием
соединений ROFeCl2, дающих
окрашенныеионыROFe2+.Обычновозникаетфиолетоваяилисиняя
Для
большинства фенолов характерна
интенсивная цветная реакцияс
FeCl3, обусловленная образованием
соединений ROFeCl2, дающих
окрашенныеионыROFe2+.Обычновозникаетфиолетоваяилисиняя
окраска,нодлянекоторыхзамещенныхфеноловонаможетбытькрасной
илизеленой.
3Промышленныеилабораторныеметодыполученияфенолов.
Применение
Природным источником фенола и его гомологов служит каменный уголь, при сухой перегонке которого образуется каменноугольная смола. Разгонкойпоследнейполучают фракцию «карболового масла»(Ткип. 160- 230 °С), содержащую фенол и крезолы.
Большую часть фенолов, используемых в промышленности и других отраслях хозяйства (более 90 %), синтезируют способами,разработанными в лаборатории.
Реакция щелочного плавления.Эту реакцию проводят сплавлением щелочных солей ароматических кислот с твердымищелочами.
SO3Na
NaOHтв. t>300o
ONa
OH
HCl
Гидролиз ароматических галогенопроизводныхпротекает в жестких условиях(при повышенной температуре и давлении). Эта реакция идет по механизму нуклеофильного ароматического замещения -SNаром.
Cl
H2O
350o,p,8%NaOH
OH
+ HCl
В более мягких условиях по механизму SN2 проходит гидролиз арилгалогенидов, содержащих сильные электроноакцепторные заместители в ароматическомядре.
 Cl
Cl
NO2
 NO2
NO2
H2ONaOH
ONa
NO2
NO2 H+
OH

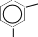 NO2
NO2
NO2
Гидролизводных растворовароматическихдиазосоединений
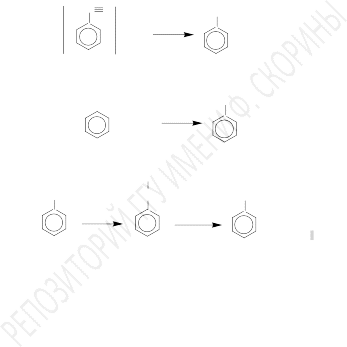 N N+
N N+
Hal-
OH
H2O
~80o +N2+HHal
Прямое гидроксилирование. Катализаторами служат солиметалловFe (II), Cu (II), Ti (III).
кат
+HOOH
OH
+Н2О
Окислениеизопропилбензола(кумола)–методСергеева-Удриса, используемый в промышленности.
CH3
H3C_CH_CH3
3
O2H3C_C_OOH
OH
Н2О
3
+ CH
_C_CH
H+
O
ацетон
Практическое применение.Фенолы имеют важное значение для органического синтеза в качестве либо исходных веществ, либо полупродуктов в производстве разнообразных органических соединений, использующихся в самых различных областях техники и хозяйства. Так, фенол применяется для синтеза алкилфенолов,-капролактама, адипиновой кислоты, анилина, бисфенола А, пестицидов, пластификаторов. Его также используют в синтезе многих лекарственных средств (аспирина, салола и др.), красителей, индикаторов (фенолфталеина). Выше уже упоминались фенол-формальдегидныесмолы, на основе которых готовят лаки и пленкообразователи, связующие иклеи,наполнители,пропиточныематериалыипенопласты,
стабилизаторы полимерных материалов и синтетические дубильныевещества.
Одно из направлений применения фенола – получение взрывчатых материалов. Пикриновая кислота в виде аммониевой соли не уступает по взрывной силе тротилу.
Экологические аспекты.Одноатомные фенолы – сильнейшие нейротоксичные вещества, поражающие печень и почки. Высшие члены этого ряда обладают очень слабой токсичностью. Многоатомные фенолы при длительном воздействии на организм человека нарушают окислительное фосфорилирование и некоторые другие ферментативныесистемы.
Фенолпоступает в окружающую среду со сточными водами предприятий по производству смол и пластиков, переработке и сухой перегонке древесины, газификации угля, сланца и торфа, и также при выбросах в атмосферу коксохимических и металлургических заводов.
В почве и поверхностных водах фенол под воздействием мик- роорганизмов подвергается биотрансформации. Его разрушение может осуществляться под действием солнечного света и в поверхностных водах происходит за 7 - 20 дней.
Фенол токсичен как для гидробионтов (рыбы, моллюски и т. д.), так и для наземных животных, в том числе и человека. У человека фенол поражает центральную нервную систему (ЦНС), желудочно-кишечный тракт, при попадании на кожу вызывает сильные ожоги. Смертельные отравления возникают при приеме внутрь 1 – 3 г фенола.
При хронических воздействиях фенол вызывает головную боль нарушение сна, одышку, сердцебиение; наблюдаются поражения периферической и центральной нервной системы, печени, нарушения белкового обмена.
В организм человека фенол может проникать как через желудочно- кишечный тракт, так и через легкие, и кожу. Быстро невсасываясь, он концентрируется главным образом в печени и почках. Часть фенола подвергается биотрансформации с образованием гидрохинона, пирокатехина и СО2, а другая часть в виде конъюгатов с глюкуроновой и серной кислотами выводится почками.
ПДКмр =0,01мг/м3;ПДКсс=0,003мг/м3;ПДКводы=0,001мг/л.
Крезолыпоступают в окружающую среду с выбросами производств, использующих и получающих эти соединения, а также выхлопными газами двигателей внутреннего сгорания.
Как и фенол, крезолы обладают сильным токсическим действием, как на гидробионтов наземных животных, так и на растения.
Крезолы хорошо всасываются через кожу, оказывая на нее раздражающеедействие,ивызываютнекроз.Прихронических
отравлениях происходит нарушение функции ЦНС, поражение легких и печени. Есть данные, указывающие на канцерогенное и эмбритоксическое действие этих веществ.
Биотрансформация крезолов идет по пути окисления в 4- гидоксибензойную кислоту и диокситолуолы с дальнейшим образованием эфиров с серной и глюкуроновой кислотами. ПДКводы= 8 0,04 мг/л.
Нафтолыпоступают в окружающую среду с выхлопными газами автотранспорта, с предприятий по производству синтетического каучука, красителей, пестицидов и резинотехнических изделий.
Нафтолы обладают способностью умеренно накапливаться в организме. Есть данные, свидетельствующие о канцерогенных и мутагенных свойствах, а также об эмбриотоксическом действии квеществ.
При отравлении 2-нафтолом наблюдаются тошнота, рвота, горная боль, повышается температура тела, появляются белок и кровь в моче.
При остромотравлении 1-нафтоломвозможен летальный исход. При хроническом воздействии наблюдается желтушность кожи,увеличиваются печень и селезенка, появляется белок в моче.
В организме 1-нафтол окисляется до 1,4-нафтохинона и некоторыхдругих (неидентифицированных) соединений. Из организма он выводится с мочой как в виде конъюгатов с глюкуроновой и серной кислотами, так и в неизменномвиде.Для1-нафтолаПДКводы=0,1мг/л3;для2-нафтолаПДКмр=
0.006мг/м3,ПДКсс=0,003мг/м3,ПДКводы =0,4мг/л.
Пирокатехин угнетает фотосинтез и развитие растений, вызывая при значительных концентрациях их гибель. Пирокатехин для гидробионтов токсичен, а для теплокровных животных является аллергеном. Есть также данные о мутагенном и канцерогенном его действии. При попадании на кожуон оказывает раздражающее действие, при повторном воздействии вызывает дерматит. ПДКводы = 0,1 мг/л.
Резорцин менее токсичен для гидробионтов, чем пирокатехин. Он может проникать через кожу человека, вызывает ее раздражение. Порциииспользуется в медицине как вяжущее средство. Значительным токсическим действием на человека не обладает. ПДКводы = 1 мг/л.
Гидрохинон попадает в окружающую среду со сточными водами предприятий по производству пластмасс, синтетического каучука кино- и фотоматериалов, красителей, а также с выхлопными газами дизельныхдвигателей.
Гидрохинон оказывает токсическое действие на гидробионты и растенияв концентрациях от 0,005 до 28 мг/л. Для человека токсичность этого вещества небольшая. Из организма он выводится главным образом в виде конъюгатов с серной и глюкуроновой кислотами. ПДКводы = 0,2 мг/л.
