
- •1. Аминокислоты. Классификация(по структуре, по характеру r-групп, заменимые и незаменимые).
- •4.Вторичная структура белка. Альфа- спираль и бета – складчатый слой.
- •5. Третичная структура белка и силы ее стабилизирующие.
- •6. Четвертичная структура белка. Понятия о денатурации и деструкции.
- •7.Кооперативный эффект связывания кислорода гемоглобином.
- •8. Отличия ферментов от неорганических катализаторов.
- •9. Классификация ферментов с примерами реакций на каждый класс.
- •10. Влияние температуры, pH и концентрации фермента на скорость ферментативной реакции.
- •11.Влияние концентрации субстрата на скорость ферментативной реакции. Вывод уравнения Михаэлиса-Ментен.
- •13. Ингибирование ферментов. Неконкурентное ингибирование.
- •14.Аллостерические ферменты.
- •15.Активный центр фермента и его свойства.
- •16. Кофакторы и коферменты. Классификация.
- •17.Молекулярные механизмы ферментативного катализа.
- •18. Способы определения активности фермента. Единицы измерения. Понятие об удельной и молярной активности.
- •19. Изоферменты.
- •20. Моносахариды. Представители и свойства. Функции углеводов.
- •22. Гомо- и гетерополисахариды.
- •23.Липиды. Классификация липидов и их функции.
- •24. Жирные кислоты. Их роль в организме.
- •26. Сфинголипиды. Церамиды. Ганглиозиды
- •27. Неомыляемые липиды. Холестерин и его свойства.
- •28. Воски
- •29. Пути превращения углеводов. Реакции гликолиза и его регуляция.
- •30. Пентозофосфатный путь и его значение.
- •31. Путь Энтнера-Дудорова
- •32. Работа пируватдегидрогеназного комплекса
- •33.Работа цикла трикарбоновых кислот(цтк). Анаплеротические реакции цтк.
- •34.Реакции глюконеогенеза
- •35. Распад и синтез гликогена. Гормональная регуляция.
- •36.Глюкозо-аланиновый и глюкозо-лактатный путь, роль в организме человека.
- •37.Дыхательная цепь митохондрий. Характеристика переносчиков
- •38. Хемиоосмотическая модель п.Митчелла (основные постулаты и доказательства).
- •39.Ингибиторы и разобщители дыхательной цепи митохондрий.
- •40. Витамины, классификация. Антивитамины. Несовместимость витаминов. Особенности водо- и жирорастворимых витаминов.
- •41. Жирорастворимые витамины(a, d, e, k).
- •42. Водорастворимые витамины группы b (b1, b2, в12)
- •43. Фолиевая кислота и пантотеновая кислота
- •44. Витамины с и н.
- •57. Окисление жирных кислот с нечетным числом углеродных атомов.
- •58.Окисление ненасыщенных жирных кислот.
- •59. Реакции синтеза жирных кислот.
- •60. Жирные кислоты. Механизм действия моющих средств.
- •61. Глиоксилатный цикл и его биологическая роль.
- •62. Метаболизм глицерина.
- •63.Пути катаболизма углеродного скелета аминокислот. Пути обмена аминокислот.
- •64. Реакции трансаминирования. Использование трансаминаз в медицине.
- •65.Прямое и непрямое дезаминирование аминокислот.
- •66.Особенности дезаминирования аминокислот в скелетных мышцах
- •67.Метаболизм аммиака.
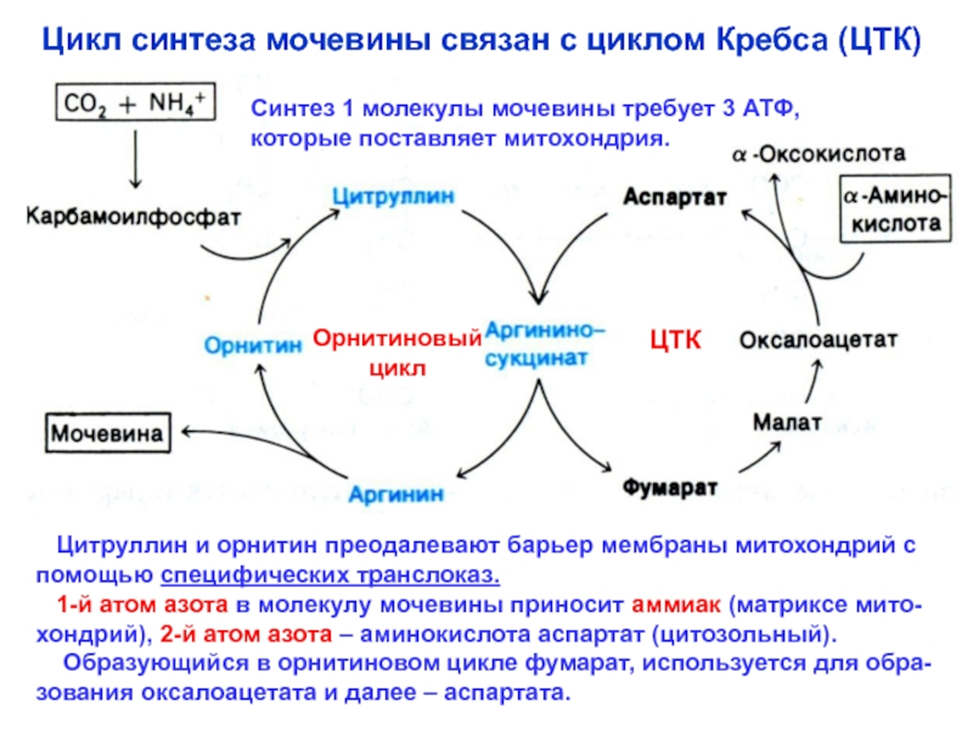
- •68. Цикл мочевины.
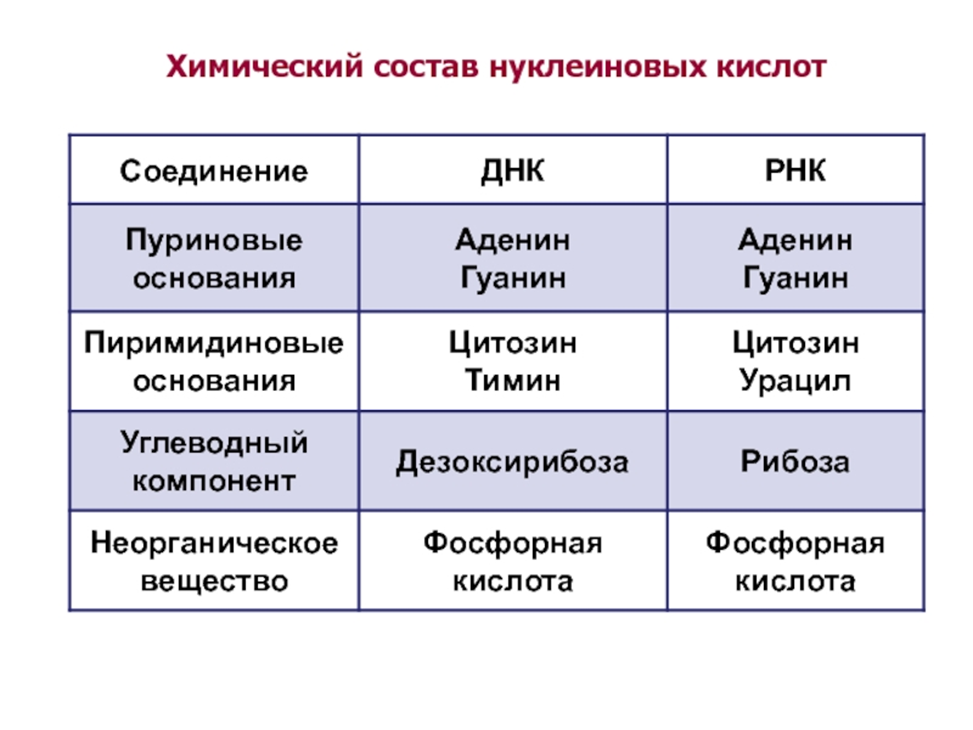
- •69.Химический состав нуклеиновых кислот. Правила Чаргаффа.
- •70.Структурная организация олиго и полинуклеотидов. Характеристика первичной структуры днк.
- •71.Вторичная структура днк. Формы двойной спирали.
- •72.Третичная структура днк.
- •73.Структура и свойства рибосомальных, матричных и транспортных рнк.
- •74. Биосинтез белка. Стадии активации и инициации.
- •75. Биосинтез белка. Стадии элонгации и терминации.
- •76. Ингибиторы биосинтеза белка. Механизм действия дифтерийного токсина.
- •77. Антибиотики-ингибиторы биосинтеза белка.
- •80. Распад липидов в желудочно-кишечном тракте.
- •Переваривание и всасывание
- •Переваривание холестерина
- •Всасывание
68. Цикл мочевины.
69.Химический состав нуклеиновых кислот. Правила Чаргаффа.

70.Структурная организация олиго и полинуклеотидов. Характеристика первичной структуры днк.
Структур единицами НК явл мономерн молекулы – мононуклеотиды. НК – полинуклеотиды - то продукты полимеризации мононуклеотидов, число и последов-ть располож кот в цепях ДНК и РНК опред в строгом соответствии с программой, залож в молекуле матрицы. Мононуклеотиды состоят из 3-х спец компонентов: азотист основания, углевода и фосфорн к-ты. Соединения азотис основания и углевода (рибозы или дезоксирибозы), получившие наз нуклеозидов, легко образ из мононуклеотида при гидролитич отщеп фосфорн к-ты в присутствии щелочи или при участии специфич ферментов – нуклеотидаз. Кажд нуклеотид содерж 3 хим различ компонента: гетероциклич азотист основание, моносахарид (пентозу) и остаток фосфорн к-ты. В зависимости от числа имеющихся в молекуле остатков фосфорн к-ты различ нуклеозидмонофосфаты(НМФ), нуклеозиддифосфаты(НДФ), нуклеозидтрифосфаты (НТФ). В состав НК входят азотист основания 2х типов: пуриновые - А, Г и пиримидиновые – Ц, Т, У. Пентозы в нуклеотидах представлены либо рибозой (в составе РНК), либо дезоксирибозой (в составе ДНК). Нуклеотиды, в кот пентоза представ рибозой - рибонуклеотидами, а НК - РНК. НК, в мономеры кот вход дезоксирибоза - ДНК. Первич стру-ра ДНК - порядок черед дезоксирибонуклеозидмонофосфатов (дНМФ) в полинукпеотид цепи. Кажд фосфатная группа в полинукпеотидн цепи, за исключ фосфорн остатка на 5'-конце молекулы, участ в образ 2-х эфирных связей с участием 3'- и 5'-углеродных атомов 2-х соседних дезоксирибоз, поэтому связь между мономерами обозначают 3', 5'-фосфодиэфирной. Концевые нуклеотиды ДНК различ по структуре: на 5'-конце наход фосфатная группа, а на 3'-конце цепи - свободная ОН-группа. Эти концы называют 5'- и 3'-концами. Линейная послед-ть дезоксирибонуклеотидов в полимерной цепи ДНК сокращённо запис с помощью однобуквенного кода, напр -A-G-C-T-T-A-C-A- от 5'- к 3'-концу. В кажд мономере НК присут остаток фосфорн к-ты. Остатки пентоз тоже прояв гидрофиль св-ва. Азотистые основан почти нераствор в воде, но некот атомы пуринового и пиримидинового циклов способны образ водород связи.
71.Вторичная структура днк. Формы двойной спирали.
Вторичная структура ДНК представляет собой двухцепочечную спираль (см. Рис. 50 ), из двух длинных полинуклеотидных цепей, закрученных относительно общей оси. Сахарофосфатный скелет обеих цепей обращён наружу от оси спирали, а азотистые основания обращены внутрь спирали.
Две цепи удерживаются вместе с помощью водородных связей между азотистыми основаниями (аденин образует две связи с тимином, а гуанин — три связи с цитозином), гидрофобных связей, стэкинг-взаимодействий и ионных связей. Одна цепь ДНК комплементарна другой, при этом цепи антипараллельны.
Структурные особенности двойной спирали ДНК (см. Рис.
51 ):
1.Две антипараллельные цепи являются правозакрученными вдоль общей оси, диаметр спирали
~23,7 Å (2,37 нм).
2.Плоскости, в которых лежат азотистые основания, образующие водородные связи, почти перпендикулярны оси спирали. В B-ДНК основания занимают центральную часть спирали, а сахарофосфатный скелет закручен и обращён наружу. Только края оснований контактируют с растворителем.
3.Каждое основание имеет приблизительно одну ширину, что придает спирали ДНК практически полную симметрию независимо от состава самих оснований. Основания в парах можно поменять местами без каких-либо последствий для спирали: Г ≡ Ц можно изменить на Ц ≡ Г или А = Т на Т = А.
4.Каноническая (идеальная) форма B- ДНК имеет 10 пар оснований в одном шаге (в одном повороте спирале). При этом на каждую пару приходится 36° (если быть точным, то число пар в шаге — 10,4, следовательно, угол составляет 34,6°). Пары оснований уло-
жены в спирали «стопками». Шаг спирали составляет 34 Å (3,4 нм).
ДНК обладает структурной гибкостью и существует в нескольких формах: A-ДНК, B-ДНК (классическая Уотсон-Криковская двойная спираль), Z-ДНК и др. A- и B-ДНК являются правозакрученными спиралями. В B-ДНК азотистые основания располагаются почти перпендикулярно к оси вращения спирали. Z-ДНК представляет собой левозакрученную спираль. Бо́льшая часть ДНК клетки находится в B-форме (см. Приложение 3).
В двойной спирали различают большую и малую бороздки — это расстояния между сахарофосфатными остовами обеих цепей в двойной спирали.
Рис. 52. Уотсон-Криковские пары комплементарных осно-
ваний: пунктиром отмечены водородные связи между атомами
H, O и N.
Длину ДНК измеряют в килоба́зах, т.е. тысячах пар нуклеотидов: 1 кб = 1 000 пар нуклеотидов. Геном одной клетки человека (т.е. все 46 хромосом клетки) имеет длину 3,2 × 106 кб (или 3,2 × 109 пар нуклеотидов).
Химические связи, стабилизирующие вторичную структуру ДНК:
1.Стэкинг-взаимодействия: пары оснований, уложенные в спирали «стопками» удерживаются силами Ван-дер-Ваальса. И несмотря на то, что связи между 2 парами оснований крайне слабые, их большое количество во всей молекуле ДНК является важным фактором её стабилизации.
2.Гидрофобные связи: гидрофобные азотистые основания «погружены» внутрь спирали и взаимодействуют друг с другом, это придаёт спирали дополнительную стабильность.
3.Водородные связи образуются между азотистыми основаниями цепей. Между аденином и тимином — 2 водородных связи, а между гуанином и цитозином — 3 (см. Рис. 52 ).
4.Электростатические взаимодействия: электростатическое отталкива-
ние между отрицательно заряженными остатками фосфорной кислоты дестабилизирует спираль ДНК, однако эти эффекты минимизированы присутствием ионов Mg2+ и катионных белков (богатых лизином и аргинином).
