
- •Министерство здравоохранения российской федерации
- •2. Ковалентные связи в соединениях углерода
- •3. Факторы, влияющие на доступность электронов
- •1. Индуктивный эффект – используется для характеристики электронного облака σ-связи
- •4. Энергетика реакции
- •5.Ароматичность Прежде чем приступить к рассмотрению темы, необходимо вспомнить теорию резонанса. Основные положения теории резонанса
- •Определение и классификация
- •Структурная формула бензола
- •Строение бензола
- •Строение и ароматичность нафталина
- •Механизм электрофильного замещения на примере бензола
- •Правила ориентации в бензольном кольце. Заместители первого и второго рода.
- •Теория ориентации
- •Электрофильное замещение в нафталине
- •Глава 1. Методы получения органических сульфокислот и сульфохлоридов
- •1. Общие сведения о процессе сульфирования
- •2. Схемы и механизм сульфирования аренов
- •3. Особенности сульфирования аренов серной кислотой
- •4. Особенности сульфирования аренов олеумом и серным ангидридом
- •5. Основные способы выделения сульфокислот
- •6. Сульфирование растворами триоксида серы в инертных растворителях
- •7. Сульфирование комплексными соединениями триоксида серы
- •8. Сульфирование хлорсульфоновой кислотой
- •9. Другие методы получения сульфокислот
- •10. Получение хлорангидридов сульфоновых кислот
- •Основные методы получения ароматических сульфохлоридов
- •Сульфохлорирование ароматических углеводородов
- •Сульфохлорирование аренов хлорсульфоновой кислотой в среде инертного органического растворителя
- •Сульфохлорирование алканов
- •Глава 2. Процессы нитрования органических соединений
- •1. Механизм реакции нитрования ароматических соединений
- •2. Влияние основных технологических параметров на процесс нитрования
- •3. Типовой процесс выделения нитропродуктов
- •4. Нитрование смесью азотной и серной кислот
- •5. Нитрование концентрированной азотной кислотой
- •6. Нитрование смесью азотной и уксусной кислот
- •7. Нитрование смесью концентрированной азотной кислоты или ее солей с уксусным ангидридом
- •8. Нитрование разбавленной азотной кислотой
- •Глава 3. Методы получения органических галогенидов
- •1. Галогенирование ароматических соединений
- •Влияние основных технологических факторов на процесс галогенирования аренов
- •Особенности технологии процесса галогенирования ароматических соединений
- •Хлорирование аренов в безводной среде
- •Бромирование ароматических соединений
- •1. Окисление растворов бромида натрия хлором
- •2. Окисление растворов бромида натрия гипохлоритом натрия:
- •Иодирование ароматических соединений
- •Примеры галогенирования ароматических соединений в производстве лекарственных веществ и витаминов
- •2. Галогенирование алканов и в боковую цепь аренов Реакции с молекулярным галогеном
- •Галогенирование с использованием специфических переносчиков галогена (спг)
- •Особенности технологии гомолитического галогенирования
- •Примеры гомолитического галогенирования в производстве лекарственных веществ и витаминов
- •3. Синтез галогенидов из непредельных соединений
- •4. Галогенирование альдегидов, кетонов и карбоновых кислот Радикальное галогенирование альдегидов, кетонов и карбоновых кислот
- •Примеры реакций галогенирования карбонильных соединений
- •Гетеролитическое галогенирование карбоновых кислот
- •Синтез геминальных полигалогеналканов из карбонильных соединений и карбоновых кислот
- •5. Замена гидроксильных групп в спиртах, фенолах и карбоновых кислотах на галоген
- •6. Замещение одних атомов галогена на другие
- •Глава 4. Процессы нитрозирования. Основные реакции диазосоединений
- •1. Химизм процесса и краткая характеристика продуктов реакции
- •2. Влияние основных технологических параметров на ход процесса диазотирования
- •3. Кислотно-основные превращения ароматических диазосоединений
- •4. Реакции замены диазониевой группы
- •5. Реакция азосочетания
- •6. Некоторые реакцииполучения нитрозо- и диазосоединений
- •Глава 5. Замещение галогена и сульфогруппы на другие функциональные группы
- •1. Нуклеофильное замещение галогена в молекуле органического соединения
- •Сведения о механизме реакции
- •Основные факторы, влияющие на ход процесса
- •Использование катализаторов
- •Процессы гидролиза галогенидов
- •Замена атома галогена на алкокси- и феноксигруппы
- •Замена атома галогена на меркапто- и алкил(арил)тиогруппы
- •Замена атома галогена на аминогруппы
- •Замена атома галогена на цианогруппу
- •Замена атома галогена на группу -so3Na
- •2. Нуклеофильное замещение сульфогруппы
- •Реакции щелочного плавления
- •Примеры нуклеофильной замены сульфогруппы в промышленности
- •Глава 6. Процессы алкилирования
- •1. Алкилирование аренов по Фриделю-Крафтсу
- •2. Особенности технологии алкилирования аренов по Фриделю-Крафтсу
- •4. Алкилирование по атому азота (n-алкилирование)
- •6. Гидрокси-, галоген- и аминометилирование
- •Глава 7. Процессы ацилирования
- •1. Ацилирование по атому углерода (с-ацилирование)
- •2. Ацилирование по атому азота (n-ацилирование)
- •Глава 8. Методы восстановления
- •1. Химические методы восстановления
- •Восстановление металлами и солями металлов
- •Восстановление натрием
- •Восстановление оловом и хлоридом олова (II) в кислой среде
- •Восстановление цинком
- •Восстановление железом
- •Восстановление алкоголятами алюминия (метод Меервейна-Понндорфа-Верлея)
- •Восстановление гидридами металлов
- •Восстановление по Кижнеру-Вольфу
- •Восстановление соединениями серы
- •Восстановление сульфидами щелочных металлов
- •Восстановление нитрогруппы серой в щелочной среде
- •Восстановление сернистой кислотой и ее солями
- •Восстановление дитионитом натрия
- •Каталитическое восстановление водородом
- •Восстановление на никелевых катализаторах
- •Восстановление на платиновых и палладиевых катализаторах
- •3. Электролитическое восстановление
- •Глава 9. Методы окисления
- •1. Синтез алкенов методами каталитического и окислительного дегидрирования
- •2. Синтез альдегидов с использованием методов окисления и дегидрирования
- •3. Окислительные методы получения кетонов
- •4. Окислительные методы получения карбоновых кислот
- •5. Окисление непредельных углеводородов
- •6. Окисление ароматического цикла
3. Кислотно-основные превращения ароматических диазосоединений
Строение и свойства диазосоединений меняются в зависимости от значения рН среды:

Катион диазония (I) в водно-щелочной среде образует гидроксид диазония, затем обратимо превращается в амфотерныйсин-диазогидрат (II) и всин-диазотат (III). Соль при нагревании относительно медленно изомеризуется ванти-форму (IV). Поскольку этот переход практически необратим, превращениеанти-диазотата (IV) в катион диазония происходит другим путем. При этом под действием кислотыанти-диазотат превращается в арилнитрозамин (V), а затем ванти-диазогидрат (IV), который может переходить всин-форму и превращаться в катион диазония.
Превращение анти-диазотата в диазоний катион сильно затруднено и сопровождается значительным разложением с выделением азота и образованием различных побочных продуктов. Это необходимо учитывать при выборе условий хранения и реакций солей диазония.
Наибольшая стабильность и реакционная способность соли диазониянаблюдается в кислой среде. При проведении реакций с диазосоединениями в нейтральной или щелочной средах необходимо обеспечить минимальное время пребывания их в неблагоприятных условиях.
4. Реакции замены диазониевой группы
Диазониевую группу можно заместить многими другими группами. Часть этих реакций представляет собой обычное нуклеофильное замещение и проходит по механизму SN1, другие протекают по гомолитическому механизму в присутствии катализаторов. Следует иметь в виду, что диазогруппа может активировать отрыв другой группы от ароматического кольца.
Замещение диазогруппы на ОН-группу ведут в два этапа. На первом аминдиазотируют в разбавленной серной кислоте,чтобы на последующей стадии не образовывалась примесь арилгалогенида, на втором полученный кислый раствор соли диазонияосвобождаютот избытка азотистой кислоты мочевиной или сульфаминовой кислотой икипятят. Значительно лучшие результаты достигаются при добавленииCu2Oс избыткомCu(NO3)2 илиCuSO4. Процесс в этом случае идет быстро и с высокими выходами даже при комнатной температуре, а в качестве интермедиатов образуются арильные радикалы.
Этот способ введения гидроксильной группы используется в синтезе гваякола,мезатона, фетанола, витамина В6и др.:


Процесс разложения диазосоединений всегда сопровождается образованием значительного количества продуктов неизвестного строения (диазосмол), загрязняющих целевой продукт.
В большинстве случаев операции диазотирования и разложения диазосоединений можно совместить, так как при высоких температурах ( 100 °С) скорость разложения солей диазония (особенно в присутствии катализаторов) значительно больше скорости диазотирования. При получении гваякола одностадийным способом к кипящему раствору о-анизидина в разбавленной серной кислоте, содержащему медный купорос, непрерывно добавляют раствор нитрита натрия и через реакционную массу пропускают перегретый водяной пар для отгонки образующегося гваякола. Выход гваякола при этом достигает 80—82 %. Основное достоинство метода — короткая аппаратурная схема и малые энергетические затраты (не требуется охлаждение на стадии диазотирования). Недостатки — трудность регулирования процесса, большое смолообразование, пенообразование, выделение окислов азота вследствие термического разложения азотистой кислоты.
Замещение диазогруппы на галоген. Для замены диазогруппы на атомы хлора или брома используют реакцию Зандмейра-Гаттермана.
![]()
Целевой продукт получается с высоким выходом. Поскольку реакцию проводят в водном растворе, в качестве побочных продуктов образуются гидроксисоединения. Процесс, по-видимому, протекает по следующей схеме:
![]()
Таким образом, галогенид меди (I) регенерируется и по существу служит катализатором. Другая точка зрения состоит в том, что соль диазония и хлорид меди (I) на холоду образуют комплекс, который при нагревании распадается по радикальному механизму с образованием арилхлорида.По методу Зандмейера раствор соли диазония обрабатывают хлоридом или бромидом меди (I) при 0—5 °С, а по методуГаттермана— медью сHClилиHBrпри температуре около 50 °С, однако выходы продукта по этому методу ниже и порошок меди должен быть свежеприготовленным (действием цинковой пыли на водный растворCuSO4). Имеются и другие модификации этого метода.
Замену диазогруппы на иод осуществляютсолями иода в отсутствие катализатора и с хорошими выходами.
![]()
По-видимому, под действием окислителей иодид-ион превращается в иод, который с иодид-ионом образует I3–. Это подтверждается выделением солейArN2+I3–, которые при стоянии превращаются в продукты реакции.
![]()
Исследователи не исключают и свободнорадикальный механизм.
Одним из лучших методов введения атома фторав ароматическое кольцо являетсяреакция Шимана.

К растворам солей диазония добавляют холодный водный раствор NaBF4,HBF4илиNH4BF4. Выпавший осадок высушивают и сухую сольArN2+BF4–нагревают. Борфториды арилдиазония гладко разлагаются с достаточно высокими выходами целевого продукта. Реакция идет помеханизму SN1, промежуточным продуктом является фенил-катион.
Ниже приводятся примеры таких реакций, встречающихся в синтезе лекарственных веществ (антитусини др.):

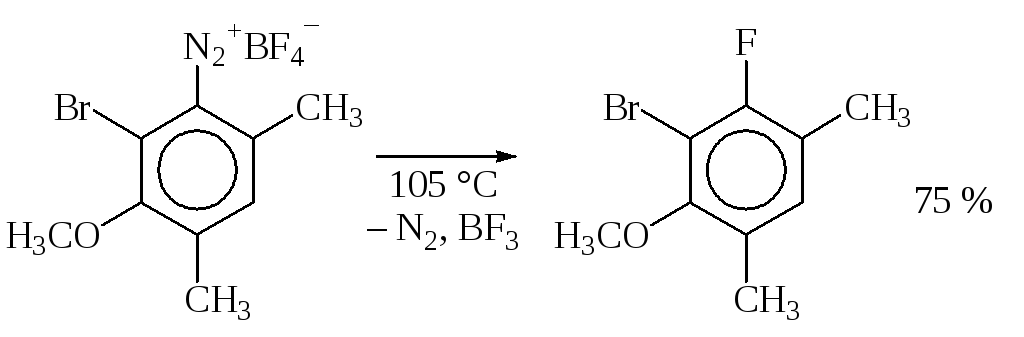
Замещение диазогруппы на CN- и другие группы. Замена диазониевой группы нациано- и нитрогруппытакже относится креакциям Зандмейера. Чтобы избежать образованияHCNнеобходимо поддерживатьнейтральную среду, а в случае нитрита натрия реакция идет тольков нейтральной или щелочной среде. Выход целевых продуктов хороший.
![]()
![]()
Для предотвращения конкурентной реакции с хлорид-ионом часто используют арилдиазоний борфториды.
Для замены диазогруппы на сульфохлоридную,соли диазония обрабатываютдиоксидом серы в присутствии хлорида меди (II):
![]()
Эта реакция применяется в синтезе некоторых сульфамидных препаратов:
![]()
Гидридное замещение диазониевой группы — хорошийметод удаления аминогруппы из ароматического кольца. Наиболее удобно использовать соли фосфорноватистой кислоты (H3PO2), однако применяют и другие восстановители (формальдегид, метанол).
![]()
С помощью этой реакции удаляют аминогруппу после того, как она направила другие заместители в заданные положения кольца:

Восстановление солей диазония сернистой кислотой и ее солями, цинком в кислой среде, боргидридом натрия в ДМФА и др. методами приводит к образованиюмонозамещенных гидразинов.
![]()
