
- •Министерство здравоохранения российской федерации
- •2. Ковалентные связи в соединениях углерода
- •3. Факторы, влияющие на доступность электронов
- •1. Индуктивный эффект – используется для характеристики электронного облака σ-связи
- •4. Энергетика реакции
- •5.Ароматичность Прежде чем приступить к рассмотрению темы, необходимо вспомнить теорию резонанса. Основные положения теории резонанса
- •Определение и классификация
- •Структурная формула бензола
- •Строение бензола
- •Строение и ароматичность нафталина
- •Механизм электрофильного замещения на примере бензола
- •Правила ориентации в бензольном кольце. Заместители первого и второго рода.
- •Теория ориентации
- •Электрофильное замещение в нафталине
- •Глава 1. Методы получения органических сульфокислот и сульфохлоридов
- •1. Общие сведения о процессе сульфирования
- •2. Схемы и механизм сульфирования аренов
- •3. Особенности сульфирования аренов серной кислотой
- •4. Особенности сульфирования аренов олеумом и серным ангидридом
- •5. Основные способы выделения сульфокислот
- •6. Сульфирование растворами триоксида серы в инертных растворителях
- •7. Сульфирование комплексными соединениями триоксида серы
- •8. Сульфирование хлорсульфоновой кислотой
- •9. Другие методы получения сульфокислот
- •10. Получение хлорангидридов сульфоновых кислот
- •Основные методы получения ароматических сульфохлоридов
- •Сульфохлорирование ароматических углеводородов
- •Сульфохлорирование аренов хлорсульфоновой кислотой в среде инертного органического растворителя
- •Сульфохлорирование алканов
- •Глава 2. Процессы нитрования органических соединений
- •1. Механизм реакции нитрования ароматических соединений
- •2. Влияние основных технологических параметров на процесс нитрования
- •3. Типовой процесс выделения нитропродуктов
- •4. Нитрование смесью азотной и серной кислот
- •5. Нитрование концентрированной азотной кислотой
- •6. Нитрование смесью азотной и уксусной кислот
- •7. Нитрование смесью концентрированной азотной кислоты или ее солей с уксусным ангидридом
- •8. Нитрование разбавленной азотной кислотой
- •Глава 3. Методы получения органических галогенидов
- •1. Галогенирование ароматических соединений
- •Влияние основных технологических факторов на процесс галогенирования аренов
- •Особенности технологии процесса галогенирования ароматических соединений
- •Хлорирование аренов в безводной среде
- •Бромирование ароматических соединений
- •1. Окисление растворов бромида натрия хлором
- •2. Окисление растворов бромида натрия гипохлоритом натрия:
- •Иодирование ароматических соединений
- •Примеры галогенирования ароматических соединений в производстве лекарственных веществ и витаминов
- •2. Галогенирование алканов и в боковую цепь аренов Реакции с молекулярным галогеном
- •Галогенирование с использованием специфических переносчиков галогена (спг)
- •Особенности технологии гомолитического галогенирования
- •Примеры гомолитического галогенирования в производстве лекарственных веществ и витаминов
- •3. Синтез галогенидов из непредельных соединений
- •4. Галогенирование альдегидов, кетонов и карбоновых кислот Радикальное галогенирование альдегидов, кетонов и карбоновых кислот
- •Примеры реакций галогенирования карбонильных соединений
- •Гетеролитическое галогенирование карбоновых кислот
- •Синтез геминальных полигалогеналканов из карбонильных соединений и карбоновых кислот
- •5. Замена гидроксильных групп в спиртах, фенолах и карбоновых кислотах на галоген
- •6. Замещение одних атомов галогена на другие
- •Глава 4. Процессы нитрозирования. Основные реакции диазосоединений
- •1. Химизм процесса и краткая характеристика продуктов реакции
- •2. Влияние основных технологических параметров на ход процесса диазотирования
- •3. Кислотно-основные превращения ароматических диазосоединений
- •4. Реакции замены диазониевой группы
- •5. Реакция азосочетания
- •6. Некоторые реакцииполучения нитрозо- и диазосоединений
- •Глава 5. Замещение галогена и сульфогруппы на другие функциональные группы
- •1. Нуклеофильное замещение галогена в молекуле органического соединения
- •Сведения о механизме реакции
- •Основные факторы, влияющие на ход процесса
- •Использование катализаторов
- •Процессы гидролиза галогенидов
- •Замена атома галогена на алкокси- и феноксигруппы
- •Замена атома галогена на меркапто- и алкил(арил)тиогруппы
- •Замена атома галогена на аминогруппы
- •Замена атома галогена на цианогруппу
- •Замена атома галогена на группу -so3Na
- •2. Нуклеофильное замещение сульфогруппы
- •Реакции щелочного плавления
- •Примеры нуклеофильной замены сульфогруппы в промышленности
- •Глава 6. Процессы алкилирования
- •1. Алкилирование аренов по Фриделю-Крафтсу
- •2. Особенности технологии алкилирования аренов по Фриделю-Крафтсу
- •4. Алкилирование по атому азота (n-алкилирование)
- •6. Гидрокси-, галоген- и аминометилирование
- •Глава 7. Процессы ацилирования
- •1. Ацилирование по атому углерода (с-ацилирование)
- •2. Ацилирование по атому азота (n-ацилирование)
- •Глава 8. Методы восстановления
- •1. Химические методы восстановления
- •Восстановление металлами и солями металлов
- •Восстановление натрием
- •Восстановление оловом и хлоридом олова (II) в кислой среде
- •Восстановление цинком
- •Восстановление железом
- •Восстановление алкоголятами алюминия (метод Меервейна-Понндорфа-Верлея)
- •Восстановление гидридами металлов
- •Восстановление по Кижнеру-Вольфу
- •Восстановление соединениями серы
- •Восстановление сульфидами щелочных металлов
- •Восстановление нитрогруппы серой в щелочной среде
- •Восстановление сернистой кислотой и ее солями
- •Восстановление дитионитом натрия
- •Каталитическое восстановление водородом
- •Восстановление на никелевых катализаторах
- •Восстановление на платиновых и палладиевых катализаторах
- •3. Электролитическое восстановление
- •Глава 9. Методы окисления
- •1. Синтез алкенов методами каталитического и окислительного дегидрирования
- •2. Синтез альдегидов с использованием методов окисления и дегидрирования
- •3. Окислительные методы получения кетонов
- •4. Окислительные методы получения карбоновых кислот
- •5. Окисление непредельных углеводородов
- •6. Окисление ароматического цикла
8. Сульфирование хлорсульфоновой кислотой
Хлорсульфоновая кислота — активный сульфирующий реагент. При ее диссоциации образуется высокая концентрацияSO3, а такжеHSO3+, которая является более активной электрофильной частицей, чем сульфотриоксид.

Однако,
хлорсульфоновая кислота является опасным реагентом. Она бурно реагирует с водой, образуяH2SO4иHClс выделением огромного количества тепла. Несоблюдение правил работы с хлорсульфоновой кислоты может привести к взрывам, выбросам реакционной массы. Из-за опасности технологии, этот метод редко используется в промышленных синтезах;
при избытке хлорсульфоновой кислоты арены образуют сульфохлориды, а не сульфокислоты, а при мольном соотношении реагентов сульфирование аренов в среде хлорсульфоновой кислоты осуществитьтехнологически трудно, так как образуется вязкая малоподвижная гетерогенная масса (как и в случае жидкогоSO3) и выделяется газообразныйHCl:
ArH+HSO3ClArSO3H+HCl
Поэтому сульфирование хлорсульфоновой кислотой предпочитают проводить в среде растворителя.
Сульфирование хлорсульфоновой кислотой в инертных растворителях (полигалогеналканы, эфиры, нитробензол и др.) используют как дляС-сульфирования(например, сульфирование 2-нафтола), так и длясульфатирования. Метод не требует избытка реагента, идет с высоким выходом и высокой селективностью.
Сульфирование аренов хлорсульфоновой кислотой в полигалогеналканах и нитробензоле идет за счет SO3 по пиросульфатной схеме, а в среде эфира и подобных ему растворителей — электрофилом являетсякомплекс SO3·L, диссоциация которого подавлена огромным избытком лиганда.
Примером О-сульфирования (сульфатирования) хлорсульфоновой кислотой в среде сухого этилового эфира может служить промышленный синтез децилата(тромбовара — препарата для лечения варикозного расширения вен):

Реакцию ведут при 10—15 °С, прибавляя раствор хлорсульфоновой кислоты в эфире (т. е. практически комплекс SO3·эфир) к эфирному раствору тетрадеканола. Содержание влаги в эфире не должно превышать 0,5 %.
Многочисленные попытки провести сульфирование иным, более технологичным способом (например, раствором SO3 в жидкомSO2) не привели к получению продукта фармакопейного качества.
9. Другие методы получения сульфокислот
Сульфогруппа может быть введена в молекулу органического соединения с использованием сульфит- и гидросульфит-ионов, которые являясь активными нуклеофилами, образуют замещенные и незамещенные сульфокислоты, реагируя с:
эпоксисоединениями (поSN2-механизму)
![]()
первичными алкилгалогенидами, а также галогензамещенными кислотами, спиртами, кетонами, (поSN2-механизму) с выходом 70—90 %

ароматическими активированными галогенидами (по SNAr-механизму)

альдегидами и кетонами (поAN-механизму), образуя α-гидроксисульфонаты
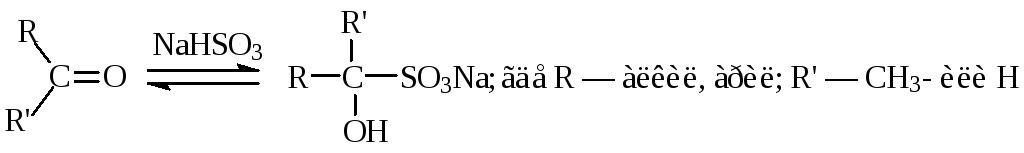
Реакция обратима, на положение равновесия существенное влияние оказывают пространственные препятствия.
ациклическими сопряженными непредельными карбонильными соединениями и их производными по С=С-связи (необратимо), и по С=О-группе (обратимо):
![]()
Присоединение можно проводить по двойной связи, не затрагивая карбонильную группу.
хинонами, а также сфенолами, ароматическими аминами и некоторыми другими соединениямив присутствии окислителя. Нуклеофил присоединяется к хиноидным формам исходных субстратов.
Например, п-фенилендиамин в отсутствие окислителя с гидросульфитом не реагирует, а при его наличии реагирует легко и с высоким выходом, что объясняют промежуточным образованием хинондиимина:

Присоединение гидросульфитов к двойной связи может проходить не только по ионному, но и по радикальному механизму в зависимости от степени поляризации связи.
