
Р-элементы V группы
Фосфорноватистая и фосфористая кислоты: получение, строение молекул, кислотно-основные и окислительно-восстановительные свойства.
Образование аммиакатов и гидроксокомплексов металлов и их разрушение кислотами при нагревании.
Аммиак, гидразин, гидроксиламин: химическая связь и строение молекул, кислотно-основные и окислительно-восстановительные свойства. Объясните агрегатное состояние аммиака, его самоионизацию в жидком состоянии.
Используя принцип Ле- Шателье определите, в какую сторону смещается равновесие реакции: PCl5 (г)
 PCl3
(г) +Cl2
(г),
PCl3
(г) +Cl2
(г),
 H
H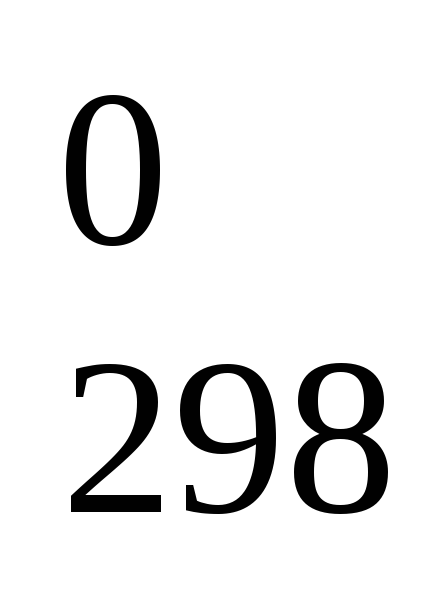 =92.6
кДж при а) повышении температуры, б)
повышении давления, в) введении
катализатора.
=92.6
кДж при а) повышении температуры, б)
повышении давления, в) введении
катализатора.Как изменяется в ряду Li3N-Be3N2-C3N4 кислотно - основные свойства? Составьте соответствующие уравнения реакций.
Объясните получение NO, NO2 в лаборатории, технике. Приведите реакции горения в атмосфере NO, NO2 металлов и неметаллов. Какие правила техники безопасности необходимо соблюдать при работе с этими веществами.
Постройте энтальпийную диаграмму образования NO.
Укажите окислитель и восстановитель в ниже перечисленных реакциях:
N2H4
(ж) +O2
(г) =N2
(г) +2H2O(г),
![]() H
H![]() =
- 622 кДж; N2H4
(ж) +NO2
(ж) =3/2N2
(г) +2H2O(г),
=
- 622 кДж; N2H4
(ж) +NO2
(ж) =3/2N2
(г) +2H2O(г),
![]() H
H![]() =
- 565 кДж. Могут ли служить эти вещества
ракетным топливом с точки зрения экологии
?
=
- 565 кДж. Могут ли служить эти вещества
ракетным топливом с точки зрения экологии
?
Исходя из строения молекул H3P и H3N, сравните их устойчивость, электронодонорные свойства.
Напишите реакции взаимодействия гидразина в кислой среде с KMnO4; какие свойства обусловливают возможность применения гидразина в качестве ракетного топлива?
Cоставьте схему гидратации P4O10 и определите основность фосфорной кислоты.
Р-элементы IV группы
Преобразуйте цепочки превращений в уравнения химических реакций:
CO → COCl2 → CO2 → Na2CO3 → (MgOH)2CO3,
SiO2 → Mg2Si → SiH4 → Na2SiO3 → Na2CO3.
Опишите строение молекулы СОСl2. «Фосген» - очень токсичное вещество. Объясните, возможно ли с помощью реакции гидролиза нейтрализовать его?
Объясните действие аппарата Киппа. Объясните взаимодействие углерода и кремния с растворами щелочей и кислот
Объясните электронную конфигурацию иона CN- с позиций теории молекулярных орбиталей.
Химические свойства простых веществ германия, олова и свинца.
Кварц, кремниевые кислоты, силикаты, гексафторокремниевая кислота: получение и свойства.
Кремниевые кислоты. Объясните склонность кремниевых кислот к образованию коллоидных растворов. Составьте уравнения реакций их получение в виде золя и геля (исходное соединение- жидкое стекло).
Составьте уравнения окислительно- восстановительных реакций:
PbO2 + MnSO4 + HNO3 HMnO4 +… CaCN2 + C + Na2CO3 NaCN+…
Как изменяются в ряду Ge(OH)4- Sn(OH)4- Pb(OH)4 кислотно- основные свойства гидроксидов? Ответ подтвердите соответствующими уравнениями реакций.
Склонность к образованию гомоцепей из атомов, образование аллотропных модификаций уменьшается в ряду: C > Si > Ge > Sn > Pb. Как это можно объяснить?
|
|
|
|
