
Презентация 6
.pdf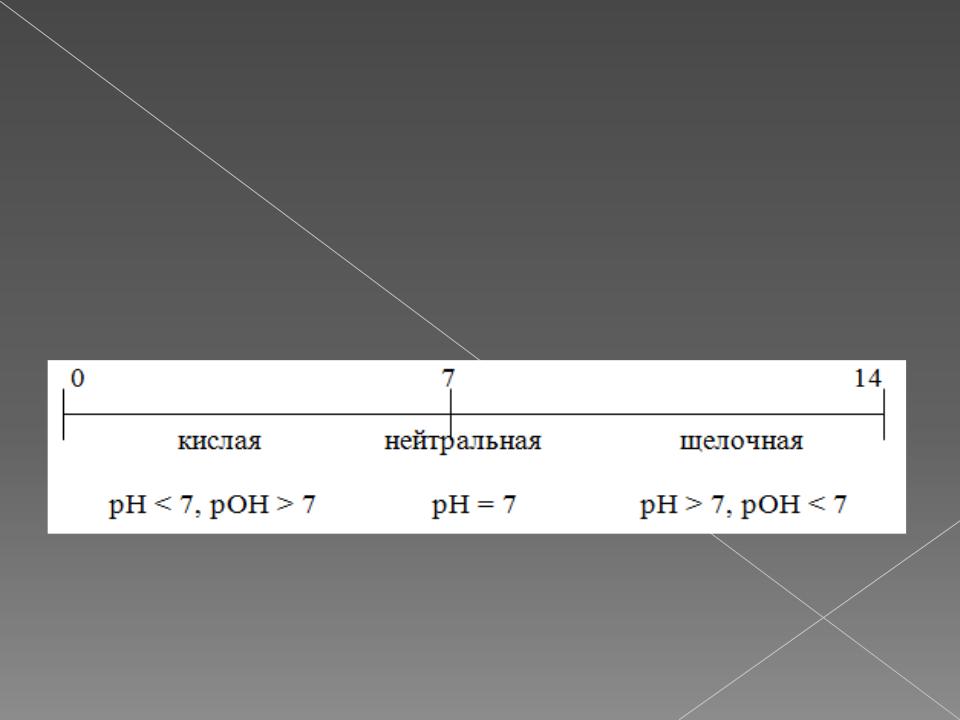
В технике для характеристики кислотности растворов используют величину водородного показателя рН:
рН = lg[H+].
рН = 14 – рОН
Гидроксидный показатель pOH = lg[OH−].] Шкала кислотности:

Уравнение диссоциации кислот (сильной и слабой):
H SO →2H+ + SO 2− |
H SO H+ + HSO 2− |
||||
2 |
4 |
4 |
2 |
3 |
3 |
При расчете рН слабых кислот учитывается только 1 ступень диссоциации: Кдис1 > Кдис2.
Гидролиз солей
Гидролиз солей
По катиону |
По аниону |
По катиону |
Совместный |
|
и аниону |
||||
|
|
|
Гидролиз солей – реакция взаимодействия солей с водой, приводящая к нарушению равновесия электролитической диссоциации воды и изменению рН раствора.
Физический смысл – в результате гидролиза образуются слабо диссоциированные частицы (ионы или молекулы), поэтому гидролизу подвергаются катионы слабых оснований и анионы слабых кислот. Не подвергаются гидролизу соли, образованные сильным основанием и сильной кислотой и нерастворимые соли. Процесс гидролиза обратимый.
Если в состав соли входит только один слабый ион (катион или анион), то гидролиз идет ступенчато, где количество ступеней соответствует численно заряду слабого иона.

Правило записи гидролиза, идущего по катиону или аниону:
1)Написать уравнение диссоциации и определить тот ион, который будет реагировать с водой
2)Написать реакцию взаимодействия слабого иона с водой:
слабый Kt: Ktm+ + H2O↔(KtOH)(m-1) + H+ pH<7 среда кислая
cлабый An: Ann- + H2O ↔ (Han)(-n+1) + OH-
3)Написать реакцию в полном мономолекулярном виде. Написать уравнение (2) добавив в левую и правую части его те ионы соли, которые с водой не реагируют.
4)Написать реакцию в молекулярном виде соединяя в левой и правой части уравнения Kt c An в электронейтральные молекулы
Гидролиз по катиону
NH4Cl |
ZnCl2 |
Cu(NO3)2 |
Al2(SO4)3 |
|
NH + |
Zn+2 |
Cu2+ |
Al+3 |
|
4 |
|
|
|
|
Катион однозаряден: |
|
|
||
NН4Cl + Н2O |
NH4OH?+ |
HCl |
|
|
NH4+ + HOH |
NH4OH + H+ |
|
Среда кислая |
|
|
pH<7 |
|||
|
|
|
|
|
Cl
Катион многозаряден:
AlCl3 + H2O = AlOHCl2 + HCl |
|
|
|
||
|
Гидроксохлорид |
|
Среда |
||
Al+3 + H+ OH_ |
алюминия |
|
|
||
|
|
кислая |
|||
(AlOH)2+ |
+ H+ |
|
|||
|
|
_ |
Cl |
_ |
pH<7 |
|
2Cl |
|
|
||
|
|
|
|
||
|
|
|
|
|
|
Гидролиз по аниону
Na2CO3 |
K2S |
NaСN |
K3PO4 |
|
2– |
S |
2– |
CN– |
PO43– |
CO3 |
|
|
|
|
Однозарядный анион :
NaСN + Н2O НСN + NaOH
НСN + NaOH
CN– + НOН НСN + OН
 Na+
Na+
Многозарядный анион:
Na2SO3 + H2O = NaHSO3 + NaOH
|
|
|
|
|
|
|
|
|
Гидросульфит натрия |
SO32 _ |
|
|
|
|
|
_ |
|||
+ |
|
H+ OH |
(HSO3)_ + OH |
||||||
|
|||||||||
|
|
|
|
|
|
|
|
|
2Na+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Среда
щелочная
pH>7
Среда
щелочная
pH>7
Гидролиз по катиону и аниону
Однозарядный катион и анион :
NН4СN + Н2O |
НСN + NН4OН |
||
CN– + NН4 + НOН НСN |
+ |
NН4OН |
|
|
|
|
|
|
|
|
|
Однозарядный катион и многозарядный
анион :
(NН4)2СО3 + Н2О NH4ОН + NH4НСО3, NH4+ + СО32 + HОН NH4OH + НСО3 .
Многозарядный катион и однозарядный
|
анион : |
|
Zn(NO2) 2 |
+ Н2О ZnОНNO2 |
+ НNO2, |
Zn2+ + NO + HОН ZnОН+ |
+ HNО . |
|
|
2 |
2 |

Реакции обмена, сопровождающиеся гидролизом
2AlCl3 + 3Na2CO3+ 3H2O 2Al(OH)3↓ + 3CO2 + 6NaCl
Cr2(SO4)3 + 3Na2S + 6H2O 2Cr(OH)3↓ + 3H2S + Na2SO4
2Cu(NO3)2 + 2Na2CO3 + H2O Cu2(OH)2CO3↓ + 4NaNO3 + CO2


