
Презентация 6
.pdf
Слабые электролиты слабые кислоты и слабые основания) диссоциируют обратимо и ступенчато, количество ступеней равно числу функциональных групп (Н+ в кислоте или ОН− в основании) в молекуле электролита, в каждой последующей происходит отрыв одной функциональной группы (Н+ в кислоте или ОН− в основании) , равновесие сдвинуто влево. Заряд иона (аниона или катиона) численно равен номеру ступени. Кислые соли – первичная диссоциация идет полностью (т.к. соль – сильный электролит), далее как у слабой кислоты. Основные соли – первичная диссоциация растворимой соли идет полностью (т.к. соль – сильный электролит) и далее как слабого основания.
1)H2SO3 H+ + НSO3− 2) НSO3− Н+ + SO32−
1) Сu(ОН)2 СuОН+ + ОН− 2) СuОН+ Сu2+ + ОН−
KHCO3 K+ + HCO3− HCO3− H+ + CO32− AIOHCI2 AIOH+2 + 2CI−
AIOH+2 AI+3 + OH−

Смещение равновесия слабого электролита
В пробирку с водой добавляем CH3COOH + МЕТИЛ ОРАНЖ –
Добавляем
CH3COONa
H2O
CH3COOH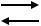 CH3COO _ + H+
CH3COO _ + H+
CH |
COONa |
CH |
COO _ + Na+ |
3 |
|
3 |
|
Растворы слабых электролитов
Диссоциация: |
|
|
|
||
• H3PO4 |
|
H2PO4 , К1= 7,1·10 – 3, |
|||
= 27 %; |
|
|
|
||
• H |
PO |
|
HPO |
, К = 6.2·10 – 8, |
|
2 |
4 |
|
|
4 |
2 |
= 0,15 %; |
|
|
|
||
• HPO |
|
PO |
3 , К = 5.0·10 –13, |
||
|
42 |
|
4 |
|
3 |
= 0,005 %. |
|
|
|
||
Константа равновесия:
СН СООН Н+ |
|
+ СН СОО |
||||||||
3 |
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
СН3ОО |
- |
|
|
Н |
+ |
|
|
|
|
|
|
× |
|
|
|||
К |
|
|
|
|
|
|
. |
|||
д |
|
СН3СООН |
|
|||||||
|
|
|
|
|
||||||
|
|
|
|
|
|
|||||
Закон разбавления Оствальда:
α |
К |
. |
|
||
|
СМ |
|
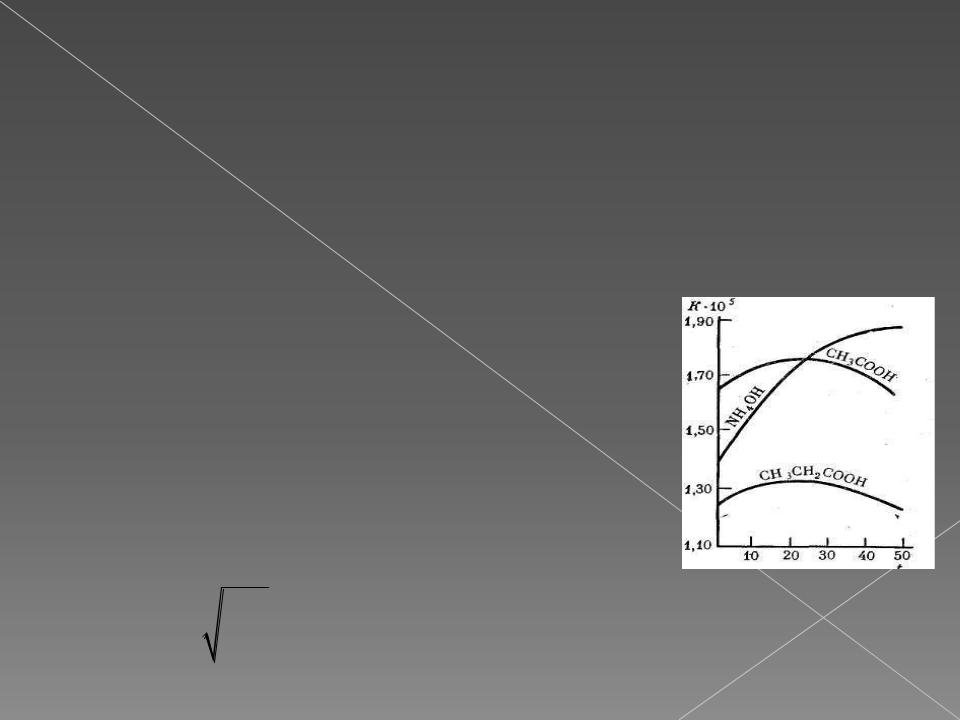
Зависимости Кд некоторых слабых электролитов в водных растворах от температуры

Индикаторы
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
|
|
|
рН < 7 |
|
|
|
|
|
|
рН > 7 |
|
|
||
Лакмус |
Красный Фиолетовый |
Синий |
|
Фенолфталеин Бесцветный Бесцветный Малиновый
Метилоранж |
Розовый |
Оранжевый |
Желтый |
|

Протолитическая теория кислот и оснований
– Протон Н+
Н+ Кислота  Основание
Основание
|
|
|
|
H О+ |
|
+ СI |
|
НСI |
(г.) |
+ H О |
(водн.) |
(водн.) |
|||
|
|
2 (ж.) |
3 |
|
|||
кисл.1 |
основ.2 |
|
кисл.2 |
||||
основ.2
NaOH(т.) + H2O(ж.) Na+(вод.) + OH (вод.)
OH (вод.) + H3O+(водн.) 2 H2O(ж)
Кислота – донор катионов водорода:
НСl H+ + Сl
NH4+ H+ + NH3 НCO3 H+ + CO32 .
Основание – акцептор катионов водорода:
NH3 + H+ NH4+ , АlОН2+ + H+ Аl3++ H2О, PO43 + H+ НPO42 .

Ионнообменные реакции
Необратимые реакции
Образуется осадок (↓)
Выделяются газообразные вещества
Образуется слабый электролит
Образуются комплексные соединения
BaCl2 + Na2SO4 = BaSO4 ↓ +
2NaCl
Na2S+ 2HCl = H2S↑ + 2NaCl
2CH3COOK + H2SO4 = 2CH3COOH +
K2SO4
Hg(NO3)2 + 4KJ = K2[HgJ4] +2KNO3

Правило Бертолле: Обменные реакции между электролитами практически необратимы и идут до конца в случае образования мало-растворимых, малодиссоциирующих, газообразных и комплексных соединений.
В уравнении реакции на ионы распадаются сильные растворимые электролиты (все сильные кислоты, сильные основания, кроме LiOH и все растворимые соли).
Слабые кислоты и слабые основания в независимости от их растворимости на ионы не распадаются и остаются в молекулярном виде (в таблице растворимости смотреть только соли).
NH4OH + HCI→NH4CI + H2O
NH4OH + H+→NH4+ + H2O
BaCI2 + K2SO4→BaSO4 + 2KCI
Ba2+ + SO42−→BaSO4
K2S + 2HCI→H2S + 2KCI
S2− + 2H+→H2S
HgI2 + 2KI→K2[HgI4]
HgI2 + 2I−→[HgI4]2−

Выпадение веществ в осадок и их растворение зависит от произведения растворимости (ПР) – это основная характеристика равновесий в гетерогенных системах «раствор-осадок».
Для малорастворимой соли Ag CI(к) Ag+(р) + CI−(р)
где [AgCI(к)] – концентрация молекул соли, моль/л; величина постоянная.
K[AgCI] = ПР = [Ag+] ∙ [CI−] = const
Произведение растворимости – произведение концентраций ионов в насыщенном растворе малорастворимого электролита.
При постоянной температуре ПР величина постоянная.
Са(OH)2→Са+2 + 2OH−;
ПР = [Са+2] ∙ [OH−]2
ПР = [Kt+n]m∙[An m]n

Условия образования и растворения осадков: [Kt+n]m[An m]n ПР – осадок выпадает;
[Kt+n]m[An m]n ПР – осадок растворяется (не выпадает); [Kt+n]m[An m]n = ПР система находится в равновесии. Обменные реакции между электролитами в растворах всегда идут в сторону образования менее диссоциированных или менее растворимых электролитов:
CaSO4 + 2NaF CaF2 + Na2SO4, ПРCaF2 = 4 10−11, ПРCaSO4 = 1,3 10 −4.
Поэтому реакция идет в сторону образования менее растворимого фторида кальция. Зная ПР можно определить растворимость данного элемента

Равновесие электролитической диссоциации воды:
Н2О Н+ + ОН−
K[H2O] = Kw
Kw = [H+]∙[OH−] = 10−14
Kw = 10−14
[H+]∙[OH−] = 10−7
Величина Kw – называется ионным произведением воды. Расчет концентраций ионов водорода и гидроксогруппы в водных растворах ведется по величине Kw:
где [H+] и [OH−] – равновесные молярные концентрации ионов, моль/л.
Внейтральном водном растворе [H+] = [OH−] = 10−7 моль/л.
Вкислом растворе [H+] [OH−], [H+] 10−7 моль/л.
Вщелочном растворе [OH−] [H+], [H+] 10−7 моль/л.
