
8_Geterogennoe_ionnoe_ravnovesie
.pdf
ЛЕКЦИЯ 8
ГЕТЕРОГЕННОЕ ИОННОЕ РАВНОВЕСИЕ. РЕАКЦИИ ОБМЕНА
ПЛАН ЛЕКЦИИ
Гетерогенное равновесие в насыщенном растворе малорастворимого сильного электролита. Произведение растворимости.
Влияние на растворимость электролита введения одноименных ионов.
Условие образования и растворения осадка.
Реакции обмена в растворах электролитов.
ГЕТЕРОГЕННОЕ РАВНОВЕСИЕ В НАСЫЩЕННОМ РАСТВОРЕ
МАЛОРАСТВОРИМОГО СИЛЬНОГО ЭЛЕКТРОЛИТА. ПРОИЗВЕДЕНИЕ
РАСТВОРИМОСТИ
В насыщенном водном растворе малорастворимого сильного электролита между осадком электролита и его ионами в растворе устанавливается гетерогенное равновесие. Для электролита KmAn равновесию соответствует уравнение
KmAn (к) |
mKn+ + nAm |
осадок |
ионы в растворе |
В условиях равновесия за единицу времени из осадка в раствор переходит столько же ионов, сколько их снова переходит из раствора в осадок, поэтому концентрация электролита в насыщенном растворе при постоянной температуре остается постоянной.
Константу данного равновесия называют произведением растворимости и обозначают символом ПР:
|
|
ПР = Kn+ m Am |
n, |
||||||||||||||
Исполнитель: |
|
Дата: |
|
|
|
|
|
|
|
|
|
|
Мероприятие № |
4 |
2 |
7 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

где Kn+ , Am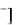 равновесные концентрации ионов, моль/л, m и n – стехиометрические коэффициенты.
равновесные концентрации ионов, моль/л, m и n – стехиометрические коэффициенты.
Таким образом, в насыщенном растворе сильного малорастворимого электролита произведение равновесных молярных концентраций катионов и анионов в степенях, равных стехиометрическим коэффициентам, при постоянной температуре есть величина постоянная. Величина ПР не зависит от концентрации ионов и для данного электролита изменяется только с
изменением температуры.
В справочных таблицах приведены значения ПР малорастворимых
электролитов при температуре 298 К (250С). |
|
|
||
Для фосфата бария |
|
|
|
|
Ba3(PO4)2(к) |
3Ba2+ + 2PO43 |
, ПР = |
Ba2+ 3 |
PO43 2 = 6,0 10 39; |
для сульфида серебра (I) |
|
|
|
|
Ag2S(к) |
2Ag+ + S2 , ПР = Ag+ 2 S2 |
= 7,2 10 50. |
||
Чем меньше |
величина ПР, |
тем |
в меньшей степени ионы |
|
малорастворимого вещества переходят в раствор, тем меньше растворимость вещества. Зная ПР, можно вычислить концентрацию ионов в насыщенном
растворе и концентрацию электролита растворимость вещества.
Пример. Рассчитайте концентрацию ионов и растворимость карбоната
кальция в насыщенном растворе при 250С. ПР CaCO |
4,4 10 9 . |
|
3 |
Решение. Обозначим символом S растворимость карбоната кальция,
моль/л. Из уравнения равновесия в насыщенном растворе соли СаСО3 (к)  Са2+ + СО32
Са2+ + СО32
следует, что молярная концентрация ионов и соответствующая концентрация соли в насыщенном растворе (S) равны:
[Ca2 ] [CO32 ] S.
Произведение растворимости карбоната кальция
Исполнитель: |
|
Дата: |
|
|
|
|
|
|
|
|
|
|
Мероприятие № |
4 |
2 |
7 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

ПР CaCO 3 [Ca 2 ][CO32 ] S2 .
Отсюда следует, что растворимость (моль/л)
|
|
|
|
|
4,4 10 9 6,6 10 5 моль / л. |
|
S |
|
ПРCaCO |
3 |
|
||
|
|
|
|
|
|
|
Концентрация ионов |
Сa2+ = СО32 |
= 6,6 10 5 моль/л. |
||||
Растворимость в г/л (обозначим символом S ) связана с растворимостью |
||||||
S (моль/л) соотношением |
|
|
|
|
||
|
|
|
|
|
S S MCaCO |
, |
|
|
|
|
|
|
3 |
где MCaCO 3 - молярная масса карбоната кальция, г/моль.
MCaCO |
100 г / моль , |
|
3 |
S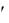 6,6 10 5 100 6,6 10 3 г / л.
6,6 10 5 100 6,6 10 3 г / л.
Растворимость S (моль/л) можно выразить через произведение растворимости.
Для малорастворимого электролита KmAn, растворимость которого S, KmAn (к)  mKn+ + nAm ,
mKn+ + nAm ,
концентрации ионов (моль/л)
Kn+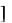 = mS; Am
= mS; Am = nS,
= nS,
произведение растворимости
ПР = Kn+ m Am n = (mS)m(nS)n = mmnnSm + n,
n = (mS)m(nS)n = mmnnSm + n,
растворимость
ПР
S m n mm n n .
Например, растворимость Сa3(PO4)2 (m = 3, n = 2)
|
|
|
|
|
|
|
|
|
|
29 |
|
S 3 2 |
ПР |
|
5 |
|
ПР |
|
5 |
2,0 10 |
7,1 10 7 моль / л , |
||
|
|
|
|
||||||||
3322 |
108 |
108 |
|
|
|||||||
растворимость Ag2S (m = 2, n = 1)
Исполнитель: |
|
Дата: |
|
|
|
|
|
|
|
|
|
|
Мероприятие № |
4 |
2 |
7 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

|
|
|
|
|
|
|
|
3 |
7,2 10 50 |
|
S 2 1 |
ПР |
|
3 |
|
ПР |
|
2,6 10 17 моль / л . |
|||
|
|
|
||||||||
22 |
4 |
4 |
|
|||||||
Для однотипных по составу веществ (с одинаковыми значениями m и n) по
величинам ПР можно |
сравнивать их растворимость. Так по значениям |
|||
ПРAg |
S 7,2 10 50 и |
ПРAg |
SO |
1,2 10 5 можно заключить, что сульфат |
2 |
|
2 |
|
4 |
серебра (I), растворим значительно лучше, чем сульфид серебра (I).
ВЛИЯНИЕ НА РАСТВОРИМОСТЬ ЭЛЕКТРОЛИТА ВВЕДЕНИЯ ОДНОИМЕННЫХ ИОНОВ
Если в равновесную систему KmAn (к)  mKn+ + nAm
mKn+ + nAm добавить сильный электролит KB, содержащий одноименные ионы Kn+,
добавить сильный электролит KB, содержащий одноименные ионы Kn+,
KB = Kn+ + Bn
или сильный электролит MA, содержащий одноименные ионы Am , MA = Mm+ + Am ,
т. е. повысить концентрацию ионов Kn+ или Am , то в соответствии с принципом Ле Шателье равновесие сместится в сторону образования осадка. Введение в раствор одноименных ионов приводит к уменьшению растворимости электролита.
Пример. Рассчитайте
а) растворимость карбоната кадмия;
б) растворимость карбоната кадмия в 0,1 М растворе карбоната натрия Na2CO3.
ПРCdCO |
5,2 10 12 . |
|
3 |
Решение. а) Равновесие в насыщенном растворе карбоната кадмия: СdСО3 (к)  Сd2+ + СО32 .
Сd2+ + СО32 .
Растворимость карбоната кадмия:
|
|
|
|
|
5,2 10 12 2,28 10 6 моль / л . |
|||||||||||||||
|
S |
ПРCdCO |
3 |
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Исполнитель: |
|
|
Дата: |
|
|
|
|
|
|
|
|
|
|
Мероприятие № |
4 |
2 |
7 |
1 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

б) Концентрация карбонат-ионов в насыщенном растворе карбоната кадмия
СО32 |
= S = 2,28 10 6 моль/л. |
В 0,1 М растворе карбоната |
натрия концентрация карбонат-ионов равна |
0,1моль/л (Na2CO3=2Na++CO32 ).
Равновесная концентрация карбонат-ионов в присутствии карбоната
натрия:
[CO2 |
] 2,28 10 6 |
0,1 0,1моль / л. |
3 |
|
|
Произведение растворимости не зависит от концентрации ионов,
ПР CdCO |
[Cd2 ] [CO32 ] , |
|
3 |
откуда концентрация ионов кадмия в присутствии карбоната натрия
[Cd |
2 |
] |
ПРCdCO 3 |
|
5,2 10 |
12 |
5,2 10 |
11 |
моль / л . |
|
[CO32 ] |
0,1 |
|
|
|||||
|
|
|
|
|
|
|
|||
Растворимость карбоната кадмия в 0,1 М растворе карбоната натрия,
S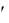 [Cd2 ]
[Cd2 ] 5,2 10 11моль/ л .
5,2 10 11моль/ л .
Понижение растворимости веществ при добавлении одноименных ионов происходит только при условии, что вещества не вступают в химическое взаимодействие, например, не происходит образования комплексных соединений.
УСЛОВИЕ ВЫПАДЕНИЯ И РАСТВОРЕНИЯ ОСАДКА
Используя значение произведения растворимости, можно определить возможность образования или растворения осадка в растворе заданного состава.
Осадок образуется из пересыщенного раствора. Обозначим символом ПК произведение молярных концентраций ионов малорастворимого сильного электролита в заданном растворе. Если значение ПК>ПР, раствор
Исполнитель: |
|
Дата: |
|
|
|
|
|
|
|
|
|
|
Мероприятие № |
4 |
2 |
7 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

пересыщенный, в нем образуется осадок. Если ПК<ПР, раствор ненасыщенный,
осадок не образуется. Когда система уже содержит осадок, и создают условия,
при которых ПК<ПР, например, разбавляют раствор, осадок частично или полностью растворяется.
Пример. Определите, образуется ли осадок BaSO4 при сливании равных объемов 0,001 М растворов Ba(NO3)2 и Na2SO4. ПР BaSO 4 1,1 10 10.
Решение. Из уравнений диссоциации солей
Ba(NO3)2 = Ba2+ + 2NO3 ,
Na2SO4 = 2Na+ + SO42
следует, что концентрации ионов в исходных растворах:
CBa 2 CBa (NO3 )2 |
0,001моль / л; CSO 2 |
CNa 2SO 4 0,001моль / л. |
|
4 |
|
После сливания равных объемов исходных растворов суммарный объем увеличивается в два раза, а молярные концентрации ионов соответственно уменьшаются в два раза:
CBa 2 |
0,001 |
0,0005моль / л; CSO 42 |
0,001 |
0,0005 моль / л. |
|||||||
|
|
|
|
|
|||||||
2 |
|
2 |
|
||||||||
|
|
|
|
|
|
|
|
|
|||
Произведение концентраций ионов в растворе: |
|
||||||||||
|
ПК C |
|
2 |
C |
2 |
0,0005 0,0005 |
|
2,5 10 7 , |
|||
|
|
|
|
Ba |
|
|
SO 4 |
|
|
|
|
В полученном растворе ПК |
ПРBaSO |
(2,5 10-7 1,1 10-10), т.е. осадок сульфата |
|||||||||
|
|
|
|
|
|
|
|
4 |
|
|
|
бария образуется.
РЕАКЦИИ ОБМЕНА В РАСТВОРАХ ЭЛЕКТРОЛИТОВ
Реакции в растворах электролитов, в ходе которых не изменяются степени окисления элементов, называют обменными или реакциями обмена.
Обменные реакции протекают практически необратимо, если в результате образуются малорастворимые, газообразные вещества или слабые электролиты.
Исполнитель: |
|
Дата: |
|
|
|
|
|
|
|
|
|
|
Мероприятие № |
4 |
2 |
7 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

Сущность происходящих в растворе процессов выражают ионными уравнениями. В ионных уравнениях, в отличие от молекулярных, учитывают растворимость и относительную степень диссоциации электролитов.
При составлении ионных уравнений в виде ионов записывают только
растворимые сильные электролиты. Все остальные вещества (неэлектролиты,
слабые или малорастворимые электролиты) записывают в молекулярной форме. Из уравнения исключают ионы, которые повторяются без изменения в левой и правой частях уравнения.
Примеры необратимых обменных реакций
 Образование малорастворимого вещества (осадка)
Образование малорастворимого вещества (осадка)
При взаимодействии нитрата свинца (II) и иодида калия образуется осадок малорастворимого иодида свинца (II):
Pb(NO3)2 + 2KI = PbI2 + 2KNO3.
Pb(NO3)2, KI и KNO3 - растворимые сильные электролиты – в ионном уравнении записывают в виде ионов;
PbI2 – электролит сильный, но малорастворимый - записывают в молекулярной форме:
Pb2+ + 2NO3 + 2K+ + 2I
+ 2K+ + 2I = PbI2 + 2K+ + 2NO3 ;
= PbI2 + 2K+ + 2NO3 ;
ионное уравнение:
Pb2+ + 2I = PbI2.
= PbI2.
 Образование газообразного вещества
Образование газообразного вещества
При взаимодействии сульфида натрия и соляной кислоты выделяется газообразный сероводород:
Na2S + 2HCl = H2S + 2NaCl
S2 + 2H+ = H2S
+ 2H+ = H2S
Исполнитель: |
|
Дата: |
|
|
|
|
|
|
|
|
|
|
Мероприятие № |
4 |
2 |
7 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

 Образование слабых электролитов
Образование слабых электролитов
При взаимодействии ацетата натрия и соляной кислоты образуется слабый электролит уксусная кислота:
CH3COONa + HCl = CH3COOH + NaCl
CH3COO + H+ = CH3COOH
+ H+ = CH3COOH
При взаимодействии оснований и кислот образуется слабый электролит 
вода:
CH3COOH + NaOH = CH3COONa + H2O
CH3COOH + OH = CH3COO + H2O
 Образование соединения, которое распадается на газообразное вещество и слабый электролит
Образование соединения, которое распадается на газообразное вещество и слабый электролит
При взаимодействии карбоната натрия и азотной кислоты образуется угольная кислота, которая разлагается на газообразный оксид углерода (IV) и
воду:
Na2CO3 + 2HNO3 = 2NaNO3 + CO2 + H2O
CO32 + 2H+ = CO2 + H2O
+ 2H+ = CO2 + H2O
 Образование комплексного соединения
Образование комплексного соединения
Гидроксид цинка растворяется в избытке гидроксида натрия с образованием слабодиссоциирующего тетрагидроксоцинкат иона:
Zn(OH)2 + 2NaOH = Na2 Zn(OH)4
Zn(OH)2 + 2OH = Zn(OH)4 2
= Zn(OH)4 2
Реакции, в которых исходные вещества и продукты реакции содержат малорастворимые соединения
Реакции такого типа должны быть обратимыми, например, реакция между кристаллическим хлоридом серебра и иодидом калия в растворе
AgCl(к) + KI  AgI(к) + KCl
AgI(к) + KCl
Исполнитель: |
|
Дата: |
|
|
|
|
|
|
|
|
|
|
Мероприятие № |
4 |
2 |
7 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

Направление реакции можно определить по величине константы равновесия. Согласно ионному уравнению реакции
AgCl(к) + I
 AgI(к) + Cl
AgI(к) + Cl
константа равновесия:
KC |
[Cl ] |
. |
|
||
|
[I ] |
|
Умножаем числитель и знаменатель на один и тот же множитель – концентрацию ионов Ag+ :
KC |
[Ag |
][Cl |
] |
ПРAgCl |
. |
|
[Ag |
][I |
] |
|
ПРAgI |
||
|
|
|
||||
Подставив табличные значения ПРAgCl |
1,8 10 10 и ПРAgI 2,3 10 16 , |
|||||
получаем КС 7,8 105 . |
|
|
|
|
|
|
Значение константы равновесия Кс |
1, данная реакция практически |
|||||
необратимо протекает в прямом направлении:
AgCl(к) + KI = AgI(к) + KCl.
Рассчитав константу равновесия реакции обмена по величинам произведений растворимости и констант диссоциации исходных веществ и
продуктов реакции, можно определить направление реакции. |
|
|
|
|
|
|||||||||||||||
Пример. Определите направление реакций: |
|
|
|
|
|
|
||||||||||||||
|
|
|
MnS + 2HCl |
H2S + MnCl2, |
|
(1) |
||||||||||||||
|
|
|
CuS + 2HCl |
H2S + CuCl2. |
|
(2) |
||||||||||||||
ПРMnS = 1,1 10 |
13; ПРCuS = 6,3 10 36; KH 2S |
1,0 10 7 и KH 2S |
1,2 10 13 |
|
|
|
|
|
||||||||||||
|
|
1 |
|
2 |
|
|
|
|
|
|
||||||||||
Решение. Ионное уравнение и выражение константы равновесия |
||||||||||||||||||||
реакции (1): |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
MnS + 2H+ |
H2S + Mn2+ |
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Исполнитель: |
|
|
Дата: |
|
|
|
|
|
|
|
|
|
|
Мероприятие № |
4 |
2 |
7 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

KС |
[H2S][Mn2 ] |
. |
||
[H |
]2 |
|
||
|
|
|
||
После умножения числителя и знаменателя на [S2 ] и перегруппировки сомножителей:
|
[H S][Mn2 |
][S2 |
] |
|
[H S] |
|
[Mn2 ][S2 ]. |
|
KС |
2 |
|
|
|
|
2 |
|
|
[H ]2[S2 ] |
|
|
[H ]2[S2 |
|
||||
|
|
|
] |
|||||
Первый сомножитель – величина, обратная суммарной константе диссоциации сероводородной кислоты, равной произведению констант диссоциации по первой и второй ступеням:
KH2S |
KH2S |
KH2S |
[HS |
][H |
] [H ][S2 |
] [H ]2[S2 ] . |
||||||||||||||
|
1 |
|
2 |
|
|
|
[H2S] |
|
|
|
|
[HS ] |
|
|
[H2S] |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Второй сомножитель |
- |
произведение |
растворимости сульфида |
|||||||||||||||||
марганца (II): [Mn 2 ][S2 |
] ПРMnS . |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Таким образом, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
KС |
|
|
ПР MnS |
|
|
, |
|
|
|
|
|||||
|
|
|
|
|
|
K H 2SK H |
2S |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
1 |
|
|
2 |
|
|
|
|
|
|
|
|
после подстановки справочных данных: |
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
KС |
|
|
1,1 10 |
13 |
|
|
|
|
|
9,2 106 . |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
1,0 |
10 |
7 |
1,2 |
10 |
13 |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||
Значение KС |
1, равновесие сильно смещено в сторону прямой реакции, |
|||||||||||||||||||
реакция (1) практически необратима: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
MnS + 2HCl = H2S + MnCl2.
Выражение константы равновесия реакции (2) аналогично выведенному для реакции (1):
Исполнитель: |
|
Дата: |
|
|
|
|
|
|
|
|
|
|
Мероприятие № |
4 |
2 |
7 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
