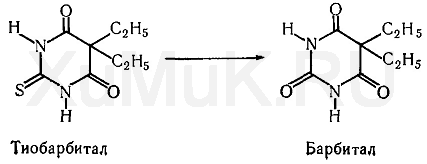- •Оглавление
- •Введение
- •Метаболические превращения загрязняющих веществ в окружающей среде
- •Метаболизм Клеточный метаболизм.
- •Потребность в энергии.
- •Источники энергии.
- •Методы исследования метаболизма.
- •Использование клеток.
- •Использование радиоактивных изотопов.
- •Выделение ферментов.
- •Метаболизм углеводов и липоидов Синтез атф.
- •Аэробный метаболизм (с использованием кислорода).
- •Липиды как источник энергии.
- •Запасание энергии.
- •Синтез липидов из углеводов.
- •Метаболизм липидов.
- •Метаболизм белков
- •Синтез других азотсодержащих соединений.
- •Общие представления о метаболизме органических веществ
- •Метаболизм чужеродных соединений
- •Окисления чужеродных веществ
- •Восстановление чужеродных веществ
- •Гидролиз чужеродных веществ
- •Дезалкилирование, дезаминирование и десульфирование чужеродных соединений
- •Другие метаболические превращения
- •Загрязняющие вещества.
- •Загрязняющие вещества в разных средах
- •Некоторые примеры загрязняющих веществ
- •Заключение
- •Список литературы
Восстановление чужеродных веществ
Кроме окислительных ферментных систем в печени, почках, крови содержатся ферментные системы, способствующие восстановлению чужеродных соединений в организме. Эти ферментные системы катализируют восстановление ароматических нитросоединений в амины.
С помощью ферментов (редуктаз) происходит восстановление нитробензола в анилин, n -нитрозобензойной кислоты в n -аминобензойную кислоту и т. д.
Восстановление нитросоединений в амины происходит через образование ряда промежуточных продуктов. Это можно показать на примере восстановления м -динитробензола:
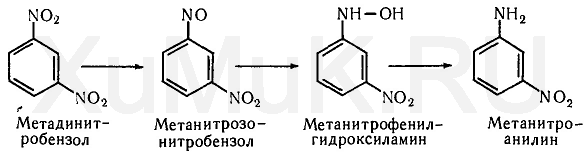
Под влиянием соответствующих ферментов в организме происходит восстановление дисульфидов, сульфоксидов, N-оксидов, гидроксамовых кислот и ряда других чужеродных соединений.
Гидролиз чужеродных веществ
В организме ряд чужеродных соединений, к числу которых относятся сложные эфиры, амиды, гидроксамовые кислоты, карбаматы, нитрилы и другие вещества, под влиянием ферментных систем подвергается гидролизу.
С помощью ряда гидролитических ферментов, находящихся в печени и плазме крови, гидролизуются сложные эфиры и амиды. Под влиянием эстеразы сложные эфиры разлагаются на соответствующие кислоты и спирты:
R—COOR' + Н 2 О ---> RСООН + R'ОН.
В организме людей и животных гидролитические ферменты в различных тканях и биологических жидкостях могут действовать неодинаково. Свидетельством этому является то, что в плазме кроликов атропин и кокаин быстро подвергаются гидролизу, а в плазме крови человека они не гидролизуются (Д. Парк, 1973).
Амиды в организме под влиянием ферментов (амидаз) подвергаются гидролизу. Однако гидролитическое расщепление амидов происходит медленнее, чем расщепление эфиров с помощью эстераз.
Дезалкилирование, дезаминирование и десульфирование чужеродных соединений
Ряд чужеродных соединений в организме под влиянием соответствующих ферментных систем подвергается дезаминированию, дезалкилированию и десульфированию.
Дезалкилирование (деалкилирование). При дезалкилирова-нии происходит отщепление алкильных групп, находящихся в молекулах чужеродных соединений. Наиболее часто дезалкилированию подвергаются соединения, содержащие алкильные группы при атомах кислорода, азота и серы. В зависимости от этого процессы отщепления алкильных групп подразделяются на О-, N- и S-дезалкилирование. При дезалкилировании указанных соединений образуются соответствующие фенолы, амины и тиолы (тиофенолы, тиоспирты).
О-Дезалкилирование. Процесс О-дезалкилирования можно показать на примере фенацетина. При О-дезалкилировании фенацетина образуется парацетамидофенол (парацетамол) и аце-тальдегид:
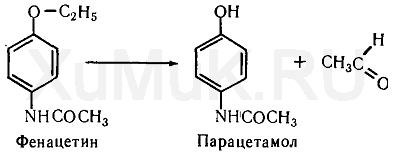
Путем О-дезалкилирования в организме происходит превращение кодеина в морфин.
N-дезалкилирование. Чужеродные соединения, являющиеся вторичными и третичными аминами, в организме подвергаются N-дезалкилированию. В результате этого образуются соответствующие амины и альдегиды. Так, диметиланилин метаболизируется с образованием метиланилина, превращающегося в анилин и формальдегид:
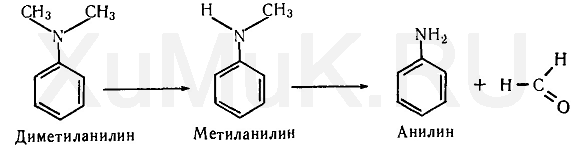
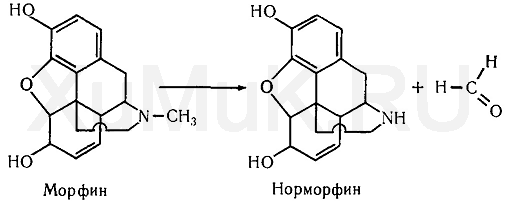
В организме N-дезалкилированию подвергаются морфин и его производные. При N-дезалкилировании морфина образуются норморфин и формальдегид:
S-дезалкилирование. Под влиянием соответствующих ферментов тиоэфиры подвергаются S-дезалкилированию с образованием тиоспиртов и альдегидов:
RSCH 3 ---> RSH + HCHO.
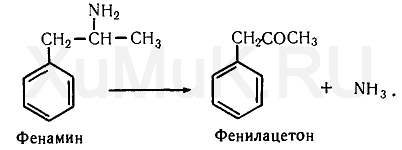
Дезаминирование. Ряд чужеродных соединений, содержащих первичные аминогруппы, под влиянием ферментов подвергается дезаминированию. В результате этого от молекулы вещества отщепляется аминогруппа в виде аммиака. Одним из препаратов, подвергающихся дезаминированию, является фенамин, который под влиянием ферментов печени превращается в фенилацетон и аммиак:
Многие другие чужеродные соединения, содержащие первичную аминогруппу, также подвергаются дезаминированию в организме.
Десульфирование. Некоторые чужеродные соединения, содержащие атомы серы (инсектициды, тиобарбитураты, производные фенилтиомочевины и др.), под влиянием ферментов превращаются в соответствующие кислородные аналоги. В таких соединениях атомы серы замещаются атомами кислорода. Процесс десульфирования чужеродных соединений в организме можно показать на примере тиобарбитала: