
- •Частная патология
- •Полицитемическая нормоволемия
- •Полицитемическая гиповолемия
- •Кровопотеря
- •Условия, влияющие на течение и исходы кровопотери
- •Патогенез
- •Адаптивные механизмы
- •Стадии компенсации кровопотери
- •Виды кровопотери
- •Проявления
- •Вторичные относительные эритроцитозы
- •Хронические постгеморрагические анемии
- •Этиология
- •Патогенез гемолитических анемий
- •Анемия вследствие нарушения синтеза глобиновых днк
- •Анемии, развивающиеся при нарушениях обмена железа
- •Анемии, развивающиеся вследствие нарушения синтеза глобинов
- •Типовые изменения количества лейкоцитов в единице объёма крови
- •Механизмы развития лейкопений
- •Проявления лейкопений
- •Механизмы развития лейкоцитозов
- •Проявления лейкоцитозов
- •Изменения лейкоцитарной формулы при лейкоцитозах
- •Ядерные сдвиги лейкоцитарной формулы
- •Виды и значение лейкоцитозов
- •Типовые изменения лейкоцитарной формулы
- •Относительные и абсолютные изменения в лейкоцитарной формуле
- •При характеристике изменений состава лейкоцитов необходимо оценивать как относительное, так и (обязательно!) абсолютное их содержание.
- •Относительные тромбоцитозы
- •Проявления тромбоцитопений
- •Патогенез тромбоцитопатий
- •Проявления тромбоцитопатий
- •Последствия гиперкоагуляции и тромбоза
- •Виды геморрагических заболеваний
- •Типы кровоточивости
- •Диссеминированное внутрисосудистое свёртывание
- •Причины
- •Патогенез
- •Стадия гиперкоагуляции
- •Проявления
- •Патогенез
- •Атипизм обмена
- •Острый лимфоидный лейкоз
- •Проявления
- •Пункция костного мозга
- •Лечение острых лейкозов
- •Общие принципы сопутствующего лечения
- •Методы заместительной терапии
- •Патогенез
- •Проявления:
- •Лейкемоидные реакции
- •Выраженность признаков
- •Факторы риска
- •Необратимые нарушения коронарного кровотока
- •Увеличение потребления миокардом кислорода
- •Расстройство энергообеспечения кардиомиоцитов
- •Повреждение мембран и ферментов кардиомиоцитов
- •Дисбаланс ионов и жидкости
- •В связи с существенными отклонениями трансмембранного электрогенеза развиваются аритмии сердца.
- •Расстройства механизмов регуляции сердечной деятельности
- •Эффекты постокклюзионной реперфузии миокарда
- •Реперфузия
- •Реперфузионное повреждение миокарда
- •Изменение основных показателей функции сердца при коронарной недостаточности
- •Виды номотопных и гетеротопных аритмий
- •Патогенез и проявления номотопных аритмий
- •Патогенез и проявления эктопических аритмий
- •Причины
- •Механизмы возникновения
- •Виды комбинированных аритмий
- •Экстрасистолия
- •Электрофизиологические механизмы
- •Сердечная недостаточность
- •Перегрузка сердца
- •По преимущественно поражённому отделу сердца
- •По преимущественной недостаточности фазы сердечного цикла
- •Общие механизмы развития сердечной недостаточности
- •Механизмы экстренной компенсации сократительной функции
- •Клеточно-молекулярные механизмы сердечной недостаточности
- •Проявления сердечной недостаточности
- •Классификация
- •Проявления
- •Лечение
- •Оценка индивидуального риска
- •Группы риска
- •Органы-мишени и группы риска
- •Виды артериальной гипертензии
- •Этиология и патогенез артериальных гипертензий
- •Факторы риска
- •Общие артериальные гипертензии
- •Гипертоническая болезнь
- •Принципы лечения артериальных гипертензий
- •Немедикаментозное лечение
- •Лекарственная терапия
- •Эндокринные артериальные гипотензии
- •Метаболические артериальные гипотензии
- •Механизмы возникновения
- •Виды артериальных гиперемий
- •Проявления артериальных гиперемий
- •Последствия артериальных гиперемий
- •Патогенные эффекты венозной гиперемии
- •Механизмы возникновения ишемии
- •Виды стаза
- •Причины расстройств микроциркуляции
- •Трансмуральные нарушения микроциркуляции
- •Экстраваскулярные нарушения микроциркуляции
- •Оценка функции внешнего дыхания
- •Спирометрия
- •Данные спирометрии
- •Другие лёгочные объёмы
- •Другие исследования функции лёгких
- •Спирометрические признаки дыхательной недостаточности
- •Газы артериальной крови
- •Вентиляционно-перфузионные нарушения
- •Альвеолярная гипервентиляция
- •Нарушения диффузии кислорода и углекислого газа
- •Причины снижения диффузионной способности
- •Причины
- •Формы дыхательной недостаточности
- •Vip стимулирует моторику и секрецию в желудке, перистальтику и секрецию в кишечнике. Мощный вазодилататор. Выделяется в ответ на стимуляцию блуждающего нерва.
- •Факторы риска
- •Дисфункции пищевода
- •Нарушения моторики желудка
- •Расстройства всасывательной функции кишечника
- •Нарушение моторной функции кишечника
- •Болезнь язвенная желудка
- •Патогенез язвенной болезни
- •Проявления язвенной болезни желудка
- •Проявления язвенной болезни двенадцатиперстной кишки
- •Патогенез
- •Проявления
- •Синдром раздражённой кишки
- •Неспецифический язвенный колит
- •Функции печени
- •Обмен веществ
- •Проявления
- •Патогенез печёночных ком
- •Виды желтух
- •Печёночные желтухи
- •Энзимопатические желтухи
- •Внепечёночные желтухи
- •Общие механизмы возникновения и развития почечной патологии
- •Нарушение клубочковой фильтрации
- •Нарушения канальцевой реабсорбции
- •Виды почечной патологии по происхождению
- •Хронический диффузный гломерулонефрит
- •Механизм развития
- •Патогенез
- •Хроническая почечная недостаточность
- •Нефролитиаз
- •Показатели изменения объёма и состава крови
- •Овариально-менструальный цикл
- •Общая этиология и общий патогенез эндокринных расстройств
- •Нарушения функций гипоталамо-гипофизарной системы
- •Типовые формы патологии аденогипофиза
- •Гиперпитуитаризм
- •Синдром неадекватной секреции адг
- •Нарушения функций надпочечников
- •Вторичный гиперальдостеронизм
- •Гиперкортизолизм
- •Адреногенитальный синдром
- •Проявления
- •Надпочечниковый криз
- •Тиреотоксический криз
- •Гипотиреозы
- •Вторичный и постжелезистый гипотиреоз
- •Микседема
- •Гипотиреоидная кома
- •Основной регулятор реабсорбции фосфата в почках — птг.
- •Внутренний баланс фосфата
- •Половая дифференцировка
- •Преждевременное половое созревание
- •Задержка полового созревания
- •Гипофункция яичников
- •Гиперфункция яичников
- •Эндокриногенные нарушения полового развития и половой функции у лиц генетически мужского пола
- •Преждевременное половое развитие
- •Задержка полового созревания
- •Мужской гипогонадизм
- •Нарушение функций шишковидной железы
- •Нарушения эндокринной функции тимуса
- •Факторы риска
- •Специфические механизмы повреждения нейронов.
- •Механизмы расстройств интегративной деятельности нервной системы
- •Типовые формы нарушений деятельности нервной системы
- •Патологическое ослабление нервных влияний
- •Патологическое усиление нервных влияний
- •Фазовые состояния
- •Характеристика типовых форм расстройств движения
- •Типовые формы расстройств чувствительности
- •Общие механизмы расстройств чувствительности
- •Механизмы формирования боли
- •Антиноцицептивная система
- •Нейрогенные расстройства трофики
- •Вероятные механизмы нейротрофического контроля
- •Нейродистрофический процесс
- •Нарушения внд
- •Экспериментальные неврозы
- •Этиология неврозов
- •Классификация неврозов
- •Общие проявления невротических состояний
- •Понятие о «вегетоневрозе»
Синдром неадекватной секреции адг
Синдром неадекватной секреции АДГ (СНАДГ) развивается вследствие избыточности эффектов АДГ и характеризуется олигурией и отёками. Характеристика синдрома приведена в статье «Синдром неадекватной секреции АДГ» (приложение «Справочник терминов»).
Патогенез. Ведущую роль в развитии СНАДГ играют два взаимосвязанных инициальных звена: центрогенное и первично-железистое.
• Центрогенное. Характеризуется нейрогенной корковоподкорковой стимуляцией образования АДГ в гипоталамусе и его транспорта в нейрогипофиз.
• Первичножелезистое. В данном случае речь идет о двух вариантах патогенеза: избыточной продукции и нейросекреции АДГ нейронами гипоталамуса и эктопической секреции АДГ (например, мелкоклеточными карциномами лёгких).
Проявления СНАДГ и их механизмы представлены на рис. 27–13.
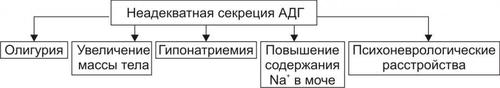
Рис. 27–13. Основные проявления синдрома неадекватной секреции АДГ.
• Олигурия. Механизм: значительная активация реабсорбции жидкости в дистальных отделах почечных канальцев под влиянием АДГ. АДГ взаимодействует с V2–рецепторами эпителия дистальных отделов канальцев и собирательных трубочек почек. Это обусловливает образование цАМФ, встраивание водных каналов в цитолемму и торможение экскреции жидкости, что приводит к увеличению реабсорбции воды и снижению диуреза.
• Нарастание массы тела. Механизм: задержка жидкости в организме (гипергидратация). Вода накапливается в тканях и сосудистом русле, что и увеличивает массу тела. Важно, что отёки при этом не развиваются в связи с уменьшением [Na+] в интерстиции.
• Гипонатриемия. Считается кардинальным признаком синдрома. [Na+] снижается до 130–135 мэкв/л, а осмоляльность плазмы до 270 носмоль/кг.
• Повышение содержания натрия в моче (обычно более 20 мэкв/л). Механизм: гипергидратация организма, стимулирующая экскрецию Na+ почками.
• Психоневрологические расстройства. Характеризуются апатией, вялостью, нарушением сознания, нередко судорогами. Механизм: набухание нейронов мозга, что характерно для состояния так называемого «водного отравления».
Нарушения функций надпочечников
Надпочечники — парные эндокринные железы — состоят из коркового вещества (мезодермального происхождения) и мозгового (нейроэктодермального генеза). Фактически это две железы: кора (на долю коры приходится около 80% массы железы) и мозговая часть. Кора надпочечников синтезирует кортикостероиды, хромаффинные клетки мозговой части — катехоловые амины. Каждый надпочечник в норме имеет массу около 4 г как у мужчин, так и у женщин. При остром стрессе или гиполипидемии масса надпочечников может существенно уменьшаться. Напротив, при длительном стрессе или некоторых хронических заболеваниях наблюдается гипертрофия и гиперплазия надпочечников с увеличением массы в 1,5–2 раза.
КОРТИКОСТЕРОИДЫ
В коре надпочечника синтезируются минералокортикоиды, глюкокортикоиды и дегидроэпиандростерон (рис. 27–14).
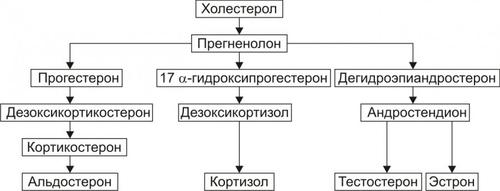
Рис. 27–14. Биосинтез стероидных гормонов в коре надпочечников.
• Минералокортикоиды. Альдостерон — основной минералокортикоид.
• Глюкокортикоиды. Основной глюкокортикоид, — кортизол (на его долю приходится 80% всех глюкокортикоидов) Остальные 20% — кортизон, кортикостерон, 11дезоксикортизол и 11дезоксикортикостерон.
• Дегидроэпиандростерон. Дальнейшие превращения этого предшественника андрогенов происходят вне надпочечника.
КАТЕХОЛОВЫЕ АМИНЫ
Катехоламины (преимущественно адреналин) синтезируют хромаффинные клетки.
• Хромаффинные клетки — основной клеточный элемент мозговой части надпочечников и параганглиев, расположенных по ходу крупных артериальных стволов (например, каротидное тело). Мелкие скопления и одиночные хромаффинные клетки находят также в сердце, почках, симпатических ганглиях.
• Адреналин и норадреналин выбрасываются в кровь из хромаффинных клеток при активации симпатической нервной системы.
• Катехоламины
имеют широкий спектр эффектов (воздействие
на гликогенолиз, липолиз, глюконеогенез,
влияние на сердечно-сосудистую систему).
Вазоконстрикция, параметры сокращения
сердечной мышцы и другие эффекты
катехоловых аминов реализуются через
α-
и βадренергические
рецепторы на поверхности клеток–мишеней
(ГМК, секреторные клетки, кардиомиоциты).
Недостаточность катехоламинов мозговой
части надпочечников крайне редко
приводит к развитию серьёзной патологии,
но чрезмерная продукция адреналина
(например,
при
феохромоцитоме) гарантирует развитие
артериальной гипертензии.
ТИПОВЫЕ ФОРМЫ ПАТОЛОГИИ НАДПОЧЕЧНИКОВ
Типовые формы патологии надпочечников подразделяются на две большие группы: гиперфункциональные и гипофункциональные состояния (рис. 27–15).
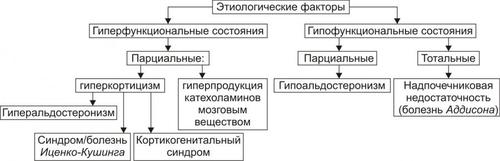
Рис. 27–15. Типовые формы патологии надпочечников.
ГИПЕРФУНКЦИОНАЛЬНЫЕ СОСТОЯНИЯ
• Кора надпочечников. К гиперфункциональным состояниям коры надпочечников относятся синдромы гиперальдостеронизма, гиперкортизолизма и адреногенитальный синдром.
• Мозговая часть надпочечников. Гиперкатехоламинемия, как правило, наблюдается при опухоли из хромаффинных клеток — феохромоцитоме.
ГИПОФУНКЦИОНАЛЬНЫЕ СОСТОЯНИЯ
К гипофункциональным состояниям относится недостаточность коры надпочечников (например, болезнь Аддисона и гипоальдостеронизм).
ГИПЕРАЛЬДОСТЕРОНИЗМ
Гиперальдостеронизм — общее название синдромов, возникающих вследствие гиперсекреции или нарушений обмена альдостерона и характеризующихся наличием отёков, асцита, гипокалиемии и реноваскулярной артериальной гипертензии.
Синдром гиперальдостеронизма может быть первичным или вторичным. В некоторых случаях развивается псевдогиперальдостеронизм.
ПЕРВИЧНЫЙ ГИПЕРАЛЬДОСТЕРОНИЗМ
• Причины: альдостеронпродуцирующая аденома клубочковой зоны коры одного из надпочечников, первичная гиперплазия клубочковой зоны коры надпочечников. При этих состояниях развивается синдром Конна (около 80% всех случаев первичного гиперальдостеронизма). Синдром Конна — расстройство, вызывающее чрезмерную секрецию альдостерона и характеризующееся головными болями, полиурией, слабостью, артериальной гипертензией, гипокалиемическим алкалозом, гиперволемией и пониженной активностью ренина.
• Проявления и механизмы гиперальдостеронизма (рис. 27–16).
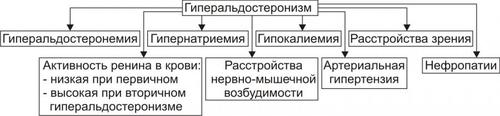
Рис. 27–16. Основные проявления гиперальдостеронизма.
† Высокий уровень альдостерона в крови в связи с его гиперпродукцией в клубочковой зоне коры надпочечников.
† Снижение содержания (активности) ренина и ангиотензина II в плазме крови. Является результатом подавления активности ренинангиотензиновой системы в условиях гиперальдостеронизма и гиперволемии, потенцирующей торможение синтеза и секреции ренина.
† Гипернатриемия и гипокалиемия вследствие активации реабсорбции Na+ и стимуляции экскреции K+ в канальцах почек в результате непосредственного влияния на них избытка альдостерона.
† Артериальная
гипертензия. Развивается вследствие
увеличение [Na+]
в плазме крови (гиперосмия), что
обусловливает цепь следующих явлений:
активация осморецепторов и стимуляция
секреции АДГ в задней доле гипофиза →
повышение реабсорбции жидкости в
дистальных отделах канальцев почек,
пропорциональное гиперосмии →
увеличение ОЦК в суженном сосудистом
русле →
повышение сердечного выброса и
увеличение АД.
† Снижение остроты зрения (иногда слепота). Механизм: нарушение кровоснабжения сетчатки глаза в связи с изменениями в её микрососудах (утолщение стенки, микроаневризмы, повышенная извитость) и расстройствами микрогемоциркуляции (замедление тока крови, ишемия, стаз).
† Нарушения функции почек: гипостенурия (из-за низкого содержания Na+ в моче), олигурия на начальном этапе болезни (в связи с повышенной реабсорбцией Na+), полиурия и никтурия на последующих этапах заболевания, протеинурия. Указанные изменения являются результатом дистрофии эпителия почечных канальцев и гипосенситизации рецепторов эпителия канальцев почек к АДГ вследствие снижением уровня K+ в клетках.
† Расстройства нервномышечной возбудимости: парестезии, мышечная слабость и гипотония, судороги, вялые (нейрогенные) параличи. Механизмы: гипернатриемия, увеличение уровня Na+ в миоцитах и нервных клетках, гипокалиемия, дефицит K+ в клетках, алкалоз. Указанные отклонения приводят к нарушениям электрогенеза и дистрофическим изменениям.
