
ап(бв-б) / 2.Бальмера
.docxЗубарев Я.Ю.
3 курс 4 группа
Лабораторная работа
«Экспериментальная проверка Боровской модели атома водорода»
Краткая теория
В
1913 г. Нильс Бор разработал первую
квантовую теорию атома. Он предположил
(следуя Резерфорду), что атом представляет
собой положительно заряженное ядро,
вокруг которого движутся электроны, но
при этом существуют некоторые стационарные
орбиты, при движении по которым вопреки
законам классической электродинамики
электрон не излучает. Излучение света
происходит только отдельными квантами
при переходе с одной стационарной орбиты
на другую, при этом выполняется закон
сохранения энергии
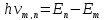 .
.
Рассмотрим простейший атом – атом водорода. Ядро атома состоит из одного протона, заряд которого по величине равен заряду электрона e. Сила взаимодействия между ними выражается законом Кулона.
Формула для линий спектра атомов водорода такова:

Линии спектра атома водорода можно разбить на несколько серий, каждая из которых характеризуется номером квантового состояния m, в которое происходит квантовый переход. Если квантовой число m – 2, то линии соответствуют серии Бальмера. Первые четыре линии попадают в видимую, а остальные в ультрафиолетовую область.
Теория Бальмера для атома водорода хорошо согласуется с экспериментом, однако создать подобную теорию для других атомов не удалось. Это полуклассическая теория в 1920-х гг. сыграла большую роль в создании квантовой механики – основы современной физики.
Обработка полученных данных
Таблица 1. Градуировочные данные
|
Цвет |
Длина волны, Å |
Деления барабана |
|
Красный |
6234,37 |
2767 |
|
Зел-гол |
4916,04 |
1791 |
|
Синий |
4358,35 |
1330 |
|
Фиолетовый |
4077,81 |
940 |
Рисунок 1. Градуировочный график

Таблица 2. Расчетные данные
|
Цвет |
Деления барабана |
Интенсивность отн. единицы |
Длина волны, Å |
Пост. Ридберга, см-1 |
Энергия, эВ |
|
Красная |
2767 |
3000 |
6234.37 |
115488,81 |
1,98 |
|
Зел-гол. |
1791 |
500 |
4916.04 |
108488,40 |
2,52 |
|
Фиолет. |
940 |
200 |
4077,81 |
116776,03 |
3,04 |
|
Фиолет |
910 |
100 |
4046,55 |
111205,84 |
3,06 |
