- •Введение
- •Выбор топлива
- •Пересчеты составов топлива
- •Теплота сгорания топлива
- •Расход воздуха на горение
- •Объем продуктов горения топлива
- •Температура горения
- •Материальный баланс горения топлива
- •Примеры расчета горения топлива Расчет горения природного газа
- •Расчет горения угольной пыли
- •Расчет горения мазута
- •Приложения
- •Рекомендуемая литература
Материальный баланс горения топлива
Материальный баланс необходим для проверки правильности расчетов, его составляют на 100 м3 газа или 100 кг мазута или твердого топлива (табл. 2).
Таблица 2
Материальный баланс процесса горения топлива.
|
Приход |
кг |
Расход |
кг |
|
а)Природный газ |
|
Продукты горения |
|
|
СН4= СН4вл ·СН4(0,717)* |
|
СО2 =VСО2·100·СО2(1,977) |
|
|
С2Н6= С2Н6вл ·С2Н6(1,356) |
|
Н2О =VН2О·100·Н2О(0,804) |
|
|
С3Н8= С3Н8вл·С3Н8(2,020) |
|
N2 = VN2·100· N2 (1,251) |
|
|
С4Н10= С4Н10вл·С4Н10(2,840) |
|
О2 =VО2·100·О2(1,429) |
|
|
С5Н12= С5Н12вл·С5Н12(3,218) |
|
для твердого топлива и мазута |
|
|
N2 = N2вл · N2 (1,251) |
|
SO2 = VSО2·100· SО2 (2,852) |
|
|
Н2О = Н2Овл·Н2О(0,804) |
|
Зола |
|
|
б) Твердое топливо, мазут |
100,0 |
Невязка |
|
|
Воздух |
|
|
|
|
О2 = Lд·100·0,21· О2 (1,429) |
|
|
|
|
N2 = Lд·100·0,79· N2 (1,251) |
|
|
|
|
Н2О = Lд·100·0,0016·10· Н2О (0,804) |
|
|
|
|
Итого |
|
Итого |
|
|
*В скобках указаны плотности газов в кг/м3. |
| ||
|
|
|
|
|
Разность между суммой прихода и суммой расхода, называемую невязкой, вносят в расходную часть, независимо от её знака («+» или «–»). Величина невязки не должна превышать 1% от суммы приходных статей, т.е. невязка составляет
![]() .
.
|
|
|
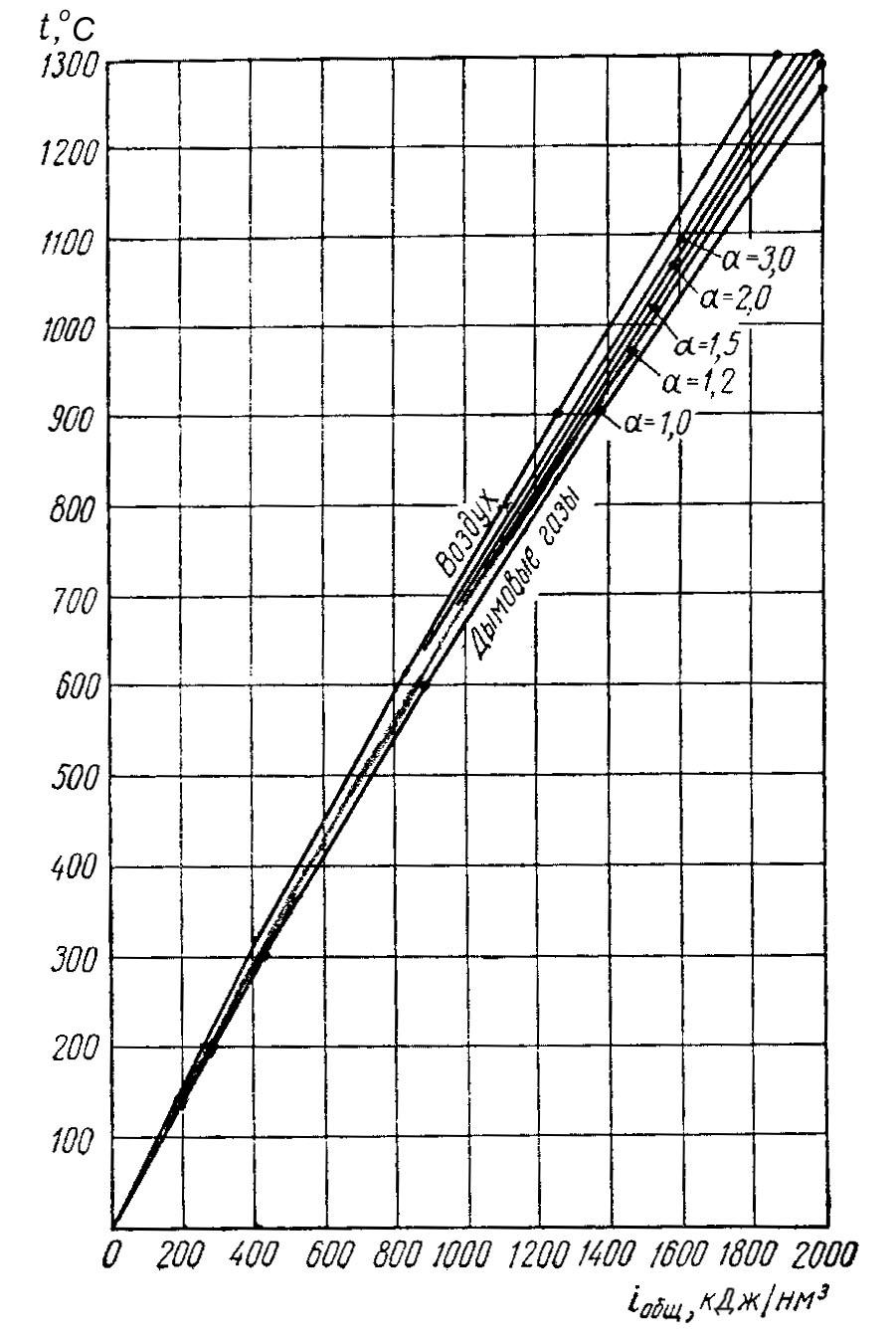
Рис. 1. i–t-диаграмма для низких температур |
|
|
|
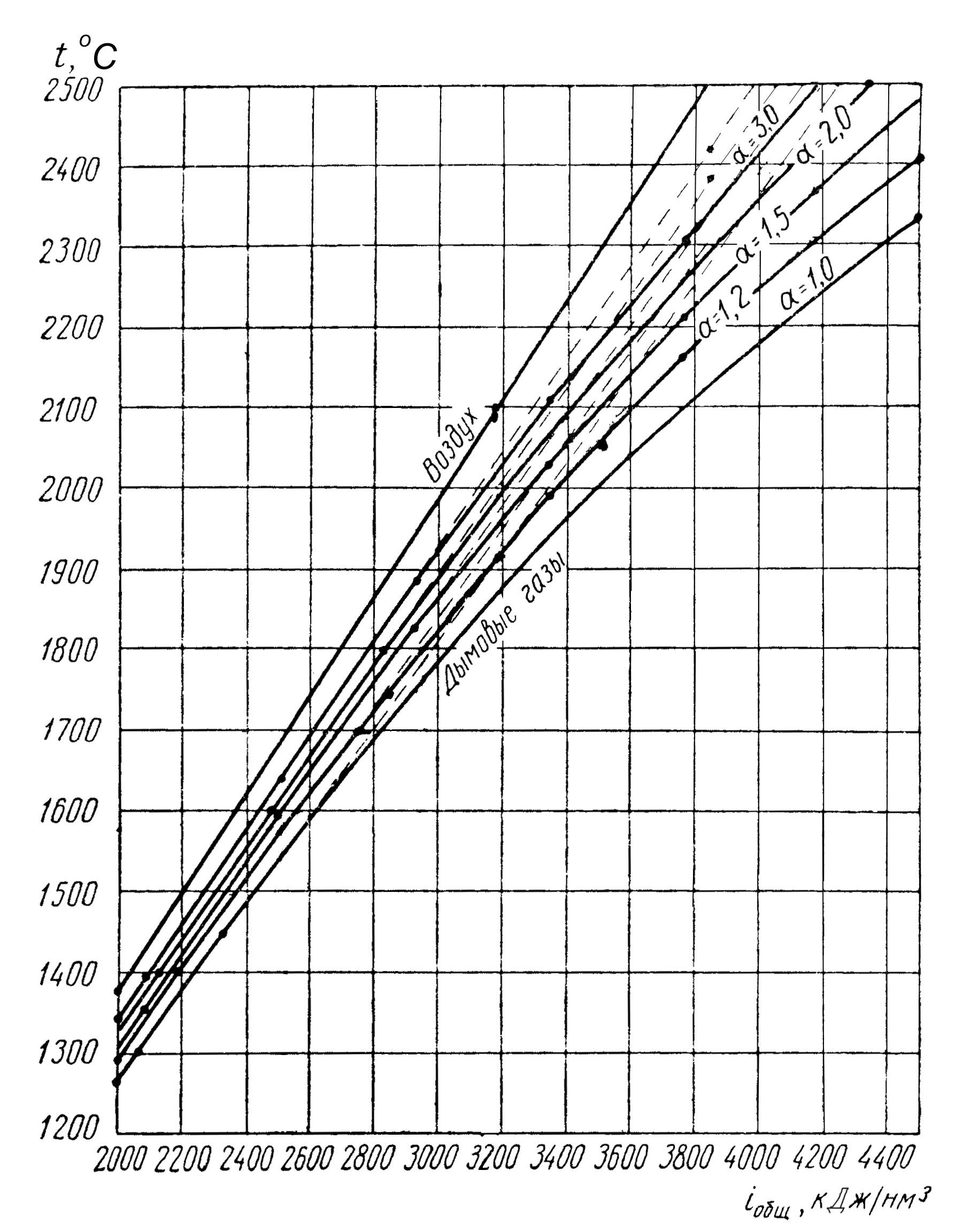
Рис. 2. i–t-диаграмма для высоких температур |
Примеры расчета горения топлива Расчет горения природного газа
Природный газ Верхне-Омринского месторождения. Содержание влаги в газе Wр= 1,0 об.%.
Содержание компонентов сухого топлива, % по объему
|
СН4с |
С2Н6с |
С3Н8с |
С4Н10с |
С5Н12си высшие |
СО2с |
N2с |
Сумма |
|
85,0 |
3,90 |
1,40 |
0,41 |
0,23 |
0,10 |
8,70 |
99,74 |
|
|
|
|
|
|
|
|
|
Коэффициент избытка воздуха при сжигании газа в горелке частичного смешивания = 1,15. Влагосодержание атмосферного воздухаd= 10 г/кг сухого воздуха (в этом и других примерах).
Определяем состав рабочего топлива. Пользуясь формулой (0), находим содержание элементов в рабочем топливе:
СН4вл=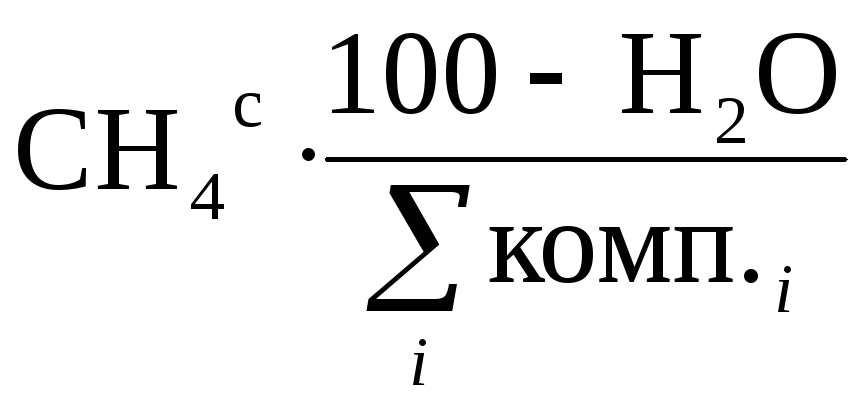 % =
% =![]() = 85,0·0,9926 = 84,37%;
= 85,0·0,9926 = 84,37%;
С2Н6вл= 3,90·0,9926 = 3,87%;
С3Н8вл=1,40·0,9926 = 1,39%;
С4Н10вл=0,41·0,9926 = 0,41%;
С5Н12вл=0,23·0,9926 = 0,23%;
СО2вл=0,10·0,9926 = 0,099%0,10%;
N2вл=8,70·0,9926 = 8,64%;
Н2Овл=1,00%.
Результаты пересчета состава сводим в таблицу.
Состав влажного рабочего топлива, объемные %
|
СН4вл |
С2Н6вл |
С3Н8вл |
С4Н10вл |
С5Н12вл |
СО2вл |
N2вл |
Н2Овл |
Сумма |
|
84,37 |
3,87 |
1,39 |
0,41 |
0,23 |
0,10 |
8,64 |
1,00 |
100,00 |
|
|
|
|
|
|
|
|
|
|
Рассчитываем теплоту сгорания природного газа по формуле (0):
![]() = 358,2·84,38 + 637,5·3,87 + 912,5·1,39 + 1186,5·0,41 +
1460,8·0,23=
= 358,2·84,38 + 637,5·3,87 + 912,5·1,39 + 1186,5·0,41 +
1460,8·0,23=
= 34773 кДж /нм3.
Тепловой эквивалент согласно формуле (0) составляет:
Эт=![]() = 1,187.
= 1,187.
Теоретически необходимое количество сухого воздуха находим по формуле (0):
L0 = 0,0476·(2·84,37 + 3,5·3,87 + 5·1,39 + 6,5·0,41 + 8·0,23) = 9,22 нм3/нм3.
Определяем действительное количество атмосферного воздуха при = 1,15 по формуле (0):
Lд= 1,15 · 9,22= 10,60 нм3/ нм3.
Рассчитываем действительное количество атмосферного воздуха по формуле (0):
Lд= (1 + 0,016d)Lд= 1,016·10,60 = 10,77 нм3/ нм3.
Количество продуктов горения газа при = 1,15 по формулам (0) ‑ – (0):
VСО2= 0,01 (0,10 + 84,37 + 2·3,87 + 3·1,39 + 4·0,41 + 5·0,23) =
= 0,991 нм3/нм3;
VН2О= 0,01 (2·84,37 + 3·3,87 + 4·1,39 + 5·0,41 + 6·0,23 + 0,99 +
+ 0,16·10·10,60) = 2,073 нм3/нм3;
VN2= 0,79·10,60 + 0,01·8,64 = 8,463 нм3/нм3;
VО2= 0,21 (1,15 – 1) 9,22 = 0,290 нм3/нм3.
Находим общий объем продуктов горения при = 1,15 по формуле (0):
V= 0,991 + 2,073 + 8,464 + 0,290 = 11,81811,82 нм3/ нм3.
Процентный состав продуктов горения:
CO2=
![]() ·100%
= 8,39%;Н2O=
·100%
= 8,39%;Н2O=
![]() ·100%
= 17,54%;
·100%
= 17,54%;
N2=
![]() ·100%
= 71,61%;О2=
·100%
= 71,61%;О2=![]() ·100%
= 2,46%.
·100%
= 2,46%.
Всего 100,00 %.
Составляем материальный баланс процесса горения на 100 нм3природного газа при= 1,15.
Материальный баланс процесса горения природного газа
|
Приход |
кг |
Расход |
кг |
|
Природный газ |
60,49 |
Продукты горения |
|
|
СН4= 84,37·0,717 |
5,25 |
СО2= 0,991·1,977 |
196,02 |
|
С2Н6= 3,87·1,356 |
2,81 |
Н2О = 2,073·0,804 |
166,65 |
|
С3Н8= 1,39·2,020 |
1,16 |
N2= 8,463·1,251 |
1058,74 |
|
С4Н10= 0,41·2,840 |
0,73 |
О2= 0,290·1,429 |
41,50 |
|
С5Н12= 0,23·3,218 |
0,20 |
|
|
|
N2= 8,64·1,251 |
10,80 |
Невязка |
-0,89 |
|
Н2О = 0,99·0,804 |
0,80 |
|
|
|
Воздух |
|
|
|
|
О2 = 10,60·0,21·100·1,429 |
318,20 |
|
|
|
N2= 10,60·0,79·100·1,251 |
1047,94 |
|
|
|
Н2О = 10,60·0,0016·10·100·0,804 |
13,64 |
|
|
|
Итого |
1462,02 |
Итого |
1462,02 |
|
|
|
|
|
Невязка
баланса составляет:
![]() = 0,061%.
= 0,061%.
Определяем теоретическую температуру горения природного газа. Для этого находим общее теплосодержание продуктов горения по формуле (0), пренебрегая теплосодержанием природного газа и воздуха и теплотой диссоциации:
i
общ =
![]() = 2942 кДж/нм3.
= 2942 кДж/нм3.
По i–t-диаграмме (рис. 2) находим теоретическую температуру горения при коэффициенте= 1,15:tтеор= 1780°С.
Находим расчетное теплосодержание продуктов горения с учетом пирометрического коэффициента, который примем равным = 0,78:
iобщ = i общ . = 2942 · 0,78 = 2295 кДж/нм3.
По i–t-диаграмме (рис. 2) находим действительную температуру горения природного газаtдейств= 1450°С.
Допустим, требуется создать в печи температуру 1680ºС.
Для этого необходимо повысить теплосодержание ПГТ. Определяем по i–t-диаграмме, что при 1680ºСiобщ = 2724 кДж/нм3.
Снизить коэффициент избытка воздуха α ,чтобы уменьшился общий объем ПГТ Vи таким образом повысилось их теплосодержаниеiобщ, нельзя, так как= 1,15 близко к минимально допустимому значению и в результате сниженияухудшится смешивание потоков топлива и воздуха.
Общее теплосодержание продуктов горения топлива iобщможет быть повышено за счет теплоты подогретого воздухаi возд, идущего на горение. Определим температуру подогрева. Вклад в теплосодержание ПГТ от нагретого воздуха:
Δiобщ=![]() =
=![]() = 550 кДж/нм3.
= 550 кДж/нм3.
Приравниваем добавочную теплоту величине теплосодержания воздуха. При сжигании газа доля вторичного воздуха может достигать 100%, т.е. в формуле (0) k= 1,00.
Δiобщ=iвозд=![]() ,
т.е.
,
т.е.
iвозд=![]() = 550
= 550![]() = 613 кДж/нм3.
= 613 кДж/нм3.
По i–t-диаграмме (рис. 1) определяем, что воздух обладает теплосодержаниемiвозд= 613 кДж/нм3при подогреве доtвозд= 420ºС.