
Химия. методические рекомендации
.pdf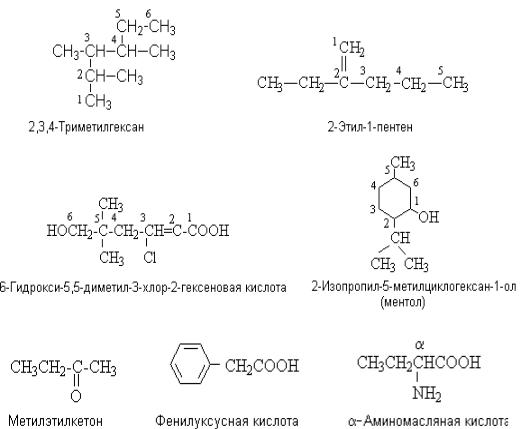
11
-ОН |
гидрокси |
ол |
|
|
|
-SH |
меркапто |
тиол |
|
|
|
-NH2 |
амино |
амин |
|
|
|
-OR** |
алкокси, |
- |
|
арокси |
|
-F, -Cl, -Br, -I |
фтор, хлор, |
- |
|
бром, иод |
|
-NO2 |
нитро |
- |
|
|
|
*
ÏолесÃÓАтом углерода, заключенный в скобки, входит в состав родоначальной структуры. **Алкокси-группы и все следующие за ними перечисляются в префиксе по алфавиту и не
имеют порядка старшинства.
Примеры:
1.5 Электронное строение и реакционная способность органических соединений
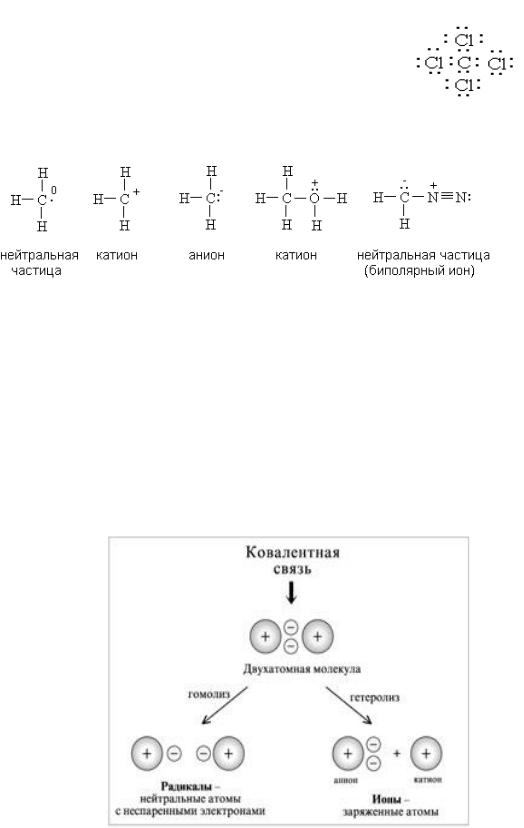
Электронное строение органических соединений изображают с помощью электронных формул Льюис.
12
Например, формула Льюиса для тетрахлорметана.
Для каждого атома в структуре Льюиса определяют формальный заряд. Сумма формальных зарядов всех атомов дает заряд частицы в целом.
прежде всего прочностью химических связей. Мерой прочности химической связи является энергия связи.
Механизмы органических реакций выражается в описании пути превращения реагентов в конечные продукты. Механизм реакции предполагает детальное описание химиче ких реакций по стадиям. При этом устанавливают, какие именно ковалентные вязи разрываются, в каком порядке и каким путем. Также опи ывают образование новых связей в процессе реакции.
Существует два способа разрыва ковалентной связи – гомолитический и гетеролитический.
ÏолесÃÓРеакционная способность органических соединений определяется
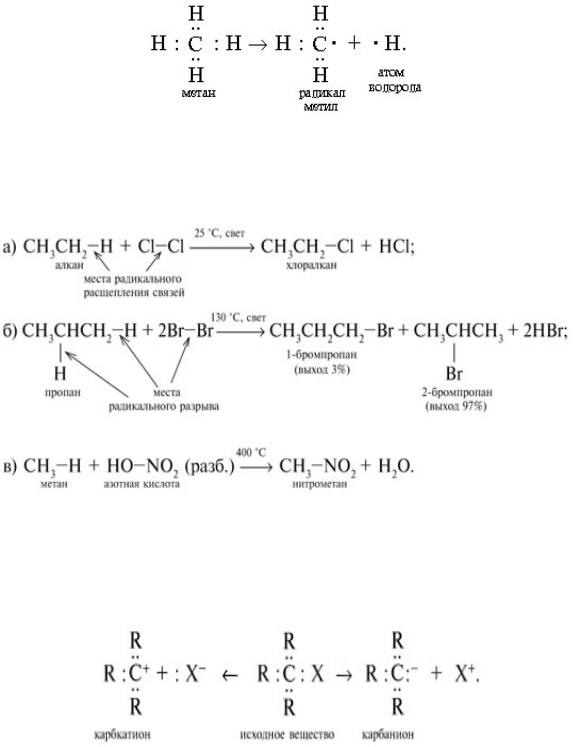
Радикальные реакции протекают путем гомолитического (радикального) разрыва ковалентной связи:
13
Радикальному разрыву подвергаются неполярные или малополярные ковалентные связи (С–С, N–N, С–Н) при высокой температуре или под действием света. Радикалы неустойчивы, они стремятся захватить недостающий электрон (до пары или до октета). Радикальные реакции – это, например, реакции хлорирования, бромирования и нитрования алканов:
карбкати ны и карбани ны – зарядом на атоме углерода. В ионных реакциях связывающая э ектронная пара не разъединяется, а целиком переходит к дн му из ат м в, превращая его в анион:
ÏолесÃÓИонные реакции прот кают г т ролитическим разрывом связи. При этом промежуточно образуются короткоживущие органические ионы –
К гетеролитическому разрыву склонны сильно полярные (Н–O, С–О) и легко поляризуемые (С–Вr, С–I) связи.
Различают нуклеофильные реакции (нуклеофил – ищущий ядро, место с недостатком электронов) и электрофильные реакции (электрофил – ищущий электроны). Утверждение, что та или иная реакция является нуклеофильной или электрофильной, условно всегда относится к реагенту.
Реагент – участвующее в реакции вещество с более простой структурой.
Субстрат – исходное вещество с более сложной структурой.
14
Уходящая группа – это замещаемый ион, который был связан с углеродом.
Продукт реакции – новое углеродсодержащее вещество
(записывается в правой части уравнения реакции).
К нуклеофильным реагентам (нуклеофилам) относят отрицательно заряженные ионы, соединения с неподеленными парами электронов, соединения с двойными углерод-углеродными связями.
К электрофильным реагентам (электрофилам) относят положительно заряженные ионы, соединения с незаполненными электронными оболочками (АlCl3, ВF3, FeCl3), cоединения с карбонильными группами, галогены. Электрофилы – любые атом, молекула или ион, способные присоединить
пару электронов в процессе образования новой связи. ÏолесÃÓДвижущая сила ионных реакций – взаимодействие противоположно
заряженных ионов или фрагментов разных молекул с частичным зарядом (+
и –).
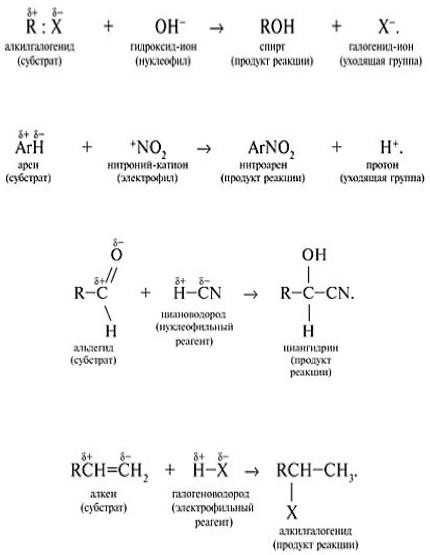
Примеры ионных реакций разных типов.
Нуклеофильное замещение:
Электрофильное зам щ ние:
Нукле фи ьн прис единение (сначала присоединяется CN–, потом
Н+):
Электрофильное присоединение (сначала присоединяется Н+, потом
Х–):
Элиминирование при действии нуклеофилов (оснований):
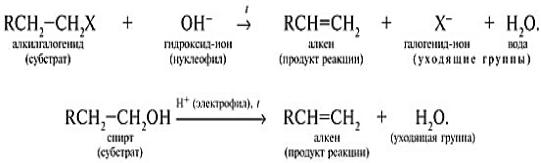
15
Элиминирование при действии электрофилов (кислот):
1.6 Взаимное влияние атомов в органических соединениях
ÏолесÃÓВ молекуле сложного органического соединения на каждый атом оказывают влияние их соседние атомы или группы атомов. Функциональные группы, смещающие электронную плотность в свою сторону, являются акцепторами, а группы, смещающие электронную плотность от себя – донорами.
Смещение электронной плотности вдоль σ–связей носит название индуктивного эффекта. Атомы или функциональные группы, «отталкивающие» от себя электронную плотность, проявляют положительный (+I) а смещающие в вою торону – отрицательный (-I) эффекты.
Индуктивный эфф кт обозначают трелкой вдоль связи, которая направлена от атома с частичным положительным зарядом (δ+) в сторону того атома, на котором возника т избыточный частичный отрицательный заряд (δ-). Индуктивный эфф кт распространяется на соседние 2-3 атома по отношению к группе, вызывающей этот эффект, и по мере удаления от группы убывает.
Смещение э ктр нн й п отности в системе сопряженных связей носит название мез мерн го эффекта (М-эффект). Мезомерный эффект охватывает всю ациклическую сопряженную систему, частичные заряды возникают на крайних атомах в сопряженной системе, а в бензольном кольце
– изменение электронной плотности происходит в положениях 2,4,6 (по отношению к группе, проявляющей эффект).
Атомы галогенов, гидрокси- и аминогруппы содержат неподеленные пары электронов, которые смещаются в сторону π-связи, образуя общую сопряженную систему. Они проявляют +М-эффект. Карбоксильная, карбонильная, нитро-группы обладают –М-эффектом, и они смещают π- электронную плотность в свою сторону.
Донорными группами, проявляющими положительный мезомерный эффект, следует считать гидрокси, амино группы, атомы галогенов фтора и хлора. Акцепторные группы: карбоксильная, альдегидная, нитро, циано.
Донор проявляет положительные + I и + М –эффекты, а акцептор - отрицательные - I и – М –эффекты.
В сопряженной системе главным считается мезомерный М-эффект.
16
РАЗДЕЛ 2
ЛАБОРАТОРНАЯ РАБОТА
КИСЛОРОДСОДЕРЖАЩИЕ ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
Цель: познакомиться со способами получения и с некоторыми химическими свойствами кислородсодержащих соединений: спиртов, альдегидов, кетонов, простых и сложных эфиров, карбоновых кислот.
Реактивы и оборудование: этиловый спирт, металлический натрий, фенолфталеин, дистиллированная вода, сульфат меди, гидроксид натрия,
глицерин, этиленгликоль, концентрированная серная кислота, хромовая смесьÏоле, борная кислота, формальдегидсÃÓ, уксусный альдегид, ацетон, фуксинсернистая кислота, гидроксид натрия, нитрат серебра, аммиак, оксид меди (II), ацетат натрия, ступки, кружки фильтровальной бумаги, пробирки с газоотводными трубками, фарфоровая пластинка, штатив с пробирками, спираль из медной проволоки, спиртовка.
Основные сведения ки лород одержащих органических соединения
Спирты, или алкоголи – производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на соответствующее число гидрокси ьных групп (–ОН).
Общая форму а одноатомных насыщ нных спиртов CnH2n+1OH.
В промыш енности по учают:
1. Гидратацией а кенов:
→
2. Бр жением глюк зы:
→
3. Метанол получают из синтез-газа:
→
В лаборатории получают:
1. Гидролизом галогеналканов водными растворами щелочей:
→
2. Восстановлением альдегидов или кетонов в присутствии катализаторов (Ni, Pt, Co):
→
Химические свойства одноатомных спиртов
1. Взаимодействие с щелочными металлами (образуются алкоголяты):
алкоголят натрия
17
2.Взаимодействие с галогенводородами:
3.Взаимодействие с аммиаком:
→
4. Внутримолекулярная дегидратация:
→
5. Межмолекулярная дегидратация:
→
6. Полное окисление (горение):
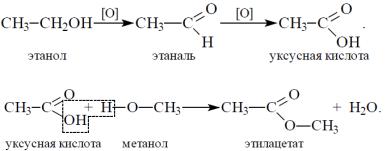
Ïоле7. Частичное окисление досÃÓальдегидов или карбоновых кислот:
8. Действие на спирты минеральных или органических кислот:
Многоатомные спирты (двухатомные и трехатомные)
Двухатомные спирты (гликоли) – спирты двумя гидроксильными группами при разных уг родных атомах. Общая формула CnH2n(OH)2.
Трехатомные спирты (г иц рины) содержат три гидроксильные группы при разных уг ер дных атомах. Общая формула CnH2n-1(OH)3.
Химические св йства многоатомных спиртов Кисл тные св йства.
1. С активными металлами:
Кисл тн сть мн г ат мных спиртов выше, чем одноатомных, что объясняется наличием в молекуле дополнительных гидроксильных групп, обладающих отрицательным индуктивным эффектом.
HO-CH2-CH2-OH + 2Na → H2↑+ NaO-CH2-CH2-ONa
гликолят натрия
2. Качественной реакцией обнаруживающей наличие многоатомного спирта, является взаимодействие со свежеприготовленным гидроксидом меди (II):
CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4;

18
Аналогично протекает взаимодействие гидроксида меди (II) с этиленгликолем. С этиловым спиртом подобная реакция не идет.
Основные свойства.
1. С галогенводородными кислотами
HO-CH -CH -OH + 2HCl ↔ Cl-CH -CH -Cl + 2H O
ÏолесÃÓ2 2 2 2 2
2. С азотной кислотой Многоатомные спирты взаимодействуют с кислотами, образуя
сложные эфиры. При взаимодействии глицерина с азотной кислотой в присутствии концентрированной серной кислоты образуется нитроглицерин (тринитрат глицерина):
C3H5(OH)3 + 3HNО3 → C3H5(ONO2)3 + 3H2O
Оксосоединения (альдегиды и кетоны)
Альдегиды и кетоны – производные углеводородов, в молекулах которых содержится одна или бол карбонильных групп >С=О. Общая
формула СnH2nO.
Если карбони ьная группа связана с одним радикалом и водородом, то такие соединения называют а ьд гидами.
Соединения, в которых карбонильная группа соединена с двумя одинаковыми и и разными радика ами, называют кетонами.
Сп бы п лучения ксосоединений
1. Гидратация ацетилена и его гомологов:
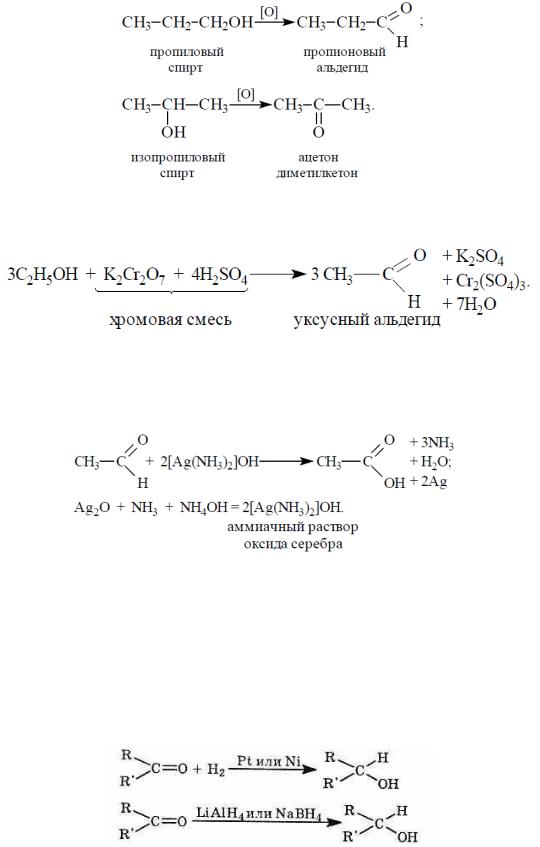
2. Дегидрирование спиртов. При окислении первичных спиртов образуются альдегиды, а вторичных – кетоны:
19
3. Окисление хромовой смесью.
Одноатомные предельные спирты окисляются хромовой смесью с
образованием альдегидов: |
|
ÏолесÃÓ |
|
Химические свойства альдегидов. |
|
1. |
Одной из качественных реакций, обнаруживающих присутствие |
альдегида, является реакция «серебряного зеркала»:
Друг й качественн й реакцией на альдегид может служить взаимодействие его c фуксинсернистой кислотой. Подобно тому, как фенолфталеин крашивает щелочной раствор в малиновый цвет, фуксинсернистая кисл та придает раствору уксусного альдегида розовофиолетовый цвет, а раств ру формальдегида – фиолетовый.
2. Реакция карбоксильной группы альдегидов Присоединение водорода (гидрирование) происходит с разрывом
двойной связи карбонильной группы альдегида, который при этом превращается в первичный спирт:
Эта реакция проводится или при действии водорода в момент выделения, или путем каталитического гидрирования (катализатором служит никель или платина).
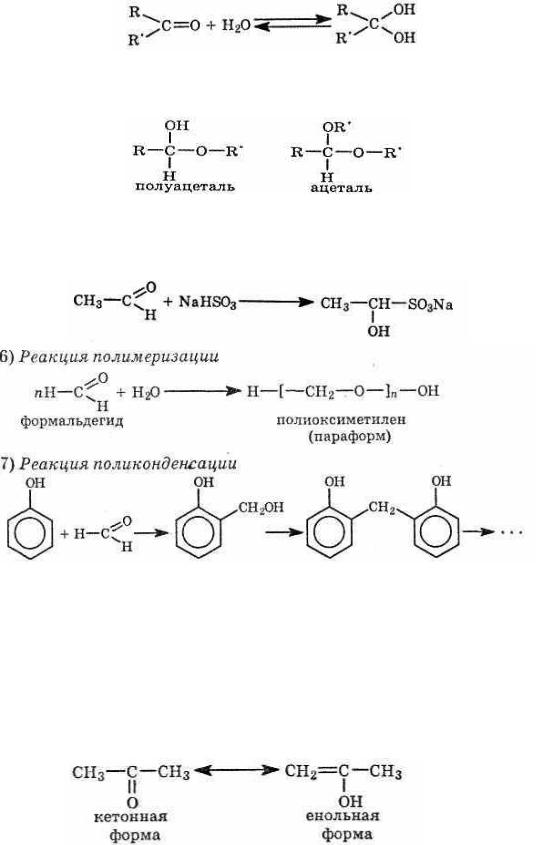
3.Взаимодействие с водой:
20
4.Взаимодействие спирта.
При взаимодействии альдегидов со спиртом приводит к образованию полуацеталя и ацетали.
5. Присоединение бисульфата натрия происходит при встряхивании растворов альдегидов с концентрированным рствором бисульфита натрия,
продукт реакции выделяется в виде осадков.
ÏолесÃÓХимические св йства кетонов.
1. Кето-ен льная таут мерия.
Таут меры – это изомеры различного строения, находящиеся в динамическом равновесии. Для альдегидов и кетонов характерно явление кето-енольной таутомерии. Таутомерные формы отличаются положением атома водорода и для ацетона показаны ниже:
Гидрирование. Присоединение водорода к кетонам происходит в
присутствии катализаторов гидрирования (Ni, Co, Cu, Pt, Pd и др.).
( ) ( )
