
met_khimija-12
.pdf2. Выпадет ли осадокMgCO3 при сливании равных объемов 0.02 M раство-
ра Mg(NO3)2 и 0.004 M раствора K2CO3? KПР(MgCO3) = 7.0×10–6 .
(Ответ: Пс = 2×10–5 , выпадет) 3. Рассчитайте молярную концентрацию и массу Ca2+ в 10 л насыщенного
раствора CaHPO4. KПР(CaHPO4) = 2.7×10–7 . (Ответ: c = 5.2×10–4 M; m = 0.2 г) 4. Выпадет ли осадок CuCO3 при сливании равных объемов 0.224 M рас-
твора диглицината меди(II) [Cu(Gly)2] и 0.2 M раствора K2CO3? Kуст. ([Cu(Gly)2]) = 3.5×1015, KПР(CuCO3) = 1.0×10–10 . Ответ подтвердите расчетом Пс.
(Ответ: Пс = 1.26×10–7 , выпадет)
Пример билета контрольной работы «Комплексы и ПР»
1. В комплексе [Pt(en)Cl2] (en=NH2CH2CH2NH2) укажите внутреннюю и внешнюю сферы, ион-комплексообразователь, его координационное число и заряд, а также заряд лигандови их дентатность. Напишите уравнения диссоциации комплекса и выражение Kуст для комплексного соединения.
2. Рассчитайтеконцентрацию иона– комплексообразователя в растворе, 1 л
которого содержит 0.03 моль |
[Ag(NH3)2]NO3 и 1 моль аммиака, Kуст. |
([Ag(NH3)2]+) = 1.12·107 |
(Ответ: 2.7×10–9 моль/л) |
3. Используя ответзадачи№2, рассчитайте, какуюмассу NaCl нужно прибавить к 1 л этого растворадо началавыпаденияосадка AgCl. KПР(AgCl) = 2.0×10–10 . Изменением объема раствора пренебречь. (Ответ: 4.33 г)
Тема 10. Электродные, восстановительные (Red–Ox) и мембранные
потенциалы. Направление окислительно-восстановительного процесса
Содержание темы. Электродныйпотенциал, зависимость его от различных факторов (уравнение Нернста). Водородный электрод. Окислительновосстановительные (ОВ) системы и окислительно-восстановительные реакции (ОВР). Зависимость ОВ-потенциала от различных факторов(ББХ, 363–375, или
ПОХ, с. 687–717).
Разделы, выносимыена самостоятельную проработку. Степень окисле-
ния, окислители и восстановители, составление уравнений ОВР (ББХ, 359–363,
или ПОХ, с. 92–99).
Письменное задание по самостоятельной проработке
1.ББХ, задание 11.18 с. 377.
2.Какие окислительно-восстановительные свойства могут проявлять приведенные частицы: Br2, CO32– , NO3– , NH3, I– (не проявляют; только окисли-
тельные; только восстановительные; окислительные и восстановительные)?
Письменное домашнее задание по теме 10
1)Выпишите определения следующих терминов: стандартный электродный потенциал, стандартный восстановительный (окислительно-восстанови- тельный) потенциал, стандартный биологическийпотенциал, электродвижущая сила химической реакции (ЭДС), мембранный потенциал.
2)Выпишите формулы: для расчета электродного потенциала (уравнение Нернста), для расчета окислительно-восстановительного потенциала (уравне-
ние Нернста– Петерса), мембранного потенциала, ЭДС химической реакции, связи ЭДС и G.
40

3) Выполнитезадания по ББХ 11.2, 11.6, 11.7, 11.13, 11.17–11.19, с. 376–377.
Важной особенностью биохимических реакций является их протекание при постоянномзначенииpH в условиях кислотно-основного гомеостаза организма. Поэтому для биологических окислительно-восстановительных систем вводится понятие стандартного биологического потенциала (Е0'), определяе-
мого при pH = 7 и Т =310К.
Ситуационные задачи (САРС), выполняемые на занятии (значения
Е0298 и Е0’310 см. в таблице СБ с 81).
1.Запишите уравнение Нернста– Петерса для систем, приведенных ниже:
а) H2O2 + 2  2 OH– ; в) НАДФ+ + H+ + 2
2 OH– ; в) НАДФ+ + H+ + 2  НАДФH;
НАДФH;
б) I2(тв.) + 2  2 I– ; г) CH3COOH + 2 H+ + 2
2 I– ; г) CH3COOH + 2 H+ + 2  CH3C
CH3C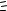 OH + H2O
OH + H2O
2.Потенциал каких систем, перечисленных в п. 1, будет зависеть от pH? В
каком направлении происходит сдвиг равновесия и изменяется потенциал при увеличении pH; при уменьшении pH?
3.Что такоестандартныйбиологическийпотенциал(Е0’310)? Рассчитайте его величину для системы 1 г, исходя из табличного значения Е0298. (Ответ: –0.532 В)
4.Рассчитайте потенциалы систем при 25 °C:
а) I2(тв.) / 2 I– ; [I– ] = 0.01 моль/л
б) CH3COOH / CH C |
O; [CH3COOH] = 0.01 M, [CH C |
O] = 0.5 M, pH = 3 |
|
3 |
H |
3 |
H |
в) MnO4– / MnO2, 4 OH– ; [MnO4– ] = 1×10–3 M, [OH– ] = 1×10–4 M |
|||
|
|
(Ответ: а) 0.656 В, б) –0.35 В, в) 0.848 В) |
|
5. Рассчитав ЭДС и величину |
G0' реакции, определите возможность ее |
||
|
|
310 |
|
самопроизвольногопротекания в указанном направлении в стандартных биоло-
гических условиях:
CH C |
O |
+ НАД+ + H2O CH3COO– + 2 H+ + НАДH |
3 |
H |
(Ответ: ЭДС = 0.21 В, G0' = –40.9 кДж) |
|
|
|
|
|
310 |
6.Мембранный потенциал нервной клетки в состоянии покоя составил – 86 мВ при 310 K. Концентрация ионов K+ внутри клетки 150 ммоль/л. Опреде- лите концентрацию ионов K+ в межклеточной жидкости. (Ответ: c = 6 ммоль/л)
Примерные вопросы билетовконтрольнойработы «Потенциалы иЭДС»
Для решения используйте данные табл. на стр. 83.
1. Запишите уравнение Нернста— Петерса для системы:
Mn04 + 2 H2O + 2 |
Mn02(тв.) + 4 OH– |
Как зависит потенциал этой системы от рН раствора? 2. Запишите уравнение Нернста— Петерса для системы:
CH3C(O)COO– + 2 H+ + 2  CH3CH(OH)COO–
CH3CH(OH)COO–
Как зависит потенциал этой системы от рН раствора?
3. Рассчитайте ЭДС и G0 реакции определите возможность самопроиз- вольногопротеканияреакциивуказанномнаправлении в стандартных условиях:
MnO2(тв.) + 4 HCl MnCl2 + Cl2 + 2 H2O |
(Ответ: –0.13 В) |
4. Рассчитайте потенциал системы: |
|
НАДФ+ + H+ + 2 НАДФH |
|
41 |
|
при 298 К, рН = 2 и молярных концентрациях НАДФ+ и НАДФН, равных 0.01 и 0.001 моль/л соответственно. (Ответ: –0.145 В)
5. РассчитайтеЭДС и G0298 реакции и определите возможность самопроизвольного протекания реакции в указанном направлении в стандартных условиях:
2 Cl– + 2 Fe3+  2 Fe2+ + Cl2 (Ответ: ЭДС = –0.58 В, G0298 = +114 кДж)
2 Fe2+ + Cl2 (Ответ: ЭДС = –0.58 В, G0298 = +114 кДж)
6. Мембранный потенциал нервной клетки составил –80 мВ при 310 K. Концентрация ионов K+ внутри клетки 150 ммоль/л. Определите концентрацию ионов K+ во внеклеточной жидкости. (Ответ: 7.69 ммоль/л)
Образец билета тестового контроля «Окислительно-восстановительные процессы»
1.Из нижеприведенных частиц выберите ту, которая проявляет восстановительные свойства:
1)SO42– ; 2) Cl– ; 3) Na+; 4) Cl2; 5) Ag+.
2.Выберите окислительно-восстановительную систему, потенциал кото-
рой не зависит от рН раствора:
1)CH3C(O)H + 2 H+ + 2е– CH3CH2OH
2)SO42– + H2О + 2е– SO32– + 2OH–
3)Br2 + 2е– 2Br–
4)H2O2 + 2е– 2 OH–
5)CH3COOH + 2 H+ + 2е– CH3C(O)H + H2O
3. Как изменится величина ОВ-потенциала системы: CH3COOH + 2 H+ + 2е– CH3C(O)H + H2O при добавлении CH3COOH?
Варианты ответа: 1) увеличится; 2) уменьшится; 3) изменится незначительно; 4) сначала увеличится, затем уменьшится; 5) сначала уменьшится, затем увеличится.
4. Как изменится величина ОВ-потенциала системы
CH3C(O)H + 2 H+ + 2е– CH3CH2OH при добавлении CH3CH2OH?
Варианты ответа: 1) увеличится; 2) уменьшится; 3) изменится незначительно; 4) сначала увеличится, затем уменьшится; 5) сначала уменьшится, затем увеличится.
5. Как изменится величина ОВ-потенциала потенциала системы MnO4– + 8 H+ + 5е- Mn2+ + 4 H2O при уменьшении рН раствора?
Варианты ответа: 1) увеличится; 2) уменьшится; 3) изменится незначительно; 4) сначала увеличится, затем уменьшится; 5) сначала уменьшится, затем увеличится.
Модульная контрольная работа №1 Домашнее задание для подготовки к модульной контрольной работе
1.Ознакомиться с программой модульной контрольной работы (сайт кафедры).
2.Разобрать примеры тестового контроля и основного билета.
42

Примеры заданий тестового контроля 1-го модуля
(билет включает 5 заданий)
В заданиях необходимо найти соответствие между пунктами левой и правой колонок (ответы в правой колонке могут использоваться неоднократно или не использоваться ни разу). При решении тестовых заданий не разрешается пользоваться таблицами и производить какие-либо расчеты.
Какой процесс в закрытой системе характеризуется следующими измене-
ниями термодинамических параметров: |
|
|
||
1) |
экзэргонический |
а) |
H < 0, |
S > 0 |
2) |
эндэргонический |
б) |
G < 0 |
|
3) |
равновесный |
в) |
H > 0, |
S < 0 |
4) |
эндотермический |
г) |
H = T |
S |
|
|
|
|
|
Соотнесите реакции и стандартные тепловые эффекты (Т = 298 К):
1) |
S(кр) + O2 (газ) = SO2 (газ) |
а) |
H0(SO3 (газ)) |
2) |
2 SO2 (газ) + O2 (газ) = 2 SO3 (газ) |
б) |
H0(SO2 (газ)) |
3) |
S (кр) + 1.5 O2 (газ) = SO3 (газ) |
в) |
H0 сгорания S(кр) |
4) |
H2SO3 (р-р) = SO2 (газ) + H2O (ж) |
г) |
другой тепловой эффект |
Cоотнесите значения стандартной молярной энтропии S0298 (Дж/моль×К) с химическими формулами веществ:
1)С (графит) а) 200
2)С2Н2 (газ) б) 220
3)С2Н6 (газ) в) 5.7
4)С2Н4 (газ) г) 230
Определите, как изменяется величина стандартной молярной энтропии в
каждом ряду веществ: |
|
|
|
1) |
S(кр) – SO 2 (газ) – SO 3 (газ) |
|
а) увеличивается |
|
|||
2) |
S(кр) – SO 3 (газ) – SO 2 (газ) |
|
б) уменьшается |
3) |
C6H12(газ) – C 6H6(газ) – C 6H6(ж) |
|
в) не изменяется |
4) |
NO (газ) – NO 2 (газ) – N 2O4(газ) |
|
г) изменяется немонотонно |
Оцените возможность самопроизвольного протекания каждого процесса,
если для него: |
|
|
|
|
1) |
H = 0, |
S < 0 |
а) |
возможен только при низких Т |
2) |
H > 0, |
S > 0 |
б) |
возможен только при высоких Т |
3) |
H < 0, |
S > 0 |
в) |
возможен при любых Т |
4)H < 0, S < 0 г) невозможен
Укажите, какие воздействия икак сместят равновесиев системе: 4 HCl (газ) + O2 (газ) 2 H2O (газ) + 2 Cl2 (газ), (DH < 0)
1) |
увеличение концентрации O2 |
а) |
вправо |
2) |
понижение давления |
б) |
влево |
3) |
повышение температуры |
в) |
нет |
4) |
введение катализатора |
|
|
|
43 |
|
|
|
|
|
Укажите, для каких реакций понижение давления вызовет смещение
равновесия и в каком направлении: |
|
|
|
|
|
||||||||
1) |
2 SO2 (газ) + O2 (газ) 2 SO3 (газ) |
|
|
|
а) |
вправо |
|||||||
|
|
|
|||||||||||
2) |
2 O3 (газ) 3 O2 (газ) |
|
|
|
|
|
б) |
влево |
|||||
3) |
CH3OH (ж) + C2H5OH (ж) CH3OC2H5 (ж) + H2O (ж) |
в) |
нет |
||||||||||
4) |
H2 (газ) |
+ I (газ) 2 HI (газ) |
|
|
|
|
|
|
|||||
|
|
Укажите, как изменится константа равновесия каждой реакции при повы- |
|||||||||||
шении температуры: |
|
|
|
|
|
|
|
|
|||||
1) |
CO (газ) |
+ 2 H2 (газ) CH3OH (газ) , |
H < 0 |
|
а) |
увеличится |
|||||||
|
|||||||||||||
2) |
3 O2 (газ) 2 O3 (газ) , |
|
|
H > 0 |
|
б) |
уменьшится |
||||||
3) |
CO (газ) |
+ H2O (газ) CO2 (газ) + H2 (газ) , |
H < 0 |
|
в) |
не изменится |
|||||||
4) H O |
(ж) |
OH- |
-р) |
+ H+ |
(р-р) |
, |
H > 0 |
|
|
|
|
||
|
|
2 |
(р |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Из нижеприведенныхреакций выберите а) гомогенныеи б) гетерогенные реакции:
1)N2 (газ) + O2 (газ) → 2 NO(газ)
2)Zn (тв) + 2 HCl (р-р) → ZnCl2 (р-р) + H2 (газ)
3)MgO (тв) + CO2 (газ) → MgCO3 (тв)
4)Pb(NO3)2(р-р) + K2S(р-р) → PbS (тв) + 2 KNO3(р-р)
Реакция А → В является простой, температурныйкоэффициент ее равен 2. Как будут изменяться приповышении температуры на 20о С:
1) |
скорость реакции |
а) |
не изменится |
2) |
константа скорости реакции |
б) |
увеличится в 2 раза |
3) |
время полупревращения реакции |
в) |
увеличится в 4 раза |
4) |
энергия активации реакции |
г) |
уменьшится в 2 раза |
|
|
д) |
уменьшится в 4 раза |
|
|
|
|
|
Как будет изменяться скорость реакции 2 А + В → С, протекающей в рас- |
|||
творе, кинетическое уравнение которой |
v = k.сА.сВ |
и γ = 2, при: |
||
1) |
увеличении концентрации А в 2 раза |
|
а) |
не изменится |
|
||||
2) |
уменьшении концентрации В в 2 раза |
|
б) |
увеличится в 2 раза |
3) |
разбавлении раствора в 2 раза |
|
в) |
увеличится в 4 раза |
4) |
повышении температуры на 20о С |
|
г) |
уменьшится в 2 раза |
|
|
|
д) |
уменьшится в 4 раза |
|
|
|
|
|
Соотнеситеследующие простыереакции или процессы и их суммарный
порядок: |
|
|
|
|
1) |
2NO2 → N2O4 |
|
а) |
0 |
|
||||
2) 2СО + О2 → 2СО2 |
|
б) |
1 |
|
3) |
радиоактивный распад изотопа 81Sr |
|
в) |
2 |
4) |
разложение лекарственного препарата |
|
г) |
3 |
|
|
|
|
|
Соотнеситевид кинетического уравнения и суммарный порядокреакции,
которойонисоответствуют |
|
|
|
1) |
v = k.с1 |
|
а) 0 |
|
|||
2) |
v = k с1.с2 |
|
б) 1 |
|
|
44 |
|

3) |
v = k.с1.с20.5 |
в) |
2 |
4) |
v = k.с12.с2 |
г) |
3 |
|
|
д) |
дробный |
|
|
|
|
Последовательная реакция протекает в 2 стадии (обе являются простыми реакциями) по схеме: 2 А → В; В → С и их энергии активации соотносятся: Еа1 >> Еа2. Можно ли определить:
1) |
какая стадия определяет скорость всего процессаа) |
1 |
|
2) |
каков порядок первой реакции |
б) |
2 |
3) |
каков порядок второй реакции |
в) |
3 |
4) |
каков будет порядок реакции в целом |
г) |
нельзя определить |
Правильно ли расположены 0.1 М растворы указанных ниже веществ в порядкеувеличения осмотическогодавления?
1) |
С6Н12О6 – HCOOH – NaCl – CaCl 2 |
а) да |
2) |
Ba(NO3)2 – KCl – CaCl 2 – CO(NH 2)2 |
б) нет |
3)C6H12O6 – NaCl – CH 3COOH – CaCl 2
4)CO(NH2)2 – HCOOH – NaBr – Na 2SO4
Оцените значение рН растворовследующих веществ:
1) |
KOH |
а) |
рН < 7 |
2) |
H2SO4 |
б) рН = 7 |
|
3) |
NaCl |
в) |
рН > 7 |
4) |
HBr |
|
|
|
|
|
|
Cоотнеситезначения осмотическогодавления (кПа) с растворамиследующих веществ при равных молярныхконцентрациях (Т = 298 К):
1) |
KBr |
а) |
50 |
2) |
CH3COOH |
б) 150 |
|
3) |
MgCl2 |
в) |
100 |
4) |
C6H12O6 |
г) |
60 |
|
|
Определите, как изменяется осмотическоедавление в каждом ряду |
|
растворов при одинаковой температуре: |
|
||
1) |
0.15 М NaCl – 0.3 М С6Н12О6 – 0.1 М CaCl2 |
а) уменьшается |
|
2) |
0.1 |
М K2SO4 – 0.1 М KBr – 0.1 М С6Н12О6 |
б) увеличивается |
3) |
0.1 |
М CaCl2 – 0.1 М CH3COOH – 0.1 М KCl |
в) не изменяется |
4)0.2 М С12Н22О11 – 0.2 М MgSO4 – 0.2 М Na2SO4 г) изменяется немонотонно
0.15М раствор NaCl (физиологическийраствор) является изотоническим по отношению к плазме крови. Охарактеризуйте относительно плазмы крови
каждый из приведенных растворов
1) |
0.3 M C12H22O11 |
а) изотонический |
2) |
0.15 M CaCl2 |
б) гипотонический |
3) |
0.15 M C6H12O6 |
в) гипертонический |
4) |
0.15 M MgSO4 |
|
|
|
|
45
Cоотнеситезначения рН растворовравныхмолярныхконцентраций веществ с составомраствора:
1) |
KOH |
а) |
7.0 |
2) |
HNO3 |
б) |
12.3 |
3) |
Ва(ОН)2 |
в) |
12.0 |
4) |
K2SO4 |
г) |
2.0 |
|
|
|
|
Оцените истинность суждений:
1)) все процессы, в результате которых упорядоченность а) верно системы возрастает, сопровождаются уменьшением б) неверно энтропии
2)в выражение константы равновесия гетерогенной реакции включают концентрации всех веществ
3)реакции радиоактивного распада являются реакциями первого порядка
4)осмос – это коллигативное свойство раствора, которое
зависит от природы и размеров частиц в растворе
Оцените истинность суждений:
1)молярная энтропия газообразного вещества больше, чема) верно его энтропия в жидком состоянии
2)увеличение концентрации продуктов реакции приводит кб) неверно смещению равновесия и увеличению константы равновесия
3)чем больше энергия активации, тем больше скорость реак-
ции
4) изотоническиерастворыимеют одинаковуюконцентрацию
осмотически активных частиц
Оцените истинность суждений:
1) тепловой эффект химической реакции не зависит от агрегат- а) верно |
|
ного состояния исходных и конечных веществ |
б) неверно |
2)при увеличении температуры равновесие смещается в сторону экзотермической реакции
3)константа скорости зависит от природы реагирующих веществ
4)при увеличении концентрации растворенного вещества осмотическое давление раствора увеличивается
Оцените истинность суждений: |
|
|
1) самопроизвольный характер |
процесса в изолированной а) верно |
|
системе определяется только |
изменением энтропии |
б) неверно |
2)константа равновесия не зависит от температуры
3)энергия активации реакции зависит от концентрации реагентов
4)плазмолиз – явление сморщивания (обезвоживания) эритроцитов в гипертоническом растворе
46

Являются ли приведенные ниже смеси электролитов буферными
системами: |
|
|
|
|
|
1) |
Na2CO3, NaHCO3 |
|
|
а) да |
|
2) |
+NH CH COO– , NH CH COO– |
б) нет |
|||
|
3 |
2 |
2 |
2 |
|
3)Na2CO3, NaOH
4)NaCl, NH3×H2O
Соотнесите частицы в левой и правой колонках так, чтобы они образовы-
вали кислотно-основную сопряженную пару: |
|
|
|
|
|
|||||||||||
|
1) |
|
OH– |
|
– |
|
|
|
а) |
H2O |
|
|
|
|
||
|
2) |
|
H PO |
|
|
|
б) |
NH CH COOH |
|
|||||||
|
|
|
2 |
4 |
|
|
|
|
|
2 |
2 |
|
|
|
||
|
3) |
|
H O+ |
|
|
|
|
|
|
в) |
H PO |
4 |
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
4) NH3+CH2COOH |
|
г) |
H+ |
|
|
|
|
|
|||||||
Укажите, какой интервал буферного действия соответствует каждой из |
||||||||||||||||
приведенных буферных систем: |
|
|
|
|
|
|
|
|
|
|
||||||
1) Na2HPO4 / NaH2PO4; pKa1 = 2.12, pKa2 = 7.2, pKa3 = 11.9 |
|
а) |
8.7–10.7 |
|||||||||||||
|
||||||||||||||||
2) Na2CO3 / NaHCO3; pKa1 = 6.35, pKa2 = 10.3 |
|
|
|
б) |
8.25–10.25 |
|||||||||||
3) NH CH COO– |
/ NH CH COOH; pK |
a1 |
= 2.3, pK |
a2 |
= 9.7 |
|
в) |
9.3–11.3 |
||||||||
2 |
2 |
|
2 |
|
2 |
|
|
|
|
|
|
|
|
|
||
4) NH4Cl / NH3×H2O; pKBH+ = 9.25, pKb = 4.75 |
|
|
|
г) |
6.2–8.2 |
|||||||||||
Какие свойствамогут проявлять нижеприведенные ионы в составе буфер- |
||||||||||||||||
ного раствора: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1) SO42− |
|
–COO − |
|
|
|
а) |
|
только кислоты |
|
|
|
|||||
|
|
|
|
|
|
|
|
|||||||||
2) |
NH –CH |
2 |
|
|
|
б) |
|
только основания |
|
|
|
|||||
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3) |
NH + |
|
|
|
|
|
|
в) |
|
или кислоты, или основания |
||||||
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4) CO32− |
|
|
|
|
|
|
г) |
|
ни кислоты, ни основания |
|||||||
Соотнесите значения рН с растворами, в которых находятся нижеприве- |
||||||||||||||||
денные вещества с равными молярными концентрациями: |
|
|
|
|||||||||||||
1) HF |
|
|
|
|
|
а) pH = 7.0 |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
||||||
2) K2SO4 |
|
|
|
|
|
б) рН = 1.7 |
|
|
|
|
|
|
||||
3) [(CH3)2NH2]Cl |
|
|
|
в) pH = 5.11 |
|
|
|
|
|
|
||||||
4) CH3NH2 |
|
|
|
|
|
г) pH = 11.81 |
|
|
|
|
|
|||||
Укажите, как изменится pH раствора HNO2 при добавлении: |
||||||||||||||||
|
1) |
HNO2 |
|
|
|
а) |
увеличится |
|
|
|
||||||
|
2) |
KNO3 |
|
|
|
б) |
уменьшится |
|
|
|
||||||
|
3) |
KNO2 |
|
|
|
в) |
не изменится |
|
|
|
||||||
4)H2O
Укажите, какая константа характеризует равновесие в водном растворе следующих электролитов:
1) |
[Cu(NH3)4]SO4 |
а) Ka |
2) |
Na2CO3 |
б) KПР |
3) |
CaCO3 |
в) Kуст |
4) |
HF |
г) Kb |
|
|
+ |
|
|
д) KBH |
|
47 |
|

Как повлияют на концентрацию иона-комплексообразователя в растворе комплексного соединения [Ag(CN)2]NO3 следующие факторы:
1) |
уменьшение давления |
а) увеличится |
2) |
добавление AgNO3 |
б) уменьшится |
3) |
добавление KCN |
в) изменится незначительно |
4) |
добавление HNO3 |
|
Как повлияют на концентрацию ионов серебрав насыщенном растворе малорастворимого соединения AgCl следующие факторы:
1) |
увеличение давления |
|
а) увеличится |
||
2) |
добавление AgNO3 |
|
б) уменьшится |
||
3) |
добавление HCl |
|
в) изменится незначительно |
||
4) |
добавление NaNO3 |
|
|
||
Как изменится величина электродного потенциала системы |
|||||
Cr2O72– + 14H+ + 6e |
|
2Cr3+ + 7H2O в следующих случаях: |
|||
|
|||||
|
|||||
1) |
добавление KNO3 |
а) |
увеличится |
||
2) |
добавление CrCl3 |
б) |
уменьшится |
||
3) |
добавление K2Cr2O7 |
в) |
изменится незначительно |
||
4)увеличение pH
Укажите, зависят ли величины потенциалов следующих окислительновосстановительных систем от pH среды:
1) |
Cl2 + 2 e |
|
|
2 Cl– |
а) |
да |
|
|
|
||||||
|
|
||||||
2) |
Hg2+ + 2 e |
|
|
Hg |
б) |
нет |
|
|
|
||||||
|
|
||||||
3)C6H4(OH)2 – 2 e 
 C 6H4O2 + 2 H+
C 6H4O2 + 2 H+
4)NO3– + H2O + 2 e 
 NO2– + 2 OH–
NO2– + 2 OH–
Вкачестве чего можно использовать систему Cl2/2Cl– (E0 = + 1.36 В) в следующих процессах при стандартных условиях:
1) |
H2O2 + 2 H+ + 2 e |
|
|
|
2 H2O |
E0 |
= + 1.77 В |
а) окислитель |
||||
|
|
|
||||||||||
|
|
|
||||||||||
2) |
O2 + 2 H+ + 2 e |
|
|
H2O2 |
E0 |
= + 0.68 В |
б) восстановитель |
|||||
|
|
|||||||||||
|
||||||||||||
3) |
MnO4– + 8 H+ + 5 e |
|
|
|
Mn2+ + 4 H2O E0 = + 1.51 В |
|
||||||
|
|
|
|
|||||||||
|
|
|
|
|||||||||
4) |
Fe3+ + e |
|
Fe2+ |
|
|
|
|
E0 |
= + 0.77 В |
|
||
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Примеры заданийосновного билета модульной контрольной работы № 1
(билет содержит 6 заданий, при их выполнении можно пользоваться
справочными таблицами и калькуляторами)
1. Качественно оцените реакцию среды 0.05 M растворов а) HCl и б) NaOH. Рассчитайтезначение pH каждого раствораисходя из молярной концен-
трации в них ионов H+. |
|
(Ответ: а) pH = 1.3, б) pH = 12.7) |
||
2. В 200 мл раствора, |
плотность которого |
1.01 г/мл, содержится 1.11 г |
||
CaCl2 (M = 111 г/моль) и |
0.585 г |
NaCl (M = 58.5 г/моль). Рассчитайте: |
||
а) массовую |
долю NaCl |
в этом |
растворе; |
б) осмолярность раствора; |
в) осмотическое давление раствора при 37 °C. |
|
|||
|
(Ответ: ω(NaCl) = 0.29%, cосм. = 0.25 моль/л, π = 644 кПа) |
|||
3. а) Рассчитайтестандартноеизменение энтальпии реакции гидролиза мо- |
||||
чевины: |
CO(NH2)2 (тв) + H2O (ж) |
CO2 (р-р) + 2 NH3 (р-р), |
||
|
|
48 |
|
|

если стандартныеэнтальпии образования CO(NH2)2 (тв), H2O (ж), CO2 (р-р), и NH3 (р-
р) равны, соответственно (кДж/моль): –333, –286, –413 и –80.8. Благоприятству- |
|
ет ли энтальпийный фактор протеканию этой реакции? |
|
б) Сколько теплоты будет поглощаться или выделяться при гидролизе 3 г |
|
мочевины, если ее молярная масса 60 г/моль. |
|
(Ответ: DH0298 = 44.4 кДж; Q = –2.2 |
кДж) |
4. Используя табличные данные, установите путем расчета DG |
возмож- |
ность протекания встандартных условиях реакции окисления этанола: |
|
C2H5OH (ж) + H2O2 (ж)  CH3C(O)H (газ) + 2 H2O (ж)
CH3C(O)H (газ) + 2 H2O (ж)
Не производя вычислений, оцените роль энтропийного фактора для этой
реакции. |
(Ответ: DG |
= –319 кДж, DS > 0) |
5. Запишитевыражениеконстантыравновесия для реакциисинтеза аммиака: |
||
N2 (газ) + 3 H2 (газ) |
2 NH3 (газ); DH |
< 0. |
Как повлияет на состояние равновесия этой системы: а) повышение температуры; б) повышение давления?
Рассчитайтеконстанту этого равновесия, если исходные концентрации N2, Н2 и NH3 были 5, 14 и 0 моль/л, соответственно, а к моменту установления равновесия в реакцию вступило 40% азота. (Ответ: Kс = 0.0104)
6. Константа скорости реакции гидролиза сахарозы (реакция первого порядка) при 25 °C равна 3.2×10–3 ч–1 . Рассчитайте а) период полупревращения реакции; б) время, за котороегидролизуподвергнется 90% исходного количества сахарозы. (Ответ: τ½ = 216 час, t = 30 суток)
7. Качественно оцените реакцию среды 0.001 М раствора NaOH и рассчитайте значение pH исходя из молярной концентрации ионов H+.(Ответ: pH = 11)
8. В 1 л раствора, плотность которого1 г/мл, содержится 0.1 моль глюкозы (C6H12O6) и 0.1 моль KCl. Вычислите: а) массовую долю KCl в этом растворе; б) осмолярность раствора; в) осмотическое давление раствора при 37 °C.
(Ответ: ω(KCl) = 0.75%, cосм. = 0.3 моль/л, π = 773 кПа) 9. Какое количество теплоты выделится при сжигании 4.48 л метана (CH4),
если его стандартная энтальпия сгорания равна –875 |
кДж/моль. Запишите тер- |
||
мохимическое уравнение реакции. |
(Ответ: Q = 175 кДж) |
||
10.Не производя вычислений, установите знак изменения энтропии реак- |
|||
ции: 2 Н2S (газ) + 3 О2 (газ) |
2 SО2 (газ) + 2 H2O (ж). |
|
|
Определите, при каких температурах (высоких, низких, любых) возможно |
|||
самопроизвольное протекание этой реакции, если DH |
< 0. |
|
|
11. Запишите выражение для константы равновесия: 2NO2 (газ) |
N2O4 (газ), |
||
DH = –57 кДж. Как |
повлияет на состояние равновесия этой |
системы: |
|
а) повышение температуры; б) понижение давления.
12. Период полувыведения лекарственного препарата (реакция первого порядка) составляет15 часов. Какая масса препарата останется в организме через
30 часов после приема 200 мг лекарства? |
(Ответ: 50 мг) |
13. Напишите уравнения протолитических |
равновесий, определяющих |
кислотность в 0.01 M растворе молочной |
кислоты CH3CH(OH)COOH; |
pKa = 3.85. Качественно оцените характер среды и рассчитайте значение pH
данного раствора. |
(Ответ: 2.93) |
14. Напишите |
уравнения протолитических равновесий, определяющих |
кислотность в 0.01 M водном растворе NaHCO3, если для угольной кислоты
49
