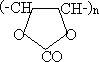
- •10. Полимеры
- •10.1. Методы получения полимеров
- •10.2. Строение полимеров
- •10.2.1.Форма и структура макромолекул полимеров
- •10.2.2. Кристаллическое состояние полимеров
- •10.2.3. Физические состояния аморфных полимеров
- •10.3. Свойства полимеров
- •10.4. Применение полимеров
- •10.4.1. Материалы, получаемые на основе полимеров
- •10.4.2. Областиприменения полимеров
- •10.5. Органические полимерные материалы
- •10.5.1. Полимеризационные термопластичные смолы
- •10.5.2. Термореактивные синтетические смолы
Кремнийорганические полимеры (КП) — это высокомолекулярные соединения, содержащие атомы кремния, углерода и др. элементов в элементарном звене макромолекулы. В зависимости от химического строения основной цепи КП делятся на 3 основные группы:
с неорганическими главными цепями макромолекул, которые состоят из чередующихся атомов кремния и др. элементов (О, N, S, Al, Ti, В и др.); при этом углерод входит лишь в состав групп, обрамляющих главную цепь;
с органонеорганическими главными цепями макромолекул, которые состоят из чередующихся атомов кремния и углерода, а иногда и кислорода;
с органическими главными цепями макромолекул (см. табл. 1).
Наиболее подробно изучены и широко применяются полиорганосилоксаны, а также полиметаллоорганосилоксаны и полиорганосилазаны.
В зависимости от строения главной полимерной цепи кремнийорганические полимеры, подобно другим полимерам, можно разделить на линейные, разветвленные, циклолинейные (лестничные) и сшитые (в т. ч. циклосетчатые).
Полиорганосилоксаны. Многие особенности механических и физико-химических свойств этих полимеров связаны с высокой гибкостью их макромолекул и относительно малым межмолекулярным взаимодействием. Высокая гибкость силоксановой цепи утрачивается при переходе от линейной структуры к лестничной.
Линейные и разветвленные полиорганосилоксаны с невысокой молярной массой — вязкие бесцветные жидкости. Высокомолекулярные линейные полиорганосилоксаны — эластомеры, а сшитые и разветвленные — эластичные или хрупкие стеклообразные вещества. Линейные, разветвленные и лестничные полимеры хорошо растворимы в большинстве органических растворителей (плохо — в низших спиртах). Полиорганосилоксаны устойчивы к действию большинства кислот и щелочей; разрыв силоксановой связи Si-O вызывают лишь концентрированные щелочи и концентрированная серная кислота.
Полиорганосилоксаны характеризуются высокой термостойкостью, обусловленной высокой энергией связи Si-O, а также отличными диэлектрическими характеристиками. Так, сшитый полидиметилфенилсилоксан при 20°С имеет тангенс угла диэлектрических потерь (1-2) Ч10-3, диэлектрическую проницаемость 3-3,5 (при 800 Гц), удельное объемное электрическое сопротивление 103 ТомЧм (1017омЧсм) и электрическую прочность 70-100 кв/мм при толщине образца 50 мкм.
Таблица 1. Основные типы линейных кремнийорганических полимеров
Название
Структура главной цепи
Полимеры с неорганическими главными цепями:
Полиорганосилоксаны
Полиэлементоорганосилоксаны*
Полиорганосилазаны
Полиорганосилтианы
Полиорганосиланы
Полиорганосилазоксаны
Полимеры с органонеорганическими главными цепями:
Полиорганоалкиленсиланы
Полиорганофениленсиланы
Полиорганоалкиленсилоксаны
Полиорганофениленалюмосилоксаны
Полимеры с органическими главными цепями:
Полиалкенилсиланы
—
* Если Э — металл, полимеры называются полиметаллоорганосилоксанами.
Механическая прочность полиорганосилоксанов невысока по сравнению с прочностью таких высокополярных полимеров, как, например, полиамиды.
Полиорганосилоксаны получают следующими методами.
1) Гидролитическая поликонденсация кремнийорганических соединений — важнейший промышленный метод синтеза КП Он основан на том, что многие функциональные группы, связанные с кремнием (алкокси-, ацилокси-, аминогруппы, галогены), легко гидролизуются, например:
R2SiC2+2H2O®R2Si (OH)2+2HCI.
Образующиеся органосиланолы немедленно вступают в поликонденсацию с образованием циклических соединений
nR2Si (OH)2®[—SiR2—O—] n+H2O,
которые затем полимеризуются по катионному или анионному механизму. В зависимости от функциональности мономеров образуются полимеры линейной, разветвленной, лестничной или сшитой структуры.
2) Ионная полимеризация циклических органосилоксанов. Применяется для синтеза каучуков с молярной массой ~600000 и более, а также лестничных и разветвленных полимеров.
3) Гетерофункциональная поликонденсация кремнийорганических соединений, содержащих различные функциональные группы, например:
n SiCl2+nR2Si (OCOCH3)2®Cl [—Si —О—SiR2— О—] nCOCH3+CH3COCl.
4) Реакция обменного разложения, при которой натриевые соли органосиланолов реагируют с органохлорсиланами или с галогенсодержащими солями металлов. Этот метод нашел практическое использование для синтеза полиметаллоорганосилоксанов.
Полиорганосилоксаны применяют в производстве различных электроизоляционных материалов (например, кремнийорганических лаков, полимерных компаундов), а также теплостойких пластмасс (в частности, стеклопластиков) и кремнийорганических клеев. Широкое применение в технике находят кремнийорганические каучуки и кремнийорганические жидкости.
Полиэлементоорганосилоксаны. Введение атомов металлов в полимерную силоксановую цепь существенно меняет физические и химические свойства полимеров. Полиалюмофенилсилоксан и полититанфенилсилоксан, содержащие 1 атом металла на 3-10 атомов кремния, не размягчаются при нагревании и имеют термомеханические кривые, типичные для сшитых полимеров, но сохраняют растворимость в органических растворителях. При введении пластификаторов (совола, минерального масла) эти полимеры приобретают текучесть при 120-150°С. Такое своеобразное сочетание свойств объясняется лестничной структурой макромолекул, обладающих большой жесткостью и потому имеющих температуру плавления значительно выше температуры разложения.
Связь Si—O—Э в полиметаллоорганосилоксанах более полярна, чем связь Si—O—Si, вследствие чего эти полимеры легче разлагаются под действием воды в присутствии кислот, чем полиорганосилоксаны.
При уменьшении содержания гетероэлемента в цепи полиэлементоорганосилоксаны приближаются по свойствам к полиорганосилоксанам, но влияние гетероатома на свойства полимера еще сказывается в том случае, когда на 100-200 атомов кремния приходится 1 гетероатом. Так, полибордиметилсилоксан с элементарным звеном при n=100-200 не вулканизуется перекисями в условиях, обычных для полидиметилсилоксанов, и сохраняет способность к самосклеиванию. Полибордиметилсилоксаны проявляют способность к упругим деформациям при кратковременном приложении нагрузки с одновременным сохранением пластических свойств при длительном действии нагрузки. При введении в полидиметилсилоксановые цепи титана в сочетании с некоторыми другими элементами, в частности, с фосфором, термоокислительная стабильность полимера значительно возрастает. Это явление наблюдается уже при содержании 1 атома Ti на 100-300 атомов Si. Основные методы получения полиэлементоорганосилоксанов — реакция обменного разложения и гетерофункциональная поликонденсация (см. выше).
Практическое применение находят:
полиборорганосилоксаны, которые используют для изготовления клеев и самосклеивающихся резин;
полиалюмоорганосилоксаны — теплостойкие материалы в прецизионном литье металлов, катализаторы полимеризации при получении полиорганосилоксанов, а также пленкообразующие для приготовления лаков, дающих термостойкие покрытия;
полититанорганосилоксаны — термостойкие материалы и герметики.
Полиорганосилазаны. Линейные полимеры — вязкие продукты, хорошо растворимые в органических растворителях, полимеры полициклической структуры — твердые бесцветные хрупкие вещества, имеющие температуру плавления от 150 до 320°С. Полиорганосилазаны устойчивы к действию воды в нейтральной и слабощелочной средах, но в кислой среде разлагаются; при нагревании со спиртом подвергаются алкоголизу.
Полимеры низкой молярной массы получают аммонолизом алкилхлорсиланов аммиаком или первичными аминами, например:
n (CH3)2SiCl2+(2n-1) NH3®H2N—Si (CH3)2[—NH—Si (CH3)2—] n-1NH2+2NH4CI.
Эта реакция сопровождается образованием циклических соединений. Полимеры с молярной массой до 5000 получают ионной полимеризацией органоциклосилазанов.
Полиорганосилазаны находят практическое применение как гидрофобизаторы для различных строительных материалов и тканей, а также в качестве отвердителей кремнийорганических полимеров, эпоксидных смол и полимерных компаундов.
Полиорганоалкиленсиланы. Эти полимеры обладают довольно высокой термостойкостью. Так как полимерная цепь полиорганоалкиленсиланов содержит только связи Si—C и С—С, они отличаются высокой гидролитической устойчивостью и стойкостью к действию щелочей и кислот.
Высокомолекулярные полимеры этого класса получают путем полимеризации силациклоалканов в присутствии металлоорганических катализаторов или взаимодействием гидросиланов с дивинилсиланами в присутствии H2PtCl6, органических перекисей или третичных аминов. Полиорганоалкиленсиланы пока не нашли практического применения из-за относительно высокой стоимости соответствующих мономеров.
Прочие полимеры. Полиорганосиланы отличаются невысокой химической и термоокислительной стойкостью, т. к. связь Si—Si при действии щелочей или окислителей легко разрывается с образованием силанольной группировки Si—ОН. Поэтому практическое значение полиорганосиланов является проблематичным.
Кремнийорганические полимеры с органическими главными цепями макромолекул имеют меньшее практическое значение, чем, например, полиорганосилоксаны, так как они не обладают высокой теплостойкостью, присущей последним.
Кремнийорганические жидкости (КЖ), силиконовые масла, органосилоксановые олигомеры или полимеры невысокой молярной массы способны сохранять текучесть в широком интервале температур. Наибольшее распространение получили КЖ с макромолекулами линейной (I) и разветвленной (II) структуры и блокированными концами, чаще всего — полидиметилсилоксановые (R=R=CH3), полидиэтилсилоксановые (R=R=C2H5) и полиметилфенилсилоксановые (R=CH3, R=C6H5) с молярными массами от нескольких сотен до 30 000.
Кремнийорганические жидкости по внешнему виду напоминают нефтяные масла. Они обладают очень ценными свойствами:
гидрофобностью;
высокой сжимаемостью;
физической и химической инертностью;
относительно малым изменением вязкости при изменении температуры;
стойкостью при высокой температуре даже в окислительной среде и т. д.
Коэффициент адиабатической сжимаемости при 30°С для полидиметилсилоксанов, имеющих вязкость 0,65 и 50 мм/сек, или сст, составляет соответственно 1,74Ч10-9м2/н (1,74Ч10-10см/дин) и 1,09Ч10-9м2/н (1,09Ч10-10см2/дин) [для этиленгликоля- 0,33Ч10-9м2/н (0,33Ч10-10см2/дин)]. При сжатии КЖ их вязкость заметно возрастает. КЖ обладают высокими диэлектрическими свойствами.
При нагревании полидиметилсилоксановых жидкостей на воздухе до 175°С они заметно не изменяются; при 200°С начинается окисление. Некоторые элементы (Cu, Pb, Se, Te) катализируют разложение силоксановой цепи. В инертной атмосфере термическая деструкция становится заметной только при температуре выше 250°С. Полиметилфенилсилоксаны начинают разлагаться на воздухе при 250°С, а в инертной атмосфере лишь при 300°С.
Кремнийорганические жидкости синтезируют теми же методами, что и прочие полиорганосилоксаны.
КЖ часто используют для гидрофобизации стекла, керамики, тканей, бумаги и др. материалов. Их применяют также в гидроприводах и гидравлических муфтах сцепления; при этом благодаря малой вязкости полидиметилсилоксанов можно почти вдвое снизить общую массу гидросистемы и уменьшить диаметр трубопроводов. Высоковязкие КЖ применяют в разнообразных демпфирующих устройствах. Их высокая сжимаемость позволяет создавать "жидкие пружины". Многие кремнийорганические жидкости служат смазочными маслами или основой для консистентных смазок, часто в сочетании с нефтяными или синтетическими органическими маслами. Такие смазки по стабильности реологических свойств в широком интервале температур превосходят нефтяные масла. КЖ часто используют в качестве жидких диэлектриков в трансформаторах, конденсаторах, некоторых деталях радиоэлектронного оборудования. Они могут служить также пеногасителями, антиадгезионными смазками для прессформ, жидкостями для глубоковакуумных диффузионных насосов. КЖ находят применение в составе кремов, лосьонов и губных помад. Общие свойства[править | править исходный текст]
Устойчив к действию воды, не реагирует с щелочами любой концентрации, с растворами нейтральных, кислых и основных солей, органическими и неорганическими кислотами, даже с концентрированной серной кислотой, но разлагается при действии 50%-ой азотной кислоты при комнатной температуре и под воздействием жидкого и газообразного хлора и фтора.
При комнатной температуре нерастворим и не набухает ни в одном из известных растворителей. При повышенной температуре (80 °C) растворим в циклогексане и четырёххлористом углероде. Под высоким давлением может быть растворён в перегретой до 180 °C воде.
Со временем, деструктурирует с образованием поперечных межцепных связей, что приводит к повышению хрупкости на фоне небольшого увеличения прочности. Нестабилизированный полиэтилен на воздухе подвергается термоокислительной деструкции (термостарению). Термостарение полиэтилена проходит по радикальному механизму, сопровождается выделением альдегидов, кетонов, перекиси водорода и др.
Полиэтилен низкого давления (ПЭНД), или высокой плотности (HDPE), применяется при строительстве полигонов переработки отходов, накопителей жидких и твёрдых веществ, способных загрязнять почву и грунтовые воды.[3]
Переработка[править | править исходный текст]
Полиэтилен (кроме сверхвысокомолекулярного) перерабатывается всеми известными для пластмасс методами, такими как экструзия, экструзия с раздувом, литьё под давлением, пневматическое формование. Экструзия полиэтилена возможна на оборудовании с установленным «универсальным» червяком.
Применение[править | править исходный текст]
Полиэтиленовая плёнка (особенно упаковочная, например, пузырчатая упаковка или скотч),
Тара (бутылки, банки, ящики, канистры, садовые лейки, горшки для рассады)
Полимерные трубы для канализации, дренажа, водо-, газоснабжения.
Электроизоляционный материал.
Полиэтиленовый порошок используется как термоклей[4].
Броня (бронепанели в бронежилетах)[5]
Корпуса для лодок[6], вездеходов, деталей технической аппаратуры, диэлектрических антенн, предметов домашнего обихода и др.;
Малотоннажная марка полиэтилена — так называемый «сверхвысокомолекулярный полиэтилен», отличающийся отсутствием каких-либо низкомолекулярных добавок, высокой линейностью и молекулярной массой, используется в медицинских целях в качестве замены хрящевой ткани суставов. Несмотря на то, что он выгодно отличается от ПЭНД и ПЭВД своими физическими свойствами, применяется редко из-за трудности его переработки, так как обладает низким ПТР и перерабатывается только литьём.
Утилизация[править | править исходный текст]
Переработка[править | править исходный текст]
Изделия из полиэтилена пригодны для переработки и последующего использования.
Сжигание[править | править исходный текст]
При нагревании полиэтилена на воздухе выше 120 °С возможно выделение в атмосферу летучих продуктов термоокислительной деструкции, содержащих уксусную кислоту, формальдегид (оказывает общетоксичное действие), ацетальдегид (вызывает раздражение слизистых оболочек верхних дыхательных путей, удушье, резкий кашель, бронхиты, воспаление легких), оксид углерода (вызывает удушье). Получение[править | править исходный текст]
Полипропилен получают полимеризацией пропилена в присутствии металлокомплексных катализаторов, например, катализаторов Циглера—Натта (например, смесь TiCl4 и AlR3):
nCH2=CH(CH3) → [-CH2-CH(CH3)-]n
Параметры, необходимые для получения полипропилена близки к тем, при которых получают полиэтилен низкого давления. При этом, в зависимости от конкретного катализатора, может получаться любой тип полимера или их смеси.
Полипропилен выпускается в виде порошка белого цвета или гранул с насыпной плотностью 0,4—0,5 г/см³. Полипропилен выпускается стабилизированным, окрашенным и неокрашенным.
Молекулярное строение[править | править исходный текст]
По типу молекулярной структуры можно выделить три основных типа: изотактический, синдиотактический и атактический. Изотактическая и синдиотактическая молекулярные структуры могут характеризоваться разной степенью совершенства пространственной регулярности. Стереоизомеры полипропилена существенно различаются по механическим, физическим и химическим свойствам. Атактический полипропилен представляет собой каучукоподобный материал с высокой текучестью, температурой плавления — около 80°С, плотностью — 850 кг/м3, хорошей растворимостью в диэтиловом эфире. Изотактический полипропилен по своим свойствам выгодно отличается от атактического, а именно: он обладает высоким модулем упругости, большей плотностью — 910 кг/м3, высокой температурой плавления — 165—170°С и лучшей стойкостью к действию химических реагентов. Стереоблокполимер полипропилена при исследовании с помощью рентгеновских лучей обнаруживает определенную кристалличность, которая не может быть такой же полной, как у чисто изотактических фракций, поскольку атактические участки вызывают нарушение в кристаллической решетке. Изотактический и синдиотактический образуются случайным образом;
Физико-механические свойства[править | править исходный текст]
В отличие от полиэтилена, полипропилен менее плотный (плотность 0,91 г/см3, что является наименьшим значением вообще для всех пластмасс), более твёрдый (стоек к истиранию), более термостойкий (начинает размягчаться при 140 °C, температура плавления 175 °C), почти не подвергается коррозионному растрескиванию. Обладает высокой чувствительностью к свету и кислороду (чувствительность понижается при введении стабилизаторов).
Поведение полипропилена при растяжении ещё в большей степени, чем полиэтилена, зависит от скорости приложения нагрузки и от температуры. Чем ниже скорость растяжения полипропилена, тем выше значение показателей механических свойств. При высоких скоростях растяжения разрушающее напряжение при растяжении полипропилена значительно ниже его предела текучести при растяжении.
Показатели основных физико-механических свойств полипропилена приведены в таблице:
Физико-механические свойства полипропилена
Плотность, г/см3 0,90—0,91
Разрушающее напряжение при растяжении, кгс/см² 250—400
Относительное удлинение при разрыве, % 200—800
Модуль упругости при изгибе, кгс 6700—11900
Предел текучести при растяжении, кгс/см² 250—350
Относительно удлинение при пределе текучести, % 10—20
Ударная вязкость с надрезом, кгс·см/см2 33—80
Твердость по Бринеллю, кгс/мм2 6,0—6,5
Физико-механические свойства полипропилена разных марок приведены в таблице:
Физико-механические свойства полипропилена различных марок
Показатели / марка 01П10/002 02П10/003 03П10/005 04П10/010 05П10/020 06П10/040 07П10/080 08П10/080 09П10/200
Насыпная плотность, кг/л, не менее 0,47 0,47 0,47 0,47 0,47 0,47 0,47 0,47 0,47
Показатель текучести расплава, г/10 мин ≤0 0,2—0,4 0,4—0,7 0,7—1,2 1,2—3,5 3—6 5—15 5—15 15—25
Относительное удлинение при разрыве, %, не менее 600 500 400 300 300 - - - -
Предел текучести при разрыве, кгс/см², не менее 260 280 270 260 260 - - - -
Стойкость к растрескиванию, ч, не менее 400 400 400 400 400 - - - -
Характеристическая вязкость в декалине при 135 °C, 100 мл/г - - - - - 2,0—2,4 1,5—2,0 1,5—2,0 0,5—15
Содержание изотактической фракции, не менее - - - - - 95 93 95 93
Содержание атактической фракции, не более - - - - - 1,0 1,0 1,0 1,0
Морозостойкость, °C, не ниже -5 -5 -5 - - - - - -
Химические свойства[править | править исходный текст]
Полипропилен - химически стойкий материал. Заметное воздействие на него оказывают только сильные окислители — хлорсульфоновая кислота, дымящая азотная кислота, галогены, олеум. Концентрированная 58%-ная серная кислота и 30%-ный пероксид водорода при комнатной температуре действуют незначительно. Продолжительный контакт с этими реагентами при 60 °C и выше приводит к деструкции полипропилена.
В органических растворителях полипропилен при комнатной температуре незначительно набухает. Выше 100 °C он растворяется в ароматических углеводородах, таких, как бензол, толуол. Данные о стойкости полипропилена к воздействию некоторых химических реагентов приведены в таблице.
Химическая стойкость полипропилена
Среда Температура, °C Изменение массы, % Примечание
Продолжительность выдержки образца в среде реагента 7 суток
Азотная кислота, 50%-ная 70 -0,1 Образец растрескивается
Натр едкий, 40%-ный 70 Незначительное
90
Соляная кислота, конц. 70 +0,3
90 +0,5
Продолжительность выдержки образца в среде реагента 30 суток
Азотная кислота, 94%-ная 20 -0,2 Образец хрупкий
Ацетон 20 +2,0
Бензин 20 +13,2
Бензол 20 +12,5
Едкий натр, 40%-ный 20 Незначительное
Минеральное масло 20 +0,3
Оливковое масло 20 +0,1
Серная кислота,80%-ная 20 Незначительное Слабое окрашивание
Серная кислота,98%-ная 20 >>
Соляная кислота, конц. 20 +0,2
Трансформаторное масло 20 +0,2
Вследствие наличия третичных углеродных атомов полипропилен более чувствителен к действию кислорода, особенно при воздействии ультрафиолета и повышенных температурах. Этим и объясняется значительно большая склонность полипропилена к старению по сравнению с полиэтиленом. Старение полипропилена протекает с более высокими скоростями и сопровождается резким ухудшением его механических свойств. Поэтому полипропилен применяется только в стабилизированном виде. Стабилизаторы предохраняют полипропилен от разрушения как в процессе переработки, так и во время эксплуатации. Полипропилен меньше, чем полиэтилен подвержен растрескиванию под воздействием агрессивных сред. Он успешно выдерживает стандартные испытания на растрескивание под напряжением, проводимые в самых разнообразных средах. Стойкость к растрескиванию в 20%-ном водном растворе эмульгатора ОП-7 при 50 °C для полипропилена с показателем текучести расплава 0,5—2,0 г/10 мин, находящегося в напряженном состоянии, более 2000 ч.
Полипропилен — водостойкий материал. Даже после длительного контакта с водой в течение 6 месяцев (при комнатной температуре) водопоглощение полипропилена составляет менее 0,5 %, а при 60ºС — менее 2 %.
Теплофизические свойства[править | править исходный текст]
Полипропилен имеет более высокую температуру плавления, чем полиэтилен, и соответственно более высокую температуру разложения. Чистый изотактический полипропилен плавится при 176 °C. Максимальная температура эксплуатации полипропилена 120—140ºС. Все изделия из полипропилена выдерживают кипячение, и могут подвергаться стерилизации паром без какого-либо изменения их формы или механических свойств.
Превосходя полиэтилен по теплостойкости, полипропилен уступает ему по морозостойкости. Его температура хрупкости (морозостойкости) колеблется от −5 до −15ºС. Морозостойкость можно повысить введением в макромолекулу изотактического полипропилена звеньев этилена (например, при сополимеризации пропилена с этиленом).
Показатели основных теплофизических свойств полипропилена приведены в таблице:
Теплофизические свойства полипропилена
Температура плавления, °C 160—170
Теплостойкость по методу НИИПП, °C 160
Удельная теплоёмкость (от 20 до 60ºС), кал/(г·°C) 0,46
Термический коэффициент линейного расширения (от 20 до 100 °C), 1/°C 1,1·10−4
Температура хрупкости, °C От −5 до −15
Электрические свойства[править | править исходный текст]
Показатели электрических свойств полипропилена приведены в таблице:
Электрические свойства полипропилена
Удельное объёмное электрическое сопротивление, Ом·см 1016—1017
Диэлектрическая проницаемость при 106 Гц 2,2
Тангенс угла диэлектрических потерь при 106 Гц 2·10−4—5·10−5
Электрическая прочность (толщина образца 1 мм), кВ/мм 30—40
Переработка[править | править исходный текст]
Основные способы переработки — формование методами экструзии, вакуум- и пневмоформования, экструзионно-выдувного, инжекционно-выдувного, инжекционного, компрессионного формования, литье под давлением.
Применение[править | править исходный текст]
Материал для производства плёнок (особенно упаковочных), мешков, тары, труб, деталей технической аппаратуры, пластиковых стаканчиков, предметов домашнего обихода, нетканых материалов, электроизоляционный материал, в строительстве для вибро- и шумоизоляции межэтажных перекрытий в системах «плавающий пол». При сополимеризации пропилена с этиленом получают некристаллизующиеся сополимеры, которые проявляют свойства каучука, отличающиеся повышенной химической стойкостью и сопротивлением старению. Для вибро- и теплоизоляции также широко применяется пенополипропилен (ППП). Близок по характеристикам к пенополиэтилену. Также встречаются декоративные экструзионные профили из ППП, заменяющие пенополистирол. Атактический полипропилен используют для изготовления строительных клеев, замазок, уплотняющих мастик, дорожных покрытий и липких пленок.
Поликарбонаты — группа термопластов, сложные полиэфиры угольной кислоты и двухатомных спиртов общей формулы (-O-R-O-CO-)n. Наибольшее промышленное значение имеют ароматические поликарбонаты, в первую очередь, поликарбонат на основе Бисфенола А, благодаря доступности бисфенола А, синтезируемого конденсацией фенола и ацетона.
Содержание [убрать]
1 Методы синтеза
2 Переработка
3 Российская номенклатура марок
4 Мировое производство
5 Применение
6 См. также
7 Примечания
Методы синтеза[править | править исходный текст]
Синтез поликарбоната на основе бисфенола А проводится двумя методами: методом фосгенирования бисфенола А и методом переэтерификации в расплаве диарилкарбонатов бисфенолом А.
В случае переэтерификации в расплаве в качестве исходного сырья используется дифенилкарбонат, реакцию проводят в присутствии щелочных катализаторов (метилат натрия), температуру реакцинной смеси повышают ступенчато от 150 до 300 °C, реакцию проводят в вакуумированных реакторах периодического действия при постоянной отгонке выделяющегося в ходе реакции фенола. Полученный расплав поликарбоната охлаждают и гранулируют. Недостатком метода является относительно небольшая молекулярная масса (до 50 КДа) получаемого полимера и его загрязнённость остатками катализатора и продуктов термодеструкции бисфенола А.
Фосгенирование бисфенола А проводят в растворе хлоралканов (обычно — хлористого метилена CH2Cl2) при комнатной температуре, существует две модификации процесса — поликонденсация в растворе и межфазная поликонденсация:
Polycarbonatsynthese.svg
При поликонденсации в растворе в качестве катализатора и основания, связывающего выделяющийся хлороводород используют пиридин, гидрохлорид пиридина, образующийся в ходе реакции, нерастворим в хлористом метилене и по завершении реакции его отделяют фильтрованием. От остаточных количеств пиридина, содержащегося в реакционной смеси, избавляются отмыванием водным раствором кислоты. Поликарбонат высаждают из раствора подходящим кислородсодержащим растворителем (ацетоном и т. п.), что позволяет частично избавиться от остаточных количеств бисфенола А, осадок сушат и гранулируют. Недостатком метода является использование достаточно дорогого пиридина в больших количествах (более 2 молей на моль фосгена).
В случае фосгенирования в условиях межфазного катализа поликонденсация проводится в два этапа: сначала фосгенированием бисфенолята А натрия получают раствор смеси олигомеров, содержащих концевые хлорформиатные -OCOCl и гидроксильные -OH группы, после чего проводят поликонденсацию смеси олигомеров в полимер.
Переработка[править | править исходный текст]
При переработке поликарбонатов применяют большинство методов переработки и формовки термопластичных полимеров: литьё под давлением (производство изделий), выдувное литьё (разного рода сосуды), экструзию (производство профилей и плёнок), формовку волокон из расплава. При производстве поликарбонатных плёнок также применяется формовка из растворов — этот метод позволяет получать тонкие плёнки из поликарбонатов высокой молекулярной массы, формовка тонких плёнок из которых затруднена вследствие их высокой вязкости. В качестве растворителя обычно используют метиленхлорид.
Российская номенклатура марок[править | править исходный текст]
Обозначение поликарбонатов различных марок имеет вид
ПК — метод переработки, ПТР — модификаторы в составе,
при этом:
ПК — поликарбонат
Рекомендованный метод переработки:
Л — переработка литьём под давлением
Э — переработка экструзией
Модификаторы в составе композиции:
Т — термостабилизатор
С — светостабилизатор
О — краситель
ПТР — максимальный показатель текучести расплава: 7 или 12 или 18 или 22.
В Советском Союзе до начала 1990-х годов выпускался поликарбонат «дифлон»[1], с 2009 года запущен в эксплуатацию цех завода ОАО «КазаньОргСинтез» по производству отечественного поликарбоната новой номенклатурной линейки:
ПК-1 — высоковязкая марка, ПТР=1÷3,5, в дальнейшем заменён на ПК-ЛЭТ-7, в настоящее время РС-003 или РС-005;
ПК-2 — средневязкая марка, ПТР=3,5÷7, в дальнейшем заменён на ПК-ЛТ-10, в настоящее время РС-007;
ПК-3 — низковязкая марка, ПТР=7÷12, в дальнейшем заменён на ПК-ЛТ-12, в настоящее время РС-010;
ПК-4 — чёрный термостабилизированный, в настоящее время ПК-ЛТ-18-ОМ чёрного цвета;
ПК-5 — медицинского назначения, в настоящее время используются марки медицинского назначения импортных материалов;
ПК-6 — светотехнического назначения, в настоящее время по светопропусканию подходят практически любые марки импортных и отечественных материалов;
ПК-НКС — стеклонаполненный, в дальнейшем заменён на ПК-ЛСВ-30, в настоящее время ПК-ЛСТ-30;
ПК-М-1 — повышенные антифрикционные свойства, в настоящее время используются специальные марки импортных материалов;
ПК-М-2 — повышенная стойкость к растрескиванию и самозатухаемость, аналогов по настоящее время — нет;
ПК-М-3 — может эксплуатироваться при крайне низких температурах, в настоящее время используются специальные марки импортных материалов;
ПК-С3, ПК-ОД — самозатухающие с повышенной стойкостью к горению (категория горючести ПВ-0), в настоящее время ПК-ТС-16-ОД;
ПК-ОМ, ПК-ЛТ-12-ОМ, ПК-ЛТО-12 — непрозрачные и полупрозрачные материалы различных цветов, в настоящее время ПК-ЛТ-18-ОМ.
Мировое производство[править | править исходный текст]
Поликарбонаты являются крупнотоннажными продуктами органического синтеза, мировые производственные мощности в 2006 года составляли более 3 млн тонн в год. Основные производители поликарбоната (2006)[2]:
Производитель Объём производства Торговые марки
Bayer Material Science AG 900 000 т/год Makrolon, Apec, Bayblend, Makroblend[3]
Sabic Innovative Plastics 900 000 т/год Lexan
Samyang Busines Chemicals 360 000 т/год Trirex[4]
Dow Chemical / LG DOW Polycarbonate 300 000 т/год Calibre[5]
Teijin 300 000 т/год Panlite[6]
Всего 3 200 000 т/год
Применение[править | править исходный текст]
Сотовый поликарбонат
Благодаря сочетанию высоких механических и оптических качеств монолитный пластик также применяется в качестве материала при изготовлении линз, компакт-дисков и светотехнических изделий; листовой ячеистый пластик («сотовый поликарбонат») применяется в качестве светопрозрачного материала в строительстве. Также материал используется там, где требуется повышенная теплоустойчивость. Это могут быть компьютеры, очки, светильники, фонари и т. д.
Благодаря высокой прочности и ударной вязкости (250—500 кдж/м2) применяются в качестве конструкционных материалов в различных отраслях промышленности, используются при изготовлении защитных шлемов для экстремальных дисциплин вело- и мотоспорта. При этом для улучшения механических свойств применяются и наполненные стекловолокном композиции.
А. Органические полимеры.
1. Гомоцепные полимеры.
Предельные углеводороды
|
1 |
Полиэтилен (полиметилен) – (ПЭх) |
(- CH2– CH2-)n |
|
2 |
Полипропилен |
(- CH2– CH(CH3)-)n |
|
3 |
Полибутилен – (ПБ) |
(-CH2-CH(C2H5)-)n |
|
4 |
Полиизобутилен – (ПИБ) |
(-CH2-C(CH3)2-)n |
|
5 |
Полистирол (поливинилбензол) - ПС |
(-CH2-CH(C6H5)-)n |
|
6 |
Поли-a-метилстирол |
(-CH2-C(CH3)(C6H5)-)n |
Галогенпроизводные предельных углеводородов.
|
7 |
Поливинилхлорид - ПВХ |
(-CH2-CHCl-)n |
|
8 |
Поливинилиденфторид |
(-CH2-CF2-)n |
|
9 |
Поливиниленфторид (полиметиленфторид) |
(-CHF-CHF-)n |
|
10 |
Политетрафторэтилен (тефлон) - ПТФЭ |
(-CF2-CF2-)n |
Спирты и их эфиры
|
11 |
Поливиниловый спирт - ПВС |
(-CH2-CH(OH-)n |
|
|
Поливинилацетат - ПВА |
(-CH2-CH-)n OCOCH3 |
|
13 |
Поливиниленкарбонат |
|
Ацетали
|
|
Поливинилформаль |
(-CH2-CH-CH2-CH-)n О - CH2-O |
|
|
Поливинилбутираль |
(-CH2-CH-CH2-CH-)n O__CH__O C3H7 |
Альдегиды
|
|
Полиакролеин |
(-CH2-CH-)n CHO |
Амины
|
17 |
Поливиниламин |
(-CH2-CH(NH2)-)n |
|
18 |
Поли-N-винилпирролидон |
|
|
19 |
Поли-4-винилпиридин |
|
Кислоты и их производные
|
|
Полиакриловая кислота - ПАК |
(-CH2-CH-)n COOH |
|
|
Полиметакриловая кислота - ПМАК |
(-CH2-C(CH3)-)n СООН |
|
|
Полиметилметакрилат - ПММА |
(-CH2-C(CH3)-)n COOCH3 |
|
|
Полиметилакрилат - ПМА |
(-CH2-CH-)n COOCH3 |
|
|
Полибутилметакрилат - ПБМА |
(-CH2-C(CH3)-)n COOC4H9 |
|
|
Полиакриламид |
(-CH2-CH-)n CONH2 |
|
|
Полиакрилонитрил – ПАН |
(-CH2-CH-)n CN |
Непредельные углеводороды и их производные
|
27 |
1,4-полибутадиен |
(-СН2-CН=CH-CH2-)n |
|
|
|
|
|
|
1,4-цис-полиизопрен (натуральный каучук – НК) 1,4-транс-полиизопрен (гуттаперча) |
(-CH2-C=CH-CH2-)n CH3 |
Галогенпроизводные непредельных углеводородов
|
29 |
Полихлоропрен |
(-CH2-CCl =CH-CH2-)n |
Ароматические углеводороды
|
30 |
Полиалкилфенилен |
|
|
31 |
Полиметиленоксифенилены (фенолформальдегидные полимеры) линейный – “но-волак” |
|
|
32 |
Пространственные: (получа-ют с избытком формальде-гида) форполимер – резол; конечный продукт отверж-дения - резит |
|
Полимеры с сопряженными связями
|
33 |
Полиацетилен (поливинилем) |
(- CH = CH-)n |
|
34 |
Полифенилен |
|
П. Гетероцепные полимеры
Кислородсодержащие полимеры
|
1 |
Полиэтиленоксид (R=R’=H) и его производные |
(-CH2-CRR’-O-)n |
|
2 |
Полиформальдегид (полиацеталь) |
(-CH2-O-)n |
|
3 |
Полиэтилентерефталат- (полиэтилентерефталат, лавсан)сложный полиэфир - ПЭТФ |
(-O-(CH2)2-OOC-C6H4-CO-)n |
Азотсодержащие полимеры
|
4 |
Полигексаметиленадипинамид(полиамид-6,6) |
(-NH-(CH2)6-NHCO-(CH2)4-CO-)n |
|
5 |
Поликапроамид (полиамид-6) |
(-NH-(CH2)5-CO-)n |
|
6 |
Полипарабензамид |
(-NH-(C6H4)-CO-)n |
|
7 |
Полифталимид (полимид) |
(-CO-C6H4-CO-NR’-R-NR-)n |
|
8 |
Полиуретаны |
(-CO-NH-R-NH-COO-R’-O-)n |
|
9 |
Полинитрилы |
(-CR=N-)n |
Серосодержащие полимеры
|
10 |
Полиалкиленсульфид |
(-(CH2)x-S-)n |
|
11 |
Полиалкиленсульфоны |
(-(CH2)x-S-)n |
Б. Элементоорганические полимеры
|
12 |
Полидиметилсилоксан |
(-Si(CH3)2-O-)n |
|
13 |
Полиалюмоксан |
(-AlR-O-)n |
|
14 |
Полифосфазен |
(-PRR’= N -)n |
В. Неорганические полимеры
|
15 |
Полифосфонитрилхлорид |
(-PCl2 = N-)n |
|
16 |
Пластическая сера |
(-S-)n |
Г. Биополимеры
10. Полимеры
Полимеры– высокомолекулярные соединения, которые характеризуются молекулярной массой от нескольких тысяч до многих миллионов. Молекулы полимеров, называемые макромолекулами, состоят из большого числа повторяющихся звеньев.
Вследствие большой молекулярной массы макромолекул полимеры приобретают специфические свойства и их выделяют в особую группу соединений.
Отдельную группу составляют олигомеры, которые по значению молекулярной массы занимают промежуточное положение между низкомолекулярными и высокомолекулярными соединениями.
Различают неорганические, органические и элементорганические полимеры. Органические полимеры подразделяются на природные и синтетические. Мы рассматриваем органические синтетические полимеры.
10.1. Методы получения полимеров

![]() 1.Полимеризация–
реакция образования полимеров путем
последовательного присоединения молекул
низкомолекулярного вещества (мономера).
Побочных продуктов не образуется. В
качестве мономеров используются
соединения с кратными связями С º С, С ºN, С
= С, С = О, С =N, либо
соединения с циклическими группировками,
способными раскрываться, например
1.Полимеризация–
реакция образования полимеров путем
последовательного присоединения молекул
низкомолекулярного вещества (мономера).
Побочных продуктов не образуется. В
качестве мономеров используются
соединения с кратными связями С º С, С ºN, С
= С, С = О, С =N, либо
соединения с циклическими группировками,
способными раскрываться, например
В процессе полимеризации происходит разрыв кратных связей или раскрытие циклов у мономеров и возникновение химических связей между группами с образованием макромолекул:
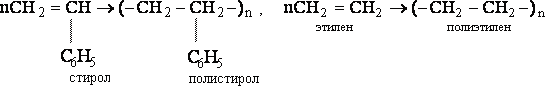
По числу участвующих мономеров различают: гомополимеризацию (один вид мономера) исополимеризацию (два и более видов мономеров).
Поликонденсация – синтез полимера с несколькими функциональными группами, сопровождающийся образованием низкомолекулярных продуктов (H2O, NH3, HClи др.).
Элементные составы полимеров и исходных веществ не совпадают, за счет образования низкомолекулярных продуктов.
Линейная поликонденсация:
![]()
® NH2 - (CH2)5 - CO - NH - (CH2)5 - COOH + NH2 - (CH2)5 - COOH ®
® NH2 - (CH2)5 - CO - NH - (CH2)5 - CO - NH -(CH2)5 - COOH + H2O и т.д.
Конечный продукт -капрон (поли - ε -капроамид)
[ - CO - NH - (CH2)5 -]n
Трехмерная поликонденсация:
|
|
NH2-CO-NH2+CH2O ® NH2-CO-NH-CH2OH Мочевина формальдегид |
|
|
NH2-CO-NH-CH2OH+CH2O ® CH2OH-NH-CO-NH-CH2OH 2CH2OH-NH-CO-NH-CH2OH ® ®H2O+CH2OH-NH-CO-NH-CH2-O-CH2-NH-CO-NH-CH2OH | ||
|
|
|
|
на 1 этапе синтезируется олигомер линейной структуры
[- CH2 - NH - CO - NH - CH2 - O]n
на 2 этапе при нагревании в кислой среде происходит дальнейшая поликонденсация олигомера с выделением CH2Oи возникновением сетчатой структуры. Такой сетчатый полимер невозможно превратить в исходное состояние, он не обладает термопластичными свойствами и называетсятермореактивным полимером.
Поликонденсация идет по ступенчатому механизму, при этом промежуточные продукты являются стабильными, т.е. поликонденсация может остановиться на любой стадии. ОбразующиесяH2O, HCl, NH3(низкомолекулярные) могут взаимодействовать с продуктами поликонденсации, вызывая их расщепление (гидролиз, аминолиз и др.), поэтому низкомолекулярные продукты приходится удалять из реакционной среды.
Методом поликонденсации получают примерно четвертую часть выпускаемых полимеров (капрон - поликапроамид, найлон - полигексаметиленадипинамин, полиуретаны, фенолформальдегидные смолы и мочевиноформальдегидные).