
- •3. Основные понятия о реакционной способности органических молекул
- •1. Концепция теории мезомерии.
- •2. Концепция теории резонанса (Полинг, 1928 г.).
- •3. Делокализованное π-облако изображается пунктиром (в цикле – сплошной линией).
- •4. Классификация химических реакций и промежуточных частиц
- •Стабилизация интермедиатов.
- •Примеры построения названий по систематической номенклатуре
- •7. Кислотные и основные свойства органических соединений
- •Кислотные и основные функции веществ
- •Кислотность и основность по Бренстеду-Лоури.
- •Примеры.
- •Кислотность спиртов.
- •Сольватация аминов.
- •Кислоты и основания Льюиса.
- •Жесткие и мягкие кислоты и основания по Пирсону (жмко).
- •8. Углеводороды
- •8.1 Алканы
- •5. Воздействие анаэробных бактерий на растительные остатки:
- •6.1 Гидролиз карбидов:
- •7.1 Гидрирование алкенов:
- •7.2 Гидрирование алкадиенов:
- •7.3 Гидрирование алкинов:
- •1. Реакции замещения атомов водорода при взаимодействии с активными радикалами.
- •1.1.1 Фтор:
- •1.1.3 Бром:
8. Углеводороды
8.1 Алканы
Алканы – простейший класс органических соединений, не содержащих какой-либо функциональной группы. Алканы отвечают общей формуле – СnН2n+2. Для неразветвленных (нормальных) алканов с длиной цепочкой она может быть представлена следующим образом:
Н–(СН2)n–H
Номенклатура алканов. Простейшим соединением ряда алканов является метан СН4. Для названия алканов используют следующие номенклатуры:
тривиальную;
рациональную;
систематическую.
Тривиальная. Первые четыре представителя с неразветвленной цепью имеют тривиальные названия:
метан (корень «мет» обозначает группировку, содержащую один атом углерода, первым таким веществом в истории химии был метиловый спирт (древесный спирт, метанол) от гр. methy –вино, hile – лес);
этан, содержащий группировку из двух атомов углерода (от гр. aither – небесная субстанция, улетающая к небесам) дух эфира, летучий газ);
пропан – трехатомная группировка (от гр. protos – первый, pion – жир);
бутан – черырехатомная группировка (от лат. butyron – масло).
Названия последующих членов ряда, начиная с пентана, образуются от греческих числительных, указывая число атомов углерода в цепи, и окончания "ан".
Рациональная. В основу названия положен простейший представитель – метан, остальные предельные углеводороды рассматривают как его производные. Перед названием прототипа перечисляют радикалы (табл. 8) в порядке увеличения числа углеродных атомов.
Систематическая (заместительная, международная, ИЮПАК). По заместительной номенклатуре предельные углеводороды рассматриваются как производные линейных углеводородов, у которых один или несколько атомов водорода замещены на алкильные радикалы.
Изомерия. Для алканов характерны следующие виды изомерии:
Структурная:
скелетная.
Пространственная:
конформационная;
оптическая.
Способы получения.
Промышленные методы:
1. Получение из нефти. Алканы С1 – С40 является основной составляющей нефти, где наряду с предельными углеводородами содержатся циклоалканы, ароматические углеводороды, сернистые соединения и другие компоненты. В зависимости от числа атомов углерода алканы, содержащиеся в нефти, подразделяются на следующие группы:
газообразные алканы состава С1 – С4 содержатся в газовой фракции нефти;
жидкие алканы от С5 до С10 входят в состав бензиновых фракций, выделены в чистом виде все 5 изомеров гексана, 7 из 9 изомерных гептанов, 16 из 18 изомеров октана и 24 из 35 теоретически возможных изомеров нонана;
углеводороды состава С11 – С20 содержатся в средних фракциях нефти (180–350 оС), причем содержание нормальных алканов снижается с увеличением молекулярной массы;
твердые алканы С16 и выше находятся в высококипящих фракциях (350 – 500 оС), их называют в зависимости от состава и температуры плавления парафинами (в основном алканы с Тпл= 45–65 оС) и церезинами (разветвленные алканы).
2. Природный газ. Природный газ состоит на 75% из СН4, 15% СН3–СН3, 5% СН3–СН2–СН3, остальное составляют высшие алканы и другие соединения. Природный газ используют как топливо и сырье для химической промышленности.
3. Гидрогенизация угля. (400–500 оС, 30 МПа, Ф. Бергиус, 1925 г.). катализатор – оксиды и сульфиды молибдена, никеля, кобальта:
С+Н2
![]() СН4
СН4
4. Метод Фишера – Тропша. Каталитическое гидрирование СО и СО2 обычно дает метан. В качестве катализатора используют никель (П. Сабатье, И. Сандеран, 1902 г.):
СO+3Н2
![]() СН4+H2O
СН4+H2O
СO2+4Н2
![]() СН4+2H2O
СН4+2H2O
Процесс каталитического гидрирования СО протекает в зависимости от применяемого катализатора и температуры. В основном образуются низкомолекулярные неразветвленные алканы (Ф. Фишер, Х. Тропш 1913 – 1926 г.):
СO+3Н2
![]() СН4+H2O
СН4+H2O
В последующие годы метод был усовершенствован: изменен катализатор, давление и температура реакции (Ф. Фишер, Х. Пихлер 1936 – 1941 г.). В настоящее время методом Фишера – Тропша могут быть получены моторные топлива и отдельные углеводороды (алканы, циклоалканы, арены). В основе реакции лежит сорбция СО поверхностью катализатора в результате чего образуются карбонилы кобальта. Водород присоединяется к сорбированному оксиду углерода, образуя карбены и метильные радикалы. Карбен может внедрятся по связи Со – СН3, что приводит к росту углеродной цепи:
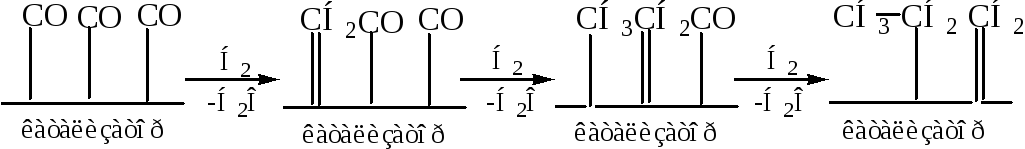
В качестве побочных продуктов могут образовываться кислородсодержащие соединения (спирты, альдегиды).
