
БХ Экзамен 2021
.pdfрезультате чего кости становятся болезненными, мягкими и легко деформируются.
3. Гиповитаминоз витамина Е (токоферола):
-бесплодие;
-гемолитическая анемия из-за окисления мембран эритроцитов;
-поражение нервной системы, атаксия, мышечная дистрофия.
Причиной гиповитаминоза Е является нарушение переваривания, всасывания и транспорта липидов.
4. Гиповитаминоз витамина К (нафтохинона):
Нарушение синтеза и модификации факторов свертывания крови и, как следствие, снижение свертываемости крови и кровотечения.
Наиболее частыми причинами гиповитаминоза К являются нарушения всасывания липидов и самого витамина, а также длительный прием антибиотиков, подавляющих микрофлору кишечника, или средств для
лечения тромбозов – антивитаминов К.
5. Гипо(а)витаминоз витамина В1 (тиамина):
Основной признак недостаточности витамина В1 – это полиневрит, в основе которого лежат дегенеративные изменения нервов. Вначале развивается болезненность вдоль нервных стволов, затем – потеря кожной чувствительности, и наступает паралич (бери-бери).
Также одним из признаков недостаточности или полного отсутствия витамина В1 является нарушение сердечной деятельности (нарушении сердечного ритма, увеличении размеров сердца и появление болей в области сердца).
Помимо вышеперечисленного могут встречаться следующие проявления: нарушения секреторной и моторной функций ЖКТ; снижение кислотности желудочного сока; потеря аппетита; атония кишечника.
6. Гипо(а)витаминоз витамина В2 (рибофлавина):
В первую очередь страдают высокоаэробные ткани – эпителий кожи и слизистых. Проявляется как сухость ротовой полости, губ и роговицы; хейлит, т.е. трещины в уголках рта и на губах, глоссит (воспаление языка, «фуксиновый язык»), шелушение кожи в районе носогубного треугольника, мошонки, ушей и шеи, конъюнктивит и блефарит. Сухость конъюнктивы и ее воспаление ведут к компенсаторному увеличению кровотока в этой зоне и улучшению снабжения ее кислородом, что проявляется как васкуляризация роговицы. Кроме того, при авитаминозе В2 развиваются общая мышечная слабость и слабость сердечной мышцы.
7. Гипо(а)витаминоз витамина В3 (пантотеновой кислоты):
- |
дерматиты; |
- |
поражения слизистых оболочек; |
- |
дистрофические изменения желез внутренней секреции; |
- |
нервной системы (невриты, параличи); |
- |
депигментация волос. |
8. Гипо(а)витаминоз витамина В5 (никотиновой кислоты, никтоинамида): Недостаток витамина РР –
|
заболевание пеллагра (шершавая кожа). Проявляется как «синдром трех Д»: |
- |
деменция (нервные и психические расстройства, слабоумие); |
- |
дерматиты (фотодерматиты); |
- |
диарея (расстройство пищеварения). |
9. Гипо(а)витаминоз витамина В6 (пиридоксина):
-повышенная возбудимость ЦНС, судороги (из-за недостатка синтеза нейромедиатора γ- аминомасляной кислоты ГАМК);
-полиневриты;
-пеллагроподобные дерматиты;
-эритемы и пигментация кожи;
-анемии.
10. Гипо(а)витаминоз витамина В9 (фолиевой кислоты):
Нарушается процесс синтеза пуриновых нуклеотидов и тимина, а, следовательно, и биосинтеза ДНК в клетках костного мозга, в которых в норме осуществляется эритропоэз. При этом клетки не теряют способности расти, но в них происходит нарушение синтеза ДНК с остановкой деления, и это приводит к образованию мегалобластов (крупных клеток) и мегалобластической анемии. Лейкопения присутствует по той же причине.
Антивитамины фолиевой кислоты: амино- и аметоптерины, сульфаниламиды, блокирующие реакции, связанные с переносом и использованием одноуглеродного радикала в синтезе нуклеиновых и других соединений. Эти вещества используют при лечении бактериальных инфекций (сульфаниламиды) и для подавления роста опухолевых клеток.
11. Гипо(а)витаминоз витамина В12 (кобаламина):
Макроцитарная (мегалобластная) анемия, при которой снижено количество эритроцитов и концентрации
гемоглобина в крови. Она возникает чаще у пожилых, но может быть и у детей. Непосредственной причиной анемии является потеря фолиевой кислоты (В9) клетками при недостаточности витамина В12 и, как следствие, замедление деления клеток из-за снижения ДНК.
Анемия при отсутствии кобаламина (в отличие от недостаточности фолиевой кислоты) сопровождается нарушением деятельности нервной системы из-за накопления промежуточных продуктов окисления жирных кислот с нечетным числом атомов углерода.
12. Авитаминоз витамина Н (биотина):
Себорея – у человека развиваются явления специфического дерматита, характеризующегося покраснением и шелушением кожи, а также обильной секрецией сальных желёз.
13. Гиповитаминоз витамина С (аскорбиновой кислоты):
-нарушение иммунитета, особенно легочного;
-общая слабость, быстрая утомляемость;
-похудание;
-одышка;
-отек нижних конечностей.
Снижается всасываемость железа в кишечнике, что вызывает снижение синтеза гема и гемоглобина и, как следствие, железодефицитную анемию.
Авитаминоз С:
Цинга – нарушение синтеза коллагена и протеогликанов соединительной ткани:
-сосуды становятся хрупкими и проницаемыми, что служит причиной мелких точечных кровоизлияний под кожу – так называемых петехий;
-часто отмечаются кровоизлияния и кровотечения во внутренних органах и слизистых оболочках;
-кровоточивость десен;
-дегенеративные изменения со стороны одонтобластов и остеобластов приводят к развитию кариеса, расшатыванию, разламыванию, а затем и выпадению зубов;
-отеки нижних конечностей и боли при ходьбе
Антивитамины
-любые вещества, вызывающие снижение или полную потерю биологической активности витаминов независимо от механизма их действия 1)Специфические -соединения, имеющие структуру, сходную со строением нативного витамина и работающие по принципу
конкурентного ингибирования (сульфаниламидные препараты)
Они встраиваются вместо витамина в кофермент, но коферментные функции не выполняют Антивитамины вступают с витаминами в конкурентные отношения в соответствующих биохимических реакциях обмена веществ. Они частично или полностью выключают витамины из обменных реакций организма.
•Кумарины – антивитамины витамина К. Оказывают противосвертывающее действие. Применяется для профилактики и лечения тромбозов при различных заболеваниях.
•Изониазид – антивитамин витамина РР. Применяется для лечения и профилактики туберкулеза.
•Парааминобензойная кислота (ПАБК) является витамином роста для тех бактерий, в клетках которых она служит
основой для образования фолиевой кислоты. Сульфаниламиды являются структурным аналогом ПАБК. 2)Неспецифические-вещества, вызывающие модификацию или разрушение химической природы витаминов, затрудняющие их всасывание, транспорт, что сопровождается снижением или потерей биологического эффекта незаменимых пищевых факторов (авидин, аскорбиназа) ,участвуют в биодеградации витаминов
Механизмы действия
Некоторые антивитамины обладают антимикробной активностью и при-меняются в качестве химиотерапевтических средств(сульфаниламидные препараты являются структурными аналогами парааминобензойной кислоты, используемой бактериями для синтеза необходимой для их жизнедеятельно-сти фолиевой кислоты; сульфаниламид, вытесняющий парааминобензойную кислоту из комплекса с ферментом, способствует, таким образом, снижению бактерий и их гибели. Аминоптерин и аметоптерин (также антивитамины фолиевой кислоты) тормозят синтез белка и нуклеиновых кислот в клетках и применяются для лечения больных с некоторыми злокачественными новообразованиями.
Витаминоподобные соединения
1.Синтезируются в организме человека, но синтез не покрывает потребностей
2.Более низкая биологическая активность по сравнению с витаминами->потребность выше по массе
3.Могут использоваться в качестве энергетического или пластического материала
(на-пример, холин участвует в построении мембран, а полиненасыщенные жирные кислоты могут как входить в состав биомембран, так и использоваться в качестве источников энергии)
4. Организм человека чувствителен как к избытку, так и к недостатку витаминоподобных соединений, однако характерной клинической картины не наблюдается
Жирорастворимые F (полиненасыщенные жирные кислоты, ПНЖК) Коэнзим Q (убихинон)
Пирролохинолинхинон (PQQ, В14)
Водорастворимые Липоевая кислота (N)
Пангамовая кислота (В15) Оротовая кислота (В13) Инозитол (В8)
Холин (В4) Карнитин (Вт, В11)
Витамин U (S-метилметионин) Парааминобензойная кислота (ПАБК, В10
36.МИНЕРАЛЬНЫЕ ВЕЩЕСТВА ПИЩИ, ИХ ЗНАЧЕНИЕ. РЕГИОНАЛЬНЫЕ ПАТОЛОГИИ, СВЯЗАННЫЕ С НЕДОСТАТОЧНОСТЬЮ МИКРОЭЛЕМЕНТОВ В ПИЩЕ И ВОДЕ (ПРИМЕРЫ).
Роль минеральных веществ в процессах жизнедеятельности:
Входят в состав костной, зубной ткани;
Входит в состав витаминов (кобальт – B12)
Являются активаторами ферментов;
Регулируют осмотическое давление, кислотно-основное состояние.
НАТРИЙ
Создание условий для возникновения мембранного потенциала и мышечных сокращений;
Поддержание осмотической концентрации крови;
Поддержание кислотно-щелочного баланса;
Нормализация водного баланса;
Обеспечение мембранного транспорта и т.д.
Нарушения обмена:
1.Гипернатриемия (развивается синдром, обусловленный гипергидратацией организма) возникает: - Повышенном поступлении с пищей; - Паренхиматозном нефрите;
- Врожденной сердечной недостаточности; - Первичном и вторичном гиперальдостеронизме.
2.Гипонатриемия (сопровождается дегидратацией организма) возникает при:
-Пониженном поступлении с пищей;
-Гипоальдостеронизме.
КАЛИЙ
Поддерживает функционирование клеточных мембран;
Поддержание кислотно-щелочного баланса;
Нормализация водного баланса;
Принимает участие в передаче нервных импульсов и т.д.
Нарушения обмена:
1.Гиперкалиемия возникает при:
-Повышенном поступлении с пищей;
-Острой почечной недостаточности;
-Гипоальдостеронизме.
2. Гипокалиемия возникает при:
-Пониженном поступлении с пищей;
-Введении больших доз гормонов коркового вещества надпочечников - Гиперальдостеронизм.
КАЛЬЦИЙ
Принимает активное участие в процессах нервно-мышечной возбудимости;
Принимает участие в процессах мышечного сокращения;
Принимает участие в процессах свертывания крови;
Образует структурную основу костного скелета;
Влияет на проницаемость клеточных мембран, работу ионных насосов и т.д.
1.Гиперкальциемия имеет место при:
-Гиперпаратиреозе;
-Злокачественных опухолях с метастазированием в кости;
-Гипервитаминозе Д;
-Лейкозах;
-Сердечной недостаточности;
-Акромегалии и других поражениях.
Последствия:
-Снижение нервно-мышечной возбудимости;
-Повышение артериального давления;
-Тошнота, рвота, снижение массы тела, язва желудка, панкреатит;
-Ролиурия, полидипсия, дегидратация.
2.Гипокальциемия возникает при:
-Тяжелых формах рахита;
-Остеомаляции;
-Хронических заболеваниях почек;
-Черепно-мозговых травмах;
-Хроническом гипопаратиреозе;
-Патологическом течение беременности.
Последствия:
-Повышение нервно-мышечной возбудимости;
-Понижение артериального давления;
-Снижение свертываемости крови;
-Повышенная кровоточивость стенок сосудов;
- Дистрофия тканей – производных эктодермы.
ХЛОРИД
Поддерживают нормальное осмотическое давление плазмы крови, лимфы, спинномозговой жидкости;
Участвуют в регуляции водно-солевого обмена;
Участвуют в образовании соляной кислоты.
Нарушения:
1. Гиперхлоремия имеет место при:
-Задержке выведения хлоридов (поражении почек, сердечная декомпенсация);
-Приеме больших доз хлоридов;
-Лечении минералокортикоидами.
2. Гипохлоремия возникает при:
-Повышенной потере хлоридов (поносы, рвота, фистулы желудка);
-Поступлении в организм большого количества воды (водная интоксикация);
-Нефрозах (из-за нарушения реабсорбции хлоридов в почках);
-Отеках, дыхательном ацидозе.
ВОДА
Является растворителем для химических реакций;
Является компонентом химических реакций (реакции гидролиза, гидратации);
Является структурным компонентом тканей (в составе цитоплазмы, межклеточного вещества);
Участвует в образовании гидратных оболочек;
Выполняет тепло-регуляторную функцию (за счет испарения).
37.ПОНЯТИЕ О МЕТАБОЛИЗМЕ И МЕТАБОЛИЧЕСКИХ ПУТЯХ. ФЕРМЕНТЫ И МЕТАБОЛИЗМ. СПОСОБЫ РЕГУЛЯЦИИ МЕТАБОЛИЗМА. ОСНОВНЫЕ КОНЕЧНЫЕ ПРОДУКТЫ МЕТАБОЛИЗМА У ЧЕЛОВЕКА.
МЕТАБОЛИЗМ – полный процесс превращения химических веществ в организме, обеспечивающих его рост, развитие, деятельность и жизнь в целом. Обмен веществ представляет собой комплекс биохимических и энергетических процессов, обеспечивающих использование пищевых веществ для нужд организма и удовлетворения его потребностей в пластических и энергетических веществах.
МЕТАБОЛИЧЕСКИЙ ПУТЬ – это последовательный ряд превращений химического вещества из исходного состояния в необходимое, проходящий через ряд промежуточных форм, где в каждом последующем акте превращения принимает участие необходимый фермент. Промежуточные продукты, образовавшиеся в процессе метаболизма, называются метаболитами, а последнее соединение метаболического пути -
конечный продукт.
ФЕРМЕНТЫ И МЕТАБОЛИЗМ
Все химические реакции в клетке протекают при участии ферментов.
o действуют как биологические катализаторы и снижают энергию активации химических реакций;
oпозволяют регулировать метаболические пути в ответ на изменения среды клетки или сигналы от других клеток.
Поэтому, чтобы воздействовать на скорость протекания метаболического пути, достаточно регулировать количество или активность ферментов. Обычно в метаболических путях есть ключевые ферменты, благодаря которым происходит регуляция скорости всего пути. Эти ферменты (один или несколько в метаболическом пути) называются регуляторными ферментами; они катализируют, как правило, начальные реакции метаболического пути, необратимые реакции, скорость-лимитирующие реакции (самые медленные) или реакции в месте переключения метаболического пути (точки ветвления).
ОСНОВНЫЕ КОНЕЧНЫЕ ПРОДУКТЫ МЕТАБОЛИЗМА У ЧЕЛОВЕКА:
Важнейшие из них – углекислый газ, вода, мочевина, мочевая кислота, креатинин, билирубин и аммиак.
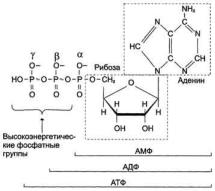
38.ЭНДЭРГОНИЧЕСКИЕ И ЭКЗЭРГОНИЧЕСКИЕ РЕАКЦИИ В ЖИВОЙ КЛЕТКЕ. МАКРОЭРГИЧЕСКИЕ СОЕДИНЕНИЯ. ПРЕДСТАВИТЕЛИ.
ЭНДЭРГОНИЧЕСКИЕ И ЭКЗЭРГОНИЧЕСКИЕ РЕАКЦИИ
Направление химической реакции определяется значением G.
Экзергоническая реакция=величина отрицательна-реакция протекает самопроизвольно и сопровождается уменьшением свободной энергии
Если при этом абсолютное значение ΔG велико, то реакция идёт практически до конца, и её можно рассматривать как необратимую.
Эндергоническая реакция= ΔG положительно, то реакция будет протекать только при поступлении свободной энергии извне
Если абсолютное значение ΔG велико, то система устойчива, и реакция в таком случае практически не осуществляется
При ΔG, равном нулю, система находится в равновесии.
Энергетически сопряжённые реакции- в биологических системах термодинамически невыгодные (эндергонические) реакции могут протекать лишь за счёт энергии экзергонических реакций
—Многие происходят при участии аденозинтрифосфата (АТФ), играющего роль сопрягающего фактора.
МАКРОЭРГИЧЕСКИЕ СОЕДИНЕНИЯ
—это соединения имеющие макроэргическую связь.
—является непрочной богатой энергетической связью
—устанавливают связь между катаболизмом и анаболизмом
—при расщеплении:1)Выделяется не менее 5ккал/моль энергии (20 и более кдж/моль) 2)Эта энергия превращается в полезную работа, минуя стадию тепла.
Типы: 1)Производные фосфорной кислоты
o |
карбоксилфосфатные (1,3-дифосфоглицерат); |
o |
аминофосфатные (креатинфосфат); |
o |
енолфосфатные (фосфоенолпируват); |
o пирофосфатные (примеры далее). Самые энергетически выгодные –(АТФ, ГТФ, ЦТФ, УТФ), они содержат 2 макроэргические связи.
2)Тиоэфирные соединения Макроэргическая связь - это такая ковалентная связь, при гидролизе которой выделяется не менее 30 кДж/моль энергии. Эта связь обозначается знаком ~
АТФ
—в клетке непрерывно участвуют в реакциях
—постоянно расщепляются до АДФ и вновь регенерируют (гидролиз концевой фосфоангидридной связи АТФ превращается в АДФ и ортофосфат)
—Цикл АТФ-АДФ - основной механизм обмена энергии в биологических системах,
—Использование АТФ как источника энергии возможно только при условии непрерывного синтеза АТФ из АДФ за счёт энергии окисления органических соединений
—главный, непосредственно используемый донор свободной энергии в биологических системах
—молекула АТФ расходуется в течение одной минуты после её образования
—У человека количество АТФ, равное массе тела, образуется и разрушается каждые 24 ч
—При условиях, существующих в клетке в норме (рН 7,0, температура 37 °С), фактическое значение G0' для процесса гидролиза составляет около -12 ккал/мол
—Величина свободной энергии гидролиза АТФ делает возможным его образование из АДФ за счёт переноса фосфатного остатка от таких высокоэнергетических фосфатов, как, например, фосфоенолпируват или 1,3- бисфосфоглицерат; в свою очередь, АТФ может участвовать в таких эндергонических реакциях, как фосфорилирование глюкозы или глицерина Энергия АТФ используется для совершения видов работ:
-механической (мышечное сокращение);
-электрической (проведение нервного импульса);
-химической (синтез веществ);
-осмотической (активный транспорт веществ через мембрану) 30% от общего количества расходуемого АТФ приходится на Na+,К+-АТФазу.
По мере использования энергии, АТФ превращается в АДФ, заряд клетки становится равным 0- начинается синтез АТФ.
Другие нуклеозидтрифосфаты (аналоги АТФ): образуются при использовании свободной энергии концевой фосфатной группы АТФ.
гуанозинтрифосфат (ГТФ)
уридинтрифосфат (УТФ)
цитидинтрифосфат (ЦТФ)
39.ДЕГИДРИРОВАНИЕ СУБСТРАТА И ОКИСЛЕНИЕ ВОДОРОДА (ОБРАЗОВАНИЕ Н2О) КАК ИСТОЧНИК ЭНЕРГИИ ДЛЯ СИНТЕЗА АТФ (ДЫХАТЕЛЬНАЯ ЦЕПЬ).
ДЫХАТЕЛЬНАЯ ЦЕПЬ (цепь тканевого дыхания, цепь переноса электронов – ЦПЭ) – комплекс ферментов, локализованных во внутренней мембране митохондрий, катализирующий реакции переноса водорода (протонов и электронов) от окисляемого субстрата на кислород. При переносе водорода на кислород образуется вода и энергия.
Компоненты дыхательной цепи:
-НАД-зависимые дегидрогеназы;
-ФАД-зависимые дегидрогеназы;
-коэнзим Q (КоQ, убихинон);
-система цитохромов;
-АТФ-синтетаза.
Способы синтеза АТФ
окислительное фосфорилирование —основной способ получения АТФ в клетке (на внутренней мембране митохондрий дыхательной цепи). —энергия для синтеза выделяется в системе МтО Во внутренней мембране митохондрий расположен интегральный белковый комплекс – Н+-зависимая АТФ-
синтаза seu Н+-зависимая АТФ-аза (два разных названия связаны с полной обратимостью катализируемой реакции), обладающий значительной молекулярной массой – более, чем 500кДа. Состоит из двух субъединиц:
FO и F1.
F1 представляет из себя грибовидный вырост на матриксной поверхности внутренней митохондриальной мембраны, FO же пронизывает эту мембрану насквозь. В толще FO расположен протонный канал, позволяющий протонам возвращаться обратно в матрикс по градиенту их концентраций.
F1 способна связывать АДФ и фосфат на своей поверхности с образованием АТФ - без затраты энергии, но обязательно в комплексе с ферментом. Энергия необходима лишь для освобождения АТФ из этого комплекса. Эта энергия выделяется в результате тока протонов через протонный канал FO.
В дыхательной цепи сопряжение абсолютно: ни одно вещество не может окисляться без восстановления другого вещества.
Но при синтезе АТФ сопряжение одностороннее: окисление может идти без фосфорилирования, а фосфорилирование без окисления никогда не идёт. Это означает, что система МтО может работать без синтеза АТФ, но АТФ не может быть синтезирована, если не работает система МтО.
субстратное фосфорилирование—связан с передачей макроэргического фосфата на АДФ.
[АТФ] + ½[АДФ] - [АТФ] + [АДФ] + [АМФ] -
субстрат связан с фосфатом, специфичен для мышц, пример: гликолиз в цитозоле КОЭФФИЦИЕНТ P/O(АТФ/О, коэффициент фосфорилирования)-для оценки эффективности работы системы МтО
—показывает, сколько молекул неорганического фосфата присоединилось к АДФ в расчете на один атом кислорода(отношение образовавшегося АТФ к одному атому поглощенного кислороду)
—экспериментально, как правило, меньше 3→процесс дыхания не полностью сопряжен с фосфорилированием(степень сопряжения зависит от целостности митохондриальной мембраны, так как она сберегает разность потенциалов, создавакмую транспортом электронов)
Для главной (полной) цепи Р/О=3
(10H+/2H+(затраты на освобождение АТФ из комплекса с ферментом) + 1H+(затраты на транспорт фосфата))=3,3 (округляют до 3-х)), коэффициент полезного действия системы - 65%,
для укороченной P/O=2
(6H+/2H+(затраты на освобождение АТФ из комплекса с ферментом) + 1H+ (затраты на транспорт фосфата)) = 2,
для максимально укороченной P/O=1
(4H+/2H+(затраты на освобождение АТФ из комплекса с ферментом) + 1H+ (затраты на транспорт фосфата)) = 1.
Система МтО потребляет 90% кислорода, поступающего в клетку. При этом в сутки образуется 62 килограмма АТФ. Но в клетках организма содержится всего 20-30 граммов АТФ. Поэтому молекула АТФ в сутки гидролизуется и снова синтезируется в среднем 2500 раз (средняя продолжительность жизни молекулы АТФ - полминуты).
—Для субстратов, которые отдают протоны и электроны на НАД-зависимые дегидрогеназы, коэффициент фосфорилирования равен 3/1=3АТФ, так как протоны и электроны транспортируются через 3 пункта сопряжения (I, III, IV комплексы). Например, изоцитрат, малат, ПВК и др.
—Для субстратов, которые отдают протоны и электроны на ФАД-зависимые дегидрогеназы и сукцинат- фумарат-дегидрогеназу (II комплекс), коэффициент фосфорилирования равен 2/1=2АТФ, так как электроны поступают на III комплекс, минуя первый пункт сопряжения (I комплекс). Например, сукцинат, глицерол-3- фосфат
40.СТРОЕНИЕ МИТОХОНДРИЙ И СТРУКТУРНАЯ ОРГАНИЗАЦИЯ ДЫХАТЕЛЬНОЙ ЦЕПИ. ТРАНСМЕМБРАННЫЙ ЭЛЕКТРОХИМИЧЕСКИЙ ПОТЕНЦИАЛ.
СТРОЕНИЕ МИТОХОНДРИЙ
Митохондрии – двухмембранные органеллы, имеющие вид округлых телец. Наружная мембрана гладкая, а внутренняя образует многочисленные впячивания – кристы. Внутри находится матрикс. Имеют собственную ДНК. Наружная мембрана проницаема практически для всех веществ, а внутренняя лишь для некоторых (например, вещества из челночных механизмов).
Внутренняя мембрана митохондрий содержит |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- |
НАД-зависимые дегидрогеназы; |
|
|
|
|
|
Организация дыхательной цепи |
|
|
|||||||||||||||||||||||||||||
- |
ФАД-зависимые дегидрогеназы; |
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
- |
коэнзим Q (КоQ, убихинон); |
|
|
|
|
Доноры протонов Н+ и электронов: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
- |
система цитохромов; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
(субстраты -S) |
|
|
|
|
|
|
|
|
|
|
|
-сукцинат |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
- |
АТФ-синтетаза |
-изоцитрат; |
|
|
|
субстраты |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
-α-кетоглутарат; ЦТК |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
2ē, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
СТРУКТУРНАЯ ОРГАНИЗАЦИЯ |
-малат; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2Н+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
-ПВК; - глутамат |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
ДЫХАТЕЛЬНОЙ ЦЕПИ |
|
|
|
H |
|
|
|
|
|
АТФ-аза |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
АТФ-аза |
|
|
АТФ-аза |
||||||||
1) Образующиеся в реакциях катаболизма |
S |
АДФ+Н3РО4 |
|
|
АТФ |
|
|
|
|
|
|
АДФ+Н3РО4 |
АТФ АДФ+Н3РО4 |
АТФ |
||||||||||||||||||||||||
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
внутренняя |
|
|
|
|
|
|
|||||||
|
НАДН и ФАДН2 передают атомы |
|
|
|
I комплекс |
|
|
|
|
|
|
|
II компл. |
|
|
мембрана |
III комплекс |
IV комплекс |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
-0,42 |
НАДН-дегидро- |
|
|
сукцинат-фумарат |
|
QH2-дегидрогеназа |
|
Цитохром |
|
|||||||||||||||||||||||||||
|
водорода (т.е. протоны водорода и |
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
геназа |
|
|
|
|
дегидрогеназа |
|
|
|
|
|
ц.b |
FeS |
ц.c1 |
|
оксидаза |
|
||||||||||||||||
|
электроны) на ферменты дыхательной |
|
|
|
|
ФМН |
ФМНН ;FeS |
|
|
ФАД |
|
ФАДН2 |
FeS |
|
|
Fe3+ |
2ē |
Fe3+ |
|
а |
а3 |
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2+ |
+ |
|
||||
|
цепи. |
|
|
|
|
|
|
|
|
|
|
2ē,2Н+ |
|
|
|
|
|
|
|
|
2ē,2Н+ |
|
|
|
|
|
2ē |
2ē |
Fe2+ 2ē |
ц. С |
Cu |
Cu |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Fe2+ |
|
Fe3+ |
Fe3+ |
Fe 2+ |
|
||||||
2) Электроны движутся по ферментам |
|
|
|
|
-0,30 |
|
|
|
|
|
|
|
|
|
2ē |
,2 |
|
|
+0,03 |
|
|
+ |
|
2ē |
|
+0,07 |
|
+0,23 |
Fe2+ 2ē +0,29 +0,55 |
|||||||||
|
дыхательной цепи и теряют энергию. |
|
|
|
2ē 1/2O2 |
1/2O= |
H2O |
|
|
|
Н+ |
|
|
2ē,2Н |
|
|
|
|
|
|
+0,25 |
|
|
|
||||||||||||||
3) Эта энергия используется на |
|
|
|
|
|
+0,82 |
|
|
|
|
|
|
2Н+ |
|
|
|
|
|
убихинон |
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
2ē,2Н+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Q QH |
|
+0,04 |
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
выкачивание протонов Н+ из матрикса в |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
2ē,2Н+ |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
межмембранное пространство. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
НАД-зависимая |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ФАД-зависимые |
|
|
|
|
|||||||||
4) В конце дыхательной цепи электроны |
|
|
|
дегидрогеназа |
|
|
Первичные акцепторы |
|
|
|
|
|
дегидрогеназы |
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
протонов и электронов |
|
|
|
|
|
ФАД |
ФАДН2 |
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
НАД |
НАДН+Н |
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
попадают на кислород и |
|
|
|
|
-0,32 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-0,05 |
матрикс |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
митохондрий |
||||
|
восстанавливают его до воды. |
|
|
|
|
|
|
|
|
|
|
|
|
Доноры протонов и электронов: |
2ē,2Н+ |
|
||||||||||||||||||||||
|
2ē,2Н+ |
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
5) Протоны Н+ стремятся обратно в |
|
|
|
|
|
|
|
|
|
|
|
|
-ацил КоА; -глицерол-3-фосфат |
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
матрикс и проходят через АТФ-синтазу.
6) При этом они теряют энергию, которая используется для синтеза АТФ.
Таким образом, восстановленные формы НАД и ФАД окисляются ферментами дыхательной цепи. Благодаря этому происходит присоединение фосфата к АДФ, т.е.фосфорилирование. Поэтому весь процесс целиком получил название окислительное фосфорилирование.
СХЕМА ГЛАВНОЙ (ПОЛНОЙ) ДЫХАТЕЛЬНОЙ ЦЕПИ МИТОХОНДРИАЛЬНОГО ОКИСЛЕНИЯ Комплекс I – НАДН-KoQ-редуктаза,
комплекс III – KoQH2-редуктаза, к
комплекс IV – цитохромоксидаза.
комплекс II – сукцинат-KoQ-редуктаза, (существует отдельно от остальных комплексов и не входит в состав главной цепи)
—Эти комплексы транспортируют водород от никотинамидных дегидрогеназ на кислород воздуха, в результате чего создается электрохимический градиент концентраций протонов - +. Он возникает на внутренней мембране митохондрий между матриксом и межмембранным пространством. Его составляют два основных фактора:
1)Электрический мембранный потенциал .
2)Градиент pH (осмотический или химический градиент).
ТРАНСМЕМБРАННЫЙ ЭЛЕКТРОХИМИЧЕСКИЙ ПОТЕНЦИАЛ.
+= - p
+ - положительная величина. Его можно выразить как в вольтах (V), так и в единицах энергии (кДж/моль). Изменение значения pH на одну единицу соответствует 0,06V или 5,7 кДж/моль.
Энергия + используется для следующих процессов:
1)Синтез АТФ.
2)Получение тепла (особенно важно для бурого жира и для мышечной ткани птиц).
3)Выполнение осмотической работы (транспорт фосфата в матрикс митохондрии).
4)Мышечная работа (в некоторых случаях).

41.ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ, КОЭФФИЦИЕНТ Р/О. РАЗОБЩЕНИЕ ТКАНЕВОГО ДЫХАНИЯ И ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ.
Окислительное фосфорилирование – это получение полезной энергии в дыхательной цепи (т.е. стадии дыхательной цепи, в которых за счет энергии переноса электронов синтезируются молекулы АТФ).
КОЭФФИЦИЕНТ Р/О
–отношение неорганического фосфата к атому О2
–количество фосфатных групп, утилизированных при восстановлении одного атома кислорода, т.е. количество образующихся молекул АТФ при переносе пары электронов и пары протонов по дыхательной цепи.
Количество молекул АТФ, а, значит, коэффициент фосфорилирования зависит от того, каким был первичный акцептор водорода: если окисление субстрата происходило при участии НАД-зависимой дегидрогеназы, образуется 3 АТФ (полная дыхательная цепь), если водород акцептировался ФАД-зависимо дегидрогеназой, то первый пункт фосфорилирования отсутствует, и образуется 2 АТФ, а цепь является укороченной. Тип дегидрогеназы зависит от её субстратной специфичности.
РАЗОБЩЕНИЕ ТКАНЕВОГО ДЫХАНИЯ И ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ
СПЕЦИФИЧЕСКИЕ ИНГИБИТОРЫ ТКАНЕВОГО ДЫХАНИЯ -К ним относятся вещества, прекращающие работу того или иного комплекса дыхательной цепи.
—Ингибитором комплекса I является ряд растительного происхождения РОТЕНОН. Некоторые народности раньше использовали его в рыбной ловле.
—Ингибиторами комплекса IV являются ЦИАНИДЫ, угарный газ СО, сероводород H2S.
ВЕЩЕСТВА-РАЗОБЩИТЕЛИ ПРОЦЕССОВ ОКИСЛЕНИЯ И ФОСФОРИЛИРОВАНИЯ (гидрофобные вещества) Они не прекращают процессов окисления, но снижают синтез АТФ. Дыхательная цепь работает, а АТФ при этом синтезируется в меньшем количестве, чем в норме. Тогда энергия, получаемая при переносе электронов по цепи МтО, выделяется в виде тепла. Такое состояние, когда происходит окисление субстратов, а фосфорилирование (образование АТФ из АДФ и Ф) не идет, называется РАЗОБЩЕНИЕМ ОКИСЛЕНИЯ И ФОСФОРИЛИРОВАНИЯ. К такому состоянию может приводить действие веществ-разобщителей:
Разобщители являются слабыми кислотами, растворимыми в жирах. В межмембранном пространстве они связывают протоны, и затем диффундируют в матрикс, тем самым снижая .
Подобным действием обладает и йодсодержащие гормоны щитовидной железы – тироксин и трийодтиронин. При состояниях, сопровождающихся гиперфункцией щитовидной железы (например, Базедова болезнь), больным не хватает энергии АТФ: они много едят (нужно большое количество субстратов для окисления), но при этом теряют в весе. Большая часть энергии выделяется в виде тепла.
Схема цепи митохондриального окисления не раскрывает механизма образования АТФ путем окислительного фософорилирования. Этот механизм объясняется гипотезой П.Митчелла.
Поцесс усиливается при замерзании →термогенез
42.РЕГУЛЯЦИЯ ЦЕПИ ПЕРЕНОСА ЭЛЕКТРОНОВ (ДЫХАТЕЛЬНЫЙ КОНТРОЛЬ). ТЕРМОРЕГУЛЯТОРНАЯ ФУНКЦИЯ ТКАНЕВОГО ДЫХАНИЯ.
РЕГУЛЯЦИЯ ЦЕПИ ПЕРЕНОСА ЭЛЕКТРОНОВ
Дыхательный контроль:
o Окисление субстратов и фосфолирирование АДФ в митохондриях прочно сопряжены.
o Скорость использования АТФ регулирует скорость потока электронов в ЦПЭ.
oЕсли АТФ не используется, и его концентрация в клетках возрастает, то прекращается поток электронов к О2
oС другой стороны, расход АТФ и превращение его в АДФ увеличивает окисление субстратов и поглощение О2
ТЕРМОРЕГУЛЯТОРНАЯ ФУНКЦИЯ ТКАНЕВОГО ДЫХАНИЯ
На синтез молекулы АТФ расходуется примерно 40-45% всей энергии электронов, переносимых по ЦПЭ, 25% тратится на работу по переносу веществ через мембрану.
Остальная часть энергии рассеивается в виде теплоты и используется на поддержание температуры тела. Дополнительное образование теплоты происходит при разобщении дыхания и фосфорилирования, которое может быть биологически полезным. Оно позволяет генерировать тепло для поддержания температуры у новорожденных, у зимнеспящих животных и у всех млекопитающих в процессе адаптации к холоду. У них существует бурый жир – особая ткань, специализирующаяся на теплопродукции посредством разобщения дыхания и фосфорилирования. Бурый жир содержит много митохондрий. Около 10% всех белков приходится на так называемый разобщающий белок (РБ-1) – термогенин.
Около 55% энергии полного расщепления глюкозы аккумулируется в виде АТФ. Остальная часть энергии является источником теплообразования. Тем самым образуется для поддержания температуры тела. Процессы разобщения тканевого дыхания и окислительного фосфорилирвания приводит к повышению температуры тела. Регуляция дыхательной цепи – состояние такой энергии, целостность мембран митохондрии и их проницаемость, состояние коферментов, наличие разобщителей. Тканевое дыхание – завершающийся этап биологического окисления, при этом 90% О2 восстанавливается до Н2О. О2 + 4Н(+)+4Е(-
)=2Н2О
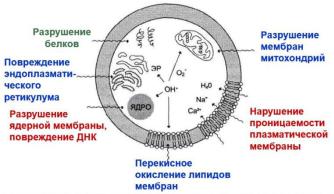
43.НАРУШЕНИЯ ЭНЕРГЕТИЧЕСКОГО ОБМЕНА: ГИПОЭНЕРГЕТИЧЕСКИЕ СОСТОЯНИЯ КАК РЕЗУЛЬТАТ ГИПОКСИИ, ГИПО-, АВИТАМИНОЗОВ И ДРУГИХ ПРИЧИН.
Гипоэнергетические состояния – это состояния, связанные со снижением синтеза АТФ
Причины: голодание, гиповитаминозы B1, B2, PP, гипоксия, поступление ингибиторов ферментов.
Наиболее частой причиной гипоэнергетических состояний является гипоксия, возникновение которой, в
свою очередь, связано с нарушением:
A.Поступления кислорода в кровь, что наблюдается при недостаточности О2 во вдыхаемом воздухе или недостаточности легочной вентиляции.
B.Транспорта кислорода в ткани при патологии кровообращения или снижении транспортной функции гемоглобина.
C.Нарушение использования кислорода в клетках: функций митоходрий, вызванных действием ядов и разобщителей.
D.Гиповитаминозы, так как в реакциях общих путей катаболизма и дыхательной цепи участвуют коферменты, содержащие витамины. Так, витамин В1 входит в состав тиаминдифосфата, В2 является составной частью FMH и FAD, витамин РР в виде никотинамида входит в состав NAD+ и NADР.
44.ОБРАЗОВАНИЕ ТОКСИЧЕСКИХ ФОРМ КИСЛОРОДА, МЕХАНИЗМ ИХ ПОВРЕЖДАЮЩЕГО ДЕЙСТВИЯ НА КЛЕТКИ. МЕХАНИЗМЫ УСТРАНЕНИЯ ТОКСИЧНЫХ ФОРМ КИСЛОРОДА. АНТИОКСИДАНТНАЯ СИСТЕМА.
ОБРАЗОВАНИЕ ТОКСИЧЕСКИХ ФОРМ КИСЛОРОДА
В процессе тканевого дыхания конечным продуктом является вода. Конечным акцептором электронов в дыхательной цепи является кислород. Он должен присоединить 4 электрона. Процессы передачи электронов в дыхательной цепи идут поэтапно и в результате образуются активные формы кислорода.
МЕХАНИЗМ ИХ ПОВРЕЖДАЮЩЕГО ДЕЙСТВИЯ
т.к. активные формы кислорода являются радикалами, они
воздействуют на многие органические вещества и запускают цепную реакцию. Т.е. они могут воздействовать на белки и обеспечивать их агрегацию («шип» между белками делать), такие белки свои функции выполнять не будут (нарушается функция белка в целом). Они могут
воздействовать и на ДНК – повреждают азотистые основания в составе нуклеотидов. Но самое большое воздействие они оказывают на перекисное окисление липидов мембраны клетки – воздействуют на непредельные ЖК фосфолипидов мембраны, превращая её в радикал. ЖК становится радикалом и воздействует на другое вещество (например, на другую ЖК), таким образом запускается цепная
реакция, что приводит к разрушению клеточной мембраны. Это приводит к преждевременному изнашиванию клеток и организма в целом и к преждевременному старению.
МЕХАНИЗМЫ УСТРАНЕНИЯ ТОКСИЧНЫХ ФОРМ КИСЛОРОДА
Для обезвреживания активных форм кислорода в нашем организме есть мощная антиоксидантная система. Она направлена на устранение токсичных форм кислорода, когда их концентрация повышается (при некрозах, при острых воспалительных процессах, при стрессах, при поступлении в организм токсичных веществ, при воздействии радиации).
АНТИОКСИДАНТНАЯ СИСТЕМА
Ферментативное звено:
o супероксиддисмутаза (СОД) – система первой линии, которая превращает все активные формы кислорода в перекись водорода;
o каталаза – превращает перекись в воду и кислород;
o пероксидаза – действует и на перекись, и на пероксиды (радикалы липидов);
oглутатионпероксидаза – обеспечивает защиту мембран от разрушающего действия пероксидных радикалов.
Неферментативное звено: o витамины А, Е и С;
o |
цинк, селен; |
o |
глутатион; |
o |
билирубин; |
o |
мочевая кислота; |
o |
убихинон. |
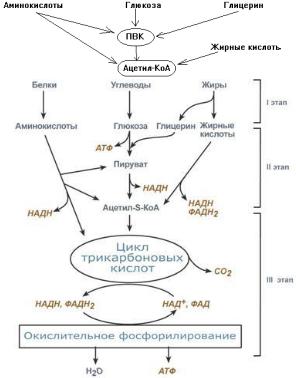
45.КАТАБОЛИЗМ ОСНОВНЫХ ПИЩЕВЫХ ВЕЩЕСТВ – УГЛЕВОДОВ, ЖИРОВ, БЕЛКОВ, ЭТАПЫ (СХЕМА). ПОНЯТИЕ О СПЕЦИФИЧЕСКИХ И ОБЩИХ ПУТЯХ КАТАБОЛИЗМА.
1-й этап. Образование мономеров из полимеров (гидролиз, деполяризация, дезинтеграция)
– расщепление в желудочно-кишечном тракте белков, жиров и углеводов до мономеров (аминокислот, высших жирных кислот и глицерина, моносахаридов).
—В процессе пищеварения теряется видовая специфичность питательных веществ
—1% энергии
Полимеры -------->Мономеры
Белки ----------->Аминокислоты
Крахмал --------->глюкоза
Жиры ------------>глицерин + жирные кислоты
2-й этап. Превращение мономеров в ПВК и Ацетил-КоА. (в-ва: ЩУК,аКГ,Фу)
–внутриклеточный катаболизмглюкоза, высшие жирные кислоты, аминокислоты подвергаются специфическим превращениям до образования ацетил-КоА (гликолиз, β-окисление высших жирных кислот, трансаминирование аминокислот)
- процессы протекают в цитоплазме
—20-30% энергии 3-й этап. Превращение Ацетил-КоА в конечные продукты
катаболизма: СО2 и Н2О.
–общий путь катаболизма
–цикл трикарбоновых кислот (цикл Кребса);
терминальная фаза окислениятканевое дыхание, ЦПЭцепь переноса электронов (дыхательная цепь).
Для всех классов веществ последний этап катаболизма одинаков: на 3-м этапе образуется большинство субстратов митохондриального окисления - 4 вещества из 9 основных и 5-й субстрат - ПВК.
—70-80 % энергии Тканевое дыхание – совокупность протекающих в каждой клетке
ферментативных процессов, в результате которых молекулы углеводов, жиров и аминокислот расщепляются, в конечном счете, до углекислоты и воды, а освобождающаяся энергия запасается клеткой в виде аденозинтрифосфорной кислоты (АТФ) и затем используется в жизнедеятельности организма (биосинтез молекул, процесс деления клеток, сокращение мышц, активный транспорт, продукция тепла и др.)
СПЕЦИФИЧЕСКИЙ ПУТЬ КАТАБОЛИЗМА – совокупность превращений, свойственная только определенному соединению (например, только углеводам, только липидам или АК), этот путь разный для разных классов веществ.
ОБЩИЙ ПУТЬ КАТАБОЛИЗМА служит единым продолжением специфических путей катаболизма. Общие пути катаболизма: окислительное декарбоксилирование ПВК и ЦТК. На этих стадиях катаболизма происходит образование основной массы первичных доноров водорода для дыхательной цепи.
