
БИОХИМИЯ КРОВИ
.pdfсоставляет всего 1-2 мм рт. ст., тогда как для гемоглобина такое насыщение кислородом наступит лишь при парциальном давлении кислорода около 26
мм рт. ст. Кривая связывания кислорода у миоглобина показывает его сравнительно малую чувствительность к небольшим изменениям концентрации растворенного кислорода. Это свойство обуславливает функцию миоглобина – депонирование кислорода в мышечной клетке и использование его только при значительном уменьшении парциального давления О2 в мышце (до 1-2 мм рт.ст.).
В отличие от миоглобина гемоглобин является белком четвертичной структуры, оксигенация которого подчиняется кооперативному аллостерическому эффекту и характеризуется значительно более низким сродством к кислороду. Сигмовидная форма кривой означает, что связывание кислорода гемоглобином происходит кооперативно, т.е. присоединение кислорода к одному гему облегчает его присоединение к остальным гемам в составе тетрамера.
Таким образом, гемоглобин и миоглобин специально приспособлены для выполнения различных кислород-связывающих функций. Для той биологической функции, которую он выполняет в мышечной ткани (запасает кислород и обеспечивает им митохондрии), миоглобин приспособлен значительно лучше, чем гемоглобин, так как его высокое сродство к кислороду при низких парциальных давлениях кислорода дает ему возможность более эффективно связывать и запасать кислород.
Сродство гемоглобина к кислороду и его регуляция (эффект
Бора, влияние 2,3-дифосфоглицерата)
Скорость и полнота переноса кислорода из легких в ткани зависит от изменения сродства гемоглобина к кислороду.
В легких сродство Hb к кислороду повышается при присоединении каждой из последующих молекул кислорода по сравнению с предыдущими.
Эта положительная регуляция описана ранее. Кроме того, существуют вещества, снижающие сродство Hb к О2. К ним относятся:

2,3-бисфосфоглицерат (2,3-БФГ)
ионы водорода — Н+
СО2
температура тела
. Влияние 2,3-бисфосфоглицерата.
2,3-БФГ синтезируется в эритроцитах из 1,3-бисфосфоглицерата — метаболита, образующегося при окислении глюкозы.
2,3-БФГ взаимодействует своими отрицательно заряженными фосфатными и карбоксильной группами с положительно заряженными группами аминокислот лиз,
гис и вал β-цепей глобина в центральной полости молекулы Hb.
2,3-БФГ взаимодействует своими отрицательно заряженными фосфатными и карбоксильной группами с положительно заряженными группами аминокислот лиз, гис и вал β-цепей глобина в центральной полости молекулы
Hb. Каждый тетрамер гемоглобина может связывать только одну молекулу
2,3-БФГ.
Концентрация 2,3-БФГ повышена в эритроцитах при гипоксии. Это имеет особенное значение при подъеме на высоту, при нехватке кислорода во вдыхаемом воздухе. В этих условиях связывание кислорода с гемоглобином в легких не нарушается, так как концентрация его относительно высока.
Однако в тканях за счет 2,3-дифосфоглицерата отдача кислорода возрастает в
2 раза.
Влияние Н+ и СО2.
СО2 является конечным продуктом катаболизма органических веществ.
Окисление органических веществ происходит с использованием кислорода,
доставляемого гемоглобином из легких. Образовавшийся СО2 поступает из тканей в кровь, и в эритроцитах происходит реакция образования Н2СО3,
катализируемая карбангидразой.
Угольная кислота затем диссоциирует на протон и ион бикарбоната.
Протоны способны присоединяться к гемоглобину в участках,
удаленных от гема.
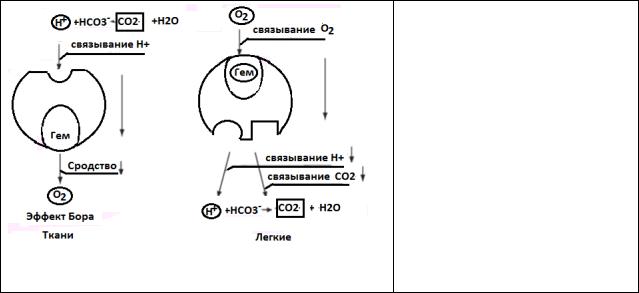
Рис. Эффект Бора
Протонирование Нb изменяет конформацию и снижает его сродство к О2, тем самым способствуя поступлению кислорода в ткани. В легких поступающий кислород "вытесняет" ион водорода из связи с остатком гистидина гемоглобиновой молекулы.
Освобождающиеся Н+ нейтрализуют НСО3- с образованием Н2СО3,которая расщепляется карбангидразой на СО2 и Н2О. Образующийся СО2 удаляется с выдыхаемым воздухом.
Равновесие реакции СО2 + Н2О ↔ Н2СО3 ↔ Н+ + НСО3 - смещается влево в капиллярах легких и вправо в капиллярах тканей.
Влияние рН на сродство гемоглобина к кислороду носит название
эффекта Бора. При закислении среды сродство снижается, при защелачивании – повышается.
Лейкоцит: функции, химический состав, особенности обмена веществ. Биохимические аспекты фагоцитоза.
Характеристика основных метаболических процессов лейкоцитов:
1.В лейкоцитах активно протекают процессы биосинтеза нуклеиновых кислот и белков.
2.Основной путь получения энергии – аэробный гликолиз. АТФ образуется также в реакциях β-окисления жирных кислот.
3.В лейкоцитах сосредоточен весь гликоген крови, который является источником энергии при недостаточном её поступлении.
4.В лизосомах лейкоцитов локализована мощная система протеолитических ферментов – протеазы, фосфатазы, эстеразы, ДНК-азы,
РНК-азы, что обеспечивает участие этих клеток в защитных реакциях организма. В результате действия этих ферментов разрушаются полимерные молекулы микроорганизмов и образуются мономеры (моносахариды,
аминокислоты, нуклеотиды), которые поступают в цитозоль и могут использоваться клеткой.
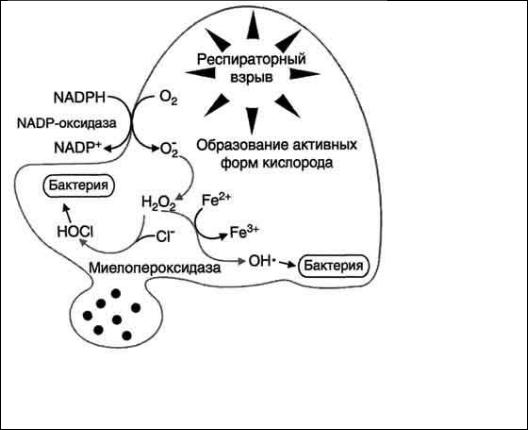
5. Поглощение бактерий лейкоцитами в процессе фагоцитоза сопровождаются резким увеличением потребления кислорода с образованием супероксидного аниона и пероксида водорода, которые оказывают бактерицидное действие. Это явление называется «респираторным взрывом».
Образование активных форм кислорода фагоцитирующими клетками при респираторном взрыве. (по Северину Е.С.)
Активация NADPH оксидазы, локализованной в мембране клетки,
вызывает образование супероксидного аниона. В результате впячивания мембраны супероксид вместе с бактериальной клеткой оказываются в фагосоме. Супероксидный анион генерирует образование других токсичных
молекул, включая Н2О2 и ОН•. Миелопероксидаза, содержащаяся в гранулах фагоцитирующих клеток, секретируется в фагосому, где образует HOCl (гипохлорит-ион).
Активные формы кислорода инициируют свободнорадикальные реакции, разрушающие липиды клеточных мембран поглощённых фагоцитами бактерий.
Наследственная недостаточность NADP-оксидазы, обусловленная дефектом одного из генов этого ферментного комплекса, приводит к хроническому гранулематозу. В результате дефекта фермента фагоциты больных не способны продуцировать супероксидный кислородный радикал и пероксид водорода и поэтому не могут быстро разрушать фагоцитированные клетки бактерий и грибов. Некоторые устойчивые микроорганизмы остаются жизнеспособными внутри фагоцитов, и их антигены вызывают в месте скопления фагоцитов клеточный иммунный ответ и формирование гранулём.

Рекомендуемая литература по дисциплине «Биохимия»
1.Северин Е.С., Биохимия [Электронный ресурс] : учебник / под ред. Е. С. Северина. - 5-е изд., испр. и доп. - М. : ГЭОТАР-Медиа, 2016. - 768 с. - ISBN 978-5-9704-3762-9 - Режим доступа: http://www.studmedlib.ru/book/ISBN9785970437629.html
2.Губарева А.Е., Биологическая химия. Ситуационные задачи и тесты [Электронный ресурс] : учеб. пособие / А. Е. Губарева [и др.] ; под ред. А.
Е. Губаревой. - М. : ГЭОТАР-Медиа, 2016. - 528 с. - ISBN 978-5-9704-3561-8 - Режим доступа: http://www.studmedlib.ru/book/ISBN9785970435618.html
3.Авдеева Л.В., Биохимия [Электронный ресурс] / Авдеева Л.В., Алейникова Т.Л., Андрианова Л.Е., Белушкина Н.Н., Волкова Н.П., Воробьева С.А., Голенченко В.А., Губарева А.Е., Корлякова О.В., Лихачева Н.В., Павлова Н.А., Рубцова Г.В., Силаева С.А., Силуянова С.Н., Титова Т.А. - М. : ГЭОТАР-
Медиа, 2014. - 752 с. - ISBN 978-5-9704-3043-9 - Режим доступа: http://www.studmedlib.ru/book/ISBN9785970430439.html
Рекомендуемая литература по дисциплине «Биохимия-БПР»
1.Вавилова Т.П., Биологическая химия. Биохимия полости рта [Электронный ресурс] / Т.П. Вавилова, А.Е. Медведев - М. : ГЭОТАР-Медиа, 2014. - 560 с. - ISBN 978-5-9704-3039-2 - Режим доступа: http://www.studmedlib.ru/book/ISBN9785970430392.html
2.Северин С.Е., Биологическая химия и биохимия полости рта. Ситуационные задачи и задания [Электронный ресурс] : учеб. пособие / под ред. С.Е. Северина. - М. : ГЭОТАР-Медиа, 2017. - 240 с. - ISBN 978-5- 9704-4015-5 - Режим доступа: http://www.studmedlib.ru/book/ISBN9785970440155.html
3.Северин Е.С., Биохимия [Электронный ресурс] : учебник / под ред. Е. С. Северина. - 5-е изд., испр. и доп. - М. : ГЭОТАР-Медиа, 2016. - 768 с. - ISBN 978-5-9704-3762-9 - Режим доступа: http://www.studmedlib.ru/book/ISBN9785970437629.html
