- •Экзаменационные вопросы по дисциплине «факультетская терапия» раздел «кардиология»
- •Атеросклероз: определение, эпидемиология, факторы риска, патогенез, патоморфология, классификация по стадиям.
- •Атеросклероз: факторы риска, клиника, диагностика, классификация типов дислипидемий по Фридрексону, воз.
- •Атеросклероз: принципы немедикаментозной и медикаментозной терапии. Профилактика.
- •Ибс. Нестабильная стенокардия. Определение. Понятие о нестабильной атеросклеротической бляшке. Классификация по ю. Браунвальду, Ризику. Принципы диагностики.
- •Ибс. Острый коронарный синдром без элевации сегмента st. Определение. Патогенез. Принципы диагностики.
- •Ибс. Острый коронарный синдром без элевации сегмента st. Определение. Стратификация риска (шкала grase, клинические принципы). Тактика лечения. Реваскуляризация.
- •Ибс. Острый коронарный синдром с подъемом (элевацией) сегмента st. Определение. Патогенез. Принципы диагностики.
- •Ибс. Острый коронарный синдром с подъемом (элевацией) сегмента st. Определение. Виды реваскуляризации миокарда. Тактика выбора способа реваскуляризации.
- •Ибс. Инфаркт миокарда. Определение. Этиология и патогенез. 5 типов инфаркта миокарда. Классификация инфаркта миокарда. Патоморфологические и клинические периоды инфаркта миокарда.
- •Ибс. Инфаркт миокарда. Определение. Лабораторно-инструментальные методы диагностики. Клинические формы инфаркта миокарда. Дифференциальная диагностика. Критерии диагностики.
- •Гипертоническая болезнь. Дифференциальный диагноз первичной и вторичных артериальных гипертензий.
- •Гипертоническая болезнь. Понятие об истинной и ложной рефрактерной артериальной гипертензии, злокачественной артериальной гипертензии. Гипертонические кризы: классификация. Принципы лечения.
- •Хроническая сердечная недостаточность (хсн). Определение. Принципы медикаментозного и немедикаментозного лечения больных хсн с сохранной фракцией выброса левого желудочка. Прогноз.
- •Миокардиты. Определение. Классификация - этиологическая, патогенетическая, патоморфологическая, клинико-морфологическая. Принципы немедикаментозного и медикаментозного лечения. Прогноз.
- •Гипертрофическая кардиомиопатия: определение, молекулярно-генетическая основа, морфология, патогенез и патофизиология. Клиника, диагностика, принципы лечения.
- •Перикардиты. Определение. Принципы лечение острого перикардита, рецидивирующего перикардита, констриктивного перикардита. Перикардиоцентез.
- •Тампонады сердца: определение, этиология, клиника, диагностика. Прогноз
- •2. Экстракардиальные:
- •3. Идиопатические
- •1. Синоатриальная блокада.
- •5. Асистолия желудочков.
- •Нарушения ритма сердца – экстрасистолия: определение экстрасистолии, этиология, классификация, клиническая картина, экг – критерии. Принципы лечения.
- •Раздел «ревматология»
- •Подагра. Определение. Стадии развития подагры. Нефармакологическое лечение. Лечение острого приступа подагрического артрита. Антигиперурикемическая терапия.
- •Раздел «пульмонология»
- •Хроническая обструктивная болезнь легких / хобл /. Этиология. Факторы риска. Роль табакокурения. Патогенетические этапы развития хобл. Бронхитическая триада.
- •Хобл: классификация gold (последняя редакция). Клинические фенотипы. Стандарт инструментальной и лабораторной диагностики хобл.
- •Принципы лечения хобл в фазу обострения и ремиссии. Классификация бронходилятаторов. Профилактика хобл.
- •Хобл: диагностика осложнений. Принципы лечения дыхательной недостаточности и декомпенсированного легочного сердца
- •Хобл: особенности бронхообструктивного синдрома. Дифференциальный диагноз с бронхиальной астмой.
- •Принципы лечения бронхообструктивного синдрома при хобл. Показания к назначению системных глюкокортикоидных гормонов.
- •Бронхиальная астма / ба /. Определение. Классификация ginа (последняя редакция). Особенности бронхообструктивного синдрома. Критерии диагностики ба.
- •Принципы лечения бронхиальной астмы. Ступенчатая схема лечения.
- •Бронхиальная астма / ба /. Факторы риска. Патогенетические механизмы бронхообструкции
- •Бронхиальная астма / ба /, атопическая форма. Определение. Ранняя и поздняя аллергические реакции. Патогенез атопической ба. Особенности клиники.
- •Атопическая бронхиальная астма: принципы лечения. Классификация бронходилататоров, механизм их действия. Профилактика
- •Бронхиальная астма / ба /. Дифференциальный диагноз с хобл. Стандарт обследования больного ба. Роль пикфлуометрии и спирографии для диагностики и оценки эффективности терапии. Профилактика ба.
- •Пневмония. Определение. Классификация. Этиология домашней и нозокомиальной пневмонии. Критерии диагностики пневмонии.
- •Пневмония: осложнения легочные, внелегочные. Принципы лечения инфекционно-токсического шока.
- •Пневмония. Определение. Патогенез, клиника пневмоний, вызванных микоплазмой, легионеллой, хламидиями. Критерии их диагностики.
- •Пневмонии, вызванные микоплазмой, легионеллой, хламидиями: особенности клинической картины, принципы лечения. Профилактика.
- •Нозокомиальная пневмония, определение. Этиология, патогенез, клиника. Диагностика.
- •Нозокомиальная пневмония: принципы лечения. Профилактика нозокомиальной пневмонии.
- •Респираторные и общие интоксикационные синдромы при пневмонии. Дифференциальный диагноз пневмонии с туберкулезом легких, раком. Профилактика домашней пневмонии.
- •1. Легочные проявления пневмонии:
- •2. Внелегочные проявления пневмонии
- •Idsa/ats критерии тяжелой вп
- •I. Природные пенициллины
- •II. Цефалоспорины
- •III. Макролиды
- •Астматический статус: причинная обусловленность, патогенез, классификация. Клиника в зависимости от стадии. Принципы лечения.
- •Раздел «анемии»
- •Анемия: определение. Классификация. Критерии диагностики анемий. Общеанемические (гипоксические) синдромы. Стандарт лабораторно- инструментального обследования больного анемией.
- •1. Анамнез, для выявления возможной причины анемии (наследственность, провоцирующие факторы).
- •2. Обследование, определение варианта анемии.
- •3. Определение основного заболевания, приведшего к анемии:
- •Железодефицитная анемия. Определение. Классификация. Причины.
- •Cидеропенический синдром. Лабораторные критерии диагностики железодефицитной анемии.
- •Железодефицитная анемия: принципы ферротерапии. Осложнения лечения. Показания для переливания крови. Профилактика.
- •Железодефицитные состояния и железодефицитная анемия. Дифференциальный диагноз.
- •Стандарт обследования больных с анемией.
- •Дифференциальный диагноз анемий: железодефицитной, мегалобластной, гемолитической, апластической. Раздел «гастроэнтерология»
- •Хронический гастрит. Факторы риска, этиология и патогенез. Классификация olga. Хронический аутоиммунный гастрит /тип а/. Особенности патогенеза, клиники. Критерии диагностики. Принципы лечения
- •Хронический гастрит. Определение. Киотская классификация. Методы диагностики пилорических геликобактеров
- •Хронический гастрит. Определение. Гастрит, ассоциированный с геликобактериозом /тип в/. Патогенез, клинико-лабораторная диагностика.
- •Хронический гастрит, ассоциированный с геликобактериозом /тип в/. Принципы лечения. Антигеликобактерная терапия.
- •Язвенная болезнь. Принципы и схемы лечения геликобактерзависимых форм /терапия первой и второй линии/. Профилактика рецидивов.
- •Язвенная болезнь. Определение. Факторы риска. Классификация. Местные факторы агрессии и защиты.
- •Язвенная болезнь желудка. Особенности патогенеза, клиники, диагностики и лечения. Осложнения.
- •Язвенная болезнь. Определение. Геликобактерная инфекция как патогенетический фактор развития язвенной болезни: современные представления. Клиника и диагностика язвенной болезни дпк.
- •Язвенная болезнь желудка и дпк. Принципы лечения. Профилактика.
- •Язвенная болезнь желудка и дпк. Осложнения. Лабораторно-инструментальная диагностика.
- •Хронический гастрит /тип с/. Этиология и патогенез, клиника. Диагностика.
- •Хронический токсико-химический гастрит /тип с – рефлюкс-гастрит/: принципы лечения. Профилактика гастритов.
- •Хронический панкреатит. Определение. Классификация. Особенности патогенеза, клиники алкогольного панкреатита. Лабораторно-инструментальная диагностика.
- •Хронический панкреатит. Классификация tigar-o. Принципы лечения. Профилактика.
- •Хронический панкреатит. Определение. Основные клинические синдромы. Методы диагностики функциональной недостаточности поджелудочной железы. Принципы лечения. Профилактика.
- •Хронический панкреатит. Классификация. Дифференциальный диагноз.
- •Хронический панкреатит. Этиология и патогенез билиарнозависимого панкреатита. Лабораторно-инструментальная диагностика. Лечение.
- •Дисфункции желчевыводящих путей. Классификация. Клиника. Лабораторно-инструментальная диагностика. Дифференцированное лечение
- •Дисфункции желчевыводящих путей. Дисфункция сфинктера Одди. Диагностика. Дифференцированное лечение.
- •1)Скрининговые (обязательные)
- •Хронический бескаменный холецистит. Классификация. Диагностика: клинические симптомы 1, 2, 3 групп; инструментальные и лабораторные методы диагностики холецистита.
- •Этиология и патогенез
- •2. С нарушением тонуса сфинктерного аппарата внепеченочных желчных путей (вжп):
- •«Маски» хронического холецистита
- •!!!Физикальная диагностика: выявление болевых точек на коже при пальпации и перкуссии и их характеристика (Циммерман я.С., Головской б.В., 1973, 1984):
- •Лабораторная диагностика
- •Динамическая сцинтиграфия гепато-билиарной системы
- •Желчнокаменная болезнь, первая стадия - билиарный сладж. Клиника. Диагностика. Лечение. (1)Билиарный сладж (бс)
- •Факторы, способствующие перенасыщению желчи холестерином.
- •Факторы, способствующие осаждению холестерина в желчи.
- •Факторы, приводящие к нарушению функции желчного пузыря(сокращение, всасывание, секреция).
- •Билиарный сладж: принципы терапии:
- •Впервые выявленный бс в форме взвешенных гиперэхогенных частиц, при отсутствии клинической симптоматики:
- •2. Бс в форме эхонеоднородной желчи с наличием сгустков и зж вне зависимости от клинической симптоматики - консервативная терапия:
- •Хронический бескаменный холецистит. Этиология, патогенез. Клиника. Клинические «маски».
- •Этиология и патогенез
- •2. С нарушением тонуса сфинктерного аппарата внепеченочных желчных путей (вжп):
- •«Маски» хронического холецистита
- •Хронический бескаменный холецистит. Дифференциальный диагноз с жкб. Принципы лечения бескаменного хронического холецистита. Лечение
- •Принципы лечени хх
- •Медикаментозная терапия хбх
- •Симптоматическая терапия
- •Прием урсофалька для профилактики образования камней
- •Хронический гепатит. Определение. Классификация. Аутоиммунный гепатит. Патогенез. Критерии клинико-лабораторной диагностики.
- •Аутоиммунный гепатит. Дифференциальный диагноз. Принципы лечения. Профилактика.
- •Хронический гепатит. Определение. Классификация. Вирусные гепатиты. Вирусологическая диагностика.
- •1. Вирусный гепатит в (hbv)
- •Хронический вирусный гепатит. Принципы противовирусной терапии. Профилактика вирусных гепатитов.
- •Хронический гепатит. Определение. Классификация. Основные клинико-лабораторные (биохимические) синдромы. Инструментальные методы диагностики.
- •Принципы лечения хронических гепатитов.
- •Хронический лекарственный гепатит. Этиология, патогенез. Методы определения активности процесса и степени фиброза печени.
- •Циррозы печени. Определение, классификация. Основные клинические синдромы. Лабораторно-инструментальная диагностика.
- •Циррозы печени: первичный и вторичный биллиарный цирроз. Патогенез, клиника, дифференциальная диагностика. Лабораторно-инструментальная диагностика. Прогноз.
- •4.Кровотечения из варикозно расширенных вен:
- •Метаболические циррозы: гемахроматоз, болезнь Вильсона. Патогенез, клинические синдромы. Лабораторно-инструментальная диагностика. Принципы лечения
- •Синдром функциональной диспепсии (сфд). Римские критерии IV. Клинические варианты. Дифференциальная диагностика. Стандарт обследования. Синдромы «тревоги". Принципы лечения.
- •Синдром раздраженной кишки (срк). "Римские критерии IV". Клинические формы. Дифференциальный диагноз. Диагностика. Синдром "тревоги". Принципы лечения.
- •Хронические энтериты. Этиология, патогенез. Лабораторно-инструментальная диагностика. Принципы лечения.
- •Хронические энтериты, классификация. Основные клинические синдромы. Дифференциальный диагноз.
- •Ферментопатии: целиакия, определение, патогенез, клиника. Лабораторно-инструментальная диагностика. Дифференциальный диагноз. Принципы лечения
- •Хронический колит. Классификация. Основные клинические синдромы. Лабораторно-инструментальная диагностика, дифференциальный диагноз. Принципы лечения. Профилактика
- •Дисбиоз кишечника, облигатная, транзиторная, факультативная микрофлора кишечника. Степени дисбиоза. Клиника. Диагностика, принципы лечения.
- •Язвенный колит, этиология, патогенез, клиника. Классификация.
- •Язвенный колит. Лабораторно-инструментальная диагностика. Осложнения.
- •Воспалительные заболевания кишечника (язвенный колит, Болезнь Крона): принципы лечения (основные базисные препараты).
- •Болезнь Крона. Этиология, патогенез. Клиника (кишечные, внекишечные проявления). Классификация.
- •Болезнь Крона. Лабораторно-инструментальная диагностика. Осложнения.
- •Гэрб, определение, этиология, предрасполагающие факторы, патогенез. Клиника (пищеводные и внепищеводные симптомы). Инструментальная диагностика. Дифференциальный диагноз
- •Гэрб: Эндоскопическая классификация. Осложнения, принципы лечения. Профилактика
- •Алкогольная и неалкогольная жировая болезнь печени. Этиология, патогенез. Лабораторно-инструментальная диагностика. Принципы лечения.
- •Раздел «нефрология»
- •Хронический гломерулонефрит. Определение. Патогенез основных клинических синдромов: мочевого, гипертензивного, нефротического, отёчного. Принципы терапии.
- •Хронический гломерулонефрит. Клинические варианты: латентный и гематурический. Патоморфология. Характеристика протеинурии и гематурии. Диагностика. Принципы терапии.
- •Хронический гломерулонефрит. Клинический вариант - гипертензивный. Патоморфология. Патогенез гипертензивного синдрома. Дифференциальная диагностика с гипертонической болезнью. Принципы терапии.
- •Хронический гломерулонефрит. Клинический вариант - нефротический. Патоморфология. Патогенез формирования компонентов нефротического синдрома. Диагностика. Принципы терапии.
- •Хроническая болезнь почек. Определение. Факторы риска. Патогенез. Классификация по стадиям, степени альбуминурии.
- •Хроническая болезнь почек. Определение. Диагностика. Медикаментозная и немедикаментозная терапия. Экстракорпоральные методы лечения. Показания для хронического гемодиализа. Прогноз.
Раздел «ревматология»
Ревматическая лихорадка. Этиология, патогенез, морфогенез. Большие и малые критерии РЛ. Клинические особенности кардита, полиартрита, поражения нервной системы. Принципы лечения РЛ. Понятие о первичной и вторичной профилактике РЛ.
Острая ревматическая лихорадка (ОРЛ) – системное воспалительное заболевание соединительной ткани с преимущественным поражением сердечно-сосудистой системы, развивающееся в связи с острой А-стрептококковой носоглоточной инфекцией у предрасположенных к нему лиц.
Этиологический фактор - В-гемолитический стрептококк группы А. Заболевание развивается в связи с острой или хронической носоглоточной инфекцией. Особенное значение имеет М-протеин, входящий в состав клеточной стенки стрептококка. Известно более 80 разновидностей М-протеина, из них ревматогенными считают М-5, 6, 14, 18, 19, 24. Необходимым условием также является наследственная предрасположенность (DR21, DR4, антитела HLA; аллоантиген В-лимфоцитов D8/17).
В патогенезе ревматизма имеет важное значение прямое или опосредованное повреждающее воздействие стрептококка на организм: стрептолизин О, гиалуронидаза, стрептокиназа обладают свойствами антигена. В ответ на первичное поступление этих антигенов в кровь организм вырабатывает антитела и осуществляет перестройку иммунологической реактивности. Развитие аллергического состояния и нарушение иммуногенеза принято считать главными факторами в патогенезе ревматизма.
При новых обострениях стрептококковой инфекции происходит накопление иммунных комплексов в повышенном количестве. В процессе циркуляции в сосудистой системе они фиксируются в стенке сосудов микроциркуляторного русла и повреждают их. Антигены при этом поступают из крови в соединительную ткань и приводят к ее деструкции (аллергическая реакция немедленного типа). Аллергия имеет важное значение в патогенезе ревматизма. Подтверждением этому служит то, что аллергия начинается не во время ангины, а через 10-14 дней и более после нее.
Важное значение в патогенезе ревматизма имеет также аутоаллергия. Общность антигенного строения стрептококка и соединительной ткани сердца приводит к повреждению оболочек сердца иммунными реакциями в них ,при этом происходит образование аутоантигенов и аутоантител (молекулярная мимикрия). Такие аутоантигены оказывают на эндомиокард большее разрушительное действие, чем один стрептококковый антиген.
Вследствие иммунокомплексной реакции развивается хроническое воспаление в сердце. Помимо нарушения гуморального иммунитета (выработка антител), при ревматизме страдает и клеточный иммунитет. Образуется клон сенсибилизированных лимфоцитов-киллеров, которые несут на себе фиксированные антитела к сердечной мышце и эндокарду и повреждают их (аллергичнеская реакция замедленного типа).
Большие критерии:
- кардит;
- полиартрит;
- хорея;
- кольцевидная эритема;
- подкожные ревматические узелки.
Малые критерии:
- клинические: артралгии, лихорадка;
- лабораторные: повышенные острофазовые показатели: СОЭ и С-реактивный белок;
- удлинение интервала Р-R на ЭКГ.
Данные, подтверждающие предшествовавшую А-стрептококковую инфекцию:
- позитивная А-стрептококковая культура, выделенная из зева или положительный тест быстрого определения А-стрептококкового антигена;
- повышенные или повышающиеся титры А-стрептококковых антител.
Наличие двух больших критериев или одного большого и двух малых в сочетании с данными, документировано подтверждающими предшествующую инфекцию стрептококками группы А, свидетельствует о высокой вероятности ОРЛ.
Клинические особенности кардита, полиартрита, поражения нервной системы.
Кардит
Является основным клиническим признаком ОРЛ, который наблюдается в 90-95% случаев.
По рекомендации Американской кардиологической ассоциации (АКА) основным критерием ревмокардита считается вальвулит. Он проявляется органическим сердечным шумом, в сочетании с миокардитом и/или перикардитом.
Ведущий симптом ревматического вальвулита – длительный дующий систолический шум, связанный с I тоном и являющийся отражением митральной регургитации. Этот шум занимает большую часть систолы, лучше всего прослушивается в области верхушки сердца и обычно проводится в левую подмышечную область. Шум может иметь различную интенсивность (в особенности на ранних стадиях заболевания); существенных изменений при перемене положения тела и при дыхании не наблюдается. Чаще всего поражается митральный клапан, затем аортальный и редко трикуспидальный и клапан легочной артерии (для подробной информации также см. подпункты I01.0, I01.1, I01.2).
Ревматический артрит
Отмечается у 75% больных при первой атаке ОРЛ.
Основные характеристики артрита:
- кратковременность;
- доброкачественность;
- летучесть поражения с преимущественным вовлечением крупных и средних суставов.
Полная регрессия воспалительных изменений в суставах происходит в течение 2-3 недель. При современной противовоспалительной терапии время регрессии можно сократить до нескольких часов или дней (подробнее см. в подпункте I00).
Малая хорея
Представляет собой ревматическое поражение нервной системы. Наблюдается преимущественно у детей (реже - у подростков) в 6-30% случаев.
Клинические проявления (пентада синдромов):
- хореические гиперкинезы;
- мышечная гипотония вплоть до дряблости мышц с имитацией параличей;
- стато-координационные нарушения;
- сосудистая дистония;
- психопатологические явления.
Постановка диагноза ревматической хореи при отсутствии других критериев ОРЛ осуществляется только после исключения других возможных причин поражения нервной системы: хорея Геттингтона, системная красная волчанка, болезнь Вильсона, лекарственные реакции и т.д. (подробнее о дифференциальной диагностике см. в заболеваниях пункта I02).
Принципы лечения РЛ.
•Эрадикация БГСА.
•Подавление активности воспалительного процесса.
•Предупреждение у больных с перенесѐнным кардитом формирования РПС.
•Компенсация застойной сердечной недостаточности у больных РПС.
Направлена на эрадикацию b-гемолитического стрептококка группы А.
Применяется бензилпенициллин в суточной дозе 1500000-4000000 ЕД у подростков и взрослых и 400000-600000 ЕД у детей в течение 10-14 дней с последующим переходом на применение дюрантной формы препарата (бензатин бензилпенициллин).
При непереносимости препаратов пенициллина применяют макролиды:
- азитромицин по схеме взрослым 0,5 г однократно в первые сутки, затем по 0,25 г один раз в день в течение четырех дней;
- или кларитромицин по 250 мг 2 р. в день 10 дней;
- или рокситромицин по 150 мг 2 р. в день 10 дней).
При непереносимотсти пенициллинов и макролидов используется антибиотикик из группы линкозамидов:
- линкомицин по 500 мг 3 р. в день 10 дней;
- или клиндамицин по 150 мг 4 р в день 10 дней.
Патогенетическое лечение ОРЛ заключается в применении глюкокортикоидов и нестероидных противовоспалительных препаратов (НПВП).
В детской кардиоревматологии в настоящее время используется преимущественно преднизолон (особенно при ярко и умеренно выраженном ревмокардите и полисерозитах). Суточная доза препарата составляет 20-30 мг до достижения терапевтического эффекта (как правило, в течение 2 нед.). Далее доза снижается (2,5 мг каждые 5-7 дней) вплоть до полной отмены.
При лечении ОРЛ у взрослых препаратами выбора считаются индометацин и диклофенак (150 мг в сутки в течение 2 мес.).
Показания для назначения НПВП:
- низкая степень активности;
- изолированный суставной синдром;
- затяжное, латентное течение.
Показания для назначения глюкокортикоидов:
- ярко и умеренно выраженный кардит;
- максимальная или умеренная степень активности;
- острое, реже - подострое и рецидивирующее течение;
- малая хорея;
- наличие вальвулита.
При наличии симптомов недостаточности кровообращения в план лечения включают сердечные гликозиды и диуретики. Схема их назначения аналогична таковой при лечении сердечной недостаточности другой этиологии.
Назначение сердечных гликозидов и диуретиков в сочетании с противовоспалительными средствами оправдано при активном течении ревматического процесса только на фоне неревматического порока сердца.
Применение кардиотонических препаратов нецелесообразно при развитии сердечной декомпенсации как следствия первичного ревмокардита (в основном встречается только в детском возрасте). В данных случаях явный терапевтический эффект может быть достигнут при использовании высоких доз преднизолона (40-60 мг в сутки).
Поскольку глюкокортикоиды оказывают специфическое воздействие на минеральный обмен, а также в связи с достаточно высоким уровенем дистрофических процессов в миокарде (особенно у больных с повторной ОРЛ на фоне порока сердца), следует применять в терапии препараты калия (панангин, аспаркам), анаболические гормоны, рибоксин и поливитамины.
В случаях тяжелого течения заболевания, когда развиваются признаки выраженной сердечной недостаточности на фоне вальвулита, может быть рекомендовано хирургическое лечение – вальвулопластика либо протезирование клапана.
Первичная профилактика ОРЛ
В основе - своевременная диагностика и адекватная терапия активной А-стрептококковой инфекции верхних дыхательных путей (фарингит, тонзиллит).
Необходимое лечение в случае возникновения острого А-стрептококкового тонзиллофарингита у лиц молодого возраста, имеющих факторы риска развития ОРЛ (отягощенная наследственность, неблагоприятные социально-бытовые условия и др.): 5-дневное лечение бензилпенициллином в суточной дозе 1500000-4000000 ЕД у подростков и взрослых и 400000-600000 ЕД у детей в течение 10-14 дней с последующей однократной инъекцией бензатин бензилпенициллина.
В других ситуациях возможно применение оральных пенициллинов в течение 10 дней (амоксициллин). Рекомендуемая схема применения амоксициллина - 1-1,5 г (для взрослых и детей старше 12 лет) и 500-750 мг (для детей от 5 до 12 лет) в сутки.
Вторичная профилактика ОРЛ
Направлена на предотвращение рецидивов заболевания.
Применяют препараты пролонгированного действия: бициллин-1 (бензатинпенициллин, экстенциллин) и бициллин-5. Бициллин-1 менее аллергичен и дольше сохраняется в необходимой концентрации (21 день против 7-14 дней у бициллина-5).
Бициллин-1 вводят в/м:
- взрослым и подросткам - 2,4 млн ЕД;
- детям при массе тела менее 25 кг - 600 000 Ед;
- детям с массой тела более 25 кг -1,2 млн ЕД.
Бициллинопрофилактика начинается в стационаре сразу после окончания ежедневной антибактериальной терапии и проводится круглогодично. Ее длительность устанавливается индивидуально для каждого пациента. Для больных, перенесших ОРЛ без кардита (артрит, хорея) длительность - не менее 5 лет после атаки или до 18 лет ( по принципу "что дольше"). Для больных с излеченным кардитом без порока сердца длительность - не менее 10 лет или до 25-летнего возраста ( по принципу "что дольше").
Ревматоидный артрит (РА). Определение. Этиология и патогенез. Клинические особенности суставного синдрома. Понятие о суставах «включения» и «исключения». Висцеральные поражения при ревматоидном артрите. Лабораторная и инструментальная диагностика. Рентгенологические стадии РА по Штейнброкеру. Классификационные критерии ревматоидного артрита ACR/EULAR 2010 г. Оценка активности РА по индексу DAS28. Оценка функциональной активности.
Ревматоидный артрит (РА) – иммуновоспалительное (аутоиммунное) ревматическое заболевание неизвестной этиологии, характеризующееся хроническим эрозивным артритом и системным поражением внутренних органов, приводящее к ранней инвалидности и сокращению продолжительности жизни пациентов.
Этиология и патогенез
В качестве фактора, инициирующего аутоиммунные механизмы, предполагается роль избыточного цитруллинирования (замены нормальной аминокислоты аргинина на атипичную – цитруллин) белков, наблюдающегося в ответ на курение, гипоксию, инфекцию полости рта (пародонтит), под влиянием фермента пептидил аргинин дезаминазы. Цитруллинированние белков может запускать активацию иммунокомпетентных клеток (дендритных клеток, макрофагов, Т- и В-лимфоцитов), связанную с нарушением толерантности к этим модифицированным белкам, обусловленная генетическими факторами (носительство HLA-DR4), приводящая к дисбалансу между синтезом «провоспалительных» цитокинов – фактор некроза опухоли (ФНО)-α, интерлейкин (ИЛ)-6, ИЛ-1, ИЛ-17 и антивоспалительных цитокинов (ИЛ-10, растворимого антагониста ИЛ1, растворимых рецепторов ФНОα, ИЛ4).
Развитие иммунного ответа на цитруллинированные белки проявляется синтезом АЦБ, иногда за долго до клинического дебюта болезни. Активированные клетки вырабатывают провоспалительные цитокины, такие как ИЛ-1, ФНО-α, ИЛ-6, ИЛ-8, активируя Т-лимфоциты-хелперы (Helper) 1-го типа (Th1) и Th17 клетки. Стимулированные Тh1 и Th17 клетки вырабатывают ИЛ-2, ФНО-α, ИФН-γ, ИЛ-17, ИЛ-21, вызывающие активацию В-лимфоцитов. Последние трансформируются в плазматические клетки, продуцирующие аутоантитела преимущественно IgG изотипа.
Одновременно активируются тучные клетки, секретирующие медиаторы воспаления (гепарин, серотонин и др.). В результате возникает экссудативно-пролиферативное воспаление синовиальной оболочки суставов (синовит), характеризующееся формированием лимфоцитарных инфильтратов, накоплением макрофагов, развитием неоангиогенеза, пролиферацией клеток синовиальной оболочки и фибробластов с образованием агрессивной ткани – паннуса.
Клетки паннуса выделяют протеолитические ферменты, разрушающие хрящ, одновременно под воздействием гиперпродукции провоспалительных цитокинов (ФНО-α и др.) происходит активация остеокластов, что ведет к осетопорозу (локальному и системному) и в дальнейшем, деструкции костной ткани с образованием эрозий (узур). При развитии внесуставных проявлений играют роль те же клеточные иммуновоспалительные механизмы, а также возникновение иммунокомлексного васкулита, связанного с продукцией аутоантител (АЦБ, РФ).
Клинические особенности суставного синдрома
Характерно разнообразие вариантов начала заболевания. В большинстве случаев заболевание начинается с полиартрита, реже проявления артрита могут быть выражены умеренно, а преобладают артралгии, утренняя скованность в суставах, ухудшение общего состояния, слабость, похудание, субфебрильная температура, лимфаденопатия, которые могут предшествовать клинически выраженному поражению суставов.
Суставы исключения: не учитываются изменения дистальных межфаланговых суставов, первых запястно-пястных суставов и первых плюснефалановых суставов.
Периферический артрит клинически проявляется болью, припухлостью, ограничением подвижности суставов. Сустава «включения» – артрит пястнофаланговых (ПЯФ), проксимальных межфаланговых (ПМФ) суставов кистей, лучезапястных суставов межфаланговые суставы больших пальцев кистей; в ряде случаев поначалу превалирует поражение плюснефаланговых (ПЛФ) или крупных суставов.
Для развёрнутой и финальной стадии заболевания характерны следующие изменения суставов и связочного аппарата: ульнарная девиация пястно-фаланговых суставов (ласта моржа), обычно развивающаяся через 1–5 лет от начала болезни; поражение пальцев кистей по типу «бутоньерки»( сгибание в проксимальных межфаланговых суставах) или «шеи лебедя»( переразгибание в проксимальных межфаланговых суставах); деформация кисти по типу «лорнетки»; подвывихи головок плюснефаланговых суставов, латеральная девиация, деформация большого пальца стопы; сгибательная и вальгусная деформация коленных суставов; подвывихи в области атлантоаксиального сустава; тендосиновит в области лучезапястного сустава и кисти; бурсит, чаще в области локтевого сустава; синовиальная киста на задней стороне коленного сустава (киста Бейкера).
Висцеральные поражения
• поражения плевры и перикарда (сухие, реже эксудативные плевритыи перикардиты)
• поражение почек (амилоидоз почек, очаговый нефрит, пиелонефрит)
• ревматоидный васкулит (сопровождается поражением внутренних органов, кожными симптомами, носовыми и маточными кровотечениями, церебральным и абдоминальным синдромом, невритами)
• поражение сердца (дистрофия миокарда, миокардит, эндокардит, что приводит к относительной недостаточности МК)
• поражение легких (хроническая интерстициальная пневмония с рецидивами в период обострения ревматоидного артрита)
• поражение нервной системы (ревматоидная нейропатия, нарушения мозгового кровообращения)
• поражение печени (сопровождается повышением патологических функциональных проб)
• изменения со стороны желудочно-кишечного тракта (гипоацидный гастрит)
• поражение глаз (ириты и ириоциклиты)
Лабораторная и инструментальная диагностика
• Ревматоидный фактор (Ig М РФ) и антител к цитруллинированным белкам (АЦБ)
• СОЭ и СРБ
Определение АЦЦП имеет важное значение для диагностики серонегативного (по РФ) РА, дифференциальной диагностики РА с другими заболеваниями, риска кардиоваскулярных осложнений.
Общий анализ крови; биохимический анализ крови: АСТ и АЛТ, креатинин, глюкоза; маркеры вирусов гепатита В, С и вируса иммунодефицита человека (ВИЧ; тест на беременность.
Обзорная рентгенография кистей и стоп. Для РА характерно множественное и симметричное поражение мелких суставов кистей и стоп.
МРТ- более чувствительный метод выявления артрита в дебюте РА, чем стандартная рентгенография суставов. Изменения, выявляемые с помощью МРТ (синовит, теносиновит, отёк костного мозга и эрозии костной ткани), позволяют прогнозировать прогрессирование деструкции суставов.
УЗИ для выявления «субклинического» синовита, что позволяет судить о выраженности воспаления
Рекомендуется проводить денситометрию с целью диагностики остеопороза у пациентов с РА любого возраста и пола, длительно (>3мес) принимающих системные глюкокортикоиды (ГК).
Рентгенологическая стадия (по Штейнброкеру, в модификации):
стадия. Небольшой околосуставной остеопороз. Единичные кистовидные просветления костной ткани. Незначительное сужение суставных щелей в отдельных суставах.
стадия. Умеренный (выраженный) околосуставной остеопороз. Множественные кистовидные просветления костной ткани. Сужение суставных щелей. Единичные эрозии суставных поверхностей (1-4). Небольшие деформации костей.
стадия. Умеренный (выраженный) околосуставной остеопороз. Множественные кистовидные просветления костной ткани. Сужение суставных щелей. Множественные эрозии суставных поверхностей (5 и более). Множественные выраженные деформации костей. Подвывихи и вывихи суставов.
стадия. Умеренный (выраженный) околосуставной (распространённый) остеопороз. Множественные кистовидные просветления костной ткани. Сужение суставных щелей. Множественые эрозии костей и суставных поверхностей. Множественные выраженные деформации костей. Подвывихи и вывихи суставов. Единичные (множественные) костные анкилозы. Субхондральный остеосклероз. Остеофиты на краях суставных поверхностей.
Классификационные критерии РА ACR/EULAR
|
Баллы |
А. Клинические признаки поражения суставов (припухлость и/или болезненность при объективном исследовании) (0-5 баллов)
>10 суставов (как минимум 1 мелкий сустав) |
0 1 2 3 5 |
B. Результаты лабораторных методов определения РФ и АЦЦП (0-3 балла, требуется положительный результат как минимум 1 метода)
|
0 2 3 |
C. Результаты лабораторных методов определения «острофазовых» показателей (0-1 балл, требуется положительный результат как минимум 1 метода) Нормальные значения СОЭ и СРБ Повышение СОЭ или СРБ |
0 1 |
D. Длительность артрита (0-1 балл) |
0 1 |
Активность болезни:
n. 0 = ремиссия (индекс активности болезни -disease activity score)
o. 1 = низкая (2,6 < DAS28 <3,2)
p. 2 = средняя (DAS28 3,2 - 5,1)
q. 3 = высокая (DAS 28 > 5,1)
в оценку включается число болезненных суствов, число припухших суставов, СОЭ, ООСЗ (общая оценка больныи состояния здоровья по визуальной аналоговой шкале)
Функциональный класс:
I – полностью сохранены: самообслуживание, непрофессиональная и профессиональная деятельность
II – сохранены: самообслуживание, профессиональная деятельность, ограничена: непрофессиональная деятельность
III – сохранено: самообслуживание, ограничены: непрофессиональная и профессиональная деятельность
IV – ограничены: самообслуживание, непрофессиональная и профессиональная деятельность
Ревматоидный артрит (РА). Определение. Классификация. Немедикаментозное лечение. Показания к применению НПВП и глюкокортикоидов. Базисная противовоспалительная терапия. Терапия генно-инженерными биологическими препаратами.
Ревматоидный артрит (РА) – иммуновоспалительное (аутоиммунное) ревматическое заболевание неизвестной этиологии, характеризующееся хроническим эрозивным артритом и системным поражением внутренних органов, приводящее к ранней инвалидности и сокращению продолжительности жизни пациентов.
Классификация
Клиническая классификация ревматоидного артрита
1. Основной диагноз:
серопозитивный
серонегативный
Особые клинические формы ревматоидного артрита:
Синдром Фелти
Болезнь Стилла взрослых
Ревматоидный артрит вероятный
2. Клиническая стадия:
Очень ранняя стадия: длительность болезни <6 месяцев
Ранняя стадия: длительность болезни 6 мес. - 1 год
Развернутая стадия: длительность болезни> 1 года при наличии типичной симптоматики РА
Поздняя стадия: длительность болезни 2 года и более + выраженная деструкции мелких (III-IV рентгенологическая стадия) и крупных суставов, наличие осложнений
3. Активность болезни:
0 = ремиссия (индекс активности болезни -disease activity score)
1 = низкая (2,6 < DAS28 <3,2)
2 = средняя (DAS28 3,2 - 5,1)
3 = высокая (DAS 28 > 5,1)
Немедикаментозное лечение:
Избегать факторов, которые потенциально могут провоцировать обострение болезни (интеркуррентные инфекции, стресс и др.);
Отказ от курения и приёма алкоголя;
Поддержание идеальной массы тела;
Сбалансированная диета,
Обучение пациентов (изменение стереотипа двигательной активности и др.);
Лечебная физкультура (1 -2 раза в неделю);
Физиотерапия: тепловые или холодовые процедуры, ультразвук, иглорефлексотерапия, лазеротерапия;
Ортопедическое пособие (профилактика и коррекция типичных деформаций суставов и нестабильности шейного отдела позвоночника, ортезы, стельки, ортопедическая обувь);
санаторно-курортное лечение показано только больным в стадии ремиссии;
на протяжении болезни необходимы активная профилактика и лечение сопутствующих заболеваний.
Показания к применению НПВП и глюкокортикоидов.
Метотрексат (цитостатик) показан всем пациентам с РА. Назначение ГИБП рекомендуется пациентам с РА при недостаточной эффективности монотерапии метотрексатом или комбинированной терапии метотрексатом и стандартными БПВП.
НПВП пациентам с РА рекомендуется назначать для уменьшения болей в суставах. НПВП пациентам с РА рекомендуется назначать для уменьшения болей в суставах.
Показания для назначения низких доз ГК:
- подавление воспаления суставов до начала действия БПВП.
- при обострении заболевания или развития осложнений терапии БПВП.
- неэффективность НПВП и БПВП.
- противопоказания к назначению НПВП (например, у лиц пожилого возраста с «язвенным» анамнезом и/или нарушением функции почек).
- достижение ремиссии при некоторых вариантах РА (например, при серонегативном РА у лиц пожилого возраста, напоминающем ревматическую полимиалгию).
Базисная противовоспалительная терапия.
Рекомендуется назначение БПВП всем пациентам с РА (включая пациентов с высокой вероятностью развития РА) как можно раньше, не позднее чем через 3–6 мес от момента появления симптомов поражения суставов.
Рекомендуется лечение метотрексатом начинать с дозы 10– 15 мг/нед с быстрым увеличением дозы (по 2,5–5 мг каждые 2–4 нед) до 25–30 мг/нед в зависимости от эффективности и переносимости.
Рекомендуется прием фолиевой кислоты (не менее 5 мг/ неделя) на фоне лечения метотрексата, которую следует назначать не ранее, чем через 24 ч после приема метотрексата.
Лефлуномид (20 мг/день) или сульфасалазин (3-4 г/день) при наличии противопоказаний для назначения метотрексата или плохой переносимости препарата.
Терапия генно-инженерными биологическими препаратами.
Применение ГИБП рекомендуется при недостаточной эффективности (умеренная/высокая активность заболевания), монотерапии МТ или комбинированной терапии МТ и другими БПВП, которые должны применяться в адекватных дозах в течение ≥ 3-х месяцев. Препаратами выбора являются ингибиторы ФНО-a, которые обладают сходной эффективностью и токсичностью.
Базисные противовоспалительные препараты (БПВП) |
|||
Синтетические БПВП |
Генно-инженерные биологические препараты (Биологические БПВП) |
||
Стандартные БПВП
|
«Таргетные» БПВП Тофацитиниб |
Оригинальные ГИБП (биологические БПВП) Ингибиторы ФНО-α:
ГИБП с другим механизмом действия:
|
Биоаналоги ГИБП (биологические БПВП) |
Остеоартрозы. Этиология и патогенез. Факторы риска. Понятие о первичном и вторичном ОА. Классификация по распространенности поражения суставов. Клиническая картина (особенности суставного синдрома). Лабораторная и инструментальная диагностика. Классификация рентгенологических изменений при ОА Келлгрена и Лоуренса. Дифференциальная диагностика ОА.
Остеоартроз (ОА) - гетерогенная группа заболеваний различной этиологии со сходными биологическими, морфологическими, клиническими проявлениями и исходом, в основе которых лежит поражение всех компонентов сустава: хряща, субхондральной кости, синовиальной оболочки, связок, капсулы, околосуставных мышц.
Этиология и патогенез
ОА представляет собой сложный патологический процесс, поражающий все структуры сустава (хрящ, синовиальную оболочку, субхондральную кость, околосуставные ткани), возникающий в результате взаимодействия возрастных, гормональных, генетических и средовых факторов. В развитии ОА ключевую роль играют провоспалительные медиаторы и цитокины, вырабатываемые не только хондроцитами и синовиоцитами, но и клетками жировой (адипоциты) и костной ткани (остеобласты) ткани. Хронический воспалительный процесс, в свою очередь, приводит к изменению метаболизма клеточных структур всех тканей сустава (хондроцитов, синовиоцитов, остеобластов), и нарушению равновесия между анаболическими и катаболическими процессами в тканях в сторону преобладания последних, что в конечном итоге приводит к развитию заболевания.
Факторы риска:
возраст старше 50 лет;
женский пол
ожирение
расовая, этническая принадлежность
физическая активность
наследственность
Понятие о первичном и вторичном ОА
Выделяют две основные формы ОА: первичный (идиопатический) и вторичный, возникающий на фоне различных заболеваний. Первичный ОА может быть локальным, когда поражается одна группа суставов, или генерализованным - поражение 3-х и более суставных групп.
1. Первичный ОА:
1. коленные суставы;
2. тазобедренные суставы;
3. суставы кистей;
4. суставы стоп;
5. позвоночник;
6. другие суставы.
2. Вторичный ОА:
1) метаболические и эндокринные заболевания:
- акромегалия;
- гиперпаратиреоз;
- охроноз;
- гемахроматоз;
- болезнь Вильсона;
- болезнь Гоше;
- кристалл-ассоциированные заболевания (подагра, пирофосфатная артропатия, гидроксиапатитная артропатия); - сахарный диабет; - болезнь Шарко.
2. врожденные, приобретённые, эндемические заболевания:
- болезнь Блаунта;
- болезнь Педжета;
- болезнь Легг-Кальве-Пертеса;
- гемофилии;
- синдром гипермобильности суставов (синдром Марфана, Элерса-Данлоса и др.);
- соскальзывающий эпифиз головки бедренной кости
- врожденный вывих бедра;
- врожденное утолщение вертлужной впадины;
- эпифизарная дисплазия и другие дисплазии опорно-двигательного аппарата - нарушение механики суставов: неодинаковая длина ног, варусно/вальгусные деформации, сколиоз.
Классификация по распространенности поражения суставов.
моноартрит (воспаление одного сустава);
олигоартрит (воспаление 2-3 суставов);
полиартрит (воспаление 4 и более суставов).
Клиническая картина (особенности суставного синдрома).
Рекомендовано учитывать следующие особенности суставного синдрома при ОА:
1. постепенное начало боли;
2. боль в течение большинства дней предыдущего месяца;
3. усиление боли при ходьбе;
4. «стартовые боли», которые возникают после периодов покоя и проходят на фоне двигательной активности;
5. ночная боль (чаще при более выраженных стадиях ОА и свидетельствует о присоединении воспалительного компонента);
6. припухлость сустава (за счёт небольшого выпота или утолщения синовиальной оболочки);
7. утренняя скованность продолжительностью менее 30 мин;
8. крепитация в суставе;
9. ограничение движений в суставе;
10. изменение походки.
Лабораторная и инструментальная диагностика.
Специфичных для ОА лабораторных тестов в настоящее время нет.
ОАК, ОАМ, Б/Х (определение креатинина, глюкозы, общего билирубина, трансаминаз, общего холестерина, липопротеидов высокой плотности (ЛПВП), липопротеидов низкой плотности (ЛПНП)), исследование синовиальной жидкости:
При ОА отсутствуют выраженные воспалительные изменения в клиническом анализе крови, ревматоидный фактор (РФ) - преимущественно не обнаруживают, антитела к циклическому цитруллиновому пептиду (АЦЦП), концентрация мочевой кислоты в сыворотке крови чаще соответствует норме); для исключения воспаления (необходимо исследовать скорость оседания эритроцитов (СОЭ) и С-реактивный белок (СРБ).
Исследование синовиальной жидкости только при наличии синовита в целях дифференциального диагноза (подозрение на воспалительное заболевание суставов или инфекционный артрит, или микрокристаллические артриты);
Рентгенологическое исследование — наиболее достоверный метод для гностики ОА, который выявляет сужение суставной щели, краевые остеофиты и субхондральный склероз.
При подозрении на ОА тазобедренного сустава проводить рентгенологическое исследование костей таза с захватом обоих тазобедренных суставов
При ОА мелких суставов кистей проводить обзорную рентгенографию суставов 2 кистей в прямой проекции на одной пленке.
Классификация рентгенологических изменений при ОА Келлгрена и Лоуренса.
I ст. – Сомнительные рентгенологические признаки;
II ст. – Минимальные изменения (небольшое сужение суставной щели, единичные остеофиты);
Ш ст. – Умеренные проявления (умеренное сужение суставной щели, множественные остеофиты);
IV ст. – Выраженные изменения (суставная щель практически не прослеживается, грубые остеофиты).
Дифференциальная диагностика ОА.
Анкилозирующий спондилоартрит Псевдоподагра Реактивный артрит Псориатический артрит Подагра Фибромиалгия |
Ревматическая полимиалгия Диабетическая артропатия Посттравматический синовит Паранеопластическая артропатия Врождённая гипоплазия головки бедра Ревматоидный артрит Инфекционный артрит |
Остеоартроз (ОА). Определение. Цели лечения. Немедикаментозное лечение. Симптоматические лекарственные средства быстрого действия. Симптоматические лекарственные средства медленного действия. Показания и методы хирургического лечения.
Остеоартроз (ОА) - гетерогенная группа заболеваний различной этиологии со сходными биологическими, морфологическими, клиническими проявлениями и исходом, в основе которых лежит поражение всех компонентов сустава: хряща, субхондральной кости, синовиальной оболочки, связок, капсулы, околосуставных мышц.
Цели лечения.
- Замедление прогрессирования процесса,
- Уменьшение выраженности боли и воспаления,
- Снижение риска обострений и поражения новых суставов,
- Улучшение качество жизни и предотвращение инвалидизации.
Немедикаментозное лечение:
- Физические упражнения при OA способствуют снижению боли и сохранению функциональной активности суставов.
- Диета. Для поддержания нормальной массы тела с позиции механической разгрузки суставов, а также профилактики сердечно- сосудистой патологии.
- Ортезы для коленных суставов применяются при начальных стадиях заболевания
Симптоматические лекарственные средства быстрого действия:
Рекомендовано при слабых или умеренных болях в суставах применять парацетамол в минимальной эффективной дозе, но не выше 3,0 г/сут.
НПВП при неэффективности парацетамола, при наличии признаков воспаления. При сильной боли в суставах лечение следует начинать сразу с НПВП. НПВП применяются в минимальной эффективной дозе, назначаются на максимально короткие сроки. Для купирования боли при ОА коленных и суставов кистей и при нежелании больного принимать НПВП внутрь рекомендуются трансдермальные (топические) формы НПВП.
Трамадол (опиоидный анальгетик) рекомендовано применять для купирования в течение короткого периода сильной боли при неэффективности парацетамола или НПВП, а также невозможности назначения оптимальных доз этих ЛС. Применяют в первые дни по 50 мг/сутки с постепенным увеличение дозы до 200–300 мг/сут в течение короткого периода времени.
Внутрисуставное введение глюкокортикоидов (ГКС) рекомендовано при ОА с синовитом. Длительность эффекта от 1 нед. до 1 мес. Рекомендуется использовать однократные инъекции метилпреднизолона** (40 мг) или триамцинолона (20 мг или 40 мг). Не рекомендуется выполнять более 1-2 инъекций в год в один и тот же сустав.
Симптоматические лекарственные средства замедленного действия (СЛСЗД)
Рекомендовано всем больным сразу после установления диагноза первичного ОА назначение СЛСЗД.
Симптоматический эффект от применения СЛСЗД развивается через 8-12 недель после начала приема, для структурно-модифицирующего действия препаратов продолжительность лечения должна составлять не менее 2-х лет. В отличие от НПВП после прекращения лечения обладают эффектом последействия в течение 2-4-х месяцев.
Назначение препаратов, содержащие хондроитин сульфат и глюкозамин сульфат или их комбинацию, рекомендовано для уменьшения боли, улучшения функции суставов; эффект сохраняется в течение нескольких месяцев после их отмены, хорошо переносятся
Хондроитин сульфат применяют по 500 мг 2 раза в сутки, длительно. Глюкозамин сульфат назначают по 1500 мг/сутки в течение 4–12 нед., курсы повторяют 2–3 раза в год. Комбинированные препараты содержат 500 мг глюкозамина и 400-500 мг хондроитин сульфата, применяют длительно.
Назначение препарата группы ингибиторы интерлейкина 1 – диацереин рекомендовано для лечения ОА коленных и тазобедренных суставов в качестве симптоматического средства для уменьшения боли и как альтернатива НПВП.
Диацереин оказывает небольшой эффект на уменьшение боли в коленных и тазобедренных суставах. Действие препарата развивается через 2-4 недели, а эффект сохраняется в течение нескольких месяцев после завершения лечения. Из-за высокого риска развития диареи и возможного влияния диацереина на печень, препарат желательно назначать в возрасте до 65 лет. Лечение начинают с 50 мг в сутки на протяжении 2-4 недель, затем дозу увеличивают до 50 мг 2 раза в сутки, длительно.
Назначение препарата группы неомыляемые соединения авокадо и сои (НСАС) – пиаскледин рекомендовано для уменьшения боли, улучшения функции суставов и, вероятно, замедления прогрессирования ОА.
Пиаскледин применяют по 300 мг 1раз в сутки, длительно.
Внутрисуставное введения препаратов группы производные гиалуроната при ОА рекомендовано для уменьшения боли и улучшении функции сустава.
Хирургическое лечение. Эндопротезирование суставов показано у больных ОА с выраженным болевым синдромом, не поддающимся консервативному лечению, при наличии серьёзного нарушения функций сустава (до развития значительных деформаций, нестабильности сустава, контрактур и мышечной атрофии). Наилучшие результаты эндопротезирования отмечены у больных в возрасте 45–75 лет, с массой тела <70 кг, с высоким социальным уровнем жизни.
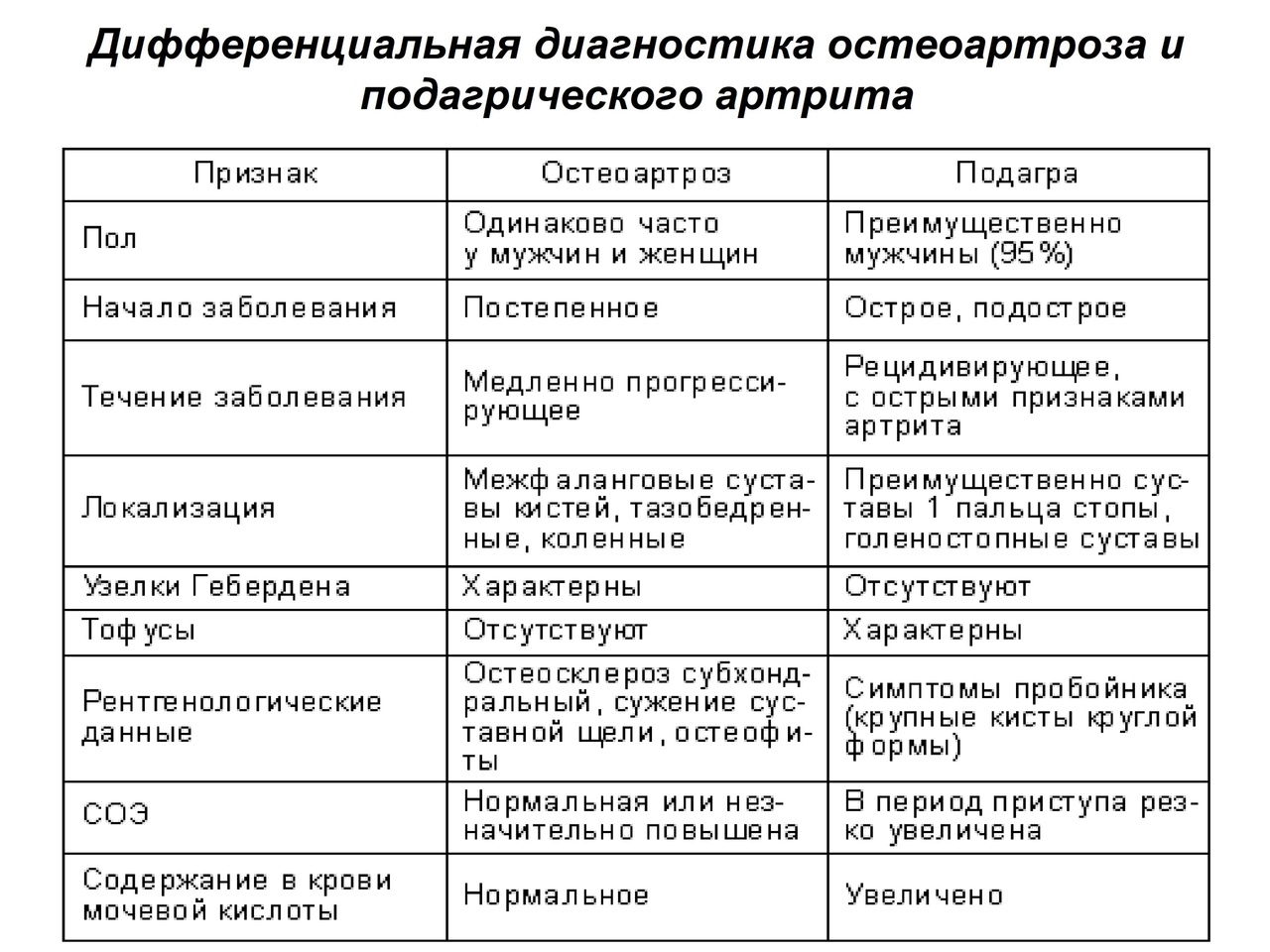
Подагра. Определение. Этиология и патогенез. Факторы риска. Клинические проявления острого подагрического артрита, тофусной подагры, нефролитиаза, подагрической нефропатии. Лабораторная и инструментальная диагностика. Дифференциальная диагностика.
Подагра – системное тофусное заболевание, характеризующееся отложением в различных тканях кристаллов моноурата натрия и развивающимся в связи с этим воспалением у лиц с гиперурикемией, обусловленной внешнесредовыми и/или генетическими факторами.
Этиология и патогенез.
Облигатным фактором развития подагры является гиперурикемия, повышение сывороточного уровня мочевой кислоты выше 420 мкмоль/л, при котором у части пациентов происходит образование кристаллов моноурата натрия. Чем выше сывороточный уровень мочевой кислоты, тем выше риск развития подагры. Формирования кристаллов возможно и при более низком уровне показателя (360 мкмоль/л), прежде всего, у женщин.
Основными причинами гиперурикемии являются генетические факторы, приводящие к повышению реабсорбции и снижению экскреции мочевой кислоты с мочой либо к её гиперпродукции; избыточная масса тела и ожирение, повышение артериального давления, приём алкоголя, потребление большого количества животного белка, приём мочегонных препаратов, заболевания и состояния, характеризующиеся гиперурикемией.
Кристаллы моноурата натрия, формирующиеся в синовиальной жидкости и близлежащих тканях, выступают в качестве триггера острого подагрического артрита, запуская каскад иммунных реакций. Исходно происходит фагоцитоз кристаллов, благодаря высокой в клетках повышается концентрация натрия, вследствие этого происходит компенсаторный приток воды в цитоплазму и набухание клеток, параллельно резко уменьшается содержание калия, индуцируя активацию внутриклеточных инфламмасом, в результате которого синтезируется широкий спектр провоспалительных цитокинов, хемокинов (прежде всего интерлейкина-1 (ИЛ-1), а также ИЛ-6, ИЛ-8, ИЛ-18, фактора некроза опухоли-α(ФНО-α) и др.). Их продукция способствует развитию острой массивной воспалительной реакции, вазодилатации, быстрой миграции к месту воспаления иммунных клеток, преимущественно нейтрофилов [5-7]. Клинически это проявляется острым приступом артрита.
Хронический, вялотекущий воспалительный процесс, связанный с наличием в суставах и окружающих тканях кристаллов моноурата натрия, протекает и вне острого приступа артрита
Факторы риска.
Факторы риска: преобладает у мужчин, ожирение; артериальная гипертензия; инсулинорезистентность, прием лекарств (диуретики); избыточное употребление пива и алкогольных напитков (замедляют выведение мочевой кислоты); генетические дефекты, приводящие к гиперпродукции уратов; другие сопутствующие болезни.
Клинические проявления острого подагрического артрита, тофусной подагры, нефролитиаза, подагрической нефропатии.
ОСТРЫЙ ПОДАГРИЧЕСКИЙ АРТРИТ
- Внезапное начало, быстрое нарастание интенсивных болей, как правило, в одном суставе, гиперемия кожи над суставом, припухлость и нарушение функции поражённого сустава.
- Чаще развивается в ночное время или ранние утренние часы, длительность атаки без лечения варьирует от 1 до 10 дней.
- Острый подагрический артрит может быть спровоцирован травмой, приёмом алкоголя, погрешностями в диете, хирургическими процедурами, обострением сопутствующих заболеваний, локальным воспалением (например, при остеоартрозе).
- Более чем у половины больных первая подагрическая атака проявляется поражением первого плюснефалангового сустава стопы (эта локализация подагрического артрита характерна для 90% больных).
- Общие проявления: лихорадка и лейкоцитоз.
- Характерная особенность острого подагрического артрита - полное спонтанное выздоровление и отсутствие симптомов между приступами до развития хронического подагрического артрита. Без лечения наблюдаются учащение атак, более затяжное течение, вовлечение в процесс новых суставов.
- Особенности подагрического артрита в зависимости от пола и возраста:
- У мужчин преимущественно поражаются суставы стопы, особенно большого пальца (артрит большого пальца в 50% случаев является первым проявлением подагры; в целом развивается более у 80% пациентов).
- У женщин в начале заболевания чаще развивается олиго- и полиартрит (по-видимому, это связано с возрастными особенностями, поскольку у женщин подагра развивается в более пожилом возрасте), чаще поражаются суставы кистей.
- У лиц пожилого возраста чаще наблюдается полиартрикулярный вариант начала подагрического артрита: поражение суставов верхних конечностей (включая мелкие суставы кистей), быстрое развитие тофусов. Развитие артрита часто ассоциируется с приёмом диуретиков.
ХРОНИЧЕСКАЯ ТОФУСНАЯ ПОДАГРА
- Развитие тофусов (часто множественных), хронического артрита, поражения почек, мочекаменной болезни.
- Локализация тофусов: подкожно или внутрикожно в области пальцев кистей и стоп, коленных суставов, на локтях, ушных раковинах, хотя тофусы могут образовываться практически в любых участках тела и во внутренних органах. У женщин в постменопаузе тофусы нередко располагаются в области узелков Гебердена. Иногда наблюдается изъязвление кожи над тофусами со спонтанным выделением содержимого в виде пастообразной белой массы. Раннее появление тофусов наблюдается при некоторых формах ювенильной подагры, у принимающих диуретики женщин пожилого возраста, при миелопролиферативных заболеваниях, при некоторых заболеваниях почек, приводящих к выраженной гиперурикемии.
- Почечные осложнения хроническойгиперурикемии. Мочекаменная болезнь и хроническая уратная (подагрическая) нефропатия являются частыми проявлениями хронической подагры. У 20-40% пациентов наблюдаются протеинурия и «мягкая» артериальная гипертензия, реже нефросклероз, тяжёлая артериальная гипертензия, нарушение функции почек.
- Скудный мочевой синдром (небольшая протеинурия с цилиндрурией, микрогематурией и лейкоцитурией) долгое время может оставаться единственным проявлением подагрической нефропатии, пока не возникают признаки почечной недостаточности с более или менее длительным периодом снижения концентрационной способности почек, а затем азотемией и артериальной гипертонией
- Подагрическая почка (подагрическая нефропатия) - общее понятие, объединяющее многообразные поражения почек при подагре. В основе возникающих при подагре изменений в почках лежит нарушение взаимозависимости гиперурикемии (повышение уровня мочевой кислоты в крови более 0,325 ммоль/л) и гиперурикозурии: при сохранной способности почек удалять избыток мочевой кислоты ее концентрация в крови снижается, но возникает угроза конечной внутриканальцевой задержки мочевой кислоты (например, при дегидратации), что приводит к уменьшению выделения ее почками, а следовательно, появлению гиперурикемии. Такая ситуация возникает прежде всего при первичной подагре- заболевании, при котором первично усилен синтез мочевой кислоты в результате нарушенного обмена нуклеопротеидов и дефицита фермента гипоксантин-гуанинфосфорибозил-трансферазы, что приводит к гиперурикемии.
- Поражение почек может возникнуть и при вторичной подагре, когда гиперурикемия обусловлена применением различных лекарств (тиазидовые диуретики, салицилаты, цитостатики), употреблением алкоголя, вызывающего гиперлактатацидемию, которая тормозит выделение мочевой кислоты почками, а также рядом заболеваний (эритремия, миелолей-коз, гемолитические состояния, миеломная болезнь). При этом и собственно болезни почек еще до стадии ХПН, которым свойственна задержка мочевой кислоты, также могут усугубляться гиперурикемией.
Лабораторная и инструментальная диагностика.
Сывороточный уровень мочевой кислоты.
Выявление кристаллов моноурата натрия в синовиальной жидкости или в содержимом тофуса.
Всем пациентам с отсутствием артрита на момент осмотра проведение диагностической пункции сустава в межприступный период (в этом случае желательно проводить пункцию сустава, воспаленного ранее). Идентификация кристаллов моноурата натрия из невоспаленного сустава позволяет диагностировать подагру в межприступном периоде, хотя вероятность их обнаружения в этом случае несколько меньше.
УЗИ суставов. Этот метод может быть использован для ранней диагностики подагры, в том числе, на преклинической стадии заболевания, так как у части пациентов с гиперурикемией типичные ультразвуковые признаки подагры («двойной контур», вид «метели» в синовиальной жидкости, гиперэхогенные гетерогенные повреждения, окруженные анэхогенными краями (тофусы)) могут выявляться раньше, чем болезнь манифестирует острым приступом артрита.
Не рекомендуется проведение рентгенологического исследования суставов на ранних этапах болезни. Проведение рентгенологического исследования помогает в проведении дифференциального диагноза и может демонстрировать типичные признаки хронической подагры, но не информативно в ранней диагностике подагры.
Дифференциальная диагностика.