
диссертации / 81
.pdf
61
соответствующая значению 95 перцентиля данного показателя у доноров
(n=33): 0,6 пмоль/л.
Рисунок 9
Калибровочная кривая для определения sRANCL методом ИФА.
2.2.9. Методика определения олигомерного матриксного белка хряща
Количественное определение COMP в сыворотке крови проводилось методом ИФА с использованием коммерческого набора реагентов Human Cartilage Oligomeric Matrix Protein ELISA (“BioVendor”, ФРГ) согласно инструкции фирмы-изготовителя. Чувствительность определения COMP
равнялась 4,0 нг/мл (рис. 10). В качестве верхней границы нормы была принята концентрация, соответствующая значению 95 перцентиля данного показателя у доноров (n=33): 1400 нг/мл.

62
Рисунок 10
Калибровочная кривая для определения COMP методом ИФА.
2.2.10. Методика определения матриксной металлопротеиназы-3
Количественное определение ММП-3 в сыворотке крови проводилось методом ИФА с использованием коммерческого набора реагентов (“Bender MedSystems”, Aвстрия) согласно инструкции фирмы-изготовителя.
Чувствительность определения ММП-3 равнялась 0,4 нг/мл (рис. 11). В
качестве верхней границы нормы была принята концентрация,
соответствующая значению 95 перцентиля данного показателя у доноров
(n=24): 9,3 нг/мл.
Рисунок 11
Калибровочная кривая для определения ММП-3 методом ИФА.

63
2.2.11. Методика очистки сыворотки крови от IgM ревматоидного
фактора
Удаление IgM РФ из исследуемых образцов сывороток крови производился с использованием набора реагентов “ВектоРФ-
иммуносорбент” ( ЗАО “Вектор Бест”, Россия) согласно инструкции фирмы изготовителя. Основным компонентом набора является аффинный сорбент, в
котором в качестве лиганда используется IgG человека, специфически связывающие IgM РФ.
2.2.12. Методика определения цитокинового профиля.
Количественное определение 27 цитокинов (IL-1β, -1ra, -2, -4, -5, -6, -7, -8, -9, -10, -12, -13, -15, -17, FGF, эотаксина, G-CSF, GM-CSF, IFN-γ, IP-10, MCP-1, MIP-1α, MIP-1β, PDGF-BB, RANTES, TNF-α, VEGF) в сыворотке крови и синовиальной жидкости проводилось методом мультиплексного анализа, технологией “xMAP”, на анализаторе Bio-Plex 200 (“Bio-Rad”,
США) с использованием коммерческого набора реагентов Bio-Plex Pro Human Cytokine 27 plex assay (“Bio-Rad”, США) согласно инструкции
Таблица 13 Аналитическая чувствительность и верхняя граница нормы при определении
концентраций цитокинов методом xMAP
Цитокин |
Аналитическая |
Верхняя граница |
|
чувствительность (пг/мл) |
нормы (пг/мл) |
|
|
|
IL-1β |
0,1 |
7,6 |
|
|
|
IL-1ra |
0,4 |
1082,8 |
|
|
|
IL-2 |
2,2 |
37,5 |
|
|
|
IL-4 |
0,1 |
8,9 |
|
|
|
IL-5 |
0,1 |
9,5 |
|
|
|

64
|
|
Продолжение таблицы 13 |
|
|
|
Цитокин |
Аналитическая |
Верхняя граница |
|
чувствительность (пг/мл) |
нормы (пг/мл) |
|
|
|
IL-6 |
0,0 |
33,47 |
|
|
|
IL-7 |
0,0 |
76,5 |
|
|
|
IL-8 |
0,1 |
28,15 |
|
|
|
IL-9 |
0,5 |
186,2 |
|
|
|
IL-10 |
0,1 |
411,3 |
|
|
|
IL-12 |
0,1 |
27,6 |
|
|
|
IL-13 |
0,1 |
63,3 |
|
|
|
IL-15 |
0,1 |
40,8 |
|
|
|
IL-17 |
0,4 |
385,7 |
|
|
|
Эотаксин |
1,7 |
1247,9 |
|
|
|
FGF |
4,1 |
70,1 |
|
|
|
G-CSF |
0,4 |
31,5 |
|
|
|
GM-CSF |
5,4 |
182,1 |
|
|
|
IFN-γ |
0,3 |
2342,6 |
|
|
|
IP-10 |
1,6 |
4064,0 |
|
|
|
MCP-1 |
0,2 |
248,5 |
|
|
|
MIP-1α |
0,4 |
37,2 |
|
|
|
MIP-1β |
0,1 |
153,3 |
|
|
|
PDGF-BB |
1,4 |
93646,9 |
|
|
|
RANTES |
0,4 |
6169,5 |
|
|
|
TNF-α |
2,9 |
65,0 |
|
|
|
VEGF |
0,1 |
313,0 |
|
|
|
фирмы-изготовителя (рис.8). Аналитическая чувствительность определения представлена в табл. 5. В качестве верхней границы нормы была приняты концентрации, соответствующие значению 95 перцентиля данного показателя у доноров (n=30) (табл. 13)
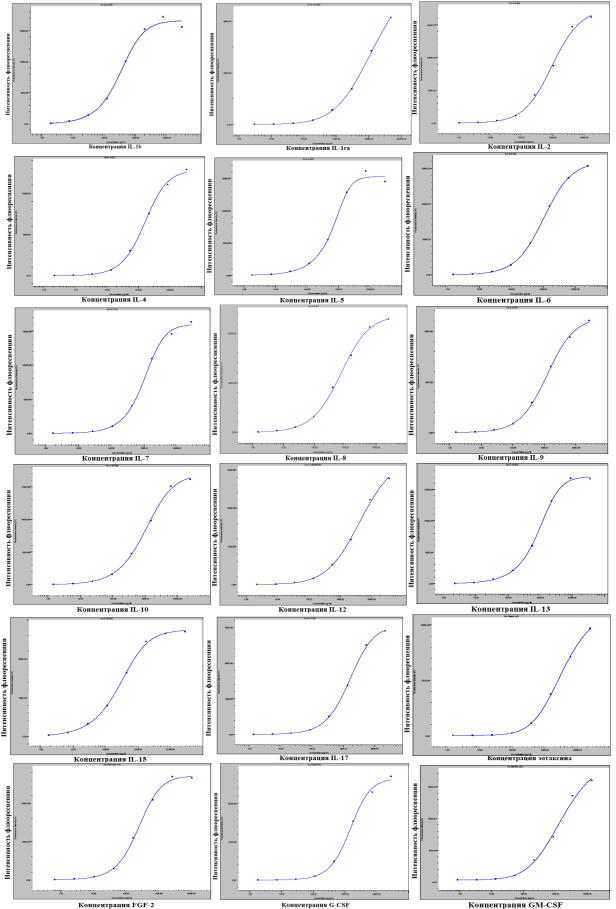
65
Рисунок 8 (а)
Калибровочные кривые исследуемых цитокинов, хемокинов, факторов роста
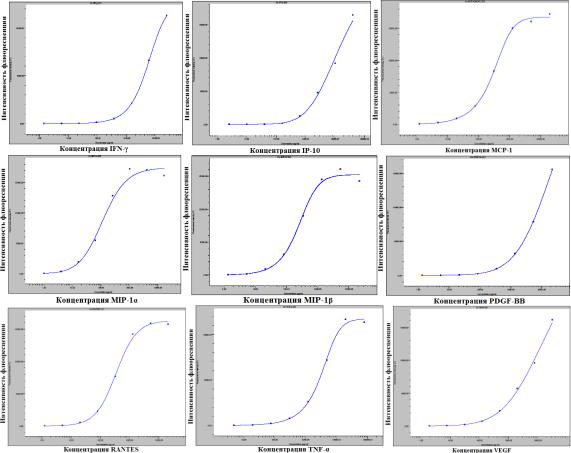
66
Рисунок 8 (б)
Калибровочные кривые исследуемых цитокинов, хемокинов, факторов роста
2.2.13. Методы оценки диагностического значения биомаркеров
при ревматоидном артрите
Оценка диагностического значения биомаркеров РА осуществлялась путем расчета операционных характеристик теста: диагностической чувствительности (ДЧ), диагностической специфичности (ДС), отношения правдоподобия положительного и отрицательного результатов (ОППР и ОПОР) (табл. 14) [296].
Согласно рекомендациям ACR наиболее полезными для диагностики РА считались лабораторные тесты с ОППР>5 и ОПОР<0,2; полезными – с
ОППР>2 и ≤5, ОПОР>0,2 и ≤0,5; не имеющими пользы - с ОППР≤2 и
67
ОПОР>0,5 [43]. Для анализа диагностической эффективности лабораторных тестов использовалась также характеристическая кривая (ROC-кривая),
Таблица 14 Параметры оценки диагностической точности лабораторного теста
Параметры |
Болезнь присутствует |
Болезнь отсутствует |
Результат |
a – истинно |
b - |
положительный |
положительный |
ложноположительный |
Результат |
c – |
d – истинно |
отрицательный |
ложноотрицательный |
отрицательный |
ДЧ |
a/(a+c) |
|
ДС |
d/(b+d) |
|
ОППР |
a/(a+c)/b/(b+d) |
|
ОПОР |
c/(a+c)/d/(b+d) |
|
отражающая зависимость частоты истинно положительных результатов
(чувствительность) от частоты ложноположительных результатов (1-
специфичность). Для оценки ROC-кривых вычислялась площадь под кривой
(ППК), варьирующая от 0,5 (отсутствие диагностической эффективности теста) до 1,0 (максимальная эффективность теста) [297].
2.2.14. Методы статистической обработки результатов исследования
Статистический анализ результатов проводили при участии зав. кафедры медицинской статистики Московской Медицинской Академии им. И.М.
Сеченова, д.м.н. Герасимова А.Н., с помощью программного комплекса
EpiInfo 7.0, рекомендованного для использования в медико-биологических приложениях. Дистрибутив взят с сайта www.cdc.gov (центр слежения за заболеваемостью и смертностью, США, Атланта). Обработка результатов включала общепринятые методы параметрического и непараметрического анализа. Для описания распределения анализируемых показателей рассчитывали частоты встречаемости для дискретных переменных или параметры для непрерывных, используя стандартное представление M±m,
68
где M – среднее арифметическое, а m – статистическая погрешность его определения (среднеквадратичное отклонение среднего по группе) [298], а
также другие параметры, включая перцентили. Для поверки корректности использования методов параметрической статистики анализировали формы распределения переменных. В случае их не компактности (с целью исключения погрешностей при расчете достоверности различий средних по группам) использовали аналогичные методы непараметрической статистики,
т.е. проводили сравнение не исходных значений переменных, а их рангов.
При сравнении параметров с нормальным распределением применялся парный t-тест для независимых выборок. Для параметров, распределение которых отличалось от нормального, при сравнении двух групп использовали критерий Манна-Уитни, а при сравнении трех и более групп – критерий Краскела-Уоллеса, результаты представлены в виде медианы (Ме) с
интерквартильным размахом (25-й - 75-й перцентили). Корреляционный анализ проводился по методу Спирмена. Различия считались достоверными при p<0,05.
Прогноз значений одной переменной по другим проводили при помощи метода многомерной линейной регрессии (многофакторного анализа), при котором прогноз показателя по показателям 1… n
n
осуществляется в виде прогноз с bk k . Коэффициенты bk в приведенных
k 1
таблицах называются нестандартизованными коэффициентами. Для сравнительного анализа вклада факторов в прогностическую модель приведены также таблицы стандартизованных коэффициентов k,
определяемых как |
|
b |
|
( ) |
, а также статистическая достоверность p их |
||
|
( |
|
|
||||
|
k |
k |
|
k |
) |
|
|
|
|
|
|
|
|
|
|
отличия от нуля. Клиническую значимость полученного прогностического правила определяли при помощи построения ROC-кривой.

69
ГЛАВА 3. РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
3.1.Клиническое значение аутоантител при ревматоидном артрите
3.1.1.Ревматоидные факторы
3.2.1.1. IgM ревматоидный фактор
Обследовано 993 пациента из них, 102 с ранним РА, (длительность <6 месяцев; 79 женщин и 23 мужчины; возраст: 51; 41-62 лет), 891 – с развернутым РА
(длительность >6 месяцев; 733 женщины и 158 мужчин; возраст: 51; 43-56 лет).
Статистически значимых различий по уровню IgМ РФ между группами больных ранним РА и развернутым РА не обнаружено (табл. 15).
Таблица 15 Концентрация IgМ РФ (МЕ/мл) при РА и в группе сравнения
Группы обследованных |
n |
IgМ РФ, Ме (25-75%) |
раннний РА (<6 мес.) |
102 |
39 (5-137) *•† |
развернутый РА (>6 мес.) |
891 |
49 (9,5-200) *•† |
Другие РЗ |
319 |
0 (0-14,3) |
НА |
168 |
0 (0-19) |
СКВ |
27 |
0 (0-0) |
СШ |
15 |
0 (0-0) |
АС |
25 |
0 (0-0) |
ОА |
33 |
0 (0-0) |
OVERLAP |
20 |
36 (5,25-262,0) |
ПА |
9 |
0 (0-0) |
ПСА |
22 |
0 (0-0) |
Здоровые доноры |
297 |
0 (0-0) |
Группа сравнения в целом |
616 |
0,1 (0-17) |
* - р<0,05 относительно здоровых доноров, •-отностительно других РЗ,
†- р<0,05 относительно группы сравнения в целом
Концентрация IgM РФ (МЕ/мл) при раннем РА [39(5-137)] превышала таковую в группе сравнения [0,1(0,0-17), p=0,0001] и не зависела от пола и возраста пациентов. Увеличение сывороточной концентрации IgМ РФ (>15
70
МЕ/мл) отмечалось у 67% больных ранним РА, 54% пациентов имели высокопозитивные результаты определения данного показателя, 13% -
низкопозитивные (табл. 16). Группа пациентов с ранним РА серопозитивных по
IgM РФ достоверно отличалась от серонегативных больных, преобладанием пациентов с высокой активностью заболевания по DAS28 (52% vs 32%; p=0,04), II-ым функциональным классом заболевания (24,5% vs 0,0, p=0,0001), с II
рентгенологической стадией по Стейнброкеру (79% vs 60%, p=0,02), более высокой концентрацией IgА РФ [54,5(23,0-200,1) vs 19,3(18,6-19,4) Ед/мл, p=0,01],
АЦЦП [100,0(9,1-100,0) vs 0,9(0,3-7,6) Ед/мл, p=0,0001] и АМЦВ [133,6(26,5- 823,0) vs 4,3(0,3-30,5) Ед/мл, p=0,0001]. В группе раннего РА с высокопозитивными значениями IgM РФ в отличие от низкопозитивных по данному показателю больных преобладали пациенты с II рентгенологической стадией заболевания (40% vs 12%, p=0,004). Среди больных ранним РА позитивных по IgM РФ, по сравнению с пациентами негативными по данному показателю чаще выявлялись IgA РФ (13/17, 76% vs 1/4, 25%, p=0,01), АМЦВ
(33/42, 79% vs 10/20, 50%, p=0,001) и АЦЦП (52/68, 76% vs 9/34, 26%, p=0,0001), c
преобладанием высокопозитивных значений АЦЦП (42/52, 90%, p=0,0001). АКА обнаруживались всего у 41% (9/22) больных ранним РА серопозитивных по IgM
РФ и у 30% (3/10) - серонегативных. При раннем РА, отмечена корреляция сывороточного уровня IgM РФ с концентрацией СРБ (p=0,03) и ЧПС (p=0,03)
(табл. 18). В целом, АЦБ обнаруживались одновременно c IgM РФ в 3,6 раза чаще
(58/68, 85%) чем изолированно (8/34, 23,5%, p=0,001). Концентрация IgM РФ
(МЕ/мл) при развернутом РА [49(9,5-200)] превышала таковую в группе сравнения [0,1(0,0-17), p=0,0001] и не зависела от пола и возраста пациентов. У
больных развернутым РА увеличение сывороточной концентрации IgМ РФ (>15
МЕ/мл) отмечалось у 66% больных РА: 52% пациентов имели высокопозитивные результаты определения данного показателя, 14% - низкопозитивные (табл. 17). У
позитивных по IgM РФ больных развернутым РА, по сранению с негативными,
выявлено более высокое содержание IgA РФ [263,3(100,7-500,0)1 vs 20,9(15,0-
29,4) Ед/мл, p=0,0001], АЦЦП [100,0(50,5-200,0) vs 13,8(0,6-100,0) Ед/мл.,
