

23
105  Zn + NaOH + H2O → Na[Zn(OH)3] + H2
Zn + NaOH + H2O → Na[Zn(OH)3] + H2
Взадачах 106 – 120 укажите, в каких процессах произошло окисление,
ав каких – восстановление. Укажите степени окисления атомов соответствующих элементов и количество отданных или принятых им иэлектронов:
№ п/п |
Схемы уравнений реакций |
||
106 |
а) NO2− → NO2; |
б) NH4+ → N2O; |
c) Cl2 → ClO − |
107 |
a) IO3− → I2; |
б) NO3− → N2; |
в) NO2 → NO2− |
108 |
a) NO2− → NO3−; |
б) NO3− → NO; |
в) S → SO32− |
109 |
a) Cl − → ClO3−; |
б) H2O2 → O2; |
в) NO3− → NH4+ |
110 |
a) I2 → IO3−; |
б) SO32− → S; |
в) ClO3 − → Cl − |
111 |
a) MnO4− → MnO42−; |
б) Cr 3+ → Cr2O72−; |
в) SO32− → SO2 |
112 |
a) SO32− → SO42−; |
б) MnO4− → MnO2; в) Sn 2+ → Sn 4+ |
|
113 |
a) Cl2 → Cl −; |
б) Fe → Fe 2+; |
в) Cr2O72− → Cr 3+ |
114 |
a) MnO4− → MnO(OH)2; б) SO42− → S 2−; |
в) I − → I2 |
|
115 |
a) [Сr(OH)4] − → CrO4 2−; б) Br2 → Br −; |
в) NO3− → N2O |
|
116 |
a) Al → [Al(OH)4] −; |
б) H + → H2; |
в) Cu 2+ → Cu + |
117 |
a) Zn → [Zn(OH)4] 2−; |
б) Fe 2+ → Fe; |
в) H2O2 → H2O |
118 |
a) SeO32− → SeO4 2−; |
б) Cl2 → Cl −; |
в) S 2− → S |
119 |
a) As2O3 → AsO43−; |
б) NO3− → NO; |
в) SO32− → S |
120 |
a) MnO4− → Mn 2+; |
б) SO32− → SO42−; |
в) SnO22− → SnO32− |
Кинетика гомогенных реакций
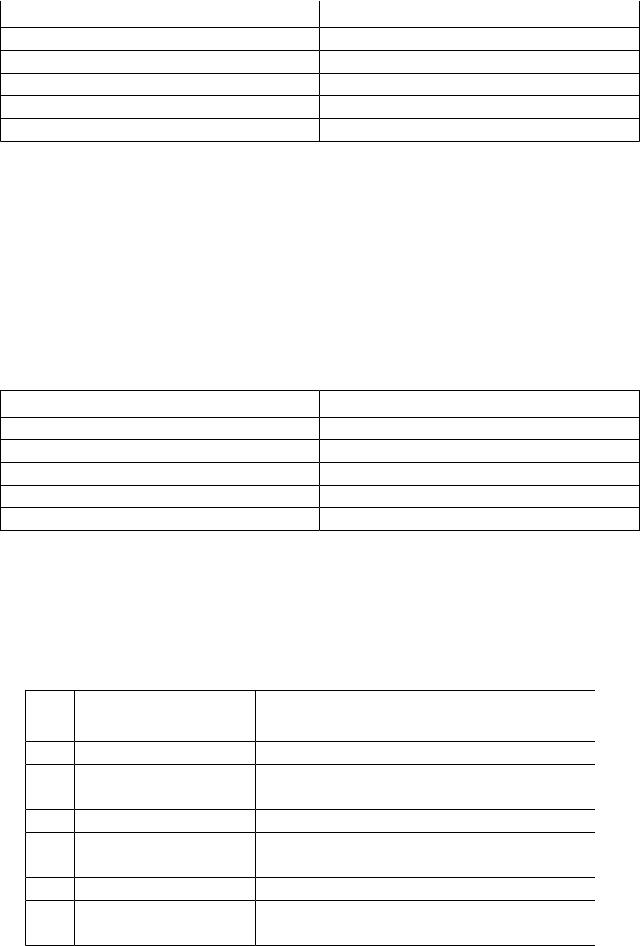
В задачах 1-10 определите, во сколько раз изменится скорость данной элементарной реакции (все участники реакции – газообразные вещества) при изменении условий ее проведения: 1) при уменьшении концентрации компонента А в 3 раза; 2) при увеличении общего давления в системе в 4 раза. Напишите выражение для скорости реакции. Укажите порядок реакции по каждому реагенту и общий порядок реакции. Температура системы постоянна.
|
|
24 |
|
№ |
Реакция |
№ |
Реакция |
1 |
2A → B |
6 |
2A + C → F + D |
2 |
2A + B → C |
7 |
A → B |
3 |
A + 2B →C |
8 |
2A → 2B + C |
4 |
3A → C + D |
9 |
A + B + C → D |
5 |
A + B → C |
10 |
A + 2C → 3D |
В задачах 11-20 определите, во сколько раз изменится скорость данной элементарной реакции реакции (все участники реакции – газообразные вещества) при изменении условий ее проведения: 1) при увеличении парциального давления компонента A в 2 раза; 2) при трехкратном увеличении объема системы. Температура системы постоянна.
№ |
Реакция |
№ |
Реакция |
|
11 |
2A |
→ B |
16 |
2A + C → F + D |
12 |
2A |
+ B → C |
17 |
A → B |
13 |
A +2B → C |
18 |
2A → 2B + C |
|
14 |
3A → C+ D |
19 |
A + B + C → D |
|
15 |
A + B → C |
20 |
A + 2C → 3D |
|
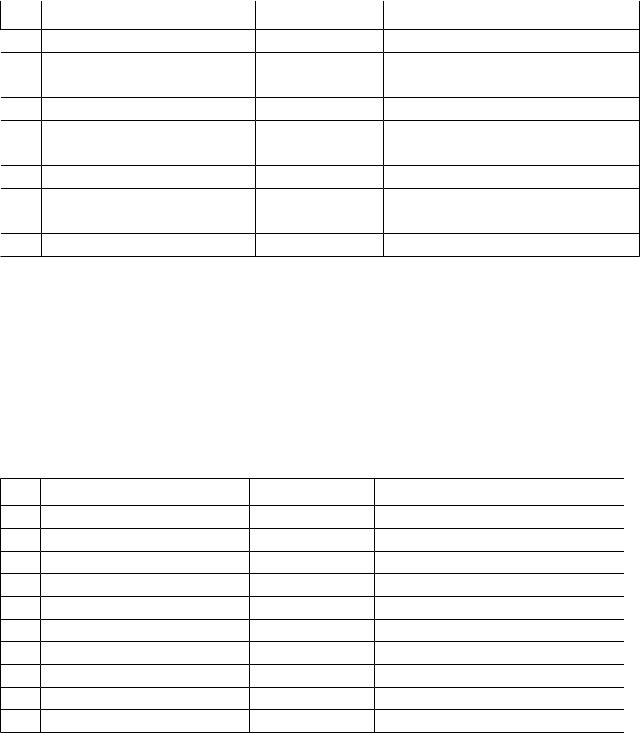
В задачах 21-30 определите, во сколько раз изменится скорость реакции после того, как прореагирует указанная доля α(%) одного из реагентов, если известны исходные концентрации реагирующих веществ.
№
21
22
23
24
25
26
27
28
29
30
Реакция |
С0 А, моль/л |
С0 В, моль/л |
α, % |
|
2B + A → 3C |
1 |
2 |
25% A |
|
2B + A → C |
1,5 |
3,0 |
25% B |
|
A + B → C + D |
1,2 |
2,0 |
75% А |
|
2A |
→ B + C |
2,6 |
0 |
90% А |
A + B → 2C |
3,0 |
3,5 |
60% В |
|
3A |
→ C+ D |
0,5 |
0 |
10% А |
A + 2B → 3D |
1,4 |
3,0 |
30% В |
|
2A |
→ 2D + B |
3,0 |
0 |
40% А |
2A |
+ B → C + D |
0,8 |
1,5 |
80% А |
3A |
→ D + 2F |
2,0 |
0 |
70% А |
25
В задачах 31-40 определите, во сколько раз изменится скорость реакции, если к некоторому моменту времени концентрации веществ уменьшились на значения, приведенные в таблице. Исходные концентрации веществ (С0) известны.
№
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
Реакция |
С0 (А), моль/л |
С0 (В), моль/л |
С(А), моль/л |
||
2A |
→ B |
3,0 |
0 |
0,5 |
|
2A |
+ B → C |
2,0 |
1,0 |
1,2 |
|
A + 2B |
→ C |
1,0 |
2,0 |
0,2 |
|
3A |
→ C +D |
2,0 |
0 |
0,6 |
|
2B + A → C + D |
1,5 |
3,0 |
0,4 |
||
2A |
+ B → D |
4,0 |
2,0 |
0,8 |
|
2B +А→ C |
2,5 |
1,2 |
0,5 |
||
A + 2B → D |
3,0 |
6,0 |
1,4 |
||
3B+А → D + F |
1,40 |
2,0 |
0,3 |
||
2A |
+ B → D + F |
1,2 |
0,6 |
0,4 |
|
В задачах 41-50 определите, во сколько раз изменится скорость реакции по сравнению с начальной скоростью к некоторому моменту времени, если известна концентрация продукта реакции D (CD). Начальные концентрации веществ (С0 ) приведены в таблице. Предполагается, что в начальный момент времени концентрация продукта реакции D равна нулю.
№ |
Реакция |
С0 А, моль/л |
С0 В, моль/л |
CD, моль/л |
|
41 |
2A → D |
3,0 |
0 |
0,5 |
|
42 |
2A |
+ B → D |
2,0 |
1,0 |
0,6 |
43 |
A + 2B → D |
1,0 |
2,0 |
0,2 |
|
44 |
3A |
→ C + D |
3,0 |
0 |
0,5 |
45 |
2B + A → C + D |
1,5 |
3,0 |
0,4 |
|
46 |
2A |
+ B → D |
4,0 |
2,0 |
0,8 |
47 |
2B → D |
0 |
1,2 |
0,2 |
|
48 |
A +2B → D |
3,0 |
6,0 |
1,4 |
|
49 |
3B → D + F |
0 |
3,0 |
0,3 |
|
50 |
2A |
+ B → D + F |
1,2 |
0,6 |
0,4 |

26
В задачах 51-64 определите величину энергии активации реакции в интервале температур от 400 К до 500 К, если известен температурный коэффициент скорости реакции γ.
№ |
γ |
№ |
γ |
51 |
1,94 |
58 |
2,0 |
52 |
2,06 |
59 |
2,5 |
53 |
2,19 |
60 |
3,06 |
54 |
2,32 |
51 |
2,96 |
55 |
2,47 |
62 |
3,14 |
56 |
2,62 |
63 |
3,33 |
57 |
2,78 |
64 |
2,2 |
В задачах 65-76 рассчитайте энергию активации и температурный коэффициент скорости реакции, если известно время протекания реакции (t) при двух температурах при прочих равных условиях. За скорость реакции принять среднюю скорость, равную ±ΔС/t.
№ |
|
Т, К |
t, мин |
№ |
|
Т, К |
t, мин |
65 |
Т1 = 303К |
t1=25мин |
71 |
Т1 = 293К |
t1=20мин |
||
|
Т2 = 323К |
t2=4мин |
|
Т2 = 313К |
t2=5мин |
||
66 |
Т1 = 298К |
t1=21мин |
72 |
Т1 = 308К |
t1=18мин |
||
|
Т2 = 318К |
t2=6мин |
|
Т2 = 328К |
t2=3мин |
||
67 |
Т1 = 313К |
t1=12мин |
73 |
Т1 = 318К |
t1=9мин |
||
|
Т2 = 333К |
t2=2мин |
|
Т2 = 338К |
t2=1,5мин |
||
68 |
Т1 = 273К |
t1=42мин |
74 |
Т1 = 323К |
t1=7,2мин |
||
|
Т2 = 293К |
t2=6,7мин |
|
Т2 = 343К |
t2=1,2мин |
||
69 |
Т1 |
= 278К |
t1=35мин |
75 |
Т1 |
= 333К |
t1=14мин |
|
Т2 |
= 298К |
t2=5мин |
|
Т2 |
= 353К |
t2=2,3мин |
70 |
Т1 |
= 283К |
t1=30мин |
76 |
Т1 |
= 288К |
t1=20мин |
|
Т2 |
= 303К |
t2=7мин |
|
Т2 |
= 308К |
t2=7мин |
В задачах 77-86 рассчитайте, сколько времени будет длиться реакция при температуре Т2 , если известен температурный коэффициент скорости (γ) и время t1, за которое реакция заканчивается при температуре Т1 при прочих

27
равных условиях. За скорость реакции принять среднюю скорость, равную ±ΔС/t.
№ |
Т1, К |
t1, мин |
Т2, К |
γ |
77 |
303 |
25 |
323 |
2,0 |
78 |
293 |
20 |
313 |
2,5 |
79 |
298 |
21 |
318 |
2,06 |
80 |
308 |
18 |
328 |
2,32 |
81 |
313 |
12 |
333 |
2,19 |
82 |
273 |
42 |
293 |
3,0 |
83 |
278 |
35 |
298 |
3,3 |
84 |
333 |
13,8 |
353 |
2,62 |
85 |
283 |
30 |
303 |
3,14 |
86 |
288 |
20 |
308 |
2,9 |
В задачах 87-96 определите, на сколько градусов нужно повысить температуру, чтобы скорость реакции возросла в n раз, если известен температурный коэффициент скорости реакции (γ).
№ |
γ |
n |
№ |
γ |
n |
87 |
2.5 |
40 |
92 |
3.14 |
150 |
88 |
3.06 |
20 |
93 |
2.9 |
60 |
89 |
2.32 |
10 |
94 |
3.3 |
200 |
90 |
3.14 |
100 |
95 |
2.06 |
10 |
91 |
2.62 |
30 |
96 |
2.19 |
50 |
В задачах 97-106 рассчитайте температурный коэффициент скорости реакции, энергию активации и предэкспоненциальный множитель в уравнении Аррениуса, если известны значения констант скоростей реакции при двух температурах.
№ |
Реакция |
T, К |
k |
|
97 |
А → В |
298 |
9 . 10—3 мин – 1 |
|
|
|
303 |
1,3 . 10 – 2 |
мин - 1 |
98 |
С → D |
303 |
2,2 . 10 –3 |
мин – 1 |
|
|
308 |
4,1 . 10 – 3 |
мин - 1 |
99 |
А → В |
273 |
2,46 . 10 – 5 мин – 1 |
|

|
|
28 |
|
|
|
313 |
5,76 . 10 – 3 мин - 1 |
100 |
А + В → С |
282 |
2,37 л / (моль . мин) |
|
|
287 |
3,204 л / (моль . мин) |
101 |
С → D |
823 |
2,5 . 105 с – 1 |
|
|
903 |
1,415 . 107 с - 1 |
102 |
А → В |
323 |
1,8 . 10 2 с – 1 |
|
|
343 |
3,2 . 102 с - 1 |
103 |
А + В → С |
298 |
3,29 л / (моль . с) |
|
|
303 |
8,1 л / (моль . с) |
104 |
С + D → F |
333 |
0,75 л / (моль . ч) |
|
|
353 |
0,94 л / (моль . ч) |
105 |
A + B → D + F |
497 |
3,6 . 10 –4 л / (моль . мин) |
|
|
547 |
8,6 . 10 – 2 л / (моль . мин) |
106 |
А + В → С |
524 |
1,59 . 10 – 3 л / (моль . мин) |
|
|
550 |
1,59 . 10 – 3 л / (моль . мин) |
В задачах 107-116 рассчитайте энергию активации и температурный коэффициент скорости реакции, если при повышении температуры от Т1 до Т2 скорость реакции увеличилась в n раз.
№ |
Т1, К |
Т2, К |
n |
№ |
Т1, К |
Т2, К |
n |
107 |
823 |
903 |
50 |
112 |
282 |
287 |
1,5 |
108 |
525 |
550 |
2 |
113 |
273 |
313 |
100 |
109 |
497 |
547 |
240 |
114 |
303 |
308 |
5 |
110 |
298 |
303 |
3 |
115 |
298 |
303 |
10 |
111 |
323 |
343 |
10 |
116 |
333 |
353 |
20 |
Кинетика гетерогенных химических реакций
В задачах 1-10 определите, во сколько раз увеличится скорость гетерогенной химической реакции А(Т ) + В → продукты с заданным общим
порядком реакции n и энергией активации ЕА |
при увеличении температуры |
||||
на |
Т, К и увеличении концентрации реагента В в заданное число раз. |
||||
№ |
n |
ЕА |
Т1, К |
Т, К |
С(В)2/С(В)1 |

|
|
|
29 |
|
|
|
|
кДж/моль |
|
|
|
1 |
2 |
54 |
298 |
40 |
2 |
2 |
1,1 |
83 |
298 |
30 |
10 |
3 |
2,0 |
172 |
298 |
20 |
3 |
4 |
1,5 |
146 |
298 |
10 |
1,5 |
5 |
3 |
121 |
298 |
20 |
10 |
6 |
1,7 |
87 |
298 |
20 |
2 |
7 |
1,1 |
109 |
298 |
10 |
10 |
8 |
1,1 |
167 |
310 |
40 |
2 |
9 |
2 |
104 |
400 |
20 |
2 |
10 |
2 |
52 |
400 |
10 |
1,5 |
В задачах 11-20 определите энергию активации гетерогенной реакции, при известном температурном коэффициенте скорости реакции и заданном температурном интервале.
№ |
γ |
T1,оС |
T2, оС |
№ |
γ |
T1,оС |
T2, оС |
11 |
3,4 |
50 |
80 |
16 |
2,6 |
40 |
70 |
12 |
2,7 |
30 |
50 |
17 |
1,8 |
5 |
27 |
13 |
1,7 |
25 |
55 |
18 |
2,9 |
15 |
34 |
14 |
3,3 |
27 |
77 |
19 |
3,7 |
23 |
61 |
15 |
2,4 |
60 |
90 |
20 |
2,1 |
38 |
88 |
В задачах 21-30 при известной энергии активации Еа гетерогенной реакции 1) определите во сколько раз увеличится скорость химической реакции при повышении температуры от Т1 до Т2 ; 2) найдите температурный коэффициент скорости реакции.
№ |
T1, оС |
T2, оС |
Еа |
|
|
|
кДж/моль |
21 |
50 |
80 |
50 |
22 |
30 |
50 |
80 |
23 |
25 |
55 |
220 |
24 |
27 |
127 |
100 |
25 |
60 |
90 |
140 |
26 |
40 |
70 |
65 |
27 |
10 |
30 |
76 |
28 |
35 |
75 |
124 |
29 |
20 |
60 |
203 |
30 |
5 |
45 |
95 |

30
В задачах 31-40 при известной начальной температуре (T1) и температурном коэффициенте реакции определите, до какого значения нужно повысить температуру, чтобы скорость реакции увеличилась в z раз.
№ |
T1, oC |
γ |
z |
31 |
50 |
3,0 |
27 |
32 |
30 |
2,7 |
10 |
33 |
25 |
1,7 |
60 |
34 |
27 |
3,0 |
100 |
35 |
60 |
2,0 |
64 |
36 |
40 |
2,0 |
200 |
37 |
20 |
2,2 |
150 |
38 |
10 |
2,5 |
40 |
39 |
150 |
3,5 |
16 |
40 |
24 |
2,6 |
8 |
В задачах 41-50 определите энергию активации и время, за которое образец твердого вещества полностью прореагирует при заданной температуре T3, если известно время реакции такого же образца при двух других температурах T1 и T2.
№ T1,оС |
τ1, с |
T2,оС |
τ 2 , с |
T3,оС |
|
41 |
18 |
150 |
38 |
10 с |
53 |
42 |
20 |
68 |
40 |
8 с |
60 |
43 |
20 |
36 |
40 |
4 |
65 |
44 |
40 |
6 |
50 |
2 |
65 |
45 |
45 |
3 |
55 |
1 |
65 |
46 |
18 |
25 |
38 |
15 с |
63 |
47 |
38 |
15 с |
63 |
0,96 с |
73 |
48 |
20 |
45 |
40 |
5 |
55 |
49 |
20 |
27 |
40 |
3 |
55 |
50 |
30 |
27 |
50 |
3 |
75 |
В задачах 51-60 определите, во сколько раз увеличится средняя скорость первой и второй гетерогенной реакций, если обе заканчиваются при 298 К за время τ, а при повышении температуры на ΔТ первая реакция заканчивается за время τ1, вторая – за τ2. Определите энергию активации каждой реакции.
№ |
τ ,мин |
Т |
τ 1 ,мин |
τ 2 ,мин |

|
|
31 |
|
|
51 |
27 |
30 |
1,0 |
3,37 |
42 |
54 |
30 |
2,0 |
6,75 |
53 |
32 |
20 |
5,12 |
8,0 |
54 |
25 |
40 |
5,0 |
6 |
55 |
40 |
10 |
3,5 |
1,5 |
56 |
32 |
25 |
1,5 |
2,4 |
57 |
16 |
15 |
10 |
8 |
58 |
28 |
35 |
8 |
2 |
59 |
35 |
5 |
18 |
24 |
60 |
56 |
45 |
8 |
15 |
В задачах 61-70 определите, во сколько раз увеличится константа скорости первой реакции при нагревании от Т1 до Т2 , если известно, что константа скорости второй реакции при нагревании от Т1 до Т2 увеличилась в «b» раз. Энергия активации Еа(1) первой реакции твердофазного взаимодействия в «а» раз больше энергии активации Еа(2) второй реакции.
№ |
61 |
62 |
63 |
64 |
65 |
66 |
67 |
68 |
69 |
70 |
a |
2 |
1,5 |
2,3 |
3 |
1,8 |
1,4 |
2,5 |
1,2 |
2,4 |
1,7 |
b |
100 |
200 |
50 |
10 |
20 |
160 |
300 |
650 |
4 |
2 |
В задачах 71-80 ответьте на вопросы, приведенные в таблице,
используя следующие данные: скорость гетерогенной реакции: |
|
|
|
|||||
|
|
А(Т ) + В(Р) → продукты |
|
|
|
|
||
при концентрации C(B)1 |
= 0,24 моль/л составляет r1 = 7,95 × 10 |
− 3 |
моль |
, когда |
||||
л × мин |
||||||||
|
|
|
|
|
|
|
||
прореагировало 65% |
вещества В, |
скорость реакции составила r2= |
||||||
1,25 × 10− 3 |
моль |
. Начальная концентрация |
C(B)0 = 0,27 моль/л. |
|
|
|
||
л × мин |
|
|
|
|||||
№ |
|
|
|
Вопрос |
|
|
|
|
71 |
|
Определите порядок реакции |
|
|
|
|
||
72 |
|
Определите степень превращения вещества В за 20 минут |
|
|||||
73 |
|
Определите начальную скорость реакции |
|
|
|
|||
74Определите τ 0,1 , время реакции, в течении которого прореагировало 10% вещества В
75 Определите τ 0,7 , время, за которое реакция завершилась на 70%
Определите τ 0,7 , время, за которое реакция завершилась на 70%
76 Определите степень превращения вещества В за 30 минут
Определите степень превращения вещества В за 30 минут

|
32 |
|
77 |
Определите время полупревращения τ 1 |
2 |
|
|
|
78 |
Определите степень превращения вещества В за 10 минут |
|
79 |
Определите константу скорости реакции |
|
80Определите τ х , время реакции, в течении которого прореагировало 65% вещества В
Каталитические реакции
(Для всех задач: изобразите энергетическую диаграмму реакции, протекающую без катализатора и с катализатором, укажите тип реакции – экзо, или эндотермическая)
В задачах 1 – 20 определите, во сколько раз возрастет скорость некоторой реакции в присутствии катализатора, если реакция протекает при 298 К, а энергия активации реакции в отсутствии катализатора равна Еа1 (кДж/моль), а в присутствии катализатора энергия активации понижается до значения Еа2 (кДж/моль)?
№ п/п |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
Еа1, |
100 |
120 |
240 |
206 |
90 |
80 |
81.5 |
150 |
60 |
95 |
|
кДж/моль |
|||||||||||
|
|
|
|
|
|
|
|
|
|
||
Еа2, |
45 |
60 |
180 |
102 |
32 |
53 |
48 |
94 |
20 |
24 |
|
кДж/моль |
|||||||||||
|
|
|
|
|
|
|
|
|
|
||
№ п/п |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|
Еа1, |
110 |
260 |
46 |
320 |
280 |
180 |
54 |
88 |
220 |
72 |
|
кДж/моль |
|||||||||||
|
|
|
|
|
|
|
|
|
|
||
Еа2, |
90 |
150 |
38 |
240 |
175 |
124 |
32 |
51 |
136 |
43 |
|
кДж/моль |
|||||||||||
|
|
|
|
|
|
|
|
|
|
В задачах 21 – 40 определите, во сколько раз возрастает скорость некоторой реакции в присутствии катализатора при указанной температуре, если энергия активации реакции в отсутствии катализатора равна 70 кДж/моль, а в присутствии катализатора равна 36 кДж/моль.
№ п/п |
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
29 |
20 |

|
|
|
|
|
33 |
|
|
|
|
|
Т, 0С |
200 |
30 |
90 |
40 |
35 |
50 |
60 |
72 |
80 |
100 |
№ п/п |
31 |
32 |
33 |
34 |
35 |
36 |
37 |
38 |
39 |
40 |
Т, 0С |
5 |
10 |
25 |
120 |
150 |
140 |
220 |
250 |
110 |
280 |
В задачах 41 – 60 определите энергию активации некоторой реакции, протекающей без катализатора, если в присутствии катализатора она равна указанной величине, а скорость реакции, протекающей в присутствии катализатора при 60 0С, в 10000 раз выше, чем скорость той же реакции при той же температуре в отсутствии катализатора.
№ п/п |
41 |
42 |
43 |
44 |
45 |
46 |
47 |
48 |
49 |
50 |
|
Еа, |
50 |
98 |
84,2 |
93,6 |
106 |
42 |
30,5 |
54 |
63 |
29 |
|
кДж/моль |
|||||||||||
|
|
|
|
|
|
|
|
|
|
||
№ п/п |
51 |
52 |
53 |
54 |
55 |
56 |
57 |
58 |
59 |
60 |
|
Еа, |
120 |
21 |
48 |
130 |
38 |
140 |
68 |
74 |
36 |
160 |
|
кДж/моль |
|||||||||||
|
|
|
|
|
|
|
|
|
|
В задачах 61 – 80 рассчитайте изменение энергии активации некоторой реакции, протекающей при 80 0С в присутствии катализатора со скоростью r1, если известно, как уменьшается скорость реакции без катализатора r2 при той же температуре.
№ п/п |
61 |
62 |
63 |
64 |
65 |
66 |
67 |
68 |
69 |
70 |
r1/ r2 |
50 |
100 |
84,2 |
300 |
38 |
400 |
700 |
74 |
1000 |
29 |
№ п/п |
71 |
72 |
73 |
74 |
75 |
76 |
77 |
78 |
79 |
80 |
r1/ r2 |
200 |
21 |
500 |
93,6 |
600 |
42 |
30,5 |
800 |
63 |
5000 |
В задачах 81 – 100 рассчитайте время протекания реакции первого порядка в присутствии катализатора при температуре 450 0С до степени завершения 90%, если известно аналогичное время протекания этой реакции (t, час) и энергия активации без катализатора (Ea, кДж/моль), а также величина уменьшения энергии активации (ΔEa, кДж/моль) при использовании катализатора.
№ п/п |
81 |
82 |
83 |
84 |
85 |
86 |
87 |
88 |
89 |
90 |

|
|
|
|
|
34 |
|
|
|
|
|
t |
1 |
8 |
12 |
24 |
168 |
720 |
1 |
8 |
12 |
24 |
Ea |
80 |
240 |
160 |
120 |
60 |
300 |
60 |
120 |
80 |
240 |
Ea |
20 |
140 |
80 |
60 |
30 |
200 |
40 |
80 |
35 |
200 |
№ п/п |
91 |
92 |
93 |
94 |
95 |
96 |
97 |
98 |
99 |
100 |
t |
168 |
720 |
1 |
8 |
12 |
24 |
168 |
720 |
1 |
8 |
Ea |
180 |
204 |
45 |
86 |
120 |
280 |
136 |
75 |
126 |
250 |
Ea |
90 |
146 |
24 |
46 |
65 |
184 |
72 |
54 |
64 |
154 |
Химическое равновесие
В задачах 1 - 20 определите стандартное изменение энергии Гиббса rGT0 при заданной температуре Т. Укажите, в каком направлении (прямом или обратном) протекает реакция и как изменится направление реакции при увеличении или уменьшении: a) температуры; б) давления.
№№ п/п |
Уравнение реакции |
Т, К |
1 |
2 Cl2 + 2H2O ↔ 4 HCl + O2 |
800 |
2 |
H2 + Cl2 ↔ 2 HCl |
2000 |
3 |
2 NO + Cl2 ↔ 2 NOCl |
570 |
4 |
PCl3 + Cl2 ↔ PCl5 |
400 |
5 |
H2 + Br2 ↔ 2 HBr |
1150 |
6 |
2 CO + O2 ↔ 2 CO2 |
2000 |
7 |
CO + Cl2 ↔ COCl2 |
1100 |
8 |
2 NO + O2↔ 2 NO2 |
690 |
9 |
N2 + O2 ↔ 2 NO |
4000 |
10 |
CO + 2 H2 ↔ CH3OH |
380 |
11 |
2CO + 2 H2 ↔ CH3 COOH |
680 |
12 |
C2H4 + H2O ↔ C2H5OH |
310 |
13 |
CH4 + 4 Cl2 ↔ CCl4 + 4 HCl |
6650 |
14 |
N2 + 3 H2 ↔ 2 NH3 |
450 |
15 |
C2H4 + H2 ↔ C2H6 |
1050 |
16 |
2SO2 + O2 ↔ 2SO3 |
510 |
17 |
2 NO2 ↔ N2O4 |
600 |
18 |
H2O + CO ↔ CO2 + H2 |
3000 |
19 |
2 H2S +3O2 ↔ 2 SO2 + 2H2O |
600 |
20 |
2CH4 ↔ C2H2 + 3 H 2 |
1900 |
