
Изучение физико-химических характеристик наноматериалов необходимы
..pdfзаряженных наночастиц при довольно низких концентрациях по сравнению с одновалентными катионами, это известно как правило Шульце–Гарди. Коагуляция идет с заметной скоростью лишь при концентрации электролита, превышающей некоторое критическое значение, называемое порогом коагуляции. Выше этой концентрации (в области медленной коагуляции) скорость коагуляции растет с ростом концентрации, пока не достигнет некоторого предела, после которого (в области быстрой коагуляции) перестает зависеть от концентрации электролита – критическая концентрация коагуляции. Очевидно, что области быстрой коагуляции соответствует полная дестабилизация частиц дисперсной фазы. При просмотре фактических диапазонов концентраций одновалентных, двухвалентных и трехвалентных катионов в поверхностных водах становится очевидно, что двухвалентные катионы являются наиболее важными и из них могут быть представлены соли Са2+.
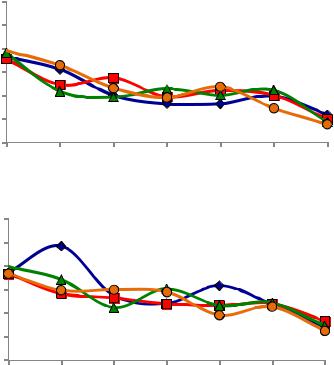
На рис. 12 приведены данные эксперимента по изучению характера коагуляции частиц нанопорошков систем ZrO2-2Y2O3-4CeO2 и ZrO2-2Y2O3-4CeO2-3Al2O3 и скорости их осаждения в зависимости от времени и концентрации электролита Ca(NO3)2 в дисперсии.
В дисперсионной системе без добавки оксида алюминия (рис. 12, а) в начале теста присутствуют примерно от 15 до 21 % от общего теоретически ожидаемого количества частиц, но потом с каждым часом количество взвешенных частиц в дисперсии снижается и к концу эксперимента достигает менее 2 % от общего теоретически ожидаемого количества частиц. В дисперсионной системе с 3%-ной добавкой оксида алюминия ( рис. 12, б) в начале теста присутствуют примерно от 19 до 24 % от общего теоретически ожидаемого количества частиц, но потом с каждым часом количество взвешенных частиц в дисперсии также снижается и к концу эксперимента достигает примерно 4 % от общего теоретически ожидаемого количества.
Можно заметить, что характер кривых в зависимости от концентрации электролита сильно не изменяется. Сравнение рисунков 12, а, б показывает, что после добавки оксида алюминия характер кривых не изменился. Также можно отметить, что все дисперсионные системы претерпевают непрерывную агломерацию с самого начала эксперимента. Это классический случай оседания частиц, вызванного их агломерацией. Также наличие соли нитрата кальция не меняет скорости коагуляции и скорости осаждения частиц, поэтому мы можем
31

сделать вывод, что данная дисперсионная система сама по себе является нестабильной независимо от концентрации электролита Ca(NO3)2 и наличия добавки оксида алюминия.
Доляот ожидаемого Zr, %
Доля от ожидаемого Zr, %
30
25
20 
15 
10
5
0
0
30
25
20 
15
10
5
0
0
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
2 |
3 |
4 |
5 |
6 |
|||||
|
|
|
Время, ч |
|
|
|
|
|
|
|
а
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
2 |
3 |
4 |
5 |
6 |
|||||
Время, ч
б
Рис. 12. Степень стабильности дисперсий порошков без соли Ca(NO3)2 и в ее присутствии: а – дисперсия наноразмерного порошка системы ZrO2-2Y2O3-4CeO2; б – дисперсия наноразмерного порошка системы
ZrO2-2Y2O3-4CeO2-3Al2O3;  – 0 мМ Ca(NO3)2;
– 0 мМ Ca(NO3)2;  – 1мМ Ca(NO3)2;
– 1мМ Ca(NO3)2;
 – 10 мМ Ca(NO3)2
– 10 мМ Ca(NO3)2
На рис. 13 представлены результаты исследования изменения степени стабильности дисперсий в зависимости от концентрации электролита. После изучения скорости и характера коагуляции при помощи двухзарядного иона Са2+ (см. рис. 12), было решено стаби-
32
лизировать дисперсионные системы электростатически при помощи однозарядного иона K+.
Доля от ожидаемого Zr, %
ожидаемого |
Zr,% |
Доляот |
|
30
25
20 
15 10
5
0
0 |
1 |
2 |
3 |
4 |
5 |
6 |
Время, ч
а
30
25
20  15
15
10 5
0
0 |
1 |
2 |
3 |
4 |
5 |
6 |
|
|
|
Время, ч |
|
|
|
б
Рис. 13. Изучение степени стабильности дисперсий наноразмерных порошков в зависимости от количества электролита:
а – система ZrO2-2Y2O3-4CeO2; б – система ZrO2-2Y2O3-4CeO2-3Al2O3;
 – 0,5 мМ KCl;
– 0,5 мМ KCl;  – 1 мМ KCl;
– 1 мМ KCl;  – 2 мМ KCl;
– 2 мМ KCl;  – 5 мМ KCl;
– 5 мМ KCl;
На обоих графиках (рис. 13, а, б) видно, что изменение концентрации электролита не влияет на стабильность дисперсионных систем. Характер кривых идентичен в системе как без добавки, так и с добавкой оксида алюминия. Максимальная степень стабильности дисперсии примерно 20 % от теоретически ожидаемого количества частиц и на-
33
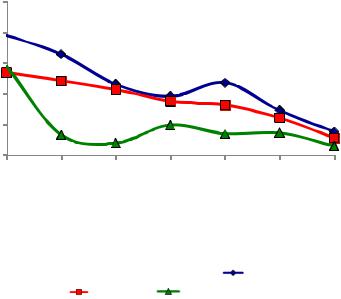
блюдается только в самом начале эксперимента (0 часов). После прохождения первого часа ожидания частицы начинают агломерировать и осаждаться. После этого с каждым часом количество взвешенных частиц в дисперсии снижается и к концу эксперимента достигает примерно 5 % от общего теоретически ожидаемого количества.
2.5. Исследование влияния концентрации порошка на степень стабильности дисперсии в присутствии электролита
В завершающей части нашего исследования была изучена стабильность дисперсий в зависимости от концентрации порошка (менее 1 г/л). На основании предыдущих результатов было решено стабилизировать дисперсии порошков электролитом KCl с концентрацией 5 мM и работать с дисперсией в области pH 2.
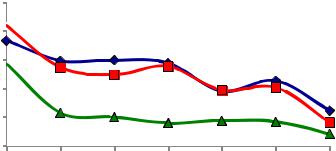
На рис. 14 представлены результаты исследования изменения степенистабильностидисперсийвзависимостиотконцентрациипорошка.
ожидаемого |
Zr,% |
Доля от |
|
25
20 
15 
10
5
0
0 |
1 |
2 |
3 |
4 |
5 |
6 |
|
|
|
Время, ч |
|
|
|
а
Рис. 14. Степень стабильности дисперсий в зависимости от концентрации наноразмерного порошка, стабилизированного при помощи электролита KCl: а – система ZrO2-2Y2O3-4CeO2;
б – система ZrO2-2Y2O3-4CeO2-3Al2O3; |
– 0,05 г/л; |
|
– 0,25 г/л; |
– 0,75 г/л |
|
34
Доляот ожидаемого Zr, %
25
20 
15 
10
5
0
0 |
1 |
2 |
3 |
4 |
5 |
6 |
|
|
|
Время, ч |
|
|
|
б
Рис. 14. Окончание
Также можно отметить, что все дисперсионные системы претерпевают непрерывную агломерацию с самого начала эксперимента. Это классический случай оседания частиц, вызванного их агломерацией, под действием гравитационных сил [71].
3. ИССЛЕДОВАНИЕ СТАБИЛЬНОСТИ ДИСПЕРСИЙ ПОРОШКОВ СИСТЕМ ZrO2-2Y2O3-4CeO2
и ZrO2-2Y2O3-4CeO2-Al2O3 ПРИ ПОМОЩИ ДИНАМИЧЕСКОГО РАССЕЯНИЯ СВЕТА
Известно, что одна из важнейших проблем приготовления стабильной дисперсии – это агломерация частиц в водной среде. В аналитическом обзоре были представлены различные состояния и конфигурации, в которых могут находиться наночастицы, как в порошковом состоянии, так и в дисперсии. Могут наблюдаться одиночные частицы, а также частицы в агломерированном и агрегированном состоянии. Чаще всего, когда измеряют размер частицы в дисперсии при помощи динамического рассеяния света (ДРС), используют понятие «гидродинамический размер». Данная величина включает в себя не только размер самой частицы/агломерата/агрегата, но и окружающий ее двойной электрический слой. Таким образом, нужно учиты-
35

вать, что размер частицы при измерении с использованием данной методики будет больше, чем при других методиках измерения [72].
3.1.Исследования гидродинамического размера частиц
вдисперсии при натуральном pH
Для более полноценного исследования характера агломерации частиц порошков систем ZrO2-2Y2O3-4CeO2 и ZrO2-2Y2O3-4CeO2- 3%Al2O3 и стабильности дисперсий этих частиц был проведен ряд экспериментов по изучению изменения гидродинамического диаметра наночастиц во времени при помощи метода ДРС.
На рис. 15 представлен график зависимости гидродинамического размера наночастиц порошка системы ZrO2-2Y2O3-4CeO2 при натуральном pH = 4,1 в течение 120 мин. Дисперсия была приготовлена в дистиллированной воде, концентрация порошка составляет 0,5 г/л (500 ppm). Измерение производилось при натуральном pH.
|
1000 |
y = 7E-09x6 – 4E-06x5 + 0,0007x4 – 0,0513x3 + 1,6245x2 – |
|||||
|
900 |
|
|
– 13,051x + 605,4 |
|
|
|
Гидродинамический диаметaр, нм |
|
|
R² = 0,7728 |
|
|
|
|
800 |
|
|
|
|
|
|
|
700 |
|
|
|
|
|
|
|
600 |
|
|
|
|
|
|
|
500 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
400 |
|
|
|
|
|
|
|
0 |
20 |
40 |
60 |
80 |
100 |
120 |
|
|
|
Время, мин |
|
|
|
|
Рис. 15. Изменение гидродинамического диаметра дисперсии наночастиц |
|||||||
|
порошка системы ZrO2-2Y2O3-4CeO2 в дистиллированной воде |
|
|||||
|
|
при натуральном pH в течение 120 мин |
|
|
|||
Зависимость показывает, что в системе без добавки оксида алюминия гидродинамический диаметр наночастиц в первые 10 минут составляет примерно 580 нм, но при этом видно, что размер частиц
36
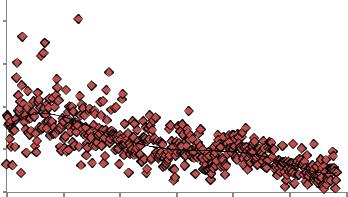
увеличивается со временем и максимальный диаметр частиц наблюдается после 35 минут от начала эксперимента и равен 750 нм. После этого гидродинамический диаметр начинает уменьшаться, и к 65-й минуте мы можем наблюдать плато, где примерный гидродинамический диаметр частиц составляет около 500 нм. Это свидетельствует о том, что в начале эксперимента (сразу после приготовления дисперсии и обработки ультразвуком) частицы еще не успели коагулировать и их средний размер составлял около 580 нм, но потом мы можем наблюдать постепенное увеличение гидродинамического диаметра. Далее частицы коагулируют, поэтому прибор фиксирует гидродинамический размер агломерата. После этого агломерированные частицы выпадают в осадок, и прибор фиксирует мелкие частицы, которые остались во взвешенном состоянии, их гидродинамический размер меньше, чем в начале эксперимента.
На рис. 16 представлены результаты изменения гидродинамического диаметра нанопорошка системы ZrO2-2Y2O3-4CeO2-3%Al2O3 в течение 120 мин.
|
|
y = 4E-09x6 – 8E-07x5 + 2E-05x4 + 0,0072x3 – 0,5921x2 + |
||||||
нм |
1500 |
|
|
+ 11,411x + 1001,3 |
|
|
||
|
|
R² = 0,5368 |
|
|
||||
|
|
|
|
|
||||
, |
|
|
|
|
|
|
|
|
диаметр |
1300 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Гидродинамический |
1100 |
|
|
|
|
|
|
|
900 |
|
|
|
|
|
|
||
700 |
|
|
|
|
|
|
||
0 |
20 |
40 |
60 |
80 |
100 |
120 |
||
|
||||||||
|
|
|
Время, мин |
|
|
|
||
Рис. 16. Изменение гидродинамического диаметра дисперсии наночастиц |
||||||||
порошка системы ZrO2-2Y2O3-4CeO2-3Al2O3 |
в дистиллированной воде |
|||||||
|
|
при натуральном pH в течение 120 мин |
|
|
||||
37
Из графика видно, что в системе с добавкой оксида алюминия гидродинамический диаметр больше, чем без добавки. В отличие от графика на рис. 15, размер частиц в начале эксперимента уже больше в 2 раза и составляет более 1000 нм. После этого происходит плавное уменьшение размера с течением времени, и к концу эксперимента он составляет примерно 800 нм. Анализируя график (см. рис. 16), также можно предположить, что уменьшение гидродинамического диаметра происходит из-за того, что частицы агломерируют и выпадают в осадок под действием гравитационных сил, поэтому прибор фиксирует более мелкие частицы, которые остались во взвешенном состоянии.
3.2. Влияние выдержки в среде этилового спирта и ультразвуковой обработки
на гидродинамический размер частиц
Прежде чем начать исследование влияния выдержки в среде этилового спирта и ультразвуковой обработки на гидродинамический размер, необходимо вспомнить данные, полученные ранее, когда проводили изучение влияния на агломерацию наночастиц таких параметров, как выдержка в среде этилового спирта и последующая ультразвуковая обработка. В этой части исследования было доказано, что после выдержки в среде этилового спирта около суток и последующей ультразвуковой обработки дисперсии наночастиц происходит уменьшение размера частиц. Данный эффект вызван тем, что этиловый спирт, применяемый для выдержки и диспергирования, обладает высокими кавитационными свойствами для обеспечения максимальной производительности диспергирования. В связи с этим нами было решено провести эксперимент (см. рис. 15 и 16), в котором выдержку порошка и ультразвуковую обработку осуществляли в среде этилового спирта, в этой же среде проводили измерение гидродинамического диаметра.
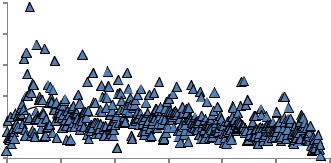
На рис. 17 представлено изменение гидродинамического диаметра в течение 120 мин наночастиц порошка системы ZrO2-2Y2O3- 4CeO2. Порошок был предварительно выдержан в среде этилового спирта в течение 12 часов, после чего также был обработан ультразвуком (40 Вт, 10 мин). Измерение осуществлялось в среде этилового спирта. Концентрация нанопорошка составляла 0,5 г/л (500 ppm).
38
|
3100 |
|
y = –7E-08x6 + 3E-05x5 – 0,0035x4 + 0,2299x3– |
||||
Гидродинамический диаметр, нм |
|
|
|||||
2600 |
|
|
– 7,4255x2 + 102,97x + 923,33 |
|
|||
2100 |
|
|
|
R² = 0,236 |
|
|
|
|
|
|
|
|
|
||
1600 |
|
|
|
|
|
|
|
1100 |
|
|
|
|
|
|
|
|
600 |
|
|
|
|
|
|
|
0 |
20 |
40 |
60 |
80 |
100 |
120 |
|
|
|
Время, мин |
|
|
|
|
Рис. 17. Изменение гидродинамического диаметра дисперсии наночастиц |
|||||||
порошка системы ZrO2-2Y2O3-4CeO2, выдержанного в среде этилового |
|||||||
спирта в течение суток. Длительность эксперимента 120 минут |
|
||||||
На графике (см. рис. 17) видно, что дисперсию можно считать относительно стабильной, так как серьезных перепадов в размере частиц не было зафиксировано. Средний гидродинамический диаметр частиц на протяжении всего эксперимента находится в области от 1000 до 1300 нм. Можно предположить, что здесь проявился эффект влияния выдержки в среде этилового спирта. По всей видимости, частицы нанопорошка все-таки агломерированы, но в кластеры примерно одного и того же размера, которые не коагулировали с другими агломератами и не осели под действием гравитационных сил, оставаясь во взвешенном состоянии на протяжении всего эксперимента.
На рис. 18 представлены результаты измерения гидродинамического диаметра в течение 120 мин наночастиц порошка системы ZrO2-2Y2O3-4CeO2-3%Al2O3. Порошок также был предварительно выдержан в среде этилового спирта в течение 12 часов, после чего также был обработан ультразвуком (40 Вт, 10 мин). Измерение проводилось в среде этилового спирта. Концентрация нанопорошка со-
ставляла 0,5 г/л (500 ppm).
Так же как и в предыдущем эксперименте при натуральном pH (см. рис. 16), малая добавка оксида алюминия постепенно уменьшает гидродинамический диаметр в течение всего эксперимента (120 ми-
39
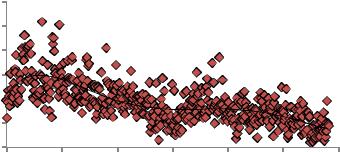
нут). В начале эксперимента средний гидродинамический размер ра- |
|||||||
вен примерно 800 нм, и к концу эксперимента он снижается и со- |
|||||||
ставляет менее 600 нм. |
|
|
|
|
|
||
|
1100 |
y = –9E-10x6 + 7E-07x5 – 0,0002x4 + 0,0183x3 – 0,8783x2+ |
|||||
Гидродинамический диаметр, нм |
1000 |
|
|
+ 14,395x + 720,51 |
|
|
|
|
|
R² = 0,5069 |
|
|
|
||
900 |
|
|
|
|
|
|
|
800 |
|
|
|
|
|
|
|
700 |
|
|
|
|
|
|
|
600 |
|
|
|
|
|
|
|
|
500 |
|
|
|
|
|
|
|
0 |
20 |
40 |
60 |
80 |
100 |
120 |
|
|
|
Время, мин |
|
|
|
|
Рис. 18. Изменение гидродинамического диаметра дисперсии наночастиц |
|||||||
порошка системы ZrO2-2Y2O3-4CeO2, выдержанного в среде этилового |
|||||||
|
спирта в течение суток. Длительность эксперимента 120 минут |
|
|||||
Характер кривой говорит о том, что, возможно, частицы в системе с добавкой оксида алюминия имеют склонность к агломерации больше, чем без данной добавки. Можно вновь сделать предположение, что уменьшение гидродинамического диаметра с течением времени (120 минут) происходит из-за того, что наблюдается агломерация частиц, которые под действием гравитационных сил оседают, и прибор фиксирует уже те частицы, которые остались во взвешенном состоянии.
3.3. Влияние добавки электролита на гидродинамический размер частиц
В данном подразделе рассмотрена возможность электростатической стабилизации дисперсии (при помощи электролита), выдержанной в среде этилового спирта в течение одних суток.
На рис. 19 представлены результаты эксперимента по стабилизации дисперсии наночастиц систем ZrO2-2Y2O3-4CeO2
40
