
Органическая химия (110
..pdf
2. Окисляемость ароматических углеводородов. Помещают в две пробирки по 1 мл раствора перманганата калия и по 1 мл разбавленной серной кислоты и затем добавляют в одну пробирку несколько капель бензола, а в другую – несколько капель толуола. Сильно встряхивают обе пробирки в течение нескольких минут. Одна из смесей в этих условиях быстро меняет окраску.
|
KMnO 4 |
|
H2 SO 4 |
CH 3 |
COOH |
|
KMnO 4 |
|
H2 SO 4 |
|
бензойная кислота |
ГИДРОКСИЛСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
Свойства предельных одноатомных спиртов
1. Образование и гидролиз алкоголята. В пробирку с безводным спиртом осторожно погружают кусочек чистого металлического натрия размером с горошину. Жидкость постепенно густеет, натрий покрывается слоем твердого алкоголята. Добавляют в пробирку 5 мл воды и испытывают фенолфталеином реакцию полученного раствора.
2C2H5OH + 2Na  2C2H5ONa + H2
2C2H5ONa + H2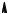
этилат натрия
C2H5ONa + H2O  C2H5OH + NaOH
C2H5OH + NaOH
2. Образование простых эфиров. Смешивают в пробирке 1 мл этилового спирта и 1 мл концентрированной серной кислоты. Сильно разогревшуюся смесь нагревают до кипения, при этом не обнаруживается ни образования горючих паров, ни появления запаха эфира. Удалив нагретую пробирку от горелки, очень осторожно приливают к смеси еще 5–10 капель спирта, при этом сразу же появляется запах эфира.
C2H5OH + HOSO2OH |
|
|
|
|
C2H5OSO2OH |
C2H5OH |
C2H5OC2H5 |
+ |
H2SO4 |
|
|
|
|
|
|
|
|||||
|
|
|
t° |
|||||||
|
|
|
|
|||||||
|
- H2O |
диэтиловый эфир |
||||||||
|
|
|
||||||||
11
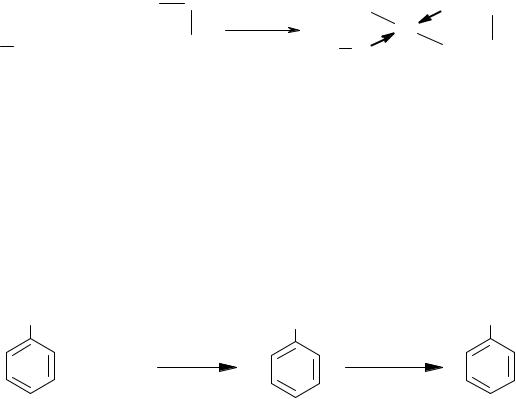
Свойства многоатомных спиртов
Комплексообразование многоатомных спиртов. В трех пробирках получают гидроокись меди, для чего в раствор сульфата меди вводят раствор щелочи. Затем в пробирки добавляют по 3–5 капель одного из спиртов: глицерина, этиленгликоля, этилового спирта. Пробирки встряхивают и отмечают появление в некоторых из них характерной окраски. Затем добавляют к этим растворам избыток разбавленной соляной кислоты и снова наблюдают изменение окраски.
R |
|
OH |
|
|
|
R |
|
|
|
H |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
OH |
|
HO |
|
|
CH2 |
- 2H2O |
|
|
|
|
O |
|
|
|
|
|
|
CH |
|
|||||||||||||||||||
|
|
|
|
|
|
CH |
|
|
O |
|
|
CH2 |
||||||||
|
|
|
|
Cu + |
|
|
|
|
|
|
|
|
||||||||
|
|
|
+ |
|
|
|
CH |
|
|
|
|
|
|
|
Cu |
|
|
|
||
|
|
|
OH |
|
HO |
|
|
|
|
|
O |
O |
|
|
|
|||||
|
CH2 |
|
|
|
CH |
|||||||||||||||
|
|
|
|
CH2 |
|
|
||||||||||||||
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
||||||||||||||||
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
||
|
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
||||||
R=H (этиленгликоль), CH2OH (глицерин); |
R=H (гликолят меди), CH2OH (глицерат меди) |
|||||||||||||||||||
Свойства фенолов
1. Образование и разложение фенолята. К 0,5 г исследуемого фенола добавляют разбавленный раствор щелочи до полного растворения. Из полученного прозрачного раствора при подкислении разбавленной серной кислотой выделяется в осадок исходное вещество.
OH |
|
ONa |
OH |
+ NaOH |
|
|
H2SO4 |
- H2O |
|
- NaHSO4 |
|
|
|
фенолят натрия
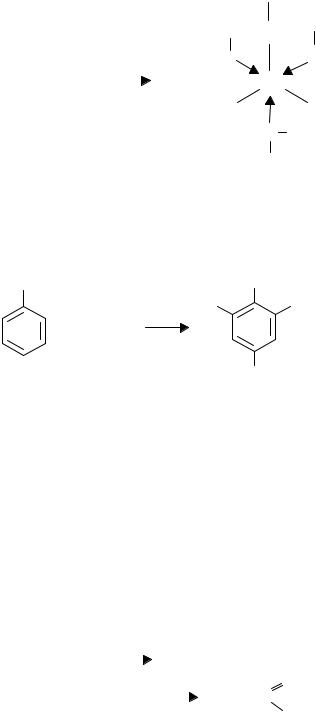
2. Реакция фенолов с хлорным железом. В пробирку наливают 2–3 мл раствора фенола и добавляют несколько капель 3%-ного раствора хлорида железа. Наблюдается появление характерного фиолетового окрашивания вследствие образования комплексного фенолята железа. Окрашивание характерно и для многоатомных фенолов (гидрохинона, пиррогаллола и т. д.) и нафтола, опыт с которыми проводят аналогично.
12
|
|
|
|
|
C6H5 |
|
|
|
|
|
H |
O |
H |
|
|
|
|
|
O - C6H5 |
|
|
|
H C |
6 |
- O |
|
|
5 |
|
|
|
|||
6C6H5OH + FeCl3 |
|
H5C6- O |
Fe |
+ 3HCl |
||
|
||||||
|
|
O H |
O - C6H5 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
C6H5 |
|
3. Бромирование фенола. В пробирку наливают 2 мл водного раствора фенола и приливают избыток бромной воды ( 5 мл). Выделяется хлопьевидный осадок 2,4,6-трибромфенола.
OH |
OH |
Br |
Br |
+ 3Br2 |
+ 3HBr |
Br
КАРБОНИЛСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
Получение и свойства алифатических альдегидов и кетонов
1. Получение ацетальдегида (уксусного альдегида). В сухую пробирку помещают 3–4 мл спирта. Медную проволоку, свернутую в спираль, накаливают в окислительном пламени горелки. Затем быстро опускают горячую медную спираль в пробирку со спиртом. Спирт бурно вскипает, происходит восстановление оксида меди до ярко-красной металлической меди, спирт окисляется до альдегида. Опыт повторить несколько раз. Полученный ацетальдегид используется для последующих опытов.
2Cu + O2 |
|
|
2CuO |
|
|
||||
|
|
|
|
O |
C2H5OH + CuO |
|
|
CH3 - C + H2O + Cu |
|
|
|
|||
|
|
|
|
H |
2. Окисление альдегидов:
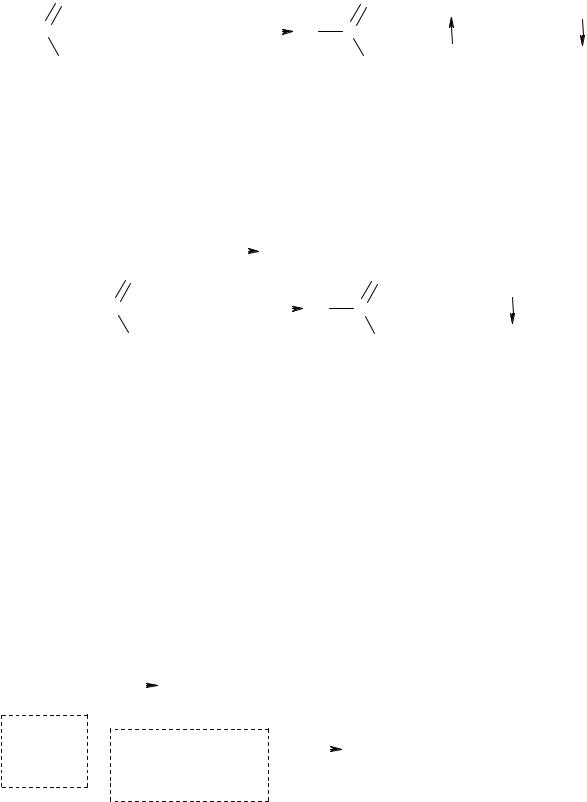
а) реакция «серебряного зеркала» (качественная реакция на альдегиды):
в чистую пробирку наливают 1 мл раствора формальдегида (муравьиного альдегида) или ацетальдегида и добавляют 1 мл аммиачного раствора окиси серебра. Если серебро не выделяется, то нагревают пробирку несколько минут на водяной бане при температуре 50–60 °С.
13
|
|
O |
|
O |
+ - |
|
|
||
R |
|
C + 2[Ag(NH3)2] OH |
|
R C + 3NH3 + H2O + 2Ag |
|
|
|||
|
|
H |
|
ONH4 |
R = H (формальдегид), CH3 (ацетальдегид)
б) восстановление альдегидами соединений двухвалентной меди: к 1 мл раствора альдегида (муравьиного или уксусного) добавляют 0,5 мл разбавленного раствора щелочи и затем по каплям раствор сульфата меди. Полученную смесь нагревают до начала кипения, при этом осадок изменяет свою окраску.
CuSO4 + |
NaOH |
|
|
Na2SO4 + Cu(OH)2 |
|||
|
|||||||
|
|
O |
|
|
|
|
O |
R |
|
C |
+ Cu(OH)2 |
|
|
R C + H2O + Cu |
|
|
|
|
|||||
|
|
H |
|
|
|
|
OH |
R= H (формальдегид), CH3 (ацетальдегид)
3.Цветные реакции:
а) реакция альдегидов с фуксинсернистой кислотой: наливают в две пробирки по 1 мл бесцветного раствора фуксинсернистой кислоты и добавляют по несколько капель раствора формальдегида и полученного ацетальдегида. Жидкость в пробирках приобретает окраску;
б) реакция кетонов с нитропруссидом натрия: в пробирку помещают
1–2 мл ацетона, прибавляют 1–2 капли раствора нитропруссида натрия и несколько капель раствора щелочи. Появляется характерное окрашивание.
4. Образование йодоформа. В пробирку наливают 0,5 мл спиртового раствора йода с йодистым калием и 2–3 мл разбавленного раствора щелочи до исчезновения окраски. При добавлении 1 мл водного раствора ацетона выпадает желтовато-белый осадок с характерным запахом йодоформа.
I2 + 2 NaOH |
|
|
|
|
|
|
|
|
NaOI |
+ |
NaI + |
H2O |
|
|||
|
|
|
|
|
|
|
|
|
||||||||
I ONa |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
I ONa + H3 C |
|
|
|
C |
|
|
|
|
CH3 |
+ |
NaO H |
|
|
CHI3 |
+ CH3COONa + 3NaOH |
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
||||||||||||||
I ONa |
|
|
|
O |
|
|
|
|
|
|
|
|
|
йодоформ |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Аналогичный опыт проводится и с полученным раствором ацетальдегида.
3NaOI + CH3 - CHO  CHI3 + HCOONa + 2 NaOH
CHI3 + HCOONa + 2 NaOH
14

Свойства ароматических альдегидов
1. Окисление бензойного альдегида. К 1–2 каплям бензальдегида до-
бавляют 2–3 мл раствора перманганата калия и нагревают смесь на водяной бане при встряхивании до исчезновения запаха бензальдегида. Фиолетовую окраску (избыток перманганата) уничтожают, добавляя несколько капель спирта. При подкислении реакционной смеси разбавленной серной кислотой выпадает осадок.
O |
KMnO4 |
|
O |
|
C6H5 - C |
C6H5 |
- C |
||
H+ |
||||
H |
|
OH |
||
|
|
бензойная кислота
КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
Свойства предельных одноосновных карбоновых кислот
иих производных
1.Разложение муравьиной кислоты. В пробирку помещают 0,5 мл муравьиной кислоты, добавляют 0,5 мл концентрированной серной кислоты, закрывают пробкой с газоотводной трубкой и осторожно нагревают пробирку над пламенем горелки. Происходит бурное разложение муравьиной кислоты. При поджигании выделяющегося газа у отверстия газоотводной трубки он горит характерным голубым пламенем:
HCOOH |
H2SO4 |
H |
O + CO ; |
2CO + O |
|
|
2 CO2 |
t |
2 |
|
|||||
|
|||||||
|
2 |
|
|
|
|
2. Окисление муравьиной кислоты. В пробирку помещают 0,5 мл му-
равьиной кислоты, 1 каплю разбавленной серной кислоты, 2 капли раствора перманганата калия. Закрывают пробирку пробкой с газоотводной трубкой, конец которой помещают в пробирку с 4–5 каплями известковой или баритовой воды. Пробирку осторожно нагревают над пламенем горелки. Наблюдают выпадение осадка в пробирке с известковой (или баритовой) водой.
HCOOH |
KMnO4 |
H2O + CO2 |
||
H2SO4 , |
tо |
|||
|
|
|||
CO2 + Ba(OH)2 → BaCO3 ↓ + H2O
15

3. Взаимодействие солей карбоновых кислот с солями тяжелых металлов. В пробирку помещают 1–2 мл раствора ацетата натрия, прибавляют 0,5 мл раствора хлорида железа (III). Образуется соль – ацетат железа (III), окрашивающая раствор в красно-бурый цвет. Затем пробирку нагревают. При кипячении полученного раствора, образуется основная соль, выпадающая в виде красно-бурого осадка.
3CH3COONa + FeCl3 → (CH3COO)3Fe + 3NaCl
ацетат натрия |
ацетат железа |
|
(CH3COO)3Fe + 2H2O → (CH3COO)Fe(OH)2 + 2CH3COOH
основной ацетат железа
4. Образование сложных эфиров. В пробирку помещают 0,5 мл этило-
вого спирта и столько же уксусной кислоты. Добавляют 5–7 капель концентрированной серной кислоты и осторожно нагревают смесь до кипения, через несколько секунд появляется характерный запах этилового эфира уксусной кислоты (этилацетата).
|
H |
SO |
, to |
|
|
O |
|||
|
|
|
|
|
|
||||
CH3COOH + C2H5OH |
2 |
4 |
CH |
|
|
C |
|
|
+ H2O |
|
|
3 |
|
|
|
||||
|
|
|
|
|
|
|
O |
|
C2H5 |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
этилацетат |
||||
Двухосновные карбоновые кислоты
Окисление щавелевой кислоты. В пробирку, снабженную газоотводной трубкой, помещают 1–2 лопаточки щавелевой кислоты, добавляют несколько капель серной кислоты и 0,5 мл раствора перманганата калия. В другую пробирку наливают 0,5 мл известковой (или баритовой) воды. Осторожно нагревают пробирку с кислотой, поместив кончик газоотводной трубки в известковую (или баритовую) воду. Происходит обесцвечивание раствора в первой пробирке и помутнение во второй.
|
|
|
KMnO |
|
|
to |
HOOC |
|
COOH |
4 |
CO2 |
+ HCOOH |
CO2 + CO + H2O |
|
H2SO4 |
|||||
|
|
|
|
|
|
|
Ba(OH)2 |
+ CO2 |
|
BaCO3 |
+ H2O |
|
|
16
Ароматические кислоты
Качественная реакция на бензойную кислоту и ее соли. В пробирку вносят лопаточку бензойной кислоты, добавляют 0,5 мл разбавленного раствора гидроксида натрия и встряхивают пробирку. При этом происходит образование бензоата натрия. Затем приливают несколько капель раствора хлорида железа (III). Образуется осадок основного бензоата железа (III).
C6H5COOH + NaOH → C6H5COONa + H2O
бензоат натрия
3C6H5COONa + FeCl3 + H2O → (C6H5COO)2FeOH + C6H5COOH + 3NaCl
основной бензоат железа (III)
УГЛЕВОДЫ
Реакции окисления сахаров
1. Реакция «серебряного зеркала». К 1–2 мл аммиачного раствора оки-
си серебра, налитому в тщательно вымытую пробирку, добавляют равный объем раствора глюкозы. Смесь нагревают в течение нескольких минут, после чего на стенках пробирки осаждается металлическое серебро в виде зеркального слоя.
H |
O |
HO |
O |
|
|
|
|
C |
|
C |
|
|
|
H |
OH Ag2O |
H |
OH |
+ |
2 Ag |
|
HO |
H |
HO |
H |
|||
|
|
|||||
H |
OH |
H |
OH |
|
|
|
H |
OH |
H |
OH |
|
|
|
|
CH2OH |
|
CH2OH |
|
|
|
|
|
глюконовая кислота |
|
|||
2. Взаимодействие сахаров с гидроксидом меди. В три пробирки на-
ливают по 2–3 мл водных растворов глюкозы, сахарозы и крахмала, в каждую пробирку прибавляют по 1 мл раствора гидроксида натрия и по 2– 3 капли раствора медного купороса. В пробирках с глюкозой и сахарозой образовавшийся осадок гидроксида меди при встряхивании растворяется. При этом раствор окрашивается в интенсивно синий цвет вследствие образования комплексных сахаратов меди. Наблюдаются ли какие-либо изменения в пробирке с крахмалом?
CuSO4 + 2NaOH → Cu(OH)2 ↓ + Na2SO4
17
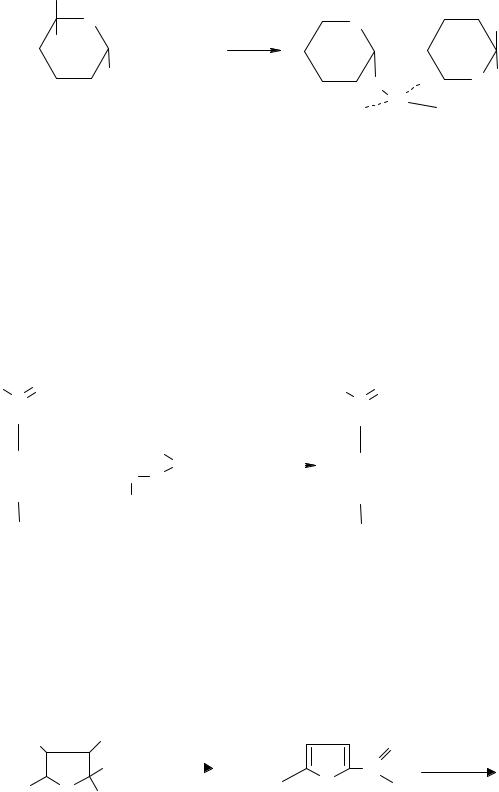
|
|
|
CH2OH |
|
|
CH OH |
|
|
OH H |
||||||||||
|
H |
|
O H |
|
H |
2 |
O H |
H |
|
|
|
CH2OH |
|||||||
|
|
|
|
|
|
|
|||||||||||||
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
2 |
|
|
|
|
|
|
H |
|
|
|
|
H |
HO |
|
|
||||
|
|
|
OH |
H |
+ Cu(OH)2 - 2H2O |
|
|
OH |
H |
|
H |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
HO |
|
|
OH |
|
|
|
|
O H |
||||||||||
|
|
|
|
HO |
|
|
O |
|
OH |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
Cu |
|
|
|
|
|
|
||
|
OH |
|
|
|
|
|
|
|
|||||||||||
|
|
H |
|
|
H HO |
|
O |
|
|
|
|||||||||
Затем осторожно нагревают в пламени горелки верхнюю часть жидкости до кипения и наблюдают за окраской смеси. При наличии свободного гликозидного гидроксила (или свободной альдегидной группы) глюкоза окисляется – синий цвет раствора при нагревании исчезает и появляется желтый осадок гидроксида или красный осадок оксида меди (I).
3. Взаимодействие сахаров с реактивом Фелинга. В две пробирки помещают по 1 мл реактива Фелинга и добавляют в одну пробирку 1 мл раствора глюкозы, а в другую 1 мл раствора сахарозы. При нагревании в пробирке с глюкозой исчезает синий цвет и появляется желтый осадок гидроксида или красный осадок оксида меди (I). Сахароза не изменяет окраски раствора.
H C O |
|
|
|
|
|
|
|
HO C O |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
H |
|
|
|
OH |
|
COOK |
|
|
|
H |
|
|
|
OH |
|
|
|
|
|
|
|
COOK |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
HO |
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
HC |
|
|
O |
|
|
|
HO |
|
|
|
H |
|
|
HC |
|
|
|
OH |
||||||||||
|
|
|
|
+ 2 |
|
|
|
Cu + 2H |
O |
|
|
|
|
|
|
|
|
+ Cu |
O + |
2 |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
H |
|
|
|
|
OH |
HC |
|
O |
2 |
|
H |
|
|
|
|
OH |
2 |
|
HC |
|
|
|
|
OH |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
H |
|
|
|
|
|
OH |
COONa |
|
|
|
H |
|
|
|
|
OH |
|
|
|
COONa |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
||||||
Цветные (качественные) реакции сахаров
1. Проба Селиванова на кетозы. В пробирку помещают 1–2 мл фрук-
тозы (или меда), 1 мл концентрированной соляной кислоты, прибавляют несколько кристаллов резорцина и нагревают. Появляется вишнево-красное окрашивание.
HO |
OH |
|
|
|
|
|
O |
|
|
|
|
HCl, to |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
||
|
OH |
|
|
|
|
|
C |
резорцин |
окраска |
HOH2C O |
|
- 3H2O |
HOCH |
2 |
O |
H |
|||
CH2OH |
|
|
|||||||
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|||
|
|
оксиметилфурфурол |
|
|
|||||
2. Качественная реакция на сахарозу. В пробирку помещают 2–3 мл раствора сахара, приливают несколько капель водного раствора сульфата кобальта (CoSO4) и избыток щелочи. Появляется фиолетовое окрашивание.
18

3. Качественная реакция на крахмал. В пробирку наливают 1 мл крахмального клейстера и добавляют 1–2 капли раствора йода. Появляется синее окрашивание. При подогревании синее окрашивание исчезает, что указывает на физический процесс – адсорбцию йода коллоидными частицами крахмала. Кроме того, образуется комплексное соединение полисахарида с йодом.
АЗОТСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
Амины
1. Взаимодействие анилина с минеральными кислотами. В две про-
бирки наливают по 1 мл раствора анилина. В одну добавляют несколько капель соляной кислоты, в другую – разбавленной серной кислоты. В первой раствор становится прозрачным вследствие растворения образующегося гидрохлорида анилина, во второй выпадает белый осадок труднорастворимой соли – гидросульфата анилина.
C6H5NH2 + HCl → [C6H5NH3]Cl
гидрохлорид анилина
2C6H5NH2 + H2SO4 → [C6H5NH3]2SO4
гидросульфат анилина
2. Получение бензальанилина. В пробирку наливают 0,5 мл бензальдегида и 0,5 мл анилина, добавляют 1–2 капли этилового спирта и сильно встряхивают. После охлаждения в пробирке застывает образовавшийся бензальанилин.
C6H5 – CHO + H2N - C6H5 → C6H5 – CH = N - C6H5 + H2O
бензальанилин
3. Бромирование анилина. В пробирку помещают 2–3 капли анилина и 1 мл воды, энергично встряхивают пробирку для получения эмульсии и добавляют 1 мл бромной воды. При этом происходит обесцвечивание бромной воды и появляется осадок.
NH2 |
NH2 |
Br |
Br |
+ 3Br2 |
+ 3HBr |
Br
2,4,6-триброманилин
19

Аминокислоты
1. Действие аминокислот на индикаторы. В две пробирки наливают по 0,5 мл метилового оранжевого, метилового красного. Добавляют по несколько капель в каждую из пробирок водного раствора аминоуксусной кислоты (глицина). Отмечают реакцию среды.
NH2CH2COOH ↔ N+H3CH2COO–
2. Действие азотистой кислоты на аминокислоты. В пробирку на-
ливают 0,5–1 мл раствора аминоуксусной кислоты и добавляют 3–5 капель нитрита натрия и столько же соляной кислоты. При встряхивании выделяются пузырьки газа.
NaNO2 + HCl → NaCl + HNO2
NH2 – CH2 – COOH + HNO2 → HOCH2 – COOH + N2 ↑ + H2O
оксиуксусная кислота
3. Получение комплексной медной соли аминоуксусной кислоты. К
1–2 мл раствора аминоуксусной кислоты добавляют 0,5 г оксида меди (II). Смесь кипятят. Появляется характерное окрашивание.
|
|
|
|
|
|
CH2 |
NH2 |
O |
|
|
CO |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
||||
2 NH |
|
CH2 |
COOH + CuO |
|
|
|
|
Cu |
|
+ H2O |
|
2 |
|
|
|
|
|
||||||
|
|
|
|
to |
CO |
O |
NH2 |
CH2 |
|||
Белки
1. Обратимые реакции осаждения.
Отношение белков к кислотам и щелочам. К 2–3 мл раствора белка до-
бавляют по каплям при встряхивании концентрированную уксусную кислоту. Наблюдается выпадение белка в осадок в виде мути или хлопьев. При дальнейшем добавлении кислоты осадок белка снова растворяется. Полученный кислый раствор делят на две части. Одну из них нагревают до кипения. При введении в горячую кислую жидкость 1–2 капель раствора сульфата аммония белок свертывается. К другой части кислого раствора белка осторожно добавляют по каплям при встряхивании разбавленный раствор щелочи. При постепенной нейтрализации кислоты образуется осадок белка, снова растворяющийся в избытке щелочи.
20
