
5605
.pdf
(рисунок 2.2.1). Опыт показывает, однако, что линейная зависимость наблюдается не всегда.
Рисунок 2.2.1 – Зависимость оптической плотности от концентрации
При практическом применении закона Бугера – Ламберта – Бера необходимо учитывать следующие основные ограничения.
1. Закон справедлив для монохроматического света. Чтобы отметить это ограничение, в уравнение (2.1) вводят индексы и записывают его в виде
А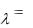
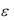 lc .
lc .
Индекс λ указывает, что величины А и ε относятся к монохроматическому излучению с длиной волны λ.
2.Коэффициент ε в уравнении (2.1) зависит от показателя преломления среды. Если концентрация раствора сравнительно невелика, его показатель преломления остаётся таким же, каким был у чистого растворителя, и отклонений от закона по этой причине не наблюдается. Изменение показателя преломления в высококонцентрированных растворах может явиться причиной отклонений от основного закона светопоглощения.
3.Уравнение (2.1) соблюдается только для систем, в которых светопоглощающими центрами являются частицы лишь одного вида. Если при изменении концентрации будет изменяться природа этих частиц вследствие, например, кислотно-основного взаимодействия, диссоциации, полимеризации и т.д., то зависимость А от «с» не будет оставаться линейной, так как молярный коэффициент поглощения вновь образующихся и исходных частиц не будет одинаковым. Так, например, при разбавлении раствора дихромата калия появляются гидрохромат - и хромат-ионы, имеющие различные молярные коэффициенты поглощения.
4.Изменение интенсивности падающего светового потока при прохождении через образец может быть вызвано светопоглощением не только определяемого
21
вещества, но и других компонентов (в частности растворителя). Поэтому необходимо использовать раствор сравнения (часто чистый растворитель) или раствор контрольного опыта.
2.3. Фотометрические реакции
Спектрофотометрический метод широко применяют в неорганическом и органическом анализе для веществ, содержащих хромофорные группы.
Так, к поглощающим веществам относятся ароматические соединения (бензол, нафталин, пиридин),ионы MnO4-, CrO42-, CrO72-, NO3-, комплексные соединения, ионы переходных металлов и др. Например, подкислённый водный раствор K2Cr2O7 поглощает при λmax = 455 нм (ε = 4900), водный раствор КMnO4
при λmax 525 нм (ε = 2020).
Непоглощающие вещества переводят в поглощающие с помощью реагентов. Требования к фотометрическим реагентам: получить продукт реакции с возможно большей величиной молярного коэффициента поглощения, у окрашенных веществ должна быть высокая контрастность, соединение должно быть устойчиво во времени. Желательно, чтобы реакция была избирательной.
В качестве фотометрических реагентов используют вещества различных классов. Используют реакции комплексообразования, окисления-восстановления, получение азокрасителей, хинон-иминовых и полиметиновых соединений и другие.
2.4. Аппаратура для измерения светопоглощения
Прибор для измерения светопоглощения должен выполнять две основные задачи:
1)разложение полихроматического света и выделение нужного интервала длин волн;
2)измерение поглощения света веществом.
При всём многообразии схем и конструктивных особенностей приборов абсорбционной спектроскопии в каждом из них имеется несколько основных узлов, функции которых примерно одинаковы в разных приборах. Такими узлами являются широкополосный источник излучения 1, монохроматизатор (монохроматор) света 2, кювета с исследуемой пробой 3 и кювета с раствором
22
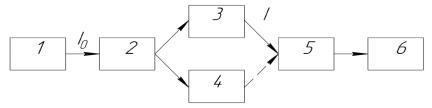
сравнения (холостой пробой) 4, приёмник излучения и регистрирующее устройство 6 (рисунок 2.4.1).
Рисунок 2.4.1 – Схема устройства для измерения поглощения
Измерения проводят с помощью однолучевых и двухлучевых приборов. В однолучевых приборах излучение пропускают последовательно через кювету с исследуемым образцом и через раствор сравнения, тогда как в двухлучевых приборах, благодаря разделению луча, поглощение измеряют одновременно в обеих кюветах.
К основным узлам приборов следует добавить оптическую систему, состоящую из линз, призм и зеркал, которая служит для создания параллельного пучка света, изменения направления и фокусировки света, а также систему для уравнивания интенсивности световых потоков (диафрагмы, оптические клинья и т.д.).
Источниками освещения (излучения) в видимой области спектра является вольфрамовая лампа накаливания (350 – 1000 нм), в УФ-спектре используют газонаполненные водородные и ртутные лампы (195 – 350 нм).
Монохроматизатором (селектором длины волны) называют устройство для получения излучения с заданной длиной волны. Различают два класса адсорбционных приборов: спектрофотометры и фотометры. В спектрофотометрах используют кварцевые призмы и дифракционные решётки с диодной матрицей. В фотометрах применяют адсорбционные и интерференционные светофильтры, которые пропускают излучение ограниченного интервала длин волн (20 – 40 нм в первом случае, и 5 – 20 нм – во втором). С помощью светофильтров не достигается полная монохроматизация света, но они дешевле и проще в использовании.
Кюветы. Основное требование к кюветам – прозрачность в области спектра, в которой ведётся измерение оптической плотности. Для работы в видимой области кюветы изготавливают из стекла, а в ультрафиолетовой – из кварца.
В качестве приёмников излучения (детекторов) может быть глаз, тогда прибор называют колориметром. Но в большинстве приборов используют фотоэлементы и фотоумножители, преобразующие энергию электромагнитного
23
излучения в электрическую, которая, согласно закону Столетова, пропорциональна мощности светового потока. Электрический сигнал регистрирующего устройства может быть очень разнообразным – от простого отклонения стрелки измерительного прибора до колонки цифр от цифропечатающих устройств электронно-вычислительной машины. Так, в нерегистрирующих спектрофотометрах и фотоэлектроколориметрах сигнал выводится на стрелочный прибор, отградуированный в единицах оптической плотности и пропускания; регистрирующие спектрофотометры – снабжены микропроцессорной системой, позволяющей непосредственно определить концентрацию.
Промышленностью выпускаются различные приборы абсорбционной спектроскопии: колориметры, фотометры, фотоэлектроколориметры, спектрофотометры, в которых используют различные комбинации осветителей, монохроматизаторов и приёмников света.
2.5. Выбор условий фотометрического определения
Фотометрическое определение компонентов следует проводить при условиях, обеспечивающих полноту образования поглощающего (окрашенного) соединения в растворе, отсутствие (или минимизацию) отклонения от основного закона светопоглощения, наибольшую точность и чувствительность анализа.
Выбор длины волны светового потока. Для измерения светопоглощения исследуемого раствора выбирают длину волны, светового потока, соответствующую максимуму полосы поглощения, для чего измеряют оптическую плотность раствора при разных длинах волн и строят график зависимости А = f(λ) – спектр поглощения. Работа в области максимума поглощения обеспечивает наибольшую чувствительность и точность определения.
Для монохроматизации светового потока в фотоэлектроколориметрах применяют набор светофильтров. Светофильтры – это специальные стёкла, пропускающие излучение определённого интервала для волн (20 – 60 нм). Для количественного анализа исследуемого компонента по светопоглощению выбирают светофильтр, пропускающий излучение, которое исследуемый компонент поглощает. То есть минимум поглощения света светофильтром должен совпадать с максимумом поглощения раствора.
24
В видимой части спектра воспринимаемый цвет есть результат избирательного поглощения веществом определённого участка сплошного спектра электромагнитного излучения (белого света). Цвет раствора всегда является дополнительным к цвету поглощённого излучения (таблица 2.5.1).
Таблица 2.5.1 – Наблюдаемые цвета и соответствующие им поглощённые участки спектра
Интервал длин волн |
Цвет поглощённого |
Наблюдаемый цвет |
поглощённого излучения, нм |
излучения |
(дополнительный цвет) |
380 – 420 |
Фиолетовый |
Жёлто-зелёный |
420 – 440 |
Синий |
Жёлтый |
440 – 470 |
Голубой |
Оранжевый |
470 – 500 |
Голубовато-зелёный |
Красный |
500 – 520 |
Зелёный |
Пурпурный |
520 – 550 |
Жёлто-зелёный |
Фиолетовый |
550 – 580 |
Жёлтый |
Синий |
580 – 620 |
Оранжевый |
Голубой |
620 – 680 |
Красный |
Голубовато-зелёный |
680 - 780 |
Пурпурный |
Зелёный |
Цвет светофильтра является дополнительным к цвету раствора и соответствует участку спектра электромагнитного излучения, который этим
светофильтром пропускается. |
|
|
|
|
Оптимальный |
диапазон |
измерения |
оптической |
плотности |
(светопропускания). Фотометрические приборы имеют определённую погрешность измерения оптической плотности (светопропускания), что приводит к погрешности ∆с определения концентрации «с» исследуемого компонента в растворе. Минимальная относительная погрешность ∆с/с получается, когда оптическая плотность исследуемого раствора находится в интервале 0,1 – 0,7. Наибольшая точность измерений достигает при А = 0,435.
Толщина поглощающего слоя. В соответствии с уравнением Бугера – Ламберта – Бера (2.1) увеличение толщины поглощающего слоя l позволяет понизить предел обнаружения исследуемого вещества при прочих равных условиях. Однако при толщине поглощающего слоя больше 5 см возрастают потери на рассеяние света. Поэтому для фотометрирования растворов обычно используют кюветы с толщиной поглощающего слоя 1 – 5 см.
Условия проведения фотометрической реакции. В результате проведения фотометрической реакции исследуемый компонент переводят в окрашенное соединение:
25
Исследуемое + Реагент → Окрашенное вещество соединение
Количество образовавшегося окрашенного соединения эквивалентно количеству исследуемого вещества. Поэтому количество исследуемого вещества определяют путём измерения светопоглощения полученного окрашенного соединения. Условия проведения фотометрической реакции должны обеспечивать полноту образования и устойчивость получающегося окрашенного соединения.
Реагент добавляют к исследуемому веществу в количестве, достаточном для обеспечения полного перевода определяемого компонента в окрашенное соединение. Оптимальной концентрацией реагента является такая, выше которой дальнейшее добавление реагента не увеличивает выхода поглощающего соединения (т.е. не увеличивает светопоглощение раствора) на верхней границе диапазона определяемых содержаний исследуемого компонента.
Интенсивность окраски может измениться во времени, поэтому надо исследовать зависимость А = f(τ), на основании которой установить оптимальное время для проведения фотометрической реакции.
Подчинение основному закону светопоглощения полученного при реакции окрашенного соединения является основным условием для количественного фотометрического определения. Подчинение окрашенного соединения закону Бугера – Ламберта – Бера в данном диапазоне концентраций проверяют следующим способом: построение градуированного графика зависимости А = f(с) при выбранной длине волны λ. Если раствор подчиняется основному закону светопоглощения, то график в координатах А – с представляет собой прямую линию, проходящую через начало координат.
2.6. Дифференциальная фотометрия
Кроме метода непосредственной спектрофотометрии разработан метод дифференциальной фотометрии, который позволяет расширить диапазон фотометрических определений.
В качестве раствора сравнения в этом методе используют не растворитель, а раствор определённого вещества с известной (чаще меньшей) концентрацией. Например, если раствор сравнения имеет поглощение Ас = 1,1 анализируемый раствор Ах = 1,6, то при измерении на приборе поглощения анализируемого раствора относительно раствора сравнения получают разность поглощений
26
Ар = Ах – Ас = 1,6 – 1,1 = 0,5. При этом снижается ошибка анализа растворов с высокими концентрациями определяемого вещества.
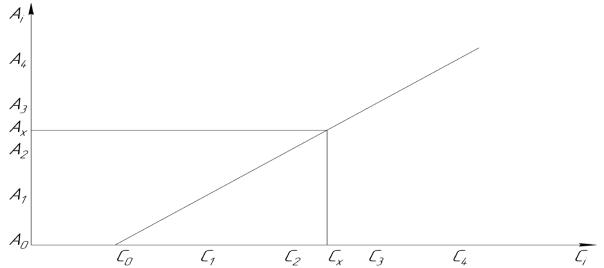
Результат анализа в дифференциальной фотометрии рассчитывают по калибровочному графику, который строят, измеряя поглощение серии стандартных растворов вещества относительно раствора сравнения (рисунок 2.6.1).
По этому графику, зная Ах находят концентрацию Сх определяемого раствора.
Рисунок 2.6.1 – Градуировочный график дифференциальной фотометрии
2.7. Понятие об экстракционно-фотометрическом анализе
Метод сочетает экстракцию и фотометрию. Сущность метода заключается в том, что определяемое вещество переводят из водной фазы в органическую, которую затем фотометрируют. Экстракционно-фотометрический метод применяют когда требуется провести разделение смеси (выделение и анализ одного соединения), очистку вещества, концентрирование вещества (при анализе малых концентраций) или когда исследуемое вещество нерастворимо в воде, но растворимо в органическом растворителе.
При использовании экстракционно-фотометрического метода необходимо, чтобы степень извлечения определяемого вещества из исходного анализируемого раствора экстрагентом была количественной, т.е. чтобы в экстракт переходило не менее 99,9 % определяемого компонента. Это достигает путём выбора подходящих органических экстрагентов, реагентов, оптимального значения рН и т.д.
Экстракционно-фотометрический метод позволяет определить многие неорганические и органические вещества. Так, металлы-комплекообразователи
27
образуют окрашенные комплексные соединения с дитизоном, 8-оксихинолином, диэтилкарбаминатом натрия, растворимые в органических растворителях, имеющие большие значения молярного коэффициента поглощения. Метод обладает большой избирательностью (селективностью), высокой чувствительностью, относительной простотой и быстротой проведения анализа.
2.8. Оценка метода спектрофотометрии
Нижняя граница определяемых содержаний составляет 10-7 М (в большинстве случаев измеряют концентрации 10-6-10-4 М, или 10-1-101 мкг/мл). Спектрофотометрический метод относят к среднечувствительным.
Погрешность метода достаточно высока, особенно при работе на фотоэлектроколориметрах (3 – 5 %), уменьшаясь в благоприятных случаях до 1 – 2 %. Спектрофотометрические методы являются спектрально неселективными за счёт перекрывания спектров компонентов, появления аддитивных систематических погрешностей. Селективность обеспечивают главным образом на стадии пробоподготовки – выбором реагента, селективно взаимодействующего с определяемым веществом с образованием окрашенного продукта, а также условий определения (варьирование рН, маскировка), разделением компонентов (например, экстракция). Сочетание фотометрии с экстракцией способствует повышению как избирательности, так и чувствительности. Методы фотометрии благодаря своей универсальности используют в различных отраслях промышленности, медицине, биологии, сельском хозяйстве; в анализе фармацевтических препаратов, парфюмерной, пищевой и другой продукции. Так, методами фотометрии определяются редуцирующие сахара в мёде, цветность сахара, полифосфаты в мясных продуктах из поджелудочной железы, антиокислители; нитраты и нитриты в мясе, примеси тяжёлых металлов (олова, свинца, железа) в консервах, витамин А в тканях и органах рыб и морепродуктах, консерванты (сорбиновую кислоту, уротропин), мочевину, органические кислоты в соках.
2.9. Примеры определений фотометрическим методом
Работа № 1. Определение меди (II) в виде аммиаката методом фотоэлектроколориметрии
В основе метода лежит фотометрическая реакция
28
Cu2+ + 4NH3 ↔ [Cu(NH3)4]2+.
Комплексное соединение имеет сине-фиолетовую окраску. Интенсивность окраски, а следовательно, и оптическое поглощение (А) раствора аммиаката меди пропорционально содержанию меди (II). Максимальное поглощение комплекса наблюдается при длине волны 620 нм.
Внимание! Прежде чем приступить к работе, необходимо познакомиться с устройством фотоэлектроколориметра и методикой измерения оптического поглощения на приборе.
Методика определения
1.Приготовление стандартных растворов соли меди (II). В мерные колбы вместимостью 25,00 см3 последовательно помещают с помощью градуированной пипетки 2,00; 4,00; 6,00; 8,00; 10,00 см3 исходного раствора соли меди (II), содержащего 2,5000 мг меди (II) в 1 см3 раствора. В каждую колбу отмеривают с помощью бюретки по 5,00 см3 10% раствора аммиака. Объём в колбах доводят водой до метки; растворы тщательно перемешивают.
Примечание: объёмы необходимо отмеривать с максимально возможной точностью, соблюдая все требования титриметрического анализа.
2.Приготовление раствора сравнения. Одновременно готовится раствор сравнения, для чего в мерную колбу вместимостью 25,00 см3 помещают 5,00 см3 10 % раствора аммиака и воды до метки.
3.Измерение оптического поглощения стандартных растворов. Измеряют оптическое поглощение А стандартных растворов меди (II) при выбранном светофильтре в кювете с толщиной слоя 1 см относительно раствора сравнения. Результаты измерений заносят в таблицу 2.9.1.
Примечание: кюветы, в которых проводят измерение интенсивности поглощения должны быть чистыми. Перед заполнением кювету ополаскивают небольшой порцией испытуемого раствора во избежание его разбавления. Кюветы заполняют до такого уровня, чтобы поток излучения целиком проходил через слой раствора, и устанавливают в кюветное отделение всегда в строго определённом положении. Измерения на приборе для каждого из растворов проводят 2 – 3 раза до получения воспроизводимых результатов. Отсчёт по шкале производят до 0,01 единицы оптического поглощения.
4.Построение градуировочного (калибровочного) графика. По данным таблицы 2.9.1 строят градуировочный график зависимости оптического
29

поглощения А от концентрации меди (ω/ или мг/см3) откладывая по оси абсцисс ω/, по оси ординат – А. При соблюдении закона Бера получают прямую, проходящую через начало координат.
Таблица 2.9.1 – Оптические характеристики стандартных растворов меди (II)
|
Объём |
Содержание меди в |
|
Удельный |
|||||
№ п/п |
исходного |
фотометрируемом |
Оптическое |
||||||
коэффициент |
|||||||||
стандартного |
раствора |
растворе |
|
поглощение |
|||||
|
поглощения |
||||||||
раствора |
меди (II) |
3 |
|
3 |
/ |
А |
|||
|
1% |
||||||||
|
см |
3 |
мг/25 см |
мг/см |
|
ω |
|
Е 1с м |
|
|
|
|
|
|
|
|
|
||
1 |
2,00 |
5,0 |
0,20 |
|
0,020 |
|
|
||
2 |
4,00 |
10,0 |
0,40 |
|
0,040 |
|
|
||
3 |
6,00 |
15,0 |
0,60 |
|
0,060 |
|
|
||
4 |
8,00 |
20,0 |
0,80 |
|
0,080 |
|
|
||
5 |
10,00 |
25,0 |
1,00 |
|
0,100 |
|
|
||
5. Определение содержания меди (II) в анализируемом растворе с помощью градуировочного графика: 5,00 см3 анализируемого раствора меди (II) помещают в мерную колбу вместимостью 25,00 см3, добавляют 5,00 см3 10% раствора аммиака и воды до метки. Раствор тщательно перемешивают и измеряют оптическое поглощение Ах (оптическую плотность) в тех же условиях, что и для стандартных растворов. По градуировочному графику определяют концентрацию меди (ω/х) в исследуемом растворе.
Массообъёмную долю меди (II) в исследуемом растворе рассчитывают по формуле:
/ / град. |
Vобщ |
, |
|
||
|
Vа |
|
где ω/град. – массо-объёмная доля меди (II) в фотометрируемом растворе, найденная по графику, построенному в координатах «А - ω/».
ω/град. = концентрация меди, найденная по графику.
6. Вычисление коэффициентов поглощения. По данным таблицы 2.9.1 рассчитывают среднее значение удельного коэффициента поглощения аммиаката меди (II) по формуле
E11%сс |
1 i n |
A |
i |
. |
||
|
|
|
|
|||
n i l |
i |
l |
||||
|
|
|||||
|
|
|
|
|
||
7. Определение содержания меди (II) в исследуемом растворе проводят и по уравнению связи, используя значение удельного коэффициента светопоглощения.
Расчёт проводят по формуле
30
