
5194
.pdf
11
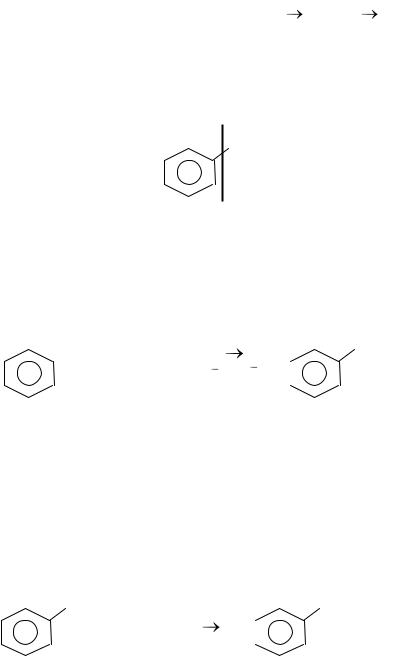
2 этап. Итак, предпочтительным для систем с сопряженными связями является 1,4-присоединение, хотя возможно и 1,2-присоединение:
3 этап. Отличительной особенностью диенов с сопряженными связями является их склонность к полимеризации. Процесс полимеризации протекает под действием катализаторов, под влиянием света и даже самопроизвольно. Макромолекула образуется за счет соединения друг с другом молекул мономера в положение 1,4:
12
Тема 4. АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
Обучающая задача
Составьте схемы следующих превращений:
|
[O] |
|
Cl |
2 ? |
|
|
|
|
|||
бензол → пропилбензол |
KMnO4 |
? |
|
||
|
|
FeCl |
3 |
||
|
|
|
|
|
|
Решение. 1 этап. Для синтеза вещества на основании его формулы нужно выбрать исходные соединения, разделив формулу искомого на фрагменты:
CH2CH2CH3
Таким образом, в молекулу бензола нужно ввести алкильный радикал – пропил. Один из способов получения гомологов бензола – синтез ФриделяКрафтса. Алкильный радикал вводится в кольцо при действии на бензол галоген алкилов в присутствии хлористого алюминия:
AlCl3 |
|
CH2CH2CH3+ HCl |
AlCl |
|
|
|
||
|
|
|
+ Cl-CH2CH2CH3 4 |
|
пропилбензол |
|
||
|
|
2 этап. Бензольное кольцо отличается стойкостью к действию окислителя. Окислению подвергаются обычно боковые цепи, причем цепи любой сложности разрушаются и «сгорают», а в кольце остается в качестве заместителя лишь один атом углерода, окисленный до карбоксильной группы. Образуется ароматическая кислота.
CH2CH2CH3 |
[0] |
|
COOH |
|
|
|
|
|
KMnO4 |
|
+ 2CО2 + 2H2O |
|
|
||
|
бензойная кислота |
||
|
|
||
3 этап. На продукт окисления по условию следует подействовать хлором в присутствии хлорного железа. Это реакция электрофильного замещения. В производных бензола, имеющих заместитель (типа C6H5 – x), атомы углерода в кольце неравноценны, поэтому при введении второго заместителя возможно
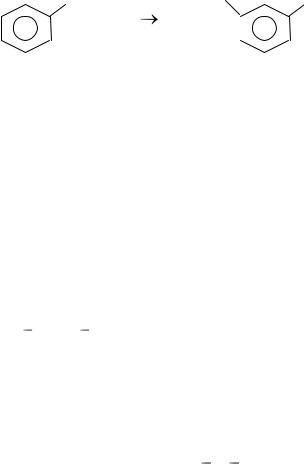
13
образование трех изомеров. Место вступления второго электрофильного заместителя определяется природой уже имеющегося (первого или ориентирующего) заместителя. Ориентирующие заместители в бензольном кольце делятся на 2 группы: ориентанты I рода или электронодоноры (алкилы, гидрокси- и аминогруппы, галогены) – вводят заместитель в орто- и параположения (2,4,6); - ориентанты II рода или электроноакцепторы (карбоксилы, карбонилы; сульфо, нитро-, нитрозо-группы) – вводят заместитель в мета положение (3,5). Карбоксильная группа – это ориентант II рода, направляющий следующий заместитель в мета – положение по отношению к себе:
COOH Cl |
Cl |
|
COOH |
FeCl3 |
|
|
+ HCl |
|
|
||
|
|
|
|
|
м-хлорбензойная кислота |
||
|
|
||
Тема 5. СПИРТЫ, ФЕНОЛЫ, ПРОСТЫЕ ЭФИРЫ. Тема 6. АЛЬДЕГИДЫ, КЕТОНЫ
Обучающая задача
Получите пропанол-2 из соответствующего кетона. На пропанол-2 подействуйте уксусной кислотой в присутствии концентрированной серной кислоты. Напишите схемы реакции и назовите полученные соединения.
Судя по названию (суффикс «ол»), следует получить спирт следующего
1 |
2 |
3 |
строения: C H3 |
C H |
C H3 . Это вторичный спирт, поскольку гидроксильная |
|
| |
|
|
OH |
|
группа расположена у вторичного атома углерода. Следовательно, кето-группа, должна быть при втором атоме углерода (т.е. там же, где был гидроксил):
CH3 |
C CH3 |
|
|| |
|
O |
пропанон-2
1 этап. Вторичный спирт и кетон связаны друг с другом взаимными окислительно-восстановительными превращениями:

14
Для получения пропанола-2 проведем каталитическое восстановление пропанона-2:
2 этап. Спирты реагируют с карбоновыми кислотами, при этом выделяется вода и образуется сложный эфир. Это реакция этерификации. Получаемый сложный эфир гидролизуется образующейся водой, поэтому идет обратимый процесс:
Для смещения равновесия вправо связывают образующуюся воду концентрированной серной кислотой.
Тема 7. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ФУНКЦИОНАЛЬНЫЕ ПРОИЗВОДНЫЕ
Обучающая задача
Из 1-хлорпропана получите масляную кислоту, используя нитрильный синтез. Напишите схемы реакций этой кислоты и бикарбонатом кальция и пятихлористым фосфором.
15
При сравнении формул исходного и конечного соединений видно, что число углеродных атомов во втором соединении больше на один атом, чем в первом:
CH3-CH2-CH2-Cl |
CH3-CH2-CH2-COOH |
1-хлорпропан |
масляная (бутановая) кислота |
Нарастить углеродную цепь можно, проведя нитрильный синтез. При действии солей синильной кислоты на галогенопроизводные углеводородов образуются нитрилы кислот, таким образом в молекулу вводится добавочный атом углерода:
R – Cl + K – C 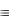 N → R – C N + KCl
N → R – C N + KCl
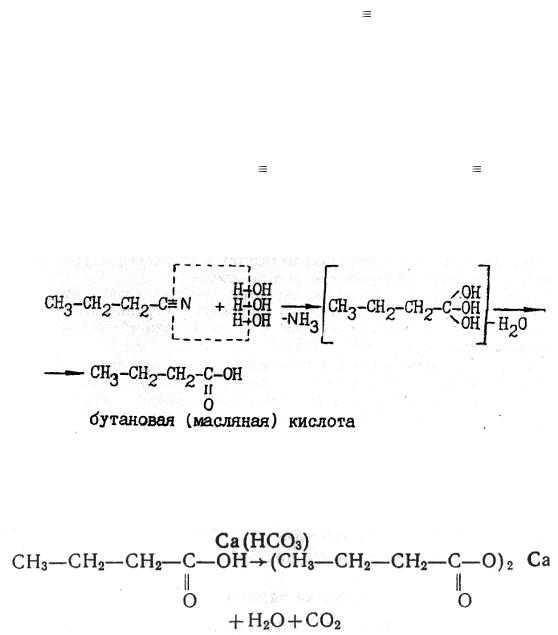
Нитрил кислоты, как и любое производное карбоновых кислот, при гидролизе превращается в кислоту.
1 этап. Из 1-хлопропана получаем нитрил кислоты, содержащей уже 4 атома углерода, т.е. бутановой (масляной)
CH3 – CH2 – CH2 – Cl + K – C N → CH3 – CH2 – CH2 – C |
N + KCl |
Гидролиз нитрилов с целью получения карбоновых кислот |
проводят в |
присутствии минеральных кислот.
2 этап. При взаимодействии кислот с основаниями, солями, оксидами или активными металлами водород карбоксильной группы кислоты замещается на металл с образованием солей карбоновых кислот:
2
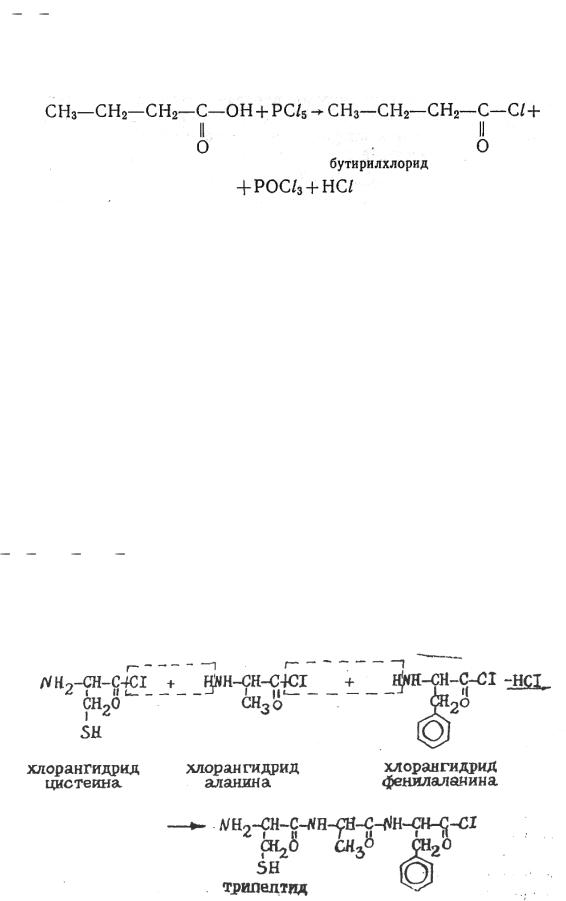
3 этап. Гидроксильная группа и карбоксиле может быть замещена различными группами атомов; образующиеся при этом соединения называются
16
функциональными производными карбоновых кислот (общая формула
RC X
||
O ). При действии на кислоту пятихлористого фосфора гидроксил замещается на галоген (атом хлора) с образованием галогенангидрида:
Темы 10 – 11. АМИНЫ, АМИНОКИСЛОТЫ, БЕЛКИ
Обучающая задача
Напишите схему образования трипептида из галогенангидридов следующих аминокислот: цистеина, аланина и фенилаланина. Какая цветная реакция доказывает присутствие в этом пептиде ароматического кольца? Напишите схему этой реакции.
Различные аминокислоты, образуя белки, соединяются за счет карбоксильных и
аминогрупп при помощи группировки – С– NH –, называемой пептидной связью.
||
О
Продукт взаимодействия двух α-аминокислот называется дипептидом, трех – трипептидом, многих – полипептидом. Образование полипептидов из α-амино- кислот лежит в основе синтеза белковых веществ в живых организмах. Общую формулу полипептида можно представить следующим образом:
[ C NH |
C H ]n |
|
|| |
| |
|
O |
R |
где R – различные группы атомов. |
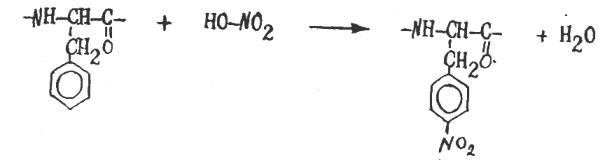
1 этап. Для синтеза белковых веществ используют галогенангидриды α- аминокислот. По условию в реакцию вводим хлорангидрид указанных аминокислот:
17
Называют пептиды по имени входящих в их состав α-аминокислот, заменяя окончание – ин на – ил в тривиальных названиях тех аминокислот, карбоксильные группы которых образовали пептидную связь. Таким образом, полученный трипептид называется цистеил-аланил-фенилаланин.
2 этап. Одной из качественных реакций на белки является ксантопротеиновая реакция, доказывающая присутствие в белке ароматических α-аминокислот. При нагревании с азотной кислотой белок окрашивается в желтый цвет. Ксантопротеиновая реакция – это реакция нитрования ароматического кольца. Схему реакции запишем с фрагментом пептидной цепи:
Тема 13. УГЛЕВОДЫ
Обучающая задача
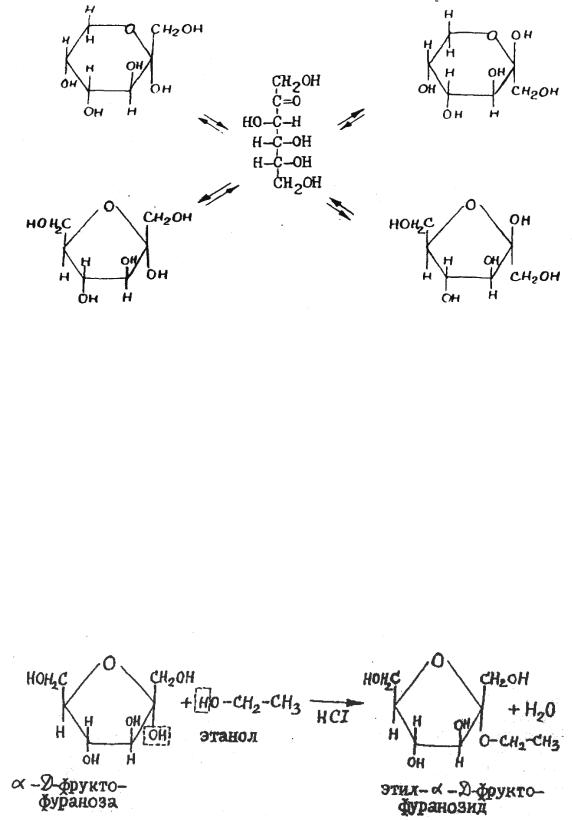
Напишите схему взаимодействия α-D-фруктофуранозы с 1 молем этилового спирта (в присутствии сухого HCl) .
α-D-фруктофураноза – представитель кетогексоз с общей формулой C6H12O6. Из приведенного в условии названия следует, что D-фруктоза находится в пятичленной (фуранозной) циклической форме в виде α-таутомера.
Принадлежность к D-стереохимическому ряду означает, что конфигурация наиболее удаленного от карбонильной группы асимметрического атома углерода совпадает с конфигурацией D-глицеринового альдегида.
1 этап. При растворении в воде моносахариды существуют в пяти таутомерных формах: в оксикарбонильной (раскрытое полукольцо) и четырех циклических полуацетальных формах (два пятичленных цикла – фуранозные формы и два шестичленных – пиранозные формы).
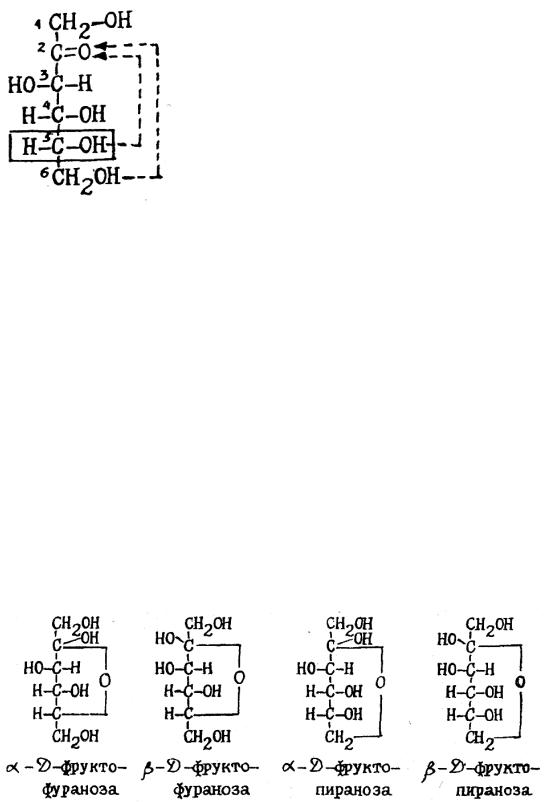
Вначале запишите оксикарбонильную форму D-фруктозы, используя проекционную формулу Фишера:
18
Фруктоза – представитель кетогексоз. Карбонильную группу здесь образует
вторичный атом углерода. Принадлежность к D-ряду определяют по конфигурации пятого углеродного атома (водород слева, а гидроксил справа от оси молекулы)
D – фруктоза
Образование циклических форм происходит при следующих превращених: атом водорода спиртового гидроксила переходит к карбонильному кислороду (по месту разрыва двойной связи), а кислород этого гидроксила соединяется со вторым атомом углерода. Если в превращении участвует гидроксил при пятом атоме углерода, образуется пятичленный цикл (фуранозный), а если участвует гидроксил при шестом атоме углерода – образуется шестичленный цикл (пиранозный). Второй углеродный атом, который в карбонильной форме был карбонильным углеродом, называется полуацетальным углеродным атомом, а соединенная с ним гидроксильная группа – полуацетальным или гликозидным гидроксилом. Этот углеродный атом в цикле становится новым асимметрическим атомом, поэтому каждая полуацетальная форма, как пиранозная, так и фуранозная, может существовать в виде двух стереоизомеров с противоположным пространственным расположением водорода и гидроксила при полуацетальном углероде; причем формы, в которых гидроксил обращен вправо, называются α-формами, а те, у которых он обращен влево – β-формами:
Формулы Фишера лишь условно отражают строение моносахарида, более правильным является способ изображения по Хеуорсу. При этом циклические формы располагают как бы перпендикулярно плоскости листа бумаги, т.е.
19
перспективно; атомы водорода и гидроксильные группы изображаются вверх и вниз от плоскости кольца.
Тогда таутомерное равновесие, существующее в растворе D-фруктозы, пользуясь формулами Хеуорса, можно изобразить следующей схемой:
2 этап. Следует различать, какая из существующих в растворе таутомерных форм может вступать в ту или иную реакцию. Если реакция идет по карбонильной группе, то реагирует, естественно, раскрытая оксикарбонильная форма (содержащая карбонильную группу)
В реакциях образования гликозидов участвуют гидроксильные группы и, прежде всего, наиболее активный полуацетальный гидроксил, поэтому схемы таких реакций следует писать с одной из полуацетальных форм.
По условию в реакцию нужно ввести α-D-фруктофуранозу. Реакция моносахаридов со спиртами идет по полуацетальному гидроксилу с образованием гликозида – производного, в котором водород в гидроксиле замещается радикалом. Реакция протекает при нагревании в присутствии сухого HCl. Остальные гидроксильные группы в этих условиях со спиртами не взаимодействуют.
20
ВАРИАНТЫ ЗАДАНИЙ ДЛЯ КОНТРОЛЬНОЙ РАБОТЫ
Вариант 1
1.Получите 2,3-диметилбутан реакцией Вюрца (действием металлического натрия на галогенопроизводные соответствующих углеводородов). Напишите четыре изомера этого соединения, назовите все углеводороды по международной номенклатуре.
2.Напишите схемы реакций получения уксусного альдегида из ацетилена и приведите следующие реакции для этого альдегида: а) окисления; б) восстановления; в) с бисульфитом натрия. Назовите полученные соединения.
3.Исходя из пропина, получите 2-хлорпропан, а также напишите реакцию гидратации пропина (реакция Кучерова). Назовите полученные вещества по международной номенклатуре.
4.Напишите схемы получения бензола из следующих исходных веществ: а) ацетилена; б) циклогексана. Объясните, в чем заключается ароматический характер бензола. Приведите примеры реакций замещения и присоединения для бензола. Назовите полученные вещества.
5.Пользуясь правилами замещения в бензольном ядре, напишите схемы реакций: а) бромирования анилина; б) сульфирования бромбензола; в) нитрования пропилбензола. Назовите полученные соединения. Реакции проведите с 1 молем каждого реагента.
6.Напишите структурные формулы спиртов: а) пропанола-1, б) бутанола-2; в) 3- метилпентанола-3. Укажите, какие из них являются первичными, вторичными и третичными. Напишите схемы реакций окисления каждого спирта. Назовите продукты реакции.
7.Подействуйте на 2-метилбутан 1 молем хлора (при облучении). Напишите и назовите по международной номенклатуре семь изомеров полученного соединения.
8.Получите уксусную кислоту из бромистого метила (с помощью нитрильного синтеза). Напишите схемы реакций уксусной кислоты с: а) этанолом в присутствии концентрированной серной кислоты; б) пятихлористым фосфором; в) гидратом окиси магния. Назовите полученные соединения.
9.Получите один трипептид из аланина и двух молекул глицина. Напишите схему реакции и назовите полученный пептид. Определите его заряд.
