
5094
.pdf
51
содержат свободную альдегидную или кетонную группу. Циклическая форма образуется при переходе атома водорода гидроксильной группы, связанной с пятым (С5) или четвертым (С4) углеродом атома в молекуле глюкозы либо шестым (С6) или пятым (С5) атомом углерода в фруктозе, к кислороду карбонильной группы. Такой переход возможен потому, что, во-первых, карбонильная группа поляризована, а во-вторых, цепная молекула монозы в пространстве расположена так, что один из перечисленных гидроксилов находится рядом с кислородом карбонильной группы. Например, для глюкозы процесс циклизации можно представить так:
При этом возникает кислородный мостик и образуется новый гидроксил, который называют полуацетатным или гликозидным. Он резко отличается своими свойствами от других гидроксилов. Так, его водород легче, чем в других гидроксильных группах, замещается на алкил, образуется простой эфир. Но этот эфир также легко подвергается омылению, что противоречит свойству простых эфиров (устойчивость к гидролизу). В глюкозе глюкозидный гидроксил находится при первом (С1) углеродом атоме, а в фруктозе – при втором (С2). Предположение о циклическом строении моносахаридов было высказано впервые русским ученым А. А. Колли (1870), который также установил и пятиатомность глюкозы.
Пятичленные циклические формы моноз по номенклатуре Хеуорзса называют фуранозами (от названия пятичленного гетероцикла – фурана), а шестичленные циклические формы – пиранозами (от названия шестичленного гетероцикла – пирана).
Две формы моносахаридов – цепная и циклическая – являются таутомерными (кольчато-цепная таутометрия) и способны самопроизвольно переходить одна в другую в водных растворах. Такой переход совершается в зависимости от условий проведения реакций и характера реагентов. Например, глюкоза в водном растворе существует в трёх формах, способных переходить одна в другую: открытой (альдегидной) и двух циклических – пятичленной и шестичленной:

|
|
|
|
|
52 |
|
|
|
|
Н 1 |
ОН |
Н 1 О |
Н 1 |
|
ОН |
||||
С |
|
|
|
|
С |
|
С |
|
|
|
|
|
|
|
|
||||
2 |
|
|
|
|
2 |
2 |
|
|
|
Н – С – ОН |
Н – С – ОН |
Н – С – ОН |
|
||||||
3 |
|
О |
3 |
3 |
|
|
|
||
|
|
|
|
||||||
НО – С – Н |
|
|
НО – С – Н |
НО – С – Н О |
|||||
|
|||||||||
4 |
|
|
|
|
4 |
4 |
|
|
|
Н – С |
|
|
|
Н – С – ОН |
Н – С – ОН |
||||
5 |
|
|
|
|
5 |
5 |
|
|
|
Н – С – ОН |
Н – С – ОН |
Н – С |
|||||||
6СН2ОН |
6СН2ОН |
6 |
СН2ОН |
||||||
циклическая полу- |
открытая (ацик- |
циклическая полу- |
|||||||
ацетатная форма |
лическая), или |
ацетатная форма |
|||||||
(пятичленное, или |
цепная, форма |
(шестичленное, или |
|||||||
-оксидное, кольцо) |
(альдегидная |
-оксидное, кольцо) |
|||||||
|
|
|
|
|
форма) |
|
|
|
|
Фруктоза также существует в виде цепной кетонной и двух циклических форм – пятичленной и шестичленной:
1 |
|
|
|
1 |
1 СН2ОН |
||
СН2ОН |
|
|
СН2ОН |
||||
|
ОН |
|
|
2 |
2 ОН |
||
2 С |
|
|
С = О |
С |
|
|
|
|
|
|
|||||
3 |
|
|
|
3 |
3 |
|
|
НО – С – Н |
|
|
НО – С – Н |
НО – С – Н |
|||
4 |
|
О |
4 |
4 |
|
|
|
Н – С – ОН |
|
|
Н – С – ОН |
Н – С – ОН О |
|||
|
|
||||||
5 |
|
|
|
5 |
5 |
|
|
Н – С |
|
|
|
Н – С – ОН |
Н – С – ОН |
||
|
|
|
|||||
6 |
|
|
|
6 |
6 |
|
|
СН2ОН |
|
|
СН2ОН |
СН2 |
|||
циклическая полуацетатная форма (пятичленное, или
-оксидное, кольцо)
открытая (ациклическая), или цепная, форма (кетонная форма)
циклическая полуацетальная форма (шестичленное, или)
-оксидное, кольцо)
Равновесие всех этих форм наблюдается только в водном растворе. Если равновесие нарушается, то одна форма переходит в другую. В кристаллическом состоянии монозы имеют циклическое строение – преимущественно шестичленное ( -оксидную форму).
Обычно для изображения изомеров моноз (в цепной форме) используют проекционные формулы Э. Фишера:
|
СНО |
СН2ОН |
|||||
Н |
|
|
ОН |
|
|
|
О |
|
|
|
|
|
|||
|
|
||||||
|
|
|
|
|
|||
|
|
|
|
|
|
|
|

|
|
|
|
|
53 |
|
|
|
|
|
НО |
|
|
Н |
НО |
|
|
Н |
|||
|
|
|
||||||||
Н |
|
|
|
ОН |
Н |
|
|
|
|
ОН |
|
|
|
|
|
|
|
||||
Н |
|
|
ОН |
Н |
|
|
|
|
ОН |
|
|
|
|
|
|
|
|||||
|
|
СН2ОН |
|
|
СН2ОН |
|||||
D–глюкоза |
D-фруктоза |
|||||||||
Однако циклическую форму моносахаридов удобнее изображать в виде «перспективных» формул Хеуорзса:
Такое изображение позволяет видеть взаимное расположение атомов водорода и гидроксильных групп относительно плоскости кольца. При этом символы углеродных атомов опускаются. Для большей наглядности изображения часть плоскости кольца, обращенной к читателю, выделяют более жирными линиями.
Получение
В растениях углеводы образуются из диоксида углерода и воды в процесс фотосинтеза:
nCO2 + nH2O |
hv |
CnH2nOn + nO2 |
|
хлорофилл
Моносахариды можно получать и синтетическим путём.
1. Гидролиз ди- и полисахаридов – один из основных методов получения моносахаридов:
С12Н22О11 + Н2О 2С6Н12О6
дисахарид
(С6Н10О5)n + nН2О nС6Н12О6
полисахарид
2. Альдольная конденсация. Из формальдегида в присутствии гидроксида кальция можно получить сиропообразное сахаристое вещество. Этот продукт был впервые синтезирован А. М. Бутлеровым в 1861 г. Позже анализ показал,

54
что полученный густой сироп представляет собой рацемическую смесь D- и L- фруктозы:
ОСа(ОН)2
|
6Н – С |
С6Н12О6 |
|
|
Н |
3. Неполное окисление шестиатомных спиртов: |
||
|
|
СН2ОН |
СН2ОН |
СНО |
|
|
|
С = О |
2(СНОН)4 |
(СНОН)4 |
+ |
|
|
(СНОН)3 |
СН2ОН |
СН2ОН |
|
|
|
СН2ОН |
шестиатом- |
альдогексоза |
кетогексоза |
ный спирт
Физические и химические свойства Физические свойства. Моносахариды – твёрдые кристаллические вещества,
обычно сладкого вкуса. Гигроскопичны, хорошо растворяются в воде, образуя растворы и сиропы. Водные растворы моносахаридов имеют нейтральную реакцию на лакмус. Оптически активны.
Химические свойства. Моносахариды проявляют свойства спиртов, карбонильных соединений и циклических полуацеталей. В открытой форме монозы участвуют в основном в реакциях, характерных для альдегидов и кетонов, а в циклической – для многоатомных спиртов. Но в некоторых реакциях могут одновременно участвовать различные формы моносахаридов.
При написании уравнений химических реакций мы будем приводить лишь ту форму моносахарида, которая участвует в данной реакции.
1. Восстановление (получение полиолов). Восстановление моносахаридов протекает подобно восстановлению обычных альдегидов и кетонов. Например, при осторожном восстановлении гексоз образуются шестиатомные спирты – гекситы. В качестве восстановителя обычно используют борогидрид натрия NaBH4, так как он, как и исходный моносахарид, растворим в воде.
При восстановлении D-глюкозы образуется D-сорбит, а D-фруктозы – D-
сорбит и D-маннит:

55
Н |
О |
|
|
|
|
|
С |
|
СН2ОН |
СН2ОН |
СН2ОН |
Н – С – ОН [H] Н – С – ОН [H] |
С = 0 |
[H] НО – С – Н |
|||
|
|
(NaBH4) |
(NaBH4) |
|
(NaBH4) |
НО – С – Н |
НО – С – Н |
НО – С – Н |
НО – С - Н |
||
Н – С – ОН |
|
Н – С – ОН |
Н – С – ОН |
Н – С – ОН |
|
Н – С – ОН |
|
Н – С – ОН |
Н – С – ОН |
Н – С – ОН |
|
|
СН2ОН |
|
СН2ОН |
СН2ОН |
СН2ОН |
D-глюкоза |
|
D-сорбит |
D-фруктоза |
D-маннит |
|
2. Окисление. Моносахариды легко окисляются. В зависимости от характера окислителя могут образовываться одноосновные (альдоновые) или двухосновные (сахарные) гидроксикислоты. Так, при окислении глюкозы образуются:
СООН |
|
СНО |
СООН |
Н – С – ОН |
|
Н – С – ОН |
Н – С – ОН |
сильный окислитель |
слабый окислитель |
||
НО – С – Н (НNO3) |
НО – С – Н |
(НВrO) НО – С – Н |
|
Н – С – ОН |
|
Н – С – ОН |
Н – С – ОН |
Н – С – О |
|
Н – С – ОН |
Н – С - ОН |
СООН |
|
СН2ОН |
СН2ОН |
(глюкаровая кислота) |
|
D-глюкоза |
(альдоновая кислота) |
D-сахарная кислота |
|
|
D- глюконовая кислота |
Альдоновые и сахарные кислоты вступают в типичные реакции гидроксикислот. Все моносахариды – восстанавливающие сахара. Для них характерна реакция «серебряного зеркала»:
Н |
О |
|
|
С |
COOH |
Н – С – ОН |
Н – С – ОН |
|
НО – С – Н + 2[Ag(NH3)2]+OH |
НО – С – Н + 2Ag + 2NH3 + H2O |
|
Н – С – ОН |
Н – С – ОН |
|
Н – С – ОН |
Н – С – ОН |
|
|
СН2ОН |
СН2ОН |
D-глюкоза |
D-глюконовая кислота |
|
56
3. Образование озазонов. При нагревании глюкозы с избытком фенилгидразина образуется озазон глюкозы:
Н |
О |
|
|
|
С |
|
H – C = N – NH – C6H5 |
Н – С – ОН |
|
С = N – NH – C6H5 |
|
НО – С – Н + 3С6Н5 |
– NH – NH2 |
НО – С – Н + C6H5 – NH2 + NH3 + 2H2O |
|
|
фенилгидразин |
анилин |
|
Н – С – ОН |
|
Н – С – ОН |
|
Н – С – ОН |
|
Н – С – ОН |
|
|
СН2ОН |
|
СН2ОН |
D-глюкоза |
|
озазон D-глюкозы |
|
Манноза, глюкоза и фруктоза дают один и тот же озазон. Озазоны представляют собой кристаллические вещества, окрашенные в жёлтый цвет.
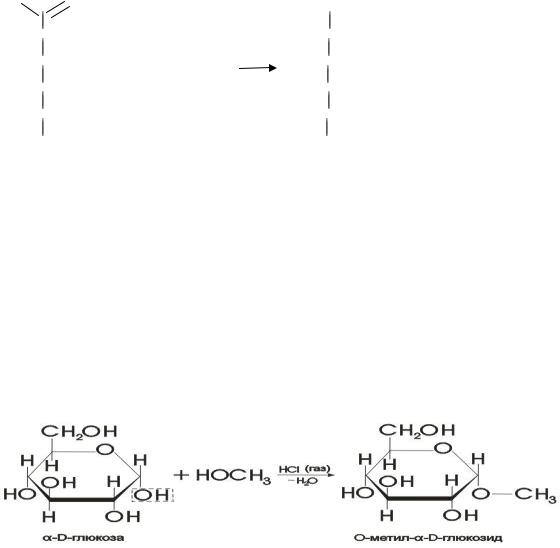
4. Реакции алкилирования. Действие алкилирующих агентов на моносахариды, например глюкозу, приводит к образованию неполных и полных простых эфиров. При этом следует отметить: из всех гидроксильных групп наиболее активно взаимодействует полуацетальный гидроксил. Эта реакция протекает в присутствии газообразного HCl. В результате образуется простой эфир – гликозид (в случае глюкозы – глюкозид):
Связь алкоксигруппы с углеродом моносахарида называют гликозидной связью. Если образовавшийся глюкозид ввести в реакцию с CH3 – I в присутствии Ag2O, то можно получить пентаметилглюкозу, частичный гидролиз который приводит к тетраметилглюкозе. При этом в первую очередь отщепляется та метильная группа, которая связана с кислородом глюкозидного (полуацетатного) гидроксила:

57
Глюкозиды часто встречаются в растительном мире.
5. Реакции ацилирования. В результате таких реакций образуются сложные эфиры. Например, при нагревании уксусного ангидрида с глюкозой получается пента – 0 – ацетилглюкоза:
6. Брожение. Брожение – процесс разложения моносахаридов под действием различных микроорганизмов. Известны многие виды брожения глюкозы –
спиртовое, молочнокислое, маслянокислое и лимоннокислое. Спиртовое брожение протекает под влиянием различных микроорганизмов. В результате спиртового брожения гексоз (для пентоз эта реакция не характерна) образуется этиловый спирт:
зимаза |
|
С6Н12О6 |
2С2Н5ОН + 2СО2 |
глюкоза |
|
Процесс спиртового брожения |
используют также в хлебопечении |
(выделяющийся при брожении СО2 поднимает тесто).
Молочнокислое брожение протекает при выработке различных молочнокислых продуктов, при солении огурцов, квашении капусты и силосовании кормов:
молочнокислые
|
бактерии |
С6Н12О6 |
2СН3 – СН - СООН |
ОН
молочная кислота (молочнокислое брожение)

58
Процессы маслянокислого и лимоннокислого брожения можно представить в следующем виде:
маслянокислые
бактерии
С6Н12О6  С3Н7 – СООН + 2СО2 + 2Н2
С3Н7 – СООН + 2СО2 + 2Н2
масляная
кислота (маслянокислое брожение)
|
ОН |
[О] |
|
С6Н12О6 |
НООС – СН2 – С – СН2 – СООН + 2Н2О |
|
СООН |
|
лимонная кислота |
(лимоннокислое брожение) |
|
Лимоннокислое брожение |
протекает в присутствии особых плесневых |
грибков. Этот процесс используют для получения лимонной кислоты.
3.6. Олигосахариды (сахароподобные полисахариды) дисахариды Олигосахариды (от греч. oligos – немногочисленный, незначительный) –
сложные углеводы, имеющие сравнительно невысокую молекулярную массу и схожие с моносахаридами свойства.
Строение. Олигосахариды состоят из остатков моносахаридов, связанных между собой гликозидными связями. При гидролизе из олигосахарида образуется несколько молекул моносахаридов (от 2 до 10). В зависимости от их числа различают дисахариды (биозы), гидролизирующиеся на две молекулы монозы, трисахариды (триозы), гидролизирующиеся на три молекулы монозы, и т.д. Наибольшее значение имеют дисахариды, которые являются природными веществами. Их общая фомула С12Н22О11.
Дисахариды можно рассматривать как гликозиды циклического моносахарида, в молекуле которого место алкила занято остатком другого моносахарида
,
где R – остаток моносахарида (С6С11О5).

Это соединение напоминает простой эфир, в молекуле которого кислородный атом соединяет два остатка моносахаридов:
C6C 11O5 O C6C 11O5
{59
C 12 H22O 11
Эти остатки могут быть одинаковыми или разными.
Связь между остатками молекул моносахаридов образуется с помощью двух гидроксильных групп – по одной от каждой молекулы монозы. Однако характер этих гидроксилов может быть разным. Если из молекул монозы всегда предоставляет для образования такой связи полуацетальный (гликозидный) гидроксил, то другая молекула участвует или полуацетальным гидроксилом (в этом случае образуется гликозид-гликозидная связь), или любым другим (обычным) гидроксилом (образуется гликозид-гликозная связь). В последнем случае в молекуле дисахарида сохраняется один полуацетальный гидроксил. Такой дисахарид способен из циклической формы перейти в таутомерную ей альдегидную (цепную) форму, которая обладает восстанавливающими свойствами. Такие дисахариды называются восстанавливающими.
Если же дисахарид образуется за счёт обоих полуацетальных гидроксилов (от двух молекул моноз), то он обладает устойчивым циклическим строением и не будет проявлять восстанавливающих свойств. Такие дисахариды называются
невосстанавливающими.
Получение. Дисахариды обычно образуются при частичном гидролизе
полисахаридов:
Н2О (Н+)
(С6Н10О5)n |
|
n |
С |
|
Н |
|
О |
|
|
2 |
12 |
22 |
11 |
||||||
|
|
|
|
||||||
|
|
|
|
|
|
|
|||
Полисахарид |
|
дисахарид |
|
||||||
(крахмал) |
(мальтоза) |
|
|||||||
Физические свойства. Дисахариды – твёрдые или сиропообразные вещества, хорошо растворимые в воде. Обладают сладким вкусом.
Химические свойства. Химические свойства невосстанавливающих дисахаридов определяют гидроксильные группы, а восстанавливающих – альдегидная или кетонная группа и гидроксилы. Поэтому восстанавливающие дисахариды вступают в реакции, характерные для моносахаридов.

60
Дисахариды легко гидролизуются при нагревании с водными растворами минеральных кислот или при действии ферментов. Это приводит к разрыву гликозидной связи и образованию моносахаридов:
|
Н+ |
С12Н22О11 + Н2О |
2С6Н12О6 |
дисахарид |
моносахарид |
Отдельные представители. Сахароза (свёкловичный или тростниковый сахар) – белое кристаллическое вещество с т.пл. 184,5 С. Хорошо растворимо в воде. Получают из сахарной свёклы или сахарного тростника.
Молекула сахарозы состоит из двух различных моноз – -D-глюкозы (в пиранозной форме) и -D-фруктозы (в фуранозной форме), которые связаны между собой -(1,4 )-гликозид-гликозидной связью:
В молекуле сахарозы гликозидная связь образуется за счёт обоих полуацетатных гидроксилов глюкозы и фруктозы. Отсутствие полуацетального гидроксила в молекуле приводит к тому, что сахароза не имеет таутомерной
(альдегидной) формы и поэтому не обладает восстанавливающими свойствами.
При гидролизе (кислотном или ферментативном) сахароза расщепляется на две молекулы – D-глюкозу и D-фруктозу:
С12Н22О11 + Н2О |
С6Н12О6 |
+ С6Н12О6 |
D(+)-сахароза |
D(+)-глю- |
D(–)-фруктоза |
(+ 66,5 ) |
коза |
(- 92 ) |
|
(+ 52,5 ) |
|
|
инвертный сахар (- 39,5 ) |
|
|
{ |
|
Образующаяся смесь глюкозы и фруктозы имеет левое вращение (-39,5 ), в то время как исходный продукт – сахароза – характеризуется противоположным углом вращения (+66,5 ). Такое изменение знака связано с тем, что при гидролизе образуется фруктоза, имеющая угол вращения, равный 92 , и глюкоза,
