
ФГБОУ ВПО “Воронежский государственный
технический университет”
ХИМИЯ, НОВЫЕ МАТЕРИАЛЫ, ХИМИЧЕСКИЕ ТЕХНОЛОГИИ
Выпуск 4
Межвузовский сборник
научных трудов
Воронеж 2013
УДК 621.38.002.3
Химия, новые материалы, химические технологии : межвуз. сб. науч. тр. [Электронный ресурс] – Электрон. текстовые и граф. данные (8,5 Мб). – Воронеж: ФГБОУ ВПО “Воронежский государственный технический университет”, 2013. – Вып. 4. – 1 электрон. опт. диск (CD-ROM) : цв. – Систем. требования : ПК 500 и выше ; 256 Мб ОЗУ ; Windows XP ; SVGA с разрешением 1024x768 ; MS Word 2007 или более поздняя версия ; CD-ROM дисковод ; мышь. – Загл. с экрана. – Диск и сопровод. материал помещены в контейнер 12х14 см.
В сборнике научных трудов представлены статьи, в которых отражены результаты теоретических и экспериментальных исследований в области физики и химии твердого тела, материаловедения, машиностроения, полученные преподавателями, аспирантами и студентами различных специальностей ВГТУ и на других предприятиях г. Воронежа.
Материалы сборника соответствуют научному направлению “Наукоемкие технологии в машиностроении, авиастроении и ракетно-космической технике” и перечню критических технологий Российской Федерации, утвержденному Президентом Российской Федерации. Публикуемые статьи предназначены студентам, аспирантам, инженерно-техническим работникам, специализирующимся в области материаловедения и машиностроения.
Редакционная коллегия:
В.А. Небольсин |
- д-р техн. наук, проф. – ответственный редактор, Воронежский государственный технический университет; |
Б.А. Спиридонов |
- канд. техн. наук, доц., Воронежский государственный технический университет; |
А.Н. Корнеева |
- канд. техн. наук, доц., Воронежский государственный технический университет; |
Д. Б. Суятин |
- канд. физ.-мат. наук, ст. науч. сотр., НИИЯФ Московского государственного университета им. М. В. Ломоносова; |
И.М. Винокурова |
- канд. техн. наук, доц. - ответственный секретарь, Воронежский государственный технический университет |
Рецензенты: |
кафедра физики и химии ВГАСУ (зав. кафедрой д-р хим. наук, проф. О. Б. Рудаков); |
|
канд. физ.-мат. наук, доц. А.Ф. Татаренков |
Издается по решению редакционно-издательского совета Воронежского государственного технического университета
|
Коллектив авторов, 2013 |
|
Оформление. ФГБОУ ВПО “Воронежский г |

В ведение
Сборник научных трудов (выпуск 4) подготовлен на кафедре химии Воронежского государственного технического университета. В нем представлены статьи, отражающие итоги научно-исследовательской работы преподавателей, аспирантов и студентов старших курсов за последние годы.
В материалах сборника рассмотрены результаты теоретических и экспериментальных исследований в области физики и химии твердого тела, материаловедения, машиностроительных технологий, коррозии и защиты металлов.
Большое число статей посвящено решению актуальной проблемы – исследованию условий роста нитевидных кристаллов кремния из газовой фазы (влияние природы и дисперсности частиц металлов-катализаторов, параметров роста кристаллов и др.).
Представлены экспериментальные данные по изучению физико-химических свойств суперконденсаторов и показаны технологические особенности их производства.
В ряде статей рассматриваются адсорбционные свойства силикагелей, алюмогелей и композитов на основе нанопористого оксида алюминия.
Представлены сведения о закономерностях электрохимической обработки поверхности некоторых металлов и сплавов, применяемых в машиностроении. Приведены данные по результатам исследований коррозионных свойств материалов, используемых в микроэлектронике.
В сборник включены статьи, отражающие решение актуальных проблем науки о материалах, физико-химические свойства функциональных и конструкционных материалов, математическое и компьютерное моделирование некоторых физико-химических процессов.
Материалы сборника могут быть полезны специалистам различного уровня знаний, занимающихся разработкой технологий в области материаловедения, машиностроения, микроэлектроники и др.
УДК 548.52: 539.216
В.А. Небольсин, C.C. Шмакова, Л. А. Харина
О кинетике гетерогенных процессов роста нитевидных кристаллов из газовой фазы
Установлены некоторые кинетические закономерности роста нитевидных кристаллов кремния из газовой фазы
Разрабатываемые сегодня технологические процессы получения микро- и наноразмерных нитевидных кристаллов (НК) могут стать основной движущей силой развития электроники на ближайшие 50 лет. Возможности одномерных микро-, нанообъектов широко изучаются как в рамках широких научно-исследовательских инициатив крупнейших электронных компаний мира, так и узконаправленных проектов, проводимых новыми фирмами, финансируемыми венчурным капиталом. Особые свойства НК определяются двумя важными факторами: геометрическими размерами, которые позволяют считать их одномерными объектами, и собственными природными свойствами материала (например, кремния или углерода). Для использования свойств поистине уникальных объектов необходимо наладить массовое производство таких кристаллов и проволок. Однако сейчас индустрия стоит перед знакомой дилеммой «курицы и яйца». Серьезные проблемы состоят, во-первых, в не разработанности производственных технологий получения нитей, волокон, трубок вследствие непонимания механизмов роста, и, во-вторых, в несовершенстве способов введения одномерных кристаллов в другие технологические продукты.
Учитывая важнейшую необходимость понимания механизмов одномерного роста кристаллов, разработки научных основ и методов регулируемого выращивания микро- и нано-НК кремния требуется проведение исследований. К настоящему времени экспериментально установлен диффузионный режим роста нитевидных кристаллов (НК) кремния из газовой фазы, определены последовательные стадии доставки питающего материала [1-3]. Однако остается открытым вопрос теоретического описания макрокинетики процесса.
В данной работе определяются кинетические условия, при которых реализуется указанный тип процесса роста НК.
Рост НК состоит из последовательных стадий, схематично представленных на рис. 1. Проведем оценку стадий, лимитирующих процесс роста НК. Экспериментально установленный диффузионный режим кристаллизации [1] не предполагает лимитирования процесса стадиями 3 и 5, поэтому исключаем их из рассмотрения.
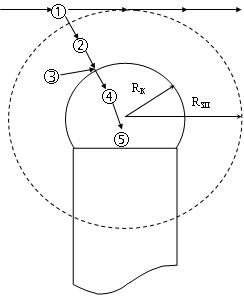
Рис. 1. Схема последовательных стадий процесса роста НК Si: 1 – конвективная диффузия кремнийсодержащих компонентов газовой смеси к реакционной зоне; 2 – молекулярная диффузия реагента в газовой фазе к поверхности жидкой капли; 3 – химическая реакция в газовой фазе; 4 – внутренняя диффузия атомов кремния в жидкой фазе к границе раздела кристалл-жидкость; 5 – кристаллохимическое превращение на границе раздела кристалл-жидкость
Полагая, что конвективная (внешняя) диффузия (стадия 1) протекает сравнительно быстро и процесс контролируется стадиями 2 или 4, найдем уравнение зависимости длины h кристалла в единицу времени t при постоянной температуре и пересыщении в газовой фазе
![]() .
(1)
.
(1)
Скорость внешней диффузии через зону питания (на рисунке 1 показана пунктиром) НК (стадия 2)
![]() ,
(2)
,
(2)
где DГ – коэффициент диффузии кремнийсодержащих компонентов (SiCl2,SiHCl) в газовой фазе; RЗП – радиус зоны питания; СОБ и СПОВ – концентрации кремнийсодержащих компонентов в газе и на поверхности жидкой капли; А – некоторый коэффициент, учитывающий геометрическое соотношение питающей и потребляющей границы.
Скорость внутренней диффузии атомов кристаллизуемого материала в жидкой капле
![]() ,
(3)
,
(3)
где DЖ – коэффициент диффузии атомов кремния в жидкой фазе; RК – радиус капли; СО – равновесная концентрация кремния в жидкости на границе с кристаллом.
Выразим из уравнения (3) величину СПОВ
![]() .
(4)
.
(4)
Подставим (4) в (2) и получим
![]() .
(5)
.
(5)
Для упрощения задачи примем равновесную концентрацию СО = 0, полагая, что все атомы кристаллизуемого вещества, достигающие границы кристалл-жидкость, претерпевают кристаллохимическое превращение.
При установившемся режиме скорости последовательных стадий и скорость процесса в целом равны между собой. Тогда с учетом сделанного выше допущения, приравняв (2) и (5) и разделив переменные, получим
![]() .
(6)
.
(6)
В начальный момент времени (t = 0) рост кристалла отсутствует h = 0. Интегрирование выражения (6) для указанных граничных условий дает следующее выражение
![]() .
(7)
.
(7)
Из выражения (7) следует, что при DГ >>DЖ, т. е. при лимитировании процесса диффузией в жидкой фазе, первым слагаемым в уравнении можно пренебречь и тогда
![]() .
(8)
.
(8)
В этом случае скорость роста НК будет зависеть от природы металла (постоянная А), объемной концентрации кремнийсодержащих компонентов в газовой фазе СОБ (молярного отношения [SiCl4]/[H2]) и радиуса RК капли.
Таким образом, при диффузионном контроле процесса в жидкой фазе скорость роста НК обратно пропорциональна радиусу капли.
При диффузионном контроле в газовой фазе (DГ <<DЖ) пренебрегаем вторым слагаемым в левой части выражения (7). Тогда
![]() .
(9)
.
(9)
В данных условиях скорость роста обратно пропорциональна линейным размерам зоны питания RЗП НК.
Из выполненных расчетов следует: для экспериментального выявления лимитирующей стадии процесса роста НК необходимо создать такие условия, при которых, например, размеры зон питания будут варьироваться, а размеры капли жидкости оставаться неизменными. Если при изменении радиуса зоны питания скорость роста НК будет также меняться, то процесс контролируется газофазной диффузией. Если скорость роста НК в этом случае окажется идентиферентной к изменениям в газовой фазе, значит, процесс лимитируется внутренней диффузией в жидкости.
Полученные экспериментальные данные подтверждают, что скорость роста НК существенно зависит от поверхностной плотности расположения кристаллов на подложке (рис. 2а).
Увеличение плотности расположения НК приводит к перекрытию их зон питания и нехватке «питающего материала», что эквивалентно увеличению зон питания. Указанное экспериментальное наблюдение характеризует диффузию в зонах питания как лимитирующую стадию роста НК. Смоделировать процесс уменьшения размеров зон питания можно увеличением скорости протекания газовой смеси в реакторе.
На рис. 2б видно, что экспериментально измеренная скорость роста НК практически линейно возрастает с увеличением расхода газовой смеси.
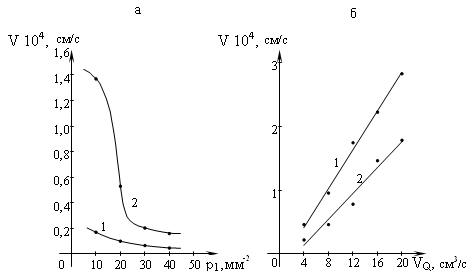
Рис. 2. Зависимость скорости аксиального роста НК Si от поверхностной плотности расположения их на кристалле (а) и расхода газовой смеси (б) для Q = 14 см3/с (1) и Q= 2,8 см3/с (2)
Данная экспериментальная зависимость также не противоречит полученным результатам.
Итак, получено уравнение, описывающее кинетику роста НК кремния и соответствующее экспериментальным результатам при диффузионно-контролируемом режиме процесса.
Литература
1. Небольсин В.А., Щетинин А.А. «Рост нитевидных кристаллов» // Воронеж. гос.ун-т, 2003. 620 с
2. Гиваргизов Е. И. Рост нитевидных и пластинчатых кристаллов из пара. Главная редакция физико-математической литературы издательства «Наука».- М., 1977, 304 с.
3. Небольсин В.А., Щетинин А.А. Роль поверхностной энергии при кристаллизации кремния по механизму пар-жидкость-кристалл. // Неорган. матер. 2003. Т. 39. №9. С. 899-903.
Воронежский государственный технический университет
УДК 502
И.Е. Рохас Риоха
ПОСЛЕДСТВИЯ ЗАГРЯЗНЕНИЯ ОКРУЖАЮЩЕЙ СРЕДЫ
СОЕДИНЕНИЯМИ СВИНЦА
Обсуждаются негативные последствия загрязнения окружающей среды соединениями свинца. Описываются антропогенные источники загрязнения свинцом. Анализируется токсическое действие свинца и его соединений на живые организмы. Рассматриваются методики определения концентрации свинца в промышленных выбросах и в биологических субстратах. Анализируются меры предотвращения отравления людей соединениями свинца
Свинец не является биофильным элементом, однако его распространение в природе и широкое использование в современной промышленности привели к тому, что он обнаруживается в живых организмах во всех точках нашей планеты [1, 2]. В почве в среднем содержится 0,02 г % свинца, в морской воде – 0,01 мг/л, в речной воде – 0,005 мг/л, в воздухе городов – от 1 до 3 мкг/м3. Человек, не занятый работой со свинцом, поглощает приблизительно 0,3 мг этого металла ежедневно [3, 4].
Особую роль среди соединений свинца в течение многих лет играл тетраэтилсвинец Pb(C2H5)4 [5, 6]. Его добавляли в бензин в качестве антидетонатора [8]. Такой бензин называется этилированным. Важной характеристикой топлива является его способность противостоять преждевременному воспламенению в камере сгорания. Детонационное свойство топлива определяют в стандартном одноцилиндровом опытном двигателе при переменном давлении и оценивают значением октанового числа. По эмпирической шкале, предложенной в 1927 году, эта величина находится в интервале от нуля для н–гептана, сильно подверженного детонации, до 100 для изооктана (2,2,4–триметилпентана), который является веществом, стойким к детонации. Октановое число данного топлива показывает содержание изооктана (в %) в смеси с н–гептаном, обладающей такими же детонационными характеристиками, как и горючее в опытном двигателе, работающее при заданных условиях. Позднее были найдены вещества, превосходящие изооктан, и октановая шкала в настоящее время экстраполирована до 120 (например, ароматические углеводороды – толуол, этилбензол – имеют очень высокие октановые числа). Топливо с низким значением октанового числа ограничивает степень сжатия и термодинамическую эффективность двигателя. В современных сортах бензина эти недостатки устраняются обработкой, в результате которой углеводороды изомеризуются с образованием более благоприятных структур, а ранее это достигалось с помощью добавок для повышения октанового числа.
В то время, когда тетраэтилсвинец применялся в качестве антидетонатора, он проникал в организм с вдыхаемым воздухом. Тетраэтилсвинец относится к ядам, оказывающим влияние на все отделы нервной системы. Токсическое действие тетраэтилсвинца объясняется образованием в организме триэтилсвинца – активного ингибитора обменных процессов. Триэтилсвинец может длительно циркулировать в организме и накапливаться в центральной нервной системе. В начальной фазе отравления тетраэтилсвинцом происходит нарушение условных рефлексов. При острых отравлениях этим веществом у человека возникают головные боли, слабость, потеря аппетита, расстройство сна, замедление сердечной деятельности, понижение кровяного давления, падение температуры тела. При хроническом отравлении небольшими дозами тетраэтилсвинца в коре головного мозга возникают сосудистые расстройства и снижение кровоснабжения.
Свинец может поступать в окружающую среду в процессе сгорания угля, при выплавке свинца и сбросе вод с рудников, при производстве аккумуляторов, свинцовых красок, например, свинцовых белил 2PbCO3Pb(OH)2 и сурика Pb3O4, при лужении, при использовании пестицидов, содержащих этот металл. В частности для производства аккумуляторов широко используются оксиды свинца PbO и PbO2. В сельском хозяйстве для борьбы с насекомыми-вредителями применяют гидроортоарсенат свинца PbHAsO4 и ортоарсенат свинца Pb3(AsO4)2. Свинец может присутствовать в пище растительного и животного происхождения [7]. Возможно поступление дополнительных количеств свинца в пищевые продукты из глиняной посуды, покрытой свинцовой глазурью PbSiO3, при пайке швов в консервных банках [7].
Свинец и его соединения оказывают токсическое действие на живые организмы [6, 8]. Негативное действие этих веществ может проявляться в поражении нервной системы, крови и сосудов. Токсическое действие свинца объясняется в первую очередь тем, что его ионы образуют с сульфгидрильными группами SH-содержащих ферментов устойчивые меркаптиды и таким образом блокируют эти ферменты. Взаимодействие свинца с сульфатами и SH–группами может вызвать повреждение генетического аппарата клетки. Соединения свинца нарушают биосинтез гемоглобина, нуклеиновых кислот, гормонов. Дети сильнее страдают от интоксикации свинцом, чем взрослые.
Свинец и его соединения могут попадать в организм при вдыхании паров и аэрозолей. Если концентрация пыли свинца в воздухе находится в интервале от 14,11 до 20,0 мг/м3, то в дыхательных путях человека задерживается около 50 %, при вдыхании воздуха, содержащего пыль свинца в концентрации от 0,04 до 0,07 мг/м3, задерживается от 11 до 12 %.
Рассмотрим одну из наиболее распространенных методик определения содержания свинца в промышленных выбросах при массовой доли этого металла в пыли от 0,02 до 0,5 %. Методика определения концентрации свинца в воздухе атомно-абсорбционным методом основана на измерении абсорбции света атомами свинца, образующимися при введении анализируемого раствора в пламя смеси ацетилена с воздухом, при длине волны 283,3 нм. Для проведения анализа навеску пыли, в которой содержится свинец, растворяют в смеси соляной и азотной кислот. Затем раствор подвергают упариванию до появления влажного остатка. Этот остаток растворяют в азотной кислоте, а потом добавляют воду. Затем исследуемые растворы распыляют в пламени атомно-абсорбционнного спектрофотометра и измеряют абсорбцию атомами свинца при длине волны 285,3 нм. Концентрацию свинца находят по градуировочной зависимости. Для ее построения готовят градуировочные растворы, которые содержат 3, 5, 10, 15 и 20 мг/дм3 свинца. Измеряют их абсорбцию и по результатам измерений строят градуировочную зависимость в координатах С мг/дм3 – А мА (А – показания атомно-абсорбционного спектрофотометра). Массовую долю свинца вычисляют по уравнению
![]() ,
,
где C – концентрация свинца, найденная по графику, мг/дм3; V – объем исходного раствора, дм3; m – навеска исследуемой пыли, г.
Из желудочно-кишечного тракта всасывается примерно от 4 до 5 % от дозы свинца, поступающей в желудок. В крови живых организмов этот металл может находиться виде коллоидального дифосфата, дифосфоглицерата, смешанных солей с кальцием и хлором и органических комплексов с белком. В костях свинец включается в состав легко распадающихся кристаллов оксиапатита. В крови свинец попадает в основном в эритроциты. Среди внутренних органов, в мягких тканях которых накапливается свинец, по интенсивности поглощения этого металла первое место занимают почки. Свинец накапливается в клетках почечных канальцев, образуя внутриядерные включения, которые окружены ограничивающей мембраной. Второе место среди внутренних органов по интенсивности поглощения свинца мягкими тканями принадлежит печени, третье – легким, четвертое – селезенке, на пятом месте находится сердце, на шестом – мышцы. Выведение свинца из организма в норме осуществляется через пищеварительный тракт и почки. Особое внимание нужно уделить накоплению свинца в скелете, так как из костей свинец может периодически выделяться, вызывая рецидивы отравления. Отложившийся в костях свинец может оставаться там, в течение всей жизни. Наибольшее накопление свинца происходит в трубчатых костях, несколько меньшее количество свинца откладывается в плоских костях.
Определению концентрации свинца в биологическом материале придается большое диагностическое значение. Считается, что концентрация свинца в крови дает меньше отклонений, чем в других биологических субстратах, и более прямо коррелирует с поглощенной дозой этого вещества.
Рассмотрим методику определения концентрации свинца в малых пробах крови с дитизоном. В пробу крови, взятую из пальца, вносят 1 мл нитрозилсерной кислоты. Потом раствор кипятят до появления большого количества белых паров. К дымящейся жидкости добавляют азотную кислоту, пока проба не приобретет слабо желтую окраску. В описанных условиях для окисления биологического материала требуется примерно 1 час. К продуктам минерализации приливают 2 мл воды, затем образец кипятят до прекращения выделения оксидов азота. В контрольную колбу вносят такие же количества реактивов, как и в колбу с исследуемой пробой. После этого в обе колбы добавляют по 1 мл раствора лимоннокислого аммония и по 1 мл раствора солянокислого гидроксиамина. Потом в оба раствора вносят аммиак, доводя рН до значения 9,0. Затем добавляют 1 мл смеси растворов цианида калия и лимоннокислого аммония концентрацией 1 %, а также смесь дитизона и хлороформа до окрашивания исследуемой пробы в лиловый цвет. После этого содержимое контрольной колбы титруют из микробюретки раствором нитрата свинца. Титрование заканчивают при совпадении окраски с исследуемым раствором. В данном случае нельзя допускать присутствия висмута и таллия, так как они искажают результаты анализа.
Концентрация свинца в крови, которая не является опасной для здоровья человека, составляет приблизительно 17 мкг %. Содержание этого металла в крови до 60 мкг % свидетельствует о носительстве свинца, концентрация, превышающая 80 мкг %, наносит вред здоровью.
Для предотвращения отравления свинцом на производстве при высокой его концентрации в пыли можно использовать респиратор или фильтрующий противогаз. Необходимо строго соблюдать меры личной гигиены. Запрещается прием пищи в рабочих помещениях. При плавке свинца и содержащих его материалов нельзя повышать температуру выше требуемой технологическим процессом. Рацион питания людей, работающих со свинцом, должен быть богат белками, особенно содержащими аминокислоты метионин и цистеин. Благоприятное влияние также оказывает употребление витамина С и витаминов группы В. Для защиты здоровья населения необходимо уменьшить поступление свинца из всех источников – воздуха, воды и пищевых продуктов.
Литература
1. Голдовская Л.Ф. Химия окружающей среды / Л.Ф. Голдовская. – М.: Бином. Лаборатория знаний, 2007. 295 с.
2. Голицын А.Н. Промышленная экология и мониторинг загрязнения природной среды / А.Н. Голицын. – М.: Оникс, 2007. 336 с.
3. Гусакова Н.В. Химия окружающей среды / Н.В. Гусакова. – Ростов н/Д: Феникс, 2004. 192 с.
4. Новиков Ю.В. Экология, окружающая среда и человек / Ю.В. Новиков – М.: ФАИР-ПРЕСС, 2005. 736 с.
5. Трифонов К.И. Физико-химические процессы в техносфере / К.И. Трифонов, В.А. Девисилов. – М.: Форум, 2007. 240 с.
6. Хван Т.А. Промышленная экология / Т.А. Хван. – Ростов н/Д: Феникс, 2003. 320 с.
7. Шарковский Е.К. Гигиена продовольственных товаров. – М.: Новое знание, 2003. – 263 с.
8. Экология и безопасность жизнедеятельности / под ред. Л.А. Муравья. – М.: ЮНИТИ, 2003. 350 с.
Воронежский государственный технический университет
УДК 541.117
А.Н. Корнеева, В.В.Корнеева
Представление о нанохимии. Азы нанохимии
Рассмотрены свойства наноразмерных частиц, методы их получения и возможности применения
Частицы нанометровых размеров стали интересовать исследователей разных областей науки последние 15 – 20 лет, а особенно с 90-х годов XX века, когда состоялись первые международные конференции по наноматериалам, появились первые специализированные научные журналы. В это же время и появился термин «нанохимия».
Изучение наноразмерных частиц в физике, химии и биологии позволяют утверждать, что наука и технологии XXI века будут иметь наноразмерный ангстремный характер (1 нм = 10-9 м; 1 Å = 10-10). Главная причина интереса химиков к наночастицам состоит в том, что исследования наночастиц элементов периодической системы открывают новые явления в химии, которые невозможно описать на основе известных закономерностей. Особого внимания заслуживают частицы размером меньше 2 нм. Это объясняется тем, что подобные образования, например, металлов, содержат около 10 атомов, которые формируют поверхностную частицу, не имеющую объёма и обладающую высокой химической активностью. В то же время известно, что химические свойства и активность частицы можно изменить добавлением одного атома или молекулы.
Физико-химические свойства и реакции небольших частиц в газовой фазе, а в последнее время также в твёрдой и жидкой фазах начинают описывать количеством атомов и молекул, а не размером в нанометрах.
Полученный экспериментальный материал позволяет определить нанохимию как область, исследующую получение свойства и реакционную способность частиц и сформированных из них ансамблей, которые, по крайней мере в одном измерении, имеют размер менее 10 нм (это условное значение). Предложенное определение и размер позволяют рассматривать в нанохимии одно-, двух- и трёхразмерные объекты типа плёнок, проводов и трубок.
Необычные химические свойства частиц, состоящих из нескольких единиц или десятков атомов, требуют серьёзной модификации представлений, развитых для систем, включающих тысячи и миллионы атомов. Исследования в области нанохимии открывают перспективы формирования новых способов синтеза веществ с необычными, ранее неизвестными свойствами.
В нанохимии выделяют два аспекта:
- первый связан с пониманием особенностей химических свойств и реакционной способности частиц, состоящих из небольшого числа атомов, изучение которых закладывает новые фундаментальные основы нанохимии;
- второй аспект состоит в применении нанохимии для получения, модификации стабилизации изолированных наночастиц и направленной самосборки их в более сложные наноструктуры.
Нанохимия находится в стадии быстрого развития, поэтому при её изучении постоянно возникают вопросы, связанные с понятиями и терминами. Чёткие различия между терминами «кластер», «наночастица» и «квантовая точка» пока не сфрмулированы. Термин «кластер» чаще используется для частиц, содержащих небольшое число атомов, термин «наночастицы» – для более крупных агрегатов атомов и распространён для описания свойств металлов и углерода. Под понятием «квантовая точка» обычно подразумеваются частицы полупроводников и островков, где квантовые ограничения носителей зарядов или экситонов влияют на их свойства. В сообщении термины «кластер» и «наночастицы» используются как равноправные.
Наночастицы и кластеры металлов – важное состояние конденсированной фазы. Подобные системы имеют много особенностей и не наблюдаемых ранее новых химических и физических свойств. Наночастицы можно рассматривать как промежуточные образования между атомами, с одной стороны, и твёрдым состоянием – с другой. Данные частицы обладают изменяемым набором свойств, зависящих от размера. Таким образом, наночастицы можно определить как объекты размером от 1 до 10 нм, состоящие из атомов одного или нескольких элементов. Можно предполагать, что это плотно упакованные частицы с произвольной формой и структурой. Изучение различных свойств обособленных наночастиц составляет одно из направлений нанонауки. Другое направление связано с изучением расположения атомов внутри структуры, формируемой из наночастиц. Относительная стабильность отдельных частей наноструктуры находится в зависимости от кинетических и термодинамических факторов. Следовательно, для наносистем характерно наличие различных флуктуаций.
Нанообъекты, как правило – многочастичные системы, и здесь также приходится сталкиваться с обилием терминов: «нанокристалл», «нанофаза», «наносистема», «наноструктура», «нанокомпозиты» и т.д. Например, наноструктуру можно определить как совокупность наночастиц определённого размера с наличием функциональных связей. Подобные системы, обладающие ограниченным объёмом, в процессе их взаимодействия с другими химическими веществами можно классифицировать как своего рода нанореакторы. Нанокомпозиты – это объекты, где наночастицы упакованы в макроскопический образец, в котором межчастичные взаимодействия становятся сильными и маскируют свойства изолированных частиц. Для каждого вида взаимодействий необходимо знать, как изменяются свойства материала в зависимости от размеров объекта [1]. Следует отметить, что с уменьшением размера частицы понятие фазы выражено менее чётко: границы между гомогенной и гетерогенной фазами, между аморфным и кристаллическим состояниями вещества определить трудно. Обычные химические представления, включающие понятия «состав – свойства», «структура – функция», дополняются в настоящее время терминами «размер» и «самоорганизация», что вызвано обнаружением новых фактов и закономерностей. Тем не менее, несмотря на успехи в развитии нанохимии, пока невозможно ответить на вопрос о зависимости свойств, например, металла от размера частиц.
Наночастицы металлов размером менее 10 нм являются системами, обладающими избыточной энергией и высокой химической активностью. Частицы размером около 1 нм практически без энергии активации вступают в процессы агрегации, приводящие к образованию наночастиц металлов, и в реакции с другими химическими соединениями, обусловливающие получение веществ с новыми свойствами. Запасённая энергия таких объектов определяется в первую очередь нескомпенсированностью связей поверхностных и приповерхностных атомов, что может стать причиной возникновения необычных поверхностных явлений и реакций.
Образование наночастиц из атомов сопровождается двумя процессами: формированием металлических ядер разного размера и взаимодействием между частицами, которые способствуют созданию из них ансамблей, представляющих наноструктуру. Практически все методы синтеза наночастиц приводят к их получению в неравновесном метастабильном состоянии. Это затрудняет изучение наночастиц, но в то же время неравновесность системы позволяет осуществлять необычные и труднопрогнозируемые новые химические превращения.
Установление связи между размером частицы и её реакционной способностью – важнейшая проблема нанохимии. Для наночастиц металла принято различать два типа размерных эффектов:
- собственный или внутренний, обусловленный специфическими изменениями в поверхностных, объёмных и химических свойствах частицы;
- внешний, являющийся размерно-зависимым ответом на внешнее действие сил, которое не связано с внутренним эффектом.
Зависимость химической активности от размера реагирующих частиц объясняется тем, что свойства индивидуальных атомов элементов и формируемых из атомов кластеров и наночастиц отличаются от свойств аналогичных макрочастиц. Для понимания и анализа химических размерно-зависимых свойств в первом приближении можно сравнивать реакционную способность компактных веществ, наночастиц и атомно-молекулярных кластеров. Границы между размерами подобных образований изменяются для каждого атома и должны рассматриваться по отдельности.
Кинетика реакций в наномасштабных системах с ограниченной геометрией отличается от классической, которая не учитывает флуктуаций концентрации реагирующих частиц. Образованиям с небольшим числом взаимодействующих молекул свойственны относительно большие колебания количества реагентов, что приводит к несовпадению во времени изменений концентрации реагентов на поверхности различных по размерам наночастиц и, как следствие, к их разной реакционной способности [2].
В наночастицах значительное число атомов находится на поверхности, и их доля увеличивается с уменьшением размера частиц. Соответственно, возрастает и вклад поверхностных атомов в энергию системы. Отсюда возникает и ряд термодинамических следствий, например, зависимость от размера температуры плавления (Tпл) наночастиц. С размером частиц, влияющим на реакционную способность, связаны и такие свойства, как изменение температуры полиморфных превращений, повышение растворимости, сдвиг химического равновесия. Итак, размер частицы является активной переменной, определяющей вместе с другими термодинамическими переменными состояние системы и её реакционную способность. Размер частицы можно рассматривать как своеобразный эквивалент температуры, и для наномасштабных частиц возможны реакции, в которые не вступают вещества, находящиеся в компактном состоянии.
Высокая активность наночастиц металлов приводит к тому, что их существование в свободном виде, без взаимодействия с окружающей средой, возможно только в вакууме. На примере частиц серебра разного размера, однако, была установлена идентичность их оптических свойств в вакууме и после конденсации в среде аргона при низких температурах. На основании этого был сделан вывод, что процессы осаждения не оказывают влияние на форму и геометрию кластеров, т.е. оптические свойства и реакционную способность наночастиц металлов в газовой фазе и на инертных носителях можно сопоставлять.
Однако, при получении наночастиц в жидкой фазе или на поверхности твёрдых тел картина будет иная, т.к. будет идти взаимодействие наночастиц с окружающей средой.
Итак, ключевая проблема нанохимии – установление влияния размера частиц на их химическую активность. Размерные эффекты в химии – это явление, выражающееся в качественном изменении химических свойств и реакционной способности в зависимости от количества атомов или молекул в частице вещества.
Размер получаемых наночастиц металлов трудно регулировать и воспроизводить, часто он определяется способом синтеза, что затрудняет возможность анализа влияния размера частицы на её реакционную способность.
Изменение химических и физических свойств наночастиц металлов, образуемых из атомов, свидетельствует об их определённой зависимости от числа атомов формы и способа организации. По аналогии с периодической системой Д.И. Менделеева, предпринимаются попытки создать электронные и геометрические таблицы кластер и наночастиц металлов. На примере атомов Na показано, что частицы Na3, Na9, Na19 являются одновалентными, а галогеноподобные кластеры Na7, и Na17 обладают повышенной активностью. Наименьшую активность имеют частицы с закрытыми электронными оболочками Na2, Na8, Na18, Na20.
Для кластеров натрия, содержащих несколько тысяч атомов, так же обнаружено явление периодичности и стабильности частиц. При наличии в частице 1500 атомов Na преобладает геометрическая упаковка в закрытые оболочки, подобные инертным газам.
С проблемой установления зависимости химических свойств от размера участвующих в реакции частиц тесно связано выявление закономерности образования наномасштабных твёрдых фаз в процессе кристаллизации. При взаимодействии атомов в газовой, жидкой фазе или при соударении с поверхностью вначале образуются небольшие кластеры, которые могут укрупняться и превращаться в нанокристалл.
При исследовании влияния частицы элемента на свойства в нанохимии имеет большое значение поверхность, на которой находится частица.
Вопросы получения наночастиц и процессы их стабилизации следует рассматривать в комплексе. Методы синтеза наночастиц можно разделить на две большие группы:
- первая объединяет способы, позволяющие получать и изучать наночастицы, но на основе этих методов трудно создавать новые материалы (конденсация при сверхнизких температурах, химическое, фотохимическое и радиационное восстановление, лазерное испарение);
- вторая включает методы, позволяющие на основе наночастиц получать наноматериалы и нанокомпозиты (это механохимическое дробление, конденсация из газовой фазы, плазмохимические методы и др.).
Это разделение условно, но выражает ещё одну особенность: получение частиц путём укрупнения отдельных атомов, или подход «снизу», и различные варианты диспергирования и агрегации, или подход «сверху». Первый подход характерен, в основном, для химических методов получения наноразмерных частиц [3]. Второй – для физических методов.
Перечислим эти методы:
- химическое восстановление в жидкой фазе, водных и неводных средах. В качестве соединений металлов обычно используют их соль, а восстановителей – алюмогидриды, борогидриды, гипофосфиты, формальдегид, соли щавелевой и винной кислот;
- фото- и радиационно-химическое восстановление. Метод по сравнению с химическим имеет преимущества: это чистота образуемых наночастиц и возможность синтеза наночастиц в твёрдых средах и при низких температурах;
- криохимический синтез; суть метода состоит в применении инертных газов при серхнизких температурах;
- физические методы, например, испарение металла в поток инертного газа с последующей конденсацией в камере с определённой температурой
и др. методы.
Для получения информации о наночастицах на поверхности используются:
- просвечивающая и сканирующая электронная микроскопия (размер/форма частиц, их распределение и топология);
дифракция электронов (размер, фаза – твёрдая/жидкая структура и длина связи);
сканирующая туннельная микроскопия (определение размера и формы частицы и внутренней структуры);
- адсорбция газов (площадь поверхности);
- фотоэлектронная спектроскопия (электронная структура);
- электропроводность (информация о зоне проводимости и топологии).
Размер и некоторые свойства наночастиц в объёме или матрице определяются различными методами.
Просвечивающая и сканирующая электронная микроскопия, электропроводность, а также дифракция электронов предоставляют сведения о частицах в объёме, т.е. информацию, аналогично получаемой для частиц на поверхности. Для частиц в объёме используется и ряд других методов. Например, рентгенография даёт информацию о размерах и внутренней структуре частиц.
Расширенная тонкая структура и адсорбция рентгеновских лучей позволяют определять размер частиц, а методы электронного парамагнитного резонанса (ЭПР) и ядерного магнитного резонанса дают информацию об электронной структуре. Для определения внутренней структуры ряда элементов, особенно такого важного, как железо, активно используется мёссбауэровская спектроскопия или резонансное поглощение гамма-квантов ядрами атомов твёрдого тела (гамма-резонанс). Энергия гамма-квантов невелика (~150 кЭв), когда гамма-квант поглощается, то ядро возбуждается. Условие резонанса – равенство энергии возбуждения ядра энергии квантового перехода, т.е. разности внутренней энергии ядра в возбуждённом и основном состояниях. Энергия перехода зависит от природы ядра даёт информацию о микроскопической структуре твёрдых тел. Метод применим не ко всем элементам. Наиболее хорошо этим методом анализируются Fe57, Sn119, Te125.
Наночастицы металлов широко применяются для получения новых керамических материалов ультрадисперсионных порошков, консолидированных и гибридных систем. Кроме того, наночастицы металлов используются для создания новых катализаторов. Горение метана на воздухе стабильно при температурах выше 1300ºС. Однако, при этой температуре выделяются вредные оксиды азота, возникает смог. Однако, новый катализатор представляет собой твёрдый кристаллический наноразмерный гексаалюминат бария, снижает температуру горения метана до 400 ºС, и вредные примеси не образуются.
Высокая активность нанокристаллических оксидов металлов была реализована с соединениями, используемыми как химическое оружие. Нанокристаллические оксиды магния и кальция взаимодействуют с фосфорорганическими соединениями и образуют нервно-паралитическое соединение.
Полупроводниковые наночастицы широко используются в гетерогенном нанокатализе и представляют интерес для лазерной техники, при изготовлении плоских дисплеев, светоиспускающих диодов и сенсоров [4].
Нанофотоника – новая область, которая изучает оптические свойства объектов с размерами много меньше длины волны оптического излучения.
Углеродные нанотрубки можно применять в виде массивных изделий и миниатюрных устройств. В первом случае множество трубок используется в качестве наполнителей для композитов, источников тока, адсорбентов или аккумуляторов газов, во втором – для изготовления различных электронных устройств, полевых эмиттеров электронов, сверхпрочных зондов, микроскопов, сенсоров [5].
Особое место в нанотехнологии принадлежит частицам, связанным с реализацией различных биопроцессов. В область нанобиологии и наномедицины перемещаются основные исследования по нанохимии. Это связано с проблемами питания, экологии, здоровья и продолжительности жизни. Активно развивается применение полупроводниковых квантовых точек в качестве меток клеток, тканей, бактерий и вирусов. Однако, при использовании наночастиц в биологии и медицине особое внимание следует уделять вопросам безопасности из-за возможной токсичности применяемых материалов и недостаточной изученности особенностей свойств частиц, связанных с уменьшением их размеров.
литература
1. Нанотехнология в ближайшем десятилетии. Прогноз направления исследований / Под ред. М.К.Роко, Р.С.Уильямса и П.Аливисатоса. Пер. с англ. - М.: Мир, 2002. - 292 с.
2. Гусев А.И., Ремпель А.А. Нанокристаллические материалы. — М.: ФИЗМАТЛИТ, 2001. — 224 с.
3. Методы получения и свойства нанообъектов: учебное пособие / Н.И. Минько и др.– М.: Флинта: Наука, 2009.– 163 с.
4. Сергеев Г. Б. Нанохимия. — М.: Изд-во МГУ, 2003. — 288 с.
5. Золотухин И.В. Углеродные нанотрубки // Соросовский образовательный журнал, 1999, №3, с. 111-115.
Воронежский государственный технический университет
УДК 502.32
О. Н. Болдырева, Р.Л. Вуйцик
МОДИФИКАЦИЯ ПОЛИМЕРНЫХ АДСОРБЕНТОВ
ДЛЯ ИЗВЛЕЧЕНИЯ ЛЕТУЧИХ ХИМИЧЕСКИХ СОЕДИНЕНИЙ
Одной из проблем химических производств – образование газовоздушных смесей, выбросы которых приводят к загрязнению окружающей среды
Для извлечения летучих химических соединений применяют способ, заключающийся в пропускании газовоздушной смеси через слой полимерного адсорбента – порошок пористого поливинилхлорида (ПВХ).
Высокая емкость полимерного адсорбента обусловлена не только удельной поверхностью (она у пористого ПВХ на несколько порядков меньше, чем у активированных углей), обеспечивающей способность пористого полимерного зерна конденсировать ВХ, но и его растворимостью в полимерной матрице при определенных условиях процесса. В работе 1 показан равноценный вклад капиллярной конденсации и растворения ВХ адсорбентом. При этом процессы адсорбции и десорбции ВХ протекают практически без выделения тепла и повышения температуры.
К достоинствам полимерного адсорбента можно отнести негорючесть, гидрофобность, стойкость к действию кислот и щелочей, возможность использования при минусовых температурах. Фаза адсорбции составляет 0,5-2 ч в зависимости от концентрации ВХ в абгазах. Десорбция осуществляет ваккуумирование адсорбента без использования водяного пара, что дает сокращение числа фаз полного цикла «адсорбция – десорбция» и экономию энергии. Небольшие значения тепловых эффектов поглощения позволяют применять полимерные адсорбенты даже для улавливания ВХ аварийных сдувок из реакторов – полимеризаторов.
Эффективность извлечения паров различных химических соединений определяли из соотношений Э≈1-С /C , где С , С – соответственно начальная и конечная (после адсорбера ) концентрация исследуемого продукта в газовой смеси.
В качестве исследуемых химических соединений использовали ВХ, толуол, хлороформ, ацетон, дихлорэтан, нефрас, бензин (смесь различных углеводородов), отличающиеся температурой кипения Т , давлением насыщенных паров Р , а также способностью взаимодействовать с ПВХ.
Как показали результаты исследования, по эффективности улавливания можно выделить две группы продуктов (таб.1).
Таблица 1
Эффективность улавливания паров органических соединений в зависимости от степени насыщения адсорбента

Отличительной особенностью двух групп химических соединений является их степень взаимодействия с ПВХ-адсорбентом.
Для химических соединений первой группы параметр их взаимодействия с ПВХ Флори – Хаггинса χ< 1 [2], что свидетельствует об их склонности растворять ПВХ, в то время как метанол, нефрас и бензин с ПВХ практически не взаимодействуют.
Для оценки растворяющей способности растворителя в полимере можно использовать значение параметра χ: чем меньше значение χ, тем выше растворяющая способность химического соединения к полимеру; объемная доля растворителя в полимере составляет е [3]. Для ВХ значения равно 0,88; ацетона – 0,6 [4], дихлорэтана – 0,46; тетрагидрофурана – 0,24; циклогексанона – 0,14, а для спиртов, например бутанола, - 1,74 [3].
В процессе реакции хлорирования возможно образование газовоздушных смесей, содержащих как не прореагировавший хлор, так и образующийся хлористый водород. Возможность использования полимерного адсорбента для улавливания данных химических соединений подтверждают значения таб. 2.
Таблица 2 Адсорбция газов, содержащих хлор и хлористый водород
Содержание до адсорбции, % об. |
Содержание после адсорбции, % об. |
CI HCI |
CI HCI |
0,57 5,8 1,63 16,3 8,23 12,7 0,62 11,0 0,53 13,9 |
Отсутствует 5,81 Отсутствует 16,0 Отсутствует 12,0 Отсутствует 8,0 Отсутствует 12,1 |
Наиболее целесообразно использование предполагаемой технологии для улавливания органических соединений (ВХ, дихлорэтан, хлористый этил, ацетон, толуол, бензол, четыреххлористый углерод, пары бензина, этилацетата, хлороформ и т.д. ) с температурой кипения 13-145 С и концентрацией от 2 до 80% об. Высокое содержание органических соединений газовоздушной смеси делает затруднительным способ адсорбции с использованием активных углей вследствие большого теплового эффекта поглощения и опасности возгорания.
Степень очистки абгазов составляет приблизительно 99%. В дальнейшем при необходимости возможна санитарная очистка газовых выбросов при содержании органических соединений менее 1%. Установлено, что степень улавливания различных фракций углеводородов составляет:
Этан – не менее 40-50%, Т - 88,6 С;
Пропан – не менее 50-60%, Т - 42,1 С;
Изобутан – не менее 58-66 %, Т - 11,7 С;
n-бутан – не менее 80 %, Т - 0,5 С;
Изопетан – не менее 97 %, Т - + 28 С;
n- пентан, гексан и др. – не более 99%, Т - + 68,7 С и более.
То есть, чем выше температура кипения углеводородов, тем эффективнее действие полимерного адсорбена. Наиболее предпочтительно его использование для улавливания высококипящих компонентов, например таких, как бензол, толуол, ксилол, этилбензол, имеющих очень низкие значения ПДК (менее 1 мг/м ).
Литература
1. Технологическое оборудование производства суспензионного поливинилхлорида : Монография / В.М. Ульянов, А.Д. Гуткович.- Нижегород. гос. тех. ун-т, 2004 . – 156 с.
2. Баррета К.Е. Дж. Дисперсионная полимеризация в органических средах. – Л.:Химия 1979.- 224 с.
3. Штаркман Б.П. Пластификация поливинилхлорида. М.:Химия. 1985.-196 с.
4. Родионов А.И., Техника защиты окружающей среды. – М.:.Химия,-2005.-124 с.
Воронежский государственный технический университет
УДК 552.3
О.Н. Болдырева, И.И. Панков
Оценка состояния металла на основе неразрушающего контроля
Выявлены информационные взаимосвязи между акустическими характеристиками и микроструктуры металла
Накопленный обширный эмпирический материал по применяемым конструкционным материалам, закономерностям изменения микроструктуры и свойств металлов при длительной службе, по типам эксплуатационных разрушений и их причинам, методам неразрушающегося контроля. При решении задач управления безопасности эксплуатацией ОПО (опасно производственный объект), возникает необходимость разработки различных моделей и критериев, формирования исходных данных для расчета остаточного ресурса, что является трудоемкой задачей.
Достоверность и качество получаемых результатов могут быть повышены, а трудоемкость оценок снижена при использовании современных информационных технологий.
Для формирования требования к системе и ее функциям, использована методология структурного анализа (Structur-ed Analysis & Design Technique). В наибольшей мере решению этой проблемы соответствует методология стандарта IDEF0, которая представляет собой совокупность методов, правил и процедур, предназначенных для построения функциональной модели объекта.
Результат применения методологии – модель, которая состоит из диаграмм, фрагментов текстов и глоссария. Имеющих ссылки друг на друга. На рис.1 показана контекстная диаграмма
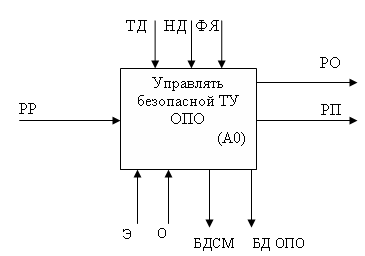
Рис. 1. Контекстная диаграмма безопасной эксплуатации ТУ ОПО
Определены и описаны главные взаимодействия (стрелки), которые активируют основную функцию:
1. В качестве ресурса принят расчетный ресурс (РР) технических устройств (до начала эксплуатации на ОПО). Эта характеристика задается в зависимости от применяемых мате-риалов, их химического состава, режимов термической обра-ботки и физико-механических свойств, а также вектора {a1,a2, …,ai,j,…}={ai} совокупности эксплуатационных пара-метров, таких как температура a1, внутреннее давление a2, действующие напряжения a3,вид напряженно-деформирован-ного состояния a? агрессивная среды a5 и т. д.
2. Продуктом выполнения данной функции является также срок эксплуатации оборудования, но уже с учетом определен-ного времени работы при заданных параметрах. Две стрелки на выходе из блока означают, что ресурс после определенной наработки может быть представлен в одном из двух видов: ресурс остаточный или индивидуальный остаточный РО(/ai) и ресурс послеремонтный РП (/ai). Под послеремонтным ресурсом понимается назначенный срок эксплуатации узла или детали технического устройства после его ремонта либо после замены.
3. В качестве управляющих воздействий приняты норматив-но-техническая документация (НД) на технические устройства (ГОСТы, ТУ и РД Ростехнадзора) и эксплуатационно-техническая документация (ТД) рассматриваемого оборудования, включая проектно-конструкторскую документацию на техническое устройство, паспорт оборудования. Инструкции по эксплуатации, ремонтную документацию, физико-хими-ческие явления (ФЯ), происходящие в металле ТУ при дли тельной эксплуатации.
4. В качестве механизмов исполнения функции приняты реальные режимы эксплуатации оборудования (Э), от параметров которых зависит состояние металла (Э), от параметров которых зависит состояние металла на данном этапе работы, экспертиза, проводимая в заданные НД сроки (О).
5. Вызов (запрос) разделяет или соединяет информацию между моделями или элементами данной модели, может отсылать для получения дополнительной информации к другой модели. В рамках данной контекстной модели в целях реализации механизмов исполнения запрашивают базу данных технических устройств (БД ТУ ОПО) и базу данных состояния металла (БДСМ) в целях получения информации о безопасности эксплуатации различных ТУ ОПО, о характере изменения физико-механических характеристики и микроструктуры. IDEF0 модели представляют собой иерархическую структуру, на вершине которой размещен блок (контекстный) всей сис-темы как единого целого, а на нижних уровнях расположены детализированные блоки диаграммы. Технические устройства (А1) эксплуатируют согласно требованиям ТД и НД, за-давая требуемый показатель gтр при фактических условиях и режимах (Э). Детализированная контекстная диаграмма показана на рис. 2 .
После некоторого срока наработки техническое состояние оборудования изменяется, соответственно уменьшается и ресурс, но должна оставаться необходимая вероятность того, что остаточный ресурс выше требуемого уровня P{g(u)≥ gтр}=y. Для определения индивидуального (остаточ-ного) ресурса (РО) оценивают g(u)=M[g(u)] реальное техни-ческое состояние ТУ ОПО (А2) путем проведения экспертизы (О). Оценка технического состояния (А2)
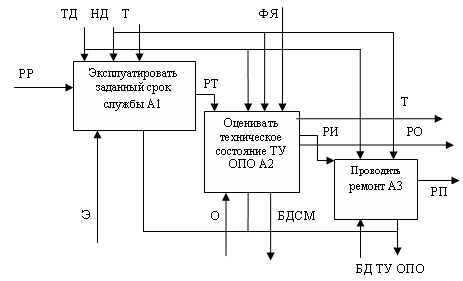
Рис. 2. Детализированная контекстная диаграмма (декомпозиция А-0). РТ – измененный (текущий) ресурс эксплуатации после определенного срока наработки оборудования при фактических режимах, РИ – исчерпанный ресурс эксплуатации ТУ ОПО
включает в себя анализ эксплуатационно-технической документации (А21) и определении статистического уровня gст, проведение решения и выдачу заключения (А23) g(u)>gтр. Декомпозиция блока оценки технического состояния ТУ ОПО (А2) показана на рис. 3. Срок дальнейшей эксплуатации определяют на основании результатов анализа документации (АД) и экспертизы (АР) с учетом результатов запросов из баз данных.
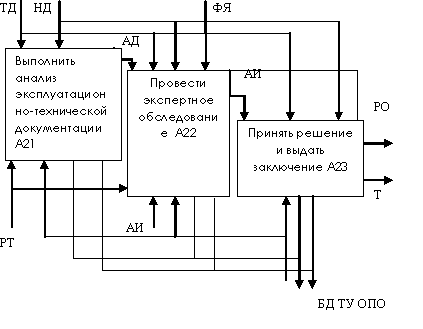
Рис. 3. Декомпозиция блока оценки технического состояния ТУ ОПО АИ – акустические изменении
Физико-механические характеристики и результат ме-таллофизических исследований (ФМ), а так же выбранный и обоснованный метод акустической структуроскопии (АВ) из комплекса методов исследования (КМ) являются исходными данными для определения акустических характеристик метал-ла. Декомпозиция блока определения состояния металла по акустическим характеристикам приведена на рис. 4.
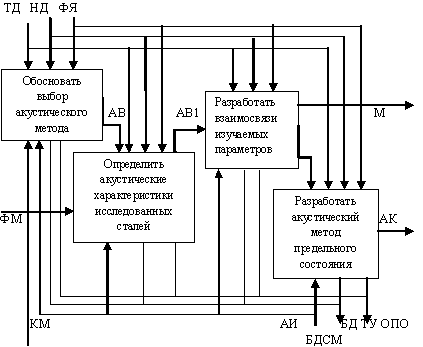
Рис. 4. Декомпозиция блока определения состояния металла по акустиче-ским характеристикам АВ – выбранные способы акустических измере-ний; АВ1 – результаты акустических изменений исследованных сталей в различном структурном состоянии и после разных сроков эксплуатации и их взаимосвязи с физико-механическими характеристиками
За величину степени поврежденности было принято отношение времени задержки ПАВ в момент диагностики Wt к времени задержки у металла, исчерпавшего свой ресурс (при наличии микротрещин) Wf с учетом времени задержки ПАВ в металле с исходным состоянием структуры W0. Ком-плексный критерий предельного состояния длительно работа-ющего металла можно выразить
Kf=![]() ,
,
где γ=1,0÷1,1 – коэффициент, учитывающий материал контро-лируемого элемента.
Комплексный критерий предельного состояния, выраженный в относительных единицах, позволяет судить о количественной величине поврежденности и прекращать эксплуата-цию технического устройства для замены контролируемого элемента, исходя из соотношения Kf≤0.7÷0.9. Значение ККПС для нового (Wt=W0) и разрушенного (Wt=Wf) элементов ТУ ОПО имеют соответственно значения 0 и 1, была отмечена его непропорциональная зависимость от вре-мени эксплуатации, в соответствии с которой время до разру-шения до разрушения можно определить из соотношения
![]() ,
,
где Т среднестатистическое время эксплуатации элемента из определенного металла до его разрушения, ч; Кf=1,0÷1,2 – коэффициент, учитывающий условия эксплуатации. Концеп-туальная модель, состоящая из диаграмм, текста и терминоло-гического словаря, выполненная в формализованном виде и представленная функциями, каждая из которых отражает ре-альное состояние длительно работающего металла на всех этапах жизненного цикла технических устройств.
Литература
1. Дэвид А. Марка, Клемент Мак-Гоурэн, Методология структурного анализа и проектирования: Пер. с англ. – М., 1993 – 240 с.
2. Вендров А.М. CASE –технологии. Современные методы и средства проектирования информационных систем. – М., Argussoft Co, 1999. – 86 c.
3. Смирнов А.Н., Муравьев В.В., Хапонен Н.А. акустический критерий предельного состояния длительно работающего металла технических устройств опасных производственных объектов // Контроль. Диагностика – 2004 - №5. – с. 19-23.
Воронежский государственный технический университет
УДК 621.039.073
И.А. Мандрыкин, А.Н. Корнеева, В.В. Корнеева
Современные методы утилизации ядерных отходов
В статье рассмотрены источники возможные радиоактивного заражения и современные методы утилизации ядерных отходов
Проблема защиты окружающей среды – одна из важнейших задач современности. Выбросы промышленных предприятий, энергетических систем и транспорта в атмосферу, водоемы и недра на современном этапе развития науки и техники достигли таких размеров, что в ряде районов, особенно в крупных промышленных центрах, уровни загрязнений в несколько раз превышают допустимые санитарные нормы.
1. Радиоактивные отходы
1.1. Откуда появляются отходы
Любой сектор, который использует радиоактивные изотопы или обрабатывает естественно встречающиеся радиоактивные материалы (ЕВРМ), может производить радиоактивные материалы, которые перестают быть полезными и поэтому должны обрабатываться как радиоактивные отходы. Ядерная промышленность, медицинский сектор, ряд других секторов промышленности, а также различные секторы, занятые исследовательской деятельностью – все генерируют радиоактивные отходы в результате своей деятельности.
1.2. Ядерная промышленность
В результате своей деятельности ядерная промышленность порождает ядерные отходы. Эти отходы относительно малы по сравнению с другими секторами промышленности. Технологии уменьшения объема отходов и их сокращения, а также высокий профессионализм персонала - все это способствуют непрерывному продолжению процесса минимизации произведенных отходов, что является ключевым принципом стратегии управления отходами.
1.3. Медицинский сектор
Использование радиоактивных изотопов для медицинской диагностики и лечения приводит к образованию отходов низкого уровня активности. Эти отходы включают бумагу, инструментальные средства, одежду и фильтры, которые обычно содержат небольшие количества короткоживущих радиоактивных веществ [1]. Отходы этого типа часто складируются на период распада, занимающий от нескольких месяцев до нескольких лет, прежде, чем удаляются на общегородские свалки.
Другие источники, типа радия-226, используемые в терапии рака, требуют, однако, более длительного хранения и геологического захоронения из-за их более высокого уровня долгоживущей радиоактивности.
1.4. Промышленность
Различные отрасли промышленности используют радиоактивные источники, находя им широкий диапазон применения. Когда эти источники перестают испускать проникающую радиацию в достаточной степени для их использования, с ними обращаются как с радиоактивными отходами. Источники, используемые в промышленности, в общем случае короткоживущие, и любые сгенерированные отходы могут удаляться в приповерхностные хранилища.
Некоторые виды промышленной деятельности включают обработку сырья, например, горных пород, почв и полезных ископаемых, которые содержат естественно встречающиеся радиоактивные материалы [2]. Это сырье известно по аббревиатуре "ЕВРМ" (естественно встречающиеся радиоактивные материалы). При промышленном производстве эти материалы иногда могут концентрироваться в больших количествах, что усиливает их естественную радиоактивность.
В результате это может приводить к:
- риску облучения персонала или населения;
- недопустимому радиоактивному загрязнению окружающей среды;
- необходимости исполнять регулирующие требования захоронения радиоактивных отходов.
Основные отрасли промышленности, которые приводят к загрязнению ЕВРМ:
Например, операции, связанные с добычей нефти и газа, каменного угля, с промышленным сбором металлолома и металлоплавильных шлаков.
2. Обращение с отходами
2.1. Обработка и кондиционирование
Процессы обработки и кондиционирования используются для трансформации радиоактивных отходов в формы, подходящие для последующего обращения с ними, например, перевозки, хранения и окончательного удаления. Защита людей и окружающей среды от радиации и возможной дисперсии радиоактивных материалов - самые важные приоритеты промышленности.
2.2. Остекловывание радиоактивных отходов
Связывание отходов высокого уровня активности требует формирования нерастворимых, твердых форм, которые останутся устойчивыми в течение многих тысяч лет. В основном в качестве среды для размещения этих отходов выбирается боросиликатное стекло [3]. Стабильная сохранность стекла с античных времен на протяжении тысячелетий подтверждает мысль о пригодности боросиликатного стекла в качестве материала для такой матрицы.
Было создано несколько других альтернативных процессов, использующих керамику, использование которых также позволило добиться желательного качества продукта.
2.3. Сжигание
Технология сжигания (прокаливания) в основном используется для уменьшения объема горючих отходов низкого уровня активности. Это - технология, которая является также предметом беспокойства населения во многих странах, поскольку местных жителей волнует проблема образующихся при сжигании выбросов в атмосферу. Пока она используется согласно строгим нормам, установленным для выбросов в атмосферу.
2.4. Уплотнение
Уплотнение - зрелая, высокотехнологичная и надежная технология уменьшения объема, которая используется при переработке РАО (радиоактивных отходов), главным образом, при обращении с твердыми промышленными отходами низкого уровня активности [4]. Некоторые страны (Германия, Великобритания и США) также используют эту технологию для уменьшения объема промышленных отходов промежуточного уровня активности. Коэффициенты уменьшения объема обычно находятся между 3 и 10, в зависимости от обрабатываемых отходов.
2.5. Цементирование радиоактивных отходов
Цементирование с помощью жидких цементных растворов, приготовленных по специальным рецептам, позволяет обеспечивать иммобилизацию радиоактивных материалов, находящихся в твердом виде, в виде ила и осадков / гелей или активированных материалов [5].
Как правило, твердые отходы помещаются в контейнеры. Затем в этот контейнер заливается жидкий цементный раствор, где он и схватывается.
В случае если отходы находятся в виде ила и хлопьев, в контейнер, куда они помещаются, добавляется порошковая цементная смесь. Эти два компонента смешиваются внутри контейнера и оставляются для схватывания бетона, также как и при обращении с отходами в твердом виде.
3. Радиоактивные отходы отправят на Солнце
В далеком будущем, радиоактивные отходы, включая отработанное ядерное топливо, можно будет хоронить на Солнце. Во всяком случае, в России разработан подобный проект.
Заключение
Подводя итог всему вышесказанному, можно сказать, что, несмотря на длительность изучения настоящей проблемы, утилизация и переработка отходов по-прежнему не ведется на должном уровне.
Литература
1. "Атомная мифология" Алексея Яблокова.
2. "Радиоактивные отходы АЭС и методы обращения с ними " Ключников А.А., Пазухин Э. М., Шигера Ю. М., Шигера В. Ю..
3. "ЯДЕРНОЕ ЭЛЕКТРИЧЕСТВО" Ян Гор Лесси, перевод на русский язык В.С. Малышевского.
4. Батырев А.Н и др. "Обеспечение ядерной безопасности при эксплуатации и утилизации ЯЭУ и реакторного оборудования кораблей ВМС ведущих зарубежных государств ". Под общ. ред. М.Н. Тихонова. Проблемы окружающей среды и природных ресурсов. 2002.
5. Довгуша В.В., М.Н. Тихонов "Концепция экологической безопасности утилизации снятых с эксплуатации атомных подводных лодок // Экология и промышленность России", 2005.
Воронежский государственный технический университет
УДК 622.279
А.А. Рукавицына, А.Н. Корнеева, В.В. Корнеева
Влияние сланцевого газа на экологию
В статье рассматривается неблагоприятное влияние сланцевого газа на экологию
В последнее время много разговоров идет о возможной революции на мировом газовом рынке. Связывают такую революцию с перспективами добычи так называемого сланцевого газа.
Сланцевый газ- это природный газ, добываемый из горючих сланцев и состоящий преимущественно из метана. Запасы отдельных сланцевых газовых коллекторов невелики, но в совокупности их достаточно для организации промышленной добычи. Сланцевые залежи встречаются на всех континентах, что теоретически предполагает обеспечение необходимыми энергоресурсами любой страны, в том числе энергозависимой. По самым скромным подсчетам, при нынешнем уровне потребления энергии технически извлекаемых запасов сланцевого газа Франции хватит на 104 года, Дании — на 156 лет. Запасы Германии, которая потребляет больше газа на душу населения, чем любая другая европейская страна, сланцевый газ увеличит более чем вдвое. Запасы Нидерландов — на треть.
Себестоимость добычи газа велика. Однако высокие цены на природный газ сделали добычу сланцевого газа экономически целесообразной. Появились новые технологии, позволяющие извлекать его без особых затрат.
Современная технология добычи сланцевого газа включает бурение одной вертикальной скважины и нескольких горизонтальных скважин с мультиотводами на одной глубине, а также многоступенчатых горизонтальных скважин с длиной горизонтального отвода до 3-х километров. В пробуренные скважины закачивается смесь воды, песка и химикатов, в результате гидроудара взрываются стенки газовых коллекторов, и весь доступный газ откачивается на поверхность.
Однако, как известно, даже у самого позитивного явления непременно имеются теневые стороны. Основная опасность для экологии при добыче сланцевого газа заключается в использовании большого количества химикатов, которые смешиваются с водой и песком. Химическая смесь составляет около 1,53 % от общего раствора и включает: соляную кислоту, формальдегид, уксусный ангидрид, пропаргиловый и метиловые спирты, хлорид аммония. В целом, газодобывающими компаниями для добычи газа используется около 85 токсичных веществ, некоторые из них имеют следующее предназначение: соляная кислота способствует растворению минералов; этиленгликоль противостоит отложениям на внутренних стенках труб; изопропиловый спирт, гуаровая камедь и борная кислота используются в качестве загустителей и веществ, поддерживающих вязкость; глютаральдегид и формамид противостоит коррозии; нефть в лёгких фракциях используется для снижения трения; пероксодисульфат аммония противостоит распаду гуаровой камеди; хлорид калия препятствует химическим реакциям между жидкостью и грунтом; карбонат натрия или калия — для поддержки баланса кислот [1].
Несмотря на то, что гидроразрывы проводятся гораздо ниже уровня грунтовых вод, токсичными веществами заражен почвенный слой, грунтовые воды и воздух. Это происходит за счет просачивания химических веществ через трещины, образовавшиеся в толще осадочных пород, в поверхностные слои почвы. В некоторых районах Пенсильвании в колодцах можно поджечь воду. Также отметим, что наиболее успешные сланцевые месторождения относятся к палеозойской и мезозойской эре, имеют высокий уровень гамма-излучения, который коррелирует с термической зрелостью сланцевого месторождения. В результате гидроразрыва радиация попадает в верхний слой осадочных пород, в районах сланцевой добычи газа наблюдается повышение радиационного фона [2].
Возникают серьезные вопросы об экологическом риске и здоровье человека. Кроме того, предполагается, что гидроразрыв может привести к возникновению небольших землетрясений. 1 сентября 2011 года в Брюсселе опубликован отчет последних исследований Агентства по охране окружающей среды США. В результате приведены неоспоримые факты, что выбросы парниковых газов при добыче сланцевого газа больше, чем у угля, нефти и обычного газа, общий объем потерь метана при добыче газа составляет 3,6-7,9%.
Операцию разрыва пластов на одной территории приходится повторять до 10 раз в год. Химическая смесь, пропитывающая породу, загрязняет большие территории реактивами, а также грунтовые воды. Возникает загрязнение воздуха не только выбросами углерода, но и 369 токсичными веществами. Наблюдается увеличение числа раковых заболеваний. Постоянные разрушительные процессы в самом грунте и в почве (проседание почвы), вплоть до сейсмической нестабильности и землетрясений [3].
Добыча сланцевого газа в XXI веке еще только набирает свои обороты в производстве, но, несмотря на короткий производственный цикл, пагубно отражается на экологии районов. Технология добычи сланцевого газа требует более безопасного и экологически чистого методов разработки, т.к. оказывается огромное воздействие на биосферу. Для того чтобы начать добычу топлива требуются большие затраты, связанные как с природными ресурсами (вода, песок), так и химическими веществами, которые закачиваются в недра Земли и «отравляют» площади вокруг района добычи. К сожалению, на фоне картины истощения традиционных запасов газа сланцевый газ не сможет стать в ближайшее время достойной альтернативой природному газу, так как не соответствует современным экологическим требованиям к энергоресурсу. Перспективы крупной добычи сланцевого газа в настоящее время имеются только в слабозаселенных районах и в странах, которые согласны на снижение экологической безопасности. Иногда стоит задуматься над тем, что важнее: окружающая нас природа или экономическое развитие страны.
Литература
1. Ж. Зеленцова. Сланцевой революции не произошло.-2011. [Электронный ресурс]. URL: www.pronedra.ru /gas/2011/12/23/ slancevyj-gaz (дата обращения 14.12.2012).
2. А.Ярошинская. Сланцевой революции не произошло.-2012. [Электронный ресурс]. URL: www.eco-pravda.ru/page.php?id=1902 (дата обращения 14.12.2012).
3. А.Ярошинская. Сланцевый кошмар для России,-2012.[Электронный ресурс]. URL: www.rosbalt.ru/main/2010/03/13/719852.html (дата обращения 14.12.2012).
Воронежский государственный технический университет
УДК 621. 367. 502.7
И. М. Винокурова, Шалимов Ю. Н.
Схематическое Определение особенностей протекания Электрохимических процессов
ПРИ АНОДНОЙ обработкЕ
В материалах статьи приводятся данные по определению процессов анодной обработки с водородной деполяризацией
Электрохимическое растворение металла – сложный процесс, состоящий из трех основных процессов (рисунок):
1) анодного процесса – образования гидратированных ионов металла в электролите и некомпенсированных электронов на анодном участке по реакции
![]()
2) процесса перетекания электронов по металлу от анодных участков к катодным и соответствующего перемещения катионов и анионов в растворе;
3)
катодного процесса - ассимиляции
электронов какими-либо ионами или
молекулами раствора (деполяризаторами),
способными к восстановлению на катодных
участках по реакции
![]()
Всякая технологическая система состоит из твердых тел, соприкасающихся между собой в той или иной последовательности, а также из жидкостей и газов, окружающих эти тела или циркулирующих внутри них. Каждое из твердых тел (деталь оборудования, заготовка, инструмент) имеет одну или несколько контактных поверхностей. Источники и стоки теплоты могут возникать как на этих поверхностях, так и за их пределами. Задача тепло-физического анализа состоит в том, чтобы выяснить влияние совокупности источников и стоков, действующих в конкретной технологической системе, на температуру любого из компонентов этой системы.
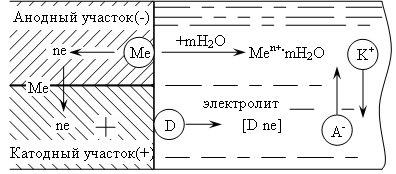
Схема электрохимического коррозионного процесса
В зависимости от целей анализа могут быть поставлены задачи определить: 1) законы распределения температур на различных участках технологической системы или подсистемы, в первую очередь в местах соприкосновения тел; 2) средние температуры на поверхности тел; 3) максимальные температуры, которые возникают в технологической системе или подсистеме на наиболее нагруженных или ответственных участках. Располагая частью этих сведений или их полным набором, конструктор и технолог могут намечать пути управления тепловыми явлениями, решать задачу об оптимизации системы, повышении производительности процессов обработки и качества изделий.
Независимо от того, какая из перечисленных выше трех задач составляет цель теплофизического анализа, а также от того, какую систему тел или вид обработки рассматривают, анализ проводят в определенном порядке, который представим в виде обобщенного алгоритма.
Обобщенный алгоритм теплофизического анализа.
Алгоритм содержит десять основных операций, которые вначале перечислим, а затем прокомментируем.
Выясняют число и местоположение источников и стоков теплоты в системе или подсистеме. Устанавливают мощность и время функционирования каждого из источников и стоков.
Определяют размеры и конфигурацию площадок или объемов, внутри которых действуют источники и стоки теплоты. Устанавливают (или принимают) законы распределения плотности потоков для каждого источника и стока.
Схематизируют форму и свойства твердых тел, а также форму и другие характерные особенности источников и стоков теплоты, действующих в технологической системе.
Принимают вид математического описания граничных условий на поверхностях твердых тел, не занятых источниками и стоками теплоты.
Разрабатывают структурную схему теплообмена, в которой в качестве отдельных компонентов фигурируют твердые тела, участвующие в технологической системе или подсистеме. Для каждого компонента схемы показывают источники и стоки теплоты как действующие фактически, так и итоговые, имитирующие теплообмен между соприкасающимися телами.
Кодируют тепловые задачи для каждого из твердых тел, входящих в структурную схему теплообмена.
В соответствии с кодом тепловой задачи устанавливают вид теоретических расчетных формул и поправок к ним, полученных экспериментальным путем. По этим формулам составляют расчетные выражения для определения средней температуры на каждой из контактных площадок каждого из твердых тел.
Решают совместно выражения для определения средних температур на контактных площадках соприкасающихся тел и таким путем рассчитывают плотности итоговых потоков теплообмена между твердыми телами, входящими в технологическую систему.
Окончательно формулируют математически закономерности, отвечающие целям теплофизического анализа (распределение температур, средняя или наибольшая температура).
10. Разрабатывают предложения по оптимизации процессов и конструкций в технологической системе, вытекающие из теплофизического анализа.
Таким образом, электрохимическая коррозия на неоднородной (гетерогенной) поверхности металла аналогична работе короткозамкнутого гальванического элемента.
При замыкании в электролите двух обратимых электродов с разными потенциалами [(Va)o6p и (VК)o6p] происходит перетекание электронов от более отрицательного электрода (анода) к менее отрицательному (или более положительному) электроду (катоду). Это перетекание электронов выравнивает значения потенциалов замкнутых электродов. Если бы при этом электродные процессы (анодный на аноде и катодный на катоде) не протекали, потенциалы электродов сравнялись бы и наступила полная поляризация. В действительности анодный и катодный электродные процессы продолжаются, препятствуя наступлению полной поляризации вследствие перетекания электронов с анода к катоду, т. е. действуют деполяризующие. Отсюда, в частности, происходит и название ионов имолекул раствора, обеспечивающих протекание катодного процесса - деполяризаторы. Однако из-за отставания электродных процессов от перетока электронов в гальваническом элементе потенциалы электродов изменяются (сближаются) и короткозамкнутая система, в конечном итоге, полностью заполяризовывается.
Особенности электрохимического процесса:
1) подразделение его на два одновременно протекающих, но в значительной степени независимых электродных процессов: анодный и катодный;
2) зависимость кинетики этих двух электрохимических процессов, а следовательно, и скорости коррозии в соответствии с законами электрохимической кинетики от величины электродного потенциала металла: смещение потенциала металла в положительную сторону (например, в результате поляризации от внешнего источника тока) обычно облегчает анодный процесс и затрудняет катодный; смещение потенциала в отрицательную сторону, наоборот, ускоряет катодный процесс и тормозит анодный;
3) возможность локализации электродных процессов на различных участках поверхности металла, где их протекание облегчено;
4) при локализации электродных процессов реализация материального эффекта (растворения металла) преимущественно на анодных участках поверхности металла.
Рассмотренные электростатические представления о механизмах растворения металла, позволяют качественно объяснить механизмы растворения, а также с учетом этого моделировать режимы обработки, состав электролита.
Литература
1. Жук Н.П. Курс теории коррозии и защиты металлов/ Н.П. Жук. М.: Металлургия, 1976. 474 с.
2. Фрумкин А.Н. Избранные труды: Электродные процессы/ А.Н. Фрумкин. М.: Наука, 1987. 336 c.
3. Скорчеллетти В.В. Теоретическая электрохимия/ В.В. Скорчеллетти. Л.: Госхимиздат, 1963. 608 с.
Воронежский государственный технический университет
УДК 621.9.047.7
В.П. Горшунова, Б.А. Спиридонов
МЕТОДЫ СИНТЕЗА НАНОСТРУКТУРИРОВАННОГО
ОКСИДА ТИТАНА
Рассмотрены условия синтеза нанопористого оксида титана и его некоторые свойства. Представлен возможный механизм протекания химических реакций при анодировании титана. Показаны перспективы применения нанопористого оксида титана в технике
В настоящее время большое внимание исследователей привлечено к изучению свойств пористых оксидных пленок, находящих все более широкое применение в качестве функциональных материалов. Интерес, проявляемый к исследованию пористых пленок на основе оксида титана, связан с его уникальными физическими и химическими свойствами. Это – уникальная смачиваемость, сенсорные и оптические свойства, биологическая совместимость. Кроме того, оксид титана обладает высокой фотокаталитической активностью, позволяющей реализовать процессы очистки поверхностей, воды и воздуха от загрязнений, в результате чего образуются нетоксичные продукты [1]. Для получения тонких оксидных пленок используются самые различные методы: нанесение из растворов (dip-coating и spin-coating), электрофорез, осаждение из газовой фазы. Однако наиболее интересной микроструктурой обладают пленки оксида титана, полученные путем анодного окисления металлического титана во фторсодержащем электролите.
Впервые пленки оксида титана методом анодного окисления были синтезированы в 1999 году профессором Звилингом [2]. Такие пленки состоят из нанотрубок оксида титана, ориентированных перпендикулярно металлической подложке. При этом внутренний и внешний диаметр нанотрубок можно варьировать в пределах нескольких десятков нанометров в зависимости от условий окисления. Несомненными достоинствами данного типа структур является открытая пористость и достаточно узкое распределение пор по размерам. Кроме того, при определенных условиях анодирования можно добиться формирования высокоупорядоченной плотной упаковки нанотрубок с достаточно большой толщиной пленки (> 10), что позволяет использовать пленки пористого TiO2 в качестве газоселективных мембран и носителей для катализаторов.
По мере изучения процесса электрохимического окисления титана с целью получения нанотрубок TiO2 удалось увеличить толщину оксидных пленок. Этого достигли за счет контроля рН в течение всего процесса окисления. Для контроля рН в электролит добавляли сульфатный или фосфатный буферный раствор [3]. Кроме того, чтобы снизить локальные флуктуации рН, можно использовать вязкий электролит, добавив, например, глицерин. В результате этого удалось вырастить пленки толщиной до 7 мкм, состоящие из трубок с гладкими стенками диаметром 65 нм [4]. В работе [5] представлены результаты синтеза и исследования свойств пленок пористого TiO2, полученных анодным окислением. Анодное окисление титана проводили в 0,5 %-ном растворе NH4F в глицерине, а также в растворе NH4F в глицерине с добавлением 0,5 % додецилсульфата натрия. Процесс электрохимического окисления состоял из двух стадий: линейного роста напряжения со скоростью 0,2 В /с до постоянного значения и окисления в течение 15 ч при постоянном напряжении, которое варьировалось в пределах от 10 до 30 В.
Отделение пленки оксида титана от подложки проводили путем растворения металлического титана в растворе брома в метаноле (1 мл Br2 на 10 мл СН3ОН). Термическую модификацию проводили путем отжига оксидной пленки на воздухе при температуре 500 оС в течение 3 ч, скорость нагрева и охлаждения 1 оС / мин.
Для исследования пористой структуры оксида титана использовался метод малоуглового рассеяния нейтронов (МУРН, нейтронный реактор FRG-1 Геестахт, Германия). Пучок рассеянных нейтронов (длина волны λ = 0,58 нм, Δλ/λ = 0,1, отклонение 1,5ּ10-3 радиан) регистрировали с помощью координатного детектора с разрешением 256х256 точек. В данном случае этот метод является уникальным инструментом для исследования упорядочения пор в структуре пленок, так как для них характерен параметр повторяемости (межплоскостное расстояние) более 10 нм. Данный метод исследования обладает и тем преимуществом, что несет информацию сразу о большом участке образца, то есть характеризует его в целом, в то время как растровая электронная микроскопия позволяет наблюдать лишь локальную структуру поверхности. Кроме того, образцы были исследованы методами растровой электронной микроскопии (микроскоп Leo Supra 50VP, напряжение на ускоряющем электроде 1-30 кВ; увеличение - от х1000 до х 4000000, (микроскоп Leo 912 AB Omega, напряжение на ускоряющем электроде 120 кВ, образцы диспергировали в водном растворе щавелевой кислоты (0,3 моль/л) с помощью ультразвука, а затем наносили на медные сеточки с пористым углеродным покрытием и высушивали на воздухе), рентгенофазового анализа (дифрактометр ДРОН-3М, шаг сканирования по 2Θ 0,1-0,01о, время накопления сигнала 1 - 2 с на СоКα-излучении (λср.= 1,78897 Ǻ); идентификацию проводили с использованием картотеки JSPDS) и термогравиметрического анализа (термоаналитическая система Diamond Pyris (Perkin Elmer). Для проведения эксперимента использовали платиновые тигли. Навески образцов составляли 1-1,5 мг при точности непрерывного взвешивания 0,1 мг; скорость нагрева составляла 1о/мин. Перед проведением анализов были отсняты базовые линии ТГ и ДТА. Для этого вместо образца в тигель помещали 2 мг прокаленного при 1500 оС оксида алюминия.
Установлено, что образцы с потенциалом окисления ниже 20 В обладают тетрагональной упорядоченностью пористой структуры. Этот факт можно объяснить тем, что при низких потенциалах окисления дисперсия среднего радиуса пор достаточно высока. В результате плотная гексагональная упаковка реализуется труднее, и более предпочтительной становится тетрагональная упаковка пор, которая является менее плотной. Кроме того, пленки, синтезированные при напряжении, меньшем 20 В, обладают сильно дефектной структурой.
Образцы, окисленные при напряжении 20 В, и образец, окисленный при напряжении 20 В с добавлением в электролит додецилсульфата натрия, по данным МУРН обладают гексагональной упорядоченной системой пор. Показано, что с увеличением напряжения анодного окисления увеличивается параметр а гексагональной структуры. Этот факт объясняется тем, что при увеличении напряжения в поре увеличивается локальное значение рН, и следовательно, увеличивается скорость растворения TiO2. Таким образом, при увеличении напряжения растет внутренний радиус поры. Толщина стенки поры равна удвоенной толщине барьерного слоя, а толщина барьерного слоя увеличивается с ростом напряжения, так как увеличивается скорость роста оксидной пленки за счет увеличения скорости диффузии иона О2-. При этом скорость химического растворения аморфного оксида титана с образованием [TiF6]2- остается постоянной. Таким образом, при росте напряжения увеличивается толщина нанотрубок TiO2.
Синтезированные пленки были исследованы также методом растровой электронной микроскопии (РЭМ). По данным РЭМ толщина пленки практически не зависит от времени, в течение которого проводилось окисление. Слабое влияние времени окисления на толщину пленки можно объяснить сравнительно высокой скоростью химического растворения оксида титана в плавиковой кислоте. Обобщение данных РЭМ было использовано для расчета внутреннего диаметра и расстояния между центрами пор пленок пористого оксида титана. Расстояния между центрами пор, рассчитанные по данным РЭМ, хорошо согласуются с расстояниями между центрами пор, полученными по данным МУРН. Из данных РЭМ не удалось вычислить внутренний диаметр пор для пленок, полученных при напряжениях менее 20 В. На микрофотографиях видно, что нанотрубки закрыты сверху. Это связано с тем, что в электролите существует равновесие растворение-осаждение оксида титана, а в поре наблюдается градиент рН: чем ближе к барьерному слою, тем рН меньше. Таким образом, за счет локального изменения рН комплекс [TiF6]2-, образованный на нижней поверхности поры, может распадаться при выходе из поры с осаждением гидратитрованного аморфного оксида титана. Кроме того, так как оксид титана имеет большую атомную плотность, чем металлический титан, в пленке возникают механические напряжения. При малых радиусах пор механические напряжения могут приводить к сжатию трубки и закрытию одного из ее концов. При высоких напряжениях скорость генерации ионов Н+ достаточно высокая, и, следовательно, ионы достаточно быстро покидают пору и по всей длине поры рН будет достаточно низким, поэтому при выходе из поры комплекс [TiF6]2- не разрушается.
Данные об упорядоченности структуры, полученные, полученные методом МУРН, согласуются с данными РЭМ. На микрофотографиях поверхности металла после отделения пленки видны области тетрагонального упорядочения для образцов, окисленных при напряжениях менее 20 В, и области гексагонального упорядочения для пленок окисленных при напряжении больше 20 В.
Данные РЭМ свидетельствуют о том, что добавление к раствору электролита поверхностно-активного вещества не изменяет внутреннего диаметра пор, а изменяет толщину стенок между порами. Возможным объяснением такого эффекта является изменение кинетической и диффузионной подвижности иона титана и кислорода в процессе анодного окисления металлического титана. Очевидно, что толщина стенки между двумя формирующимися порами равна удвоенной толщине барьерного слоя, которая определяется диффузионными длинами О2- и Ti4+. С геометрической точки зрения кратчайшим расстоянием между жидкой фазой и металлическим титаном является расстояние между двумя сферическими поверхностями, причем радиус внешней сферы равен половине расстояния между центрами пор, а радиус внутренней сферы равен внутреннему радиусу поры. Тогда ионы Ti4+ переходят в раствор только со сферической поверхности, которая является дном поры, а на боковой поверхности поры происходит только химическое растворение оксида титана, скорость которого существенно ниже скорости электрохимического растворения титана. В свою очередь процесс электрохимического растворения титана включает стадии диффузии ионов О2- и растворения Ti4+ со дна поры. Толщина барьерного слоя определяется выравниванием скоростей образования пленки (скорость диффузии ионов кислорода через оксидный слой) и ее растворения.
Скорость растворения пленки с переходом в раствор ионов Ti4+, очевидно, зависит активности TiO2, которая уменьшается при добавлении к электролиту поверхностно-активного вещества, координирующего атомы на внешней поверхности пленки так как скорость диффузии ионов кислорода при этом не уменьшается, следовательно, происходит увеличение толщины барьерного слоя. Скорость растворения титана внутри поры определяется локальным рН среды (скоростью генерации катионов Н+), которая, в свою очередь , зависит от напряжения, при котором проводится окисление. Действительно, внутренний диаметр пор оксида титана зависит от напряжения анодирования и не зависит от добавления ПАВ.
Данные просвечивающей электронной микроскопии хорошо согласуются с данными РЭМ и МУРН. На микрофотографии показаны нанотрубки, полученные при 30 В и имеющие внешний диаметр 100 нм. Нанотрубки имеют гофрированные стенки и закрыты с одной стороны (барьерный слой). Картина дифракции электронов носит кольцевой характер, что может соответствовать нанокристаллическому строению стенок трубки. Наиболее сильный рефлекс соответствует стопроцентной линии (200) оксида титана TiO. Другие рефлексы, присутствующие на дифрактограмме, имеют малую интенсивность и могут быть отнесены к фазам Ti3O5 и Ti2O3. Таким образом, при анодном окислении образуется аморфный оксид титана, а также оксидные фазы, где титан имеет формальную степень окисления меньше +4.
В данной работе была проведена термическая модификация синтезированных пленок оксида титана. Данные рентгенофазового анализа для образца (U=20 В), отожженного при 500 оС, свидетельствуют о наличии кристаллического анатаза, в то время как, неотожженный оксид титана является рентгеноаморфным. По данным РЭМ упорядоченная структура пористого оксида титана при отжиге сохраняется. Кроме того, был проведен термический анализ пленки TiO2, отделенной от металлической подложки. По данным ТГА при отжиге образца сначала происходит удаление из структуры связанной воды и, возможно, некоторого количества глицерина, находящегося в порах, а затем, предположительно, кристаллизация оксида титана в форме анатаза, начинающаяся при температуре около 400 оС.
Кроме того, в работе были синтезированы пористые пленки оксида титана. По данной растровой электронной микроскопии (РЭМ) толщина пленок составила 1,5 - 2,5 мкм, внутренний диаметр от 40 до 100 нм. По данным, полученным методом МУРН, была идентифицирована структура, в которой упорядочиваются поры. Образцы, окисленные при напряжениях менее 25 В без ПАВ, обладают тетрагональной структурой упорядочения пор, образцы, окисленные при напряжениях 25 и более вольт – гексагональной. Показано, что внутренний диаметр пор оксида титана определяется напряжением анодирования и не зависит от состава электролита или добавления к электролиту ПАВ, в то время как роль ПАВ сводится к увеличению толщины барьерного слоя вследствие ограничения диффузии и растворения компонентов.
Более широко методы синтеза и исследование свойств анодных пленок оксида титана представлены в работе [6].
В качестве исходного материала для синтеза пленок пористого оксида титана была использована титановая фольга (толщина 0,25 мм, 99 %) и высокочистый титан (Goodfellow, 99,99%). Перед окислением металлические пластинки были отполированы до зеркального блеска. На первом этапе синтез анодированного оксида титана осуществляли по методике, описанной в работе [4]. Анодное окисление проводили в двухэлектродной электрохимической ячейке с использованием источника постоянного тока Б5-50, вспомогательным электродом служила платиновая проволока, а рабочим электродом – титановая пластинка. Окисление проводили в 0,5 % (по массе) растворе NH4F (х.ч.) в глицерине, содержащем 0,5 % додецилсульфата натрия (С12Н25ОSO3Na, х.ч.) Процесс электрохимического окисления состоял из двух стадий: линейного роста напряжения со скоростью 0,2 В/с до постоянного значения и окисления в течение требуемого времени при постоянном напряжении.
Пленки пористого оксида титана, синтезированные в глицериновом электролите, были исследованы методом МУРН. По данным этого метода удалось определить локальное упорядочение нанотрубок и среднее расстояние между их центрами (параметр d). Вывод о пространственной упорядоченности был сделан на основании того, что в спектре рассеяния нейтронов наблюдается два пика, предположительно они соответствуют параметрам d10 и d11 двухмерной структуры. На основании соотношения между параметрами d10 и d11,равном отношению d10/d11 ,был сделан вывод о локальном упорядочении нанотрубок.
Образцы с потенциалом окисления ниже 20 В обладают локальным тетрагональным упорядочением нанотрубок , так как соотношение рефлексов d10/d11 ≈1,5 (близко к√2), что характерно для тетрагональной структуры. Факт тетрагонального упорядочения можно объяснить тем, что при низких потенциалах окисления высока дисперсия среднего радиуса пор. В результате плотная гексагональная упаковка реализуется труднее, и более предпочтительной становится тетрагональная упаковка нанотрубок. Образцы, окисленные при напряжении выше 20 В, и образец окисленный при напряжении 20 В с добавлением додецилсульфата натрия в качестве ПАВ, обладают локальным гексагональным упорядочением нанотрубок.
Использование метода МУРН не позволило определить параметры структуры для образца, окисленного при напряжении 10 В, что связано с тем, что данный образец обладает малой толщиной и, следовательно, интенсивность брегговского рассяния лежит в пределах ошибки.
По данным метода растровой электронной микроскопии (РЭМ) толщина синтезированных пленок слабо зависит от времени, в течение которого проводилось окисление, но сильно зависит от напряжения, при котором проводилось окисление. Данный факт связан с высокой скоростью растворения оксида титана в плавиковой кислоте, которая образуется в результате электролиза.
Расстояние между центрами пор, рассчитанные по данным РЭМ, хорошо согласуются с данными, полученными методом МУРН. Из данных РЭМ не удалось вычислить внутренний диаметр для пленок, полученных при напряжениях менее 20 В. На микрофотографии видно, что нанотрубки закрыты сверху. Это связано с тем, что в электролите существует равновесие растворение- осаждение оксида титана, а поре наблюдается градиент рН: чем ближе к барьерному слою, тем рН меньше. Таким образом, за счет локального изменения рН комплекс [TiF6]2-, образованный на нижней поверхности поры может распадаться при переходе из поры с осаждением аморфного гидратированного оксида титана. Кроме того, оксид титана имеет большую атомную плотность, чем металлический титан, поэтому в пленке возникают механические напряжения. При малых радиусах пор механические напряжения могут привести к сжатию трубки и закрытию одного из ее концов. При высоких напряжениях скорость генерации Н+ достаточно высока, и, следовательно, ионы достаточно быстро покидают пору и по всей длине поры рН является достаточно низким, и следовательно, при выходе из поры комплекс не разрушается. По данным РЭМ и МУРН наблюдается линейная зависимость внутреннего и внешнего диаметра от используемого напряжения, ранее обнаруженная для анодированного алюминия [7, 8 ,9]
В настоящей работе приведены данные просвечивающей электронной микроскопии, которые хорошо согласуются с данными РЭМ и МУРН. Картина электронной дифракции носит кольцевой характер, что соответствует нанокристаллическому строению стенок нанотрубок. Данные электронной дифракции свидетельствуют о наличии фаз анатаза и рутила в стенках нанотрубок, а также о наличии оксидных фаз с формальной степенью окисления титана меньше + 4, таких как
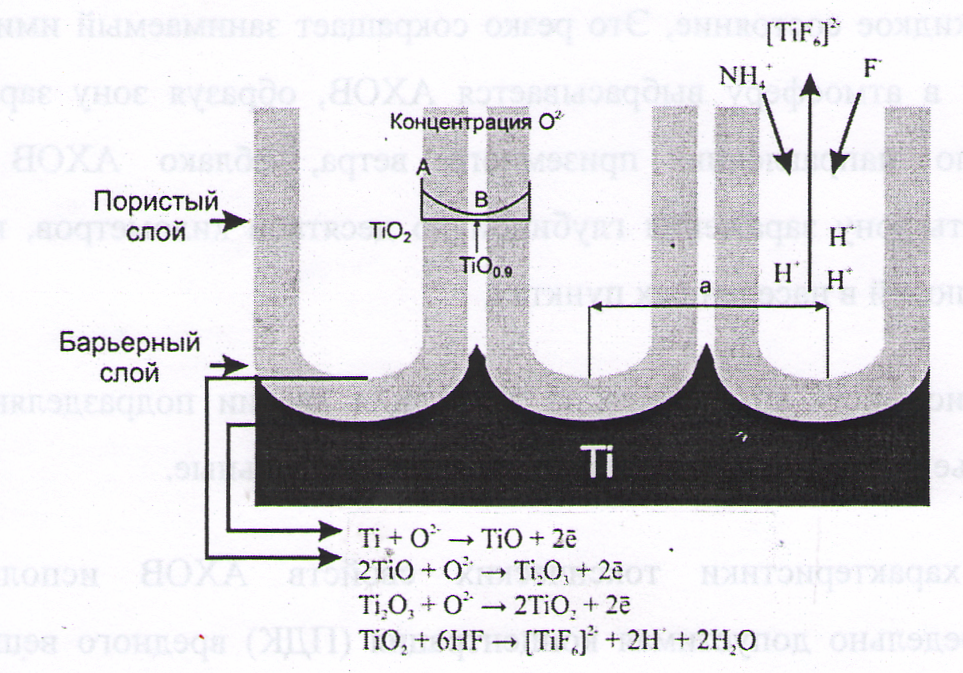
Рис. 1. Схематическое изображение процессов, происходящих при анодном окислении Ti во фторсодержащем электролите
TiO и Ti2O3, в то время как по данным HAF пористая пленка является аморфной. Ранее присутствие нанокристаллических фаз было обнаружено в анодированном оксиде алюминия [10].
Наличие данных фаз позволяет предположить, что процесс образования нанотрубок включает несколько стадий с последовательным окислением металлического титана до TiO2 через промежуточные оксидные фазы:
Ti + O2- - 2ē → TiO
2TiO + O2- - 2ē → Ti2O3
Ti2O3 + O2- - 2ē → 2 TiO2
Данное предположение позволяет объяснить образование структуры, состоящей из нанотрубок TiO2, а не образование плотной пленки с порами (структуры, характерной для анодированного оксида алюминия). При анодировании концентрация ионов O2- падает от точки А к точке В (рис.1) вследствие уменьшения напряженности электрического поля. Таким образом, в точке В вследствие недостатка ионов О2- образуется оксид титана со степенью окисления меньше, чем +4, который легче растворяется в электролите. Растворение данных оксидных фаз между стенками трубок и приводит к формированию структуры, состоящей из нанотрубок.
Так как структура синтезированных пленок содержит достаточно большое количество дефектов, авторы предположили, что образцы будут обладать достаточно хорошими сенсорными свойствами. Для того, чтобы образцы обладали хорошими сенсорными свойствами, необходимо провести их термическую модификацию. Неотожженные образцы не будут обладать сенсорными свойствами вследствие того, что содержат в своей структуре достаточно большое количество связанной воды и размер кристаллитов анатаза достаточно мал. Для измерения сенсорных свойств был проведен отжиг образцов на воздухе при температуре 500 оС в течение 3 часов. На рентгенограмме отожженного образца появляются рефлексы, соответствующие кристаллической модификации анатаза, в то время как неотожженные пленки являются рентгеноаморфными. По данным ТГА при отжиге синтезированного образца на первой стадии происходит удаление из структуры химически связанной воды, затем, предположительно, разрушение титановых кислот, и после этого происходит кристаллизация оксида титана в форме анатаза при 350 оС. По данным растровой электронной микроскопии при отжиге не происходит разрушения упорядоченной пористой структуры.
Принцип действия сенсоров на основе полупроводников n-типа, к которым относится TiO2, основан на изменении электропроводности оксидных пленок в результате каталитических реакций на поверхности пленки с донорными газами D (СО, Н2, СН4) при температурах 500 – 700К. Увеличение электропроводности в полупроводниковых сенсорах происходит за счет уменьшения толщины обедненного электронами приповерхностного запирающего слоя вследствие уменьшения величины поверхностного потенциала φs. Поверхностный барьер (φs) в оксидных полупроводниках n-типа обусловлен отрицательным заряжением поверхности пленки хемосорбированным кислородом в формах О2- и О-. Уменьшение φs происходит в результате осуществления на поверхности пленки каталитических реакций типа: D + О- → DO + e, где DO – продукт каталитической реакции [11].
В качестве модельной среды для измерения сенсорных свойств отожженных образцов была использована смесь воздуха с водородом (содержание водорода 1000 ррm) при 300 оС. Оказалось, что наилучшими сенсорными свойствами обладает пленка TiO2, полученная анодированием титана при 20 В с толщиной 1,5 мкм. Однако, после двух циклов смены зазовой среды сенсорный отклик падает, что может быть объяснено неполной десорбцией водорода из пор.
На втором этапе работы авторами была предпринята попытка увеличить толщину пленок пористого TiO2. Пленки, синтезированные в глицериновом электролите, не подходят для создания газоселективных мембран, так как имеют малую толщину (до 3 мкм). Для того, чтобы увеличить толщину пленок, в качестве электролита был использован раствор NH4F (0,25 %) в этиленгликоле при 20 оС с постоянным перемешиванием на магнитной мешалке. Процесс электрохимического окисления состоял из двух стадий: линейный рост напряжения со скоростью 1 В / с до постоянного значения и окисление в течение определенного времени при постоянном напряжении.
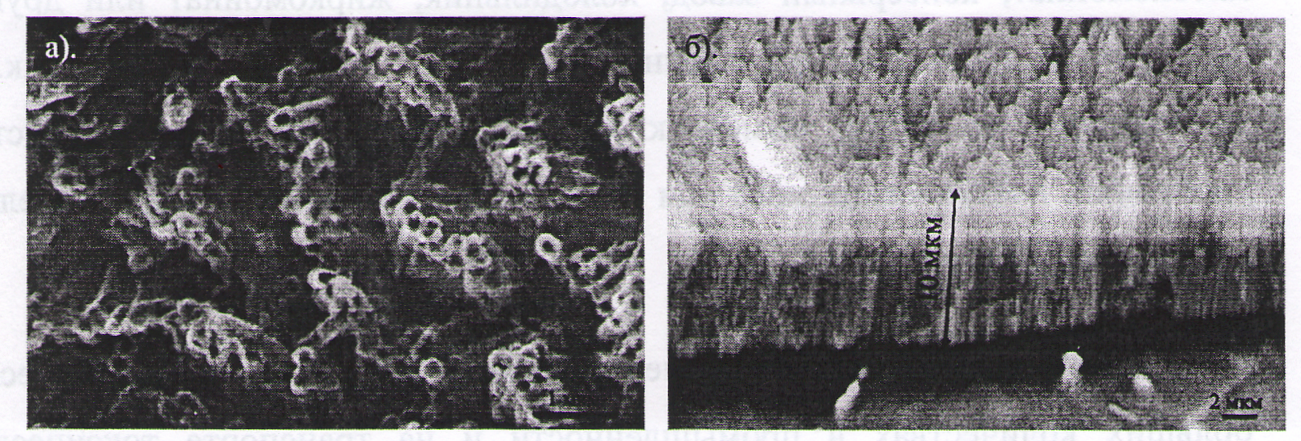
Рис. 2. Образец оксида титана (60 B), синтезированный в этиленгликольном электролите; верхняя сторона пленки (а), скол пленки (б)
По данным РЭМ (рис.2) образец, окисленный при напряжении 60 В в течение 15 часов, обладает толщиной около10 мкм. Образец обладает открытой пористостью, хотя верхние концы нанотрубок слипаются и структура является неупорядоченной, что подтверждается данными МУРН. Предположительно неупорядоченность структуры связана с тем, что для синтеза был использован технический титан.
Для увеличения упорядоченности структуры и увеличения однородности распределения пор по размерам авторами решено было использовать высокочистый титан и метод двухстадийного окисления. Суть данного метода заключается в том, что в результате первого окисления на границе раздела оксид-металл формируется упорядоченная структура углублений, затем оксидный слой растворяется и структурированная металлическая поверхность окисляется еще раз. Для того, чтобы отделить оксидную пленку от металлического титана после первого окисления была использована ультразвуковая обработка в водном растворе 0,3 М щавелевой кислоты.
По данным МУРН синтезированные образцы обладают гексагональной упорядоченной системой пор. Данные о наличии гексагонального упорядочения в пленках подтверждается методом растровой электронной микроскопии. На микрофотографии верхней стороны пленки видно, что образец обладает доменной структурой с гексагональным упорядочением пор (рис. 3). Ранее подобная доменная структура была обнаружена на пленках анодированного оксида алюминия, однако размер доменов в пленках оксида алюминия больше, чем в пленках оксида титана.
В работе также была исследована зависимость параметров структуры синтезированных пленок от напряжения (рис.3). По данным МУРН и РЭМ внутренний диаметр и расстояние между центрами пор линейно зависит от используемого напряжения (kin=1nm/V; kext = 2,2 nm/V).
Образование гладкой пленки можно объяснить тем, что при ультразвуковой обработке в щавелевой кислоте происходит предварительное окисление металлического титана, с образованием тонкого слоя плотной оксидной пленки. Данная оксидная пленка предохраняет от быстрого растворения оксидной фазы с формальной степенью окисления с формальной степенью окисления меньше, чем +4, что приводит к образованию структуры, похожей на анодированный оксид алюминия (плотная пленка с порами), а не образованию структуры, состоящей из нанотрубок. Данный тип структуры позволяет создать на основе пленок пористого оксида титана газоселективные мембраны.
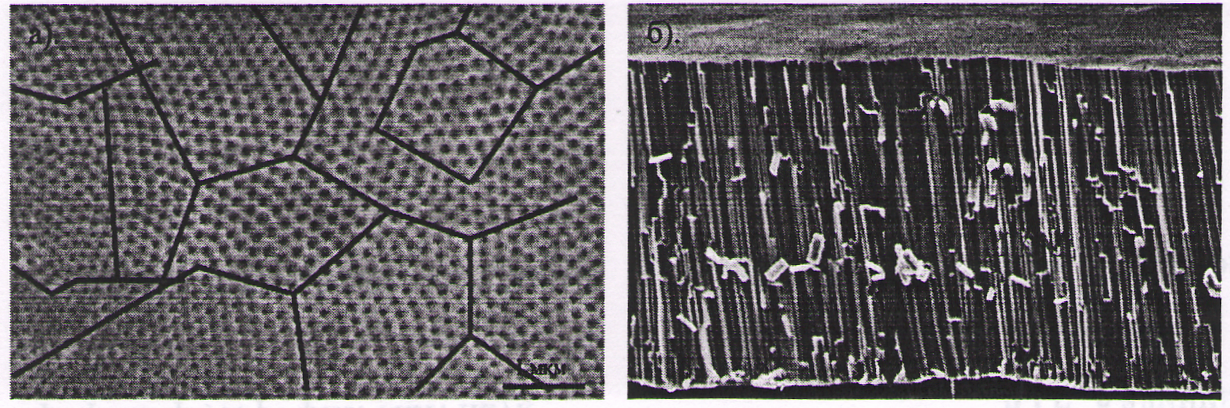
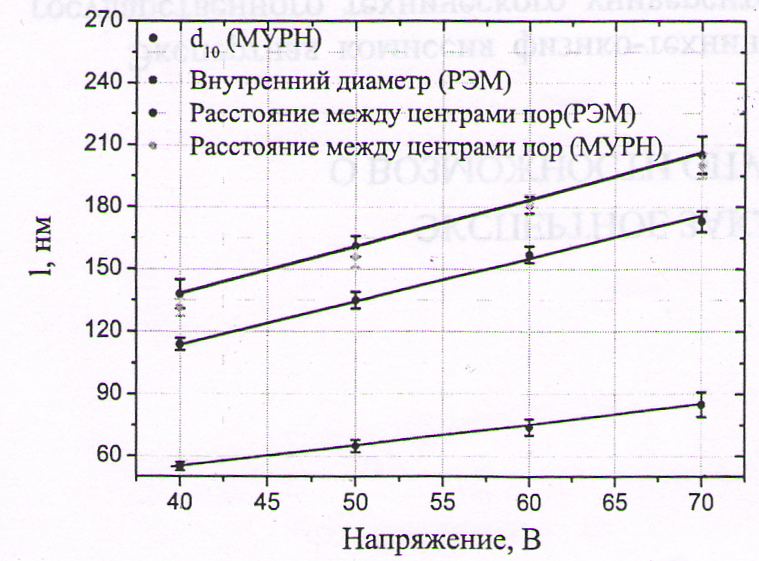
Рис. 3. Зависимость параметров структуры синтезированного пористого оксида титана от напряжения
На основе анализа результатов исследований данной работы можно сделать следующие выводы:
1. Использование метода МУРН для исследуемых пленок позволяет установить параметры структуры и локальное упорядочение нанотрубок в пленках.
2. По данным методов МУРН и РЭМ внутренний диаметр пор линейно зависит от напряжения: k = 2,3 нм/В (электролит – глицерин); k = 1 нм/В (электролит –этиленгликоль). Внешний диаметр пор также линейно зависит от напряжения: k = 4,2 нм/В и k = 2,2 нм/В (для этиленгликоля и глицерина соответственно).
3. По данным электронной дифракции синтезированный неотожженный образец пористого TiO2 содержит нанокристаллические фазы анатаза и рутила, а также фазы со степенью окисления титана меньше,чем +4, такие как Ti2O3 и TiO (по данным HAF образец является рентгеноаморфным). После отжига при 500 оС на рентгенограмме появляются рефлексы, соответствующие анатазу.
Литература
1. Masao Kaneko, Ichiro Okuro. Photocatatalysis. Springer. Kodansha 2002.
2. Zwilling М., Darque-Ceretty E., Anodic oxidation of titanium and TAGV alloy in chromic media. An electrochemical approach // Electrochim.Acta. 1999. № 44.Р. 921.
3. Ghicov A., Tsuchiya H., Masak J.M., Schmuki P. Titanium oxide nanotubes prepared in phosphate electrolytes // Electrochem. Comm. 2005. № 7. Р. 505-509.
4. Masak J.M., Tsuchiya H., Taveriya L. et al. Smooth Anodic TiO2 Nanotubes // Angew. Chem. Int. Ed. 2005. № 44. Р. 1-4.
5. Д.И. Петухов, И.В. Колесник, А.А. Елисеев, А.В. Лукашин, Ю.Д. Третьяков. Синтез и исследование свойств пленок пористого TiO2, полученных анодным окислением. Международный научный журнал «Альтернативная энергетика и экология» AЭЭ. № 1 (45) (2007).
6. Д.И. Петухов. Синтез и исследование свойств пленок пористого TiO2. Реферат на премию им. Н.Н. Олейникова. МГУ, Москва. 2007.
7. Shingubara S.Journal of Nanoparticle Research. 5 (2003) 17-30.
8. Masuda H., Hasegwa F., Ono S. Journal of the Electrochemical Sosiety. 144 (1997) L 127-L 130.
9. Masuda H., Yada K., Osaka A. Japanese Journal of Ahhlied Physics Part 2-Le. Letters. 37 (1998) L1340-L1342.
10. J. P. O’Suliva, G. C. Wood, Proceedings of the Royal Sosiety of London Series A – Mathematical and Physical Sciences, 317 (1970) 511 – 543.
11. Электронный журнал «Исследования в России», http://zhurnal.ape.relam.ru/articles/2004/179.html
Воронежский государственный технический университет
УДК 656.71.002.5
Ю.Ю. Тапилкин, А.Н. Корнеева, В.В. Корнеева
Современные антигололёдные средства
В статье рассмотрены современные антигололёдные средства, а также их экологичность и безопасность применения
Применение современных антигололедных средств на дорогах и тротуарах улиц городов существенно облегчает движение транспортных средств и пешеходов, но мы не задумываемся о том, какой состав и какой вред приносят вместе с пользой эти средства.
Все применяемые современные противогололедные средства должны удовлетворять следующим основным требованиям:
-снижать точку замерзания воды при отрицательных температурах;
- быстро взаимодействовать и плавить снежно-ледяные отложения;
- не повышать скользкость дорожного покрытия до опасных значений;
- не вызывать вредного воздействия на дорожные покрытия;
-не угнетать, зеленые насаждения;
- не оказывать отрицательного влияния на металл, резину и кожу;
- быть безвредными для здоровья человека и экологии.
Самый главный показатель безопасности того или иного вещества определяется его концентрацией, где бы это вещество ни находилось: в воде, в воздухе или на почве. Если говорить о антигололедных реагентах, то необходимо четко определить токсичность каждого из них, установить, где какие можно использовать.
Антигололедные средства и противолёдные реагенты имеют как свои плюсы, так и минусы. По своей сути – название «антигололедный реагент» свидетельствует о том, что вещество вступает в реакцию с окружающей средой т.е. ледяным покровом.В отличие от своих предшественников (соли, песка и др.), нынешние антигололедные реагенты действуют более изощренно: они постепенно плавят лед, превращая его в воду, вернее сказать в раствор реагента в воде. Этот раствор впоследствии замерзает при более низких температурах, чем простая вода, то есть антигололедные реагенты не только устраняют лед, но и частично препятствуют его появлению в дальнейшем [1]. Подобный химический процесс также зависит от ряда факторов, как внешних – природно-температурных, так и химический. Реагенты вступают в реакции не только с обледеневшим дорожным покрытием, но и с побочными продуктами, такими, как моторные масла, пары бензина, солярки, выхлопных газов, а также технической солью, в большом количестве присутствующих на дорожном покрытии, компонентами почвы.
Антигололедные реагенты бывают жидкими и твердыми, и имеют различный состав и химические свойства. При попадании твердого антигололедного реагента на ледяную поверхность снега или льда, эти частички растворяются, образуя рассол, который имеет температуру замерзания ниже температуры замерзания воды. Именно раствор антигололедного реагента пока его концентрация такова, растапливает лед и предотвращает возникновение гололедных образований. Лучше тот антигололедный реагент, который при наиболее низкой температуре расплавит большее количество снега и льда и окажет наименьшее действие на окружающую среду и материалы.
На территории нашей страны, для борьбы со льдом, комунальные службы используют в основном следующие реагенты:
Хлористый кальций - ХККМ твердый противогололедный реагент в гранулах, упакованный в мешки по 25 кг. Используется для посыпки дорог от льда и снега в зимнее время года.
Айсмелт - ХКНМ - твердый противогололедный реагент хлористый кальций натрий модифицированный. В мешках по 25кг. Применяется для обработки дорог и улиц, пешеходных зон и тротуаров в любом диапазоне температур до -20 °C.
Соль техническая - NaCl отпускается как россыпью, так и в мешках. Применяется в котельных, а также используется антигололедный реагент.
Песко-солевая смесь - смесь песка и технической соли - форма отпуска - россыпью и в мешках по 50 кг. Используют для посыпки дорог от льда в зимний период.
Мраморная крошка - мелкий мраморный щебень с размером зерен (фракцией) 2.5-5 мм - форма отпуска - россыпью и в мешках по 50кг. Используется в качестве антигололедного реагента в зимний период для посыпки дорог и пешеходных зон.
Гранитная крошка - мелкий гранитный щебень с размером зерен (фракцией) 2-5мм - форма отпуска - россыпью и в мешках по 50кг. Используется в качестве противогололедного реагента для обработки дорог и пешеходных тротуаров.
К наиболее общепринятым химическим антигололедным реагентам сейчас относят хлористый натрий, хлористый магний, хлористый кальций и песко-соляную смесь. Эти реагенты рассыпаются в местах потенциального скопления ледяного покрова в соответствующих пропорциях и консистенциях, процентное соотношение растворов которых дозируется в соответствии с руководством использования того или иного противоледного реагента.
В некоторых странах - в Финляндии, Нидерланды и др. подобные антигололедные реагенты давно уже заменяют более экологически чистыми продуктами, такими как гранитной или мраморной крошкой, препятствующими скольжения, однако и эти методы имеют свои недостатки, такие, как стоимость самого материала (гранитный отсев стоит значительно дороже химических противоледных реагентов), требуемых на единицу площади для таяния обледеневшего покрытия, так и недостатки механического воздействия на транспортные средства, испорченное покрытие которых несет ощутимый урон владельцам автотранспортных средств [2, 3].
Самым дешевым и эффективным средством для борьбы с гололедом является техническая соль. Правильное применение соли наносит минимальный вред. Поэтому на сегодняшний день соль является одним из главных средств в борьбе с обледенением.
Соль (хлористый натрий) имеет широкий спектр промышленного применения. Например, в нефтяной промышленности раствор соли используется для разморозки грунта: солевой раствор заливается в пробуренные скважины, который под давлением проникает в почву и способствует процессу таяния.
Каменная соль встречается в природе в виде минерала. Добыча соли и продажа соли происходит из регионов, богатых этим минералом. Рынок соли достаточно обширен, основная его доля приходится на Белоруссию, Украину, и Среднюю Азию.
Данные средства используются на проезжих частях дорог, а также – на тротуарах. В процессе их применения, в первую очередь, предотвращается гололед, а также устраняется ледовая корка.
Однако, противогололедные реагенты, как и все химические реагенты, требуют осторожности при их использовании. Например, если применять их без учета климатических особенностей региона, а также в больших – не соответствующих норме – количествах, то результат может оказаться неожиданным.
Отличным примером вышесказанного может служить соль техническая и ее использование сверх положенной нормы. В случаях неграмотного применения подобного реагента, его большое количество на проезжих частях и тротуарах способно оказать негативное воздействие, как на резину автомобилей, так и на обувь пешеходов.
Именно поэтому, соль техническая, так же, как и прочие антигололедные реагенты, должны использоваться в строгом соответствии с существующими нормами.
Начиная с зимнего периода 2001/2002 годов власти крупных городов (Москва, Санкт-Петербург и др.), а так же частные организации, стали отказываться от традиционной соли в пользу экологически безопасных и более технологичных противогололедных реагентов (ПГР) нового поколения.
Пескосоль (пескосоляная смесь) представляет собой смесь песка и соли в определенных пропорциях, чем ниже температура и чем больше слой льда, тем выше процент содержания соли в песчано-солевой смеси. Используют для посыпки дорог ото льда в зимний период. Песчано-соляную смесь обычно готовят, смешивая от 30/70 до 50/50%.
Наиболее популярными и эффективными среди них являются твердые химические комбинированные реагенты на основе хлористого кальция. Их можно использовать практически при любых погодных условиях и температурных режимах, а также во время снегопадов[4]. Их распределяют с помощью имеющейся у дорожных служб спецтехники, что позволяет обрабатывать большие территории.
Вопрос об экологической безопасности новых противогололедных реагентов был задан специалистам Департамента природопользования и охраны окружающей среды правительства Москвы. «Будем реалистами, — ответили специалисты, — абсолютно безвредных реагентов вообще не бывает. Все зависит от норм распределения». То есть, если использовать эти реагенты строго дозировано в зависимости от конкретного метеопрогноза, все будет хорошо. К сожалению, стопроцентной точностью наши метеорологи никогда не отличались.
Кроме того, учёные считают, что реакции противогололёдных реагентов всегда будут одинаковы, независимо от погоды. То есть сначала хлористый кальций превратит лед в воду, а потом пойдет гидролиз соли с образованием малорастворимого в воде осадка.
По свидетельству специалистов, после того как Московские улицы начали поливать новыми реагентами, резко увеличилось количество жалоб от астматиков, людей, страдающих атипическим дерматитом, аллергодерматозами, аллергическими заболеваниями кожи. Практически все реагенты, в которые входят соли и эфиры, в первую очередь уксусной кислоты, способны вызывать неспецифические реакции кожи, слизистых и бронхов [5].
Когда вместо привычной соли с песком стали использовать новые реагенты, участились жалобы на затрудненное дыхание, удушье, бронхоспазмы, зуд и слезотечение у больных, страдающих аллергией.
Для того чтобы дать объективную оценку всем этим сигналам, необходимы широкомасштабные исследования, которые позволили бы ответить на вопрос: насколько серьезно влияют антигололедные реагенты на здоровье человека. Земля и так перегружена различными выбросами: транспортными, промышленных предприятий, поэтому достаточно даже какого-то небольшого дополнительного фактора, чтобы здоровью людей и экологии был нанесен серьезный непоправимый ущерб.
Литература
1. Васильев А.П., Ушаков В.В. Анализ современного зарубежного опыта зимнего содержания дорог и разработка предложений по его использованию в условиях России. - М.: ФГУП «ИНФОРМАВТОДОР», 2003.
2. Борьба с зимней скользкостью на автомобильных дорогах / Г.В. Бялобжеский, М.М. Дербенева, В.И. Мазепова, Л.М. Рудаков. - М.: Транспорт, 1975.
3. Временные рекомендации по борьбе с зимней скользкостью на автомобильных дорогах Московской области,- М.: ГП РОСДОРНИИ, 1997. 31 с.
4. Васильев А.П., Ушаков В.В. Анализ современного зарубежного опыта зимнего содержания дорог и разработка предложений по его использованию в условиях России.- М.: Росавтодор,2003.- 27 с.
5. Николаева Л.Ф. Противогололедные реагенты и их влияние на природную среду .-М.: Логос, 1998.-60с.
Воронежский государственный технический университет
УДК 541.123.2
В.Н. Чиканов, Ю.Н. Шалимов
ВЗАИМОДЕЙСТВИЯ В РАСПЛАВАХ ХЛОРИДОВ
СО СТЕПЕНЬЮ ОКИСЛЕНИЯ КАТИОНОВ +1
В статье рассмотрено применение высокотемпературных и низкотемпературных хлоридов расплавов
Галогениды щелочных металлов отличаются целым рядом свойств (высокая коррозионная стойкость, жаростойкость, каталитические свойства), благодаря которым они нашли широкое применение во многих отраслях науки и техники. Применение высокотемпературных и низкотемпературных, особенно хлоридных, расплавов позволяет значительно улучшить качество обрабатываемых изделий и снизить их себестоимость. Кроме того, ионные расплавы, к которым относятся и хлориды щелочных металлов, характеризуются широким «электрохимическим окном», и являются прекрасной средой для осуществления электрохимических реакций, что обусловливает их прикладное использование в гальванотехнике, при создании источников тока и двухслойных конденсаторов. О некоторых процессах, происходящих в расплавах, можно судить, анализируя диаграммы плавкости [1-3].
В таблице 1 представлены типы хлоридных диаграмм плавкости со степенью окисления катионов 1+.
Таблица 1
Двойные диаграммы плавкости хлоридов
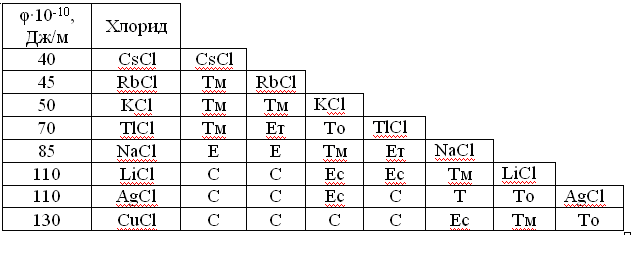
Условные обозначения: Е–диаграммы плавкости эвтектического типа близкие к идеальным; Ет–диаграммы плавкости эвтектического типа, склонные к образованию твердых растворов; Ес–диаграммы плавкости эвтектического типа с комплексообразованием в расплаве; То–диаграммы плавкости с ограниченными твердыми растворами; Тм–диаграммы плавкости с твердыми растворами и минимумом на кривой ликвидуса; Т–диаграммы плавкости с непрерывными твердыми растворами; С–диаграммы плавкости с соединениями.
Системы расположены в порядке увеличения поляризующего действия катионов (φ), которое определяли как отношение потенциала ионизации катиона (Icat) к его эффективному ионному радиусу (rcat): φ=(Icat/rcat)·10-10, Дж/м. Важными критериями, характеризующие взаимодействия в ионных расплавах (к каким и относятся расплавы рассматриваемых в настоящей работе хлоридов), являются отношения поляризующих действий катионов (φб/φм) и отношения эффективных радиусов катионов (rб/rм), где индексы «б» и «м» относятся к большим и меньшим значениям соответствующих параметров. Структурный тип кристаллических решеток, приведенных в таблице 1 хлоридов [NaCl] с координационным числом 6-6, исключение составляют TlCl – структурный тип [NaCl-деформированная] с координационным числом 6-6 и CuCl – структурный тип [ZnS-сфалерит] с координационным числом 4-4, и, как отмечалось выше, структурный тип расплавов – ионный.
Одним из важных факторов, определяющим взаимодействия расплавленных хлоридов, является параметр взаимодействия (энергия смешения), который в настоящей работе определялся как ω/RT. По его значению можно судить о процессах, происходящих в расплавах. Параметр взаимодействия рассчитывался в эвтектических точках для диаграмм плавкости эвтектического типа и с ограниченными твердыми растворами, кроме диаграмм плавкости со смещенной эвтектикой (Схлорид<7 мол.%) и в точке минимума для диаграмм плавкости с твердыми растворами с минимумом на кривой ликвидуса. В качестве отправной точки нами была взята эвтектическая диаграмма плавкости хлоридов близкая к идеальной. Для таких диаграмм плавкости параметр взаимодействия находится в интервале ±1. Таких систем всего: CsCl-NaCl и RbCl-NaCl. Рассчитанные для них параметры взаимодействия равны в первом случае ω/RTCsCl=-0,99 и ω/RTNaCl=-0,77, во втором случае ω/RTRbCl=-0,64 и ω/RTNaCl=-0,32, отношения ПДК 2,13 и 1,89, отношения радиусов катионов 1,68 и 1,52 соответственно. Максимальная энтальпия смешения этих расплавов равна ∆Нсммакс(CsCl-NaCl)=-1,000±0,01 кДж/моль, ∆Нсммакс(RbCl-NaCl)=-0,835±0,01 кДж/моль и концентрации 45-55 мол.% NaCl. Системы RbCl-TlCl и NaCl-TlCl эвтектического типа, склонные к образованию твердых растворов. Параметр взаимодействия имеет положительные значения и больше 1: ω/RTRbCl=1,15 и ω/RTTlCl=7,02, отношения ПДК и радиусов катионов 1,56 и 1,10 соответственно, и ω/RTNaCl=0,61 и ω/RTTlCl=2,34, отношения ПДК и радиусов катионов 1,21 и 1,39 соответственно. По данным [4] в системе NaCl-TlCl на основе NaCl образуются ограниченные твердые растворы 5 мол.% TlCl.
В таблице 2 представлены диаграммы плавкости хлоридов с образованием твердых растворов.
Параметр взаимодействия имеет положительные значения и больше 1. ПДК имеют небольшие значения, а их отношения не превышают 1,75, размеры катионов так же близки (rб/rм<1,70). Максимальная энтальпия смешения имеет невысокие (положительные или отрицательные) значения и находится в интервале концентраций 40-60 мол.%.
Таблица 2
Диаграммы плавкости с образованием твердых растворов

В таблице 3 приведены хлоридные диаграммы плавкости эвтектического типа, в которых отмечается комплексообразование в расплаве, о чем свидетельствуют отрицательные значения энтальпии смешения расплавов. Например,
в системе KCl-AgCl ∆Нсммакс=-2,150±0,03 кДж/моль при ссммакс=50 мол.%.
Таблица 3
Диаграммы плавкости эвтектического типа,
склонные к комплексообразованию в расплаве
Система |
ω1/RT |
ω2/RT |
φб/φм |
rб/rм |
KCl-LiCl |
-3,46 |
-3,19 |
2,20 |
1,96 |
KCl-AgCl |
-2,51 |
-2,28 |
2,20 |
1,18 |
LiCl-TlCl |
-1,20 |
0,68 |
1,57 |
2,00 |
NaCl-CuCl |
-1,80 |
-1,69 |
1,53 |
1,00 |
Параметр взаимодействия имеет отрицательное значение и меньше -1, отношение ПДК находится в интервале 1,50<φб/φм<2,20, отношение радиусов катионов 1,00≤rб/rм≤2,00. Следует так же заметить, что в аналогичных системах с участием хлорида серебра хлоридов цезия, рубидия и талия образуются соединения.
Образование соединений
В таблице 4 представлены хлоридные системы со степенью окисления катионов 1+ с образованием соединений, указан их состав, тип плавления (конгруэнтно плавящееся или инконгруэнтно плавящееся) и температура плавления (0С).
Таблица 4
Диаграммы плавкости, содержащие соединения*
Фторид |
Состав соед. |
CsCl |
RbCl |
KCl |
TlCl |
LiCl |
2:1 1:1 |
P382 P352 |
P325 |
Ес |
Ес |
AgCl |
2:1 1:1 |
D312 |
P? |
Ес |
P252 |
CuCl |
2:1 3:2 2:3 1:2 |
D300
D267 |
P254
P186 P161 |
P222 |
P204 P210 |
*Условные обозначения: D – конгруэнтно плавящееся соединение; P – инконгруэнтно плавящееся соединение; рядом с типом плавления соединения указана его температура плавления, 0С.
Для систем, в которых образуются конгруэнтно плавящиеся соединения, была проделана треангуляция и рассчитаны параметры взаимодействия (таблица 5) в эвтектических точках.
Таблица 5
Параметр взаимодействия в двойных хлоридных системах,
содержащих соединения, после их треангуляции
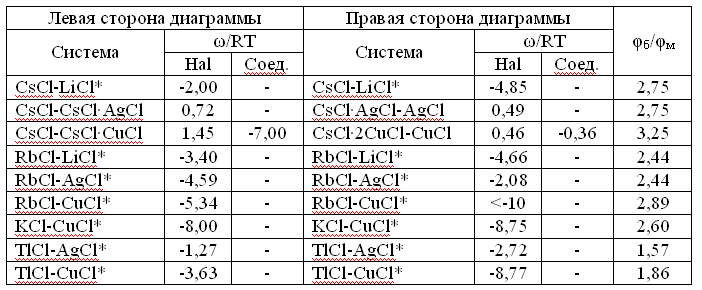
*–диаграммы плавкости с инконгруэнтно плавящимися соединениями, треангуляция не проводилась.
Таблица 6
Энтальпия смешения расплавленных хлоридов, образующих соединения
Система |
Температура расплава, К |
-∆Нсммакс, кДж/моль |
ссммакс, мол.% 2-го комп. |
CsCl-LiCl |
943 |
6,320±0,06 |
50-60 |
CsCl-AgCl |
936 |
5,530±0,05 |
50-55 |
1083 |
5,270±0,05 |
50-55 |
|
CsCl-CuCl |
936 |
10,400±0,10 |
50-60 |
1083 |
10,460±0,10 |
50-60 |
|
RbCl-LiCl |
1013 |
5,270±0,05 |
50-55 |
RbCl-AgCl |
1083 |
3,740±0,03 |
50-60 |
TlCl-AgCl |
773 |
2,320±0,02 |
40-50 |
Как видно из этой таблицы, параметр взаимодействия имеет отрицательное значение и меньше -1 (исключение составляет система CsCl-CsCl·CuCl). В других системах комплексообразовние в расплавах подтверждается значительным отрицательным отклонением кривых ликвидуса экспериментальных от идеальных. Кроме того, разница ПДК в этих системах более чем в 2,4 раза (исключение составляют диаграммы плавкости с участием TlCl). В таблице 6 приведены максимальные значения энтальпии смешения расплавленных хлоридов, их концентрация и температура расплава.
Энтальпия смешения расплавов незначительно изменяется с ростом температуры, ее максимум приходится на 50-60 мол.%. Исключение составляет система с участием таллия (TlCl-AgCl), в которой максимум несколько смещен 40-50 мол.% AgCl. Следует так же заметить, что в системах Cs(Rb)Cl-(K,Na)Cl и возможно в системе KCl-CuCl [5] образуются газообразные соединения состава 1:1.
Выводы
По отклонениям кривых ликвидуса экспериментальных от идеальных (рассчитанных по уравнению Шредера), можно делать прогнозы процессов, происходящих в расплавах хлоридов щелочных металлов, таллия (I), серебра и меди (I). В качестве такого критерия могут служить поляризующее действие катионов и параметр взаимодействия (энергия смешения), а так же отклонения кривых ликвидуса экспериментальных от идеальных (рассчитанных по уравнению Шредера). С увеличением положительных значений параметра взаимодействия наблюдается переход от эвтектических диаграмм плавкости к диаграммам плавкости, содержащих твердые растворы, а с увеличением отрицательных значений параметра взаимодействия (по абсолютной величине) к эвтектическим диаграммам плавкости с комплексообразованием в расплаве и далее к диаграммам плавкости, содержащих соединения.
литература
Применение модели регулярных растворов к взаимодействию галогенидов в расплаве / Чиканов В.Н. // Журнал неорганической химии. 2007. Т.52. №3. С.484-486.
Твердые растворы в двойных галогенидных системах с общим анионом / Чиканов В.Н. // Журнал неорганической химии. 2010. Т.55. №5. С.841-846.
Отклонения двойных фторидных эвтектических систем от идеальных / В.Н. Чиканов, Ю.Н. Шалимов // Химия, новые материалы, химические технологии. Межвузовский сборник научных трудов. ФГБОУВПО Воронежский государственный технологический университет. 2012 Вып.2. С.99-104.
Коршунов Б.Г., Сафонов В.В., Дробот Д.В. Фазовые равновесия в галогенидных системах. М.: Металлургия. 1979. 182 с.
Институт теплофизики экстремальных состояний РАН, Объединенного института высоких температур РАН. Химический факультет Московского Государственного Университета им. М.В.Ломоносова. База данных: Термические Константы Веществ. Руководители работы Иориш В.С. и Юнгман В.С.
Воронежский государственный технический университет
УДК 584.133
А. С. Кушнарёв, Б. А. Спиридонов
Возможное применение холодного ядерного синтеза
Рассмотрены принцип работы холодного ядерного синтеза, реакции и устройства, в которых возможен холодный ядерный синтез и его применение
Проблема создания альтернативных источников энергии актуальна. Холодный ядерный синтез (ХЯС) — предполагаемая возможность осуществления ядерной реакции синтеза в химических (атомно-молекулярных) системах без значительного нагрева рабочего вещества. Известные ядерные реакции синтеза проходят при температурах в миллионы кельвинов [1,2]
Экспериментальная установка камеры холодного синтеза (рис.1) состоит из палладиевых электродов, погружённых в электролит, содержащий тяжелую или сверхтяжёлую воду. Камеры для электролиза могут быть открытыми или закрытыми. В системах открытых камер газообразные продукты электролиза покидают рабочий объём, что затрудняет калькуляцию баланса полученной/затраченной энергии. В экспериментах с закрытыми камерами продукты электролиза утилизируются, например, путем каталитической рекомбинации в специальных частях системы.
Сущность синтеза заключается в том , что если два ядра дейтерия сблизить на расстояние, равное их диаметру, то в действие вступают ядерные силы и происходит ядерная реакция с выделением энергии. Ряд типов реакции может быть очень большой.
2Д+2Д --------- > 3Т+1Р+4,0 МэВ
В результате реакции получается ядро трития и протон - ядро водорода, выделяется 4 миллиона электронвольт энергии. Это почти в миллион раз больше, чем при одном акте сгорания органического топлива [1].
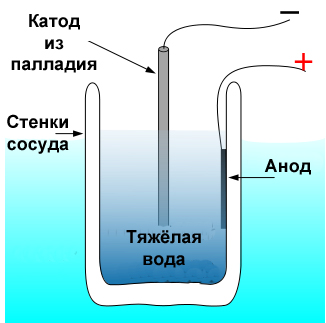
Рис. 1. Экспериментальная установка для получения ХЯС
23 марта 1989 года Университет Юты сообщил в пресс-релизе, что «двое ученых запустили самоподдерживающуюся реакцию ядерного синтеза при комнатной температуре». Президент университета Чейз Петерсон заявил, что это эпохальное достижение сравнимо лишь с овладением огнем, открытием электричества и окультуриванием растений. Законодатели штата срочно выделили $5 млн на учреждение Национального института холодного синтеза, а университет запросил у Конгресса США еще 25 млн. Так начался один из самых громких научных скандалов XX века. Печать и телевидение мгновенно разнесли новость по миру.
Ученые, сделавшие сенсационное заявление, вроде бы имели солидную репутацию и вполне заслуживали доверия. Переселившийся в США из Великобритании член Королевского общества и экс-президент Международного общества электрохимиков Мартин Флейшман обладал международной известностью, заработанной участием в открытии поверхностно-усиленного рамановского рассеяния света. Соавтор открытия Стэнли Понс возглавлял химический факультет Университета Юты.
Флейшман и Понс утверждали, что они заставили ядра дейтерия сливаться друг с другом при обычных температурах и давлениях. Их «реактор холодного синтеза» (рис. 2) представлял собой калориметр с водным раствором соли, через который пропускали электрический ток. Правда, вода была не простой, а тяжелой, D2O, катод был сделан из палладия, а в состав растворенной соли входили литий и дейтерий. Через раствор месяцами безостановочно пропускали постоянный ток, так что на аноде выделялся кислород, а на катоде — тяжелый водород. Флейшман и Понс якобы обнаружили, что температура электролита периодически возрастала на десятки градусов, а иногда и больше, хотя источник питания давал стабильную мощность. Они объяснили это поступлением внутриядерной энергии, выделяющейся при слиянии ядер дейтерия.
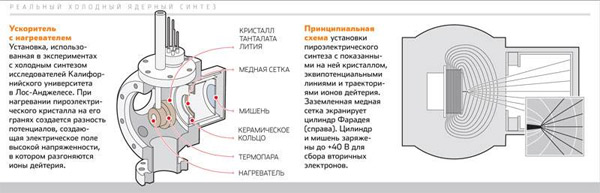
Рис. 2. Принцип работы устройства
Палладий обладает уникальной способностью к поглощению водорода. Флейшман и Понс уверовали, что внутри кристаллической решетки этого металла атомы дейтерия столь сильно сближаются, что их ядра сливаются в ядра основного изотопа гелия. Этот процесс идет с выделением энергии, которая, согласно их гипотезе, нагревала электролит. Объяснение подкупало простотой и вполне убеждало политиков, журналистов и даже химиков.
Однако некоторые физики-ядерщики и специалисты по физике плазмы считают, что два дейтрона в принципе могут дать начало ядру гелия-4 и высокоэнергичному гамма-кванту, но шансы подобного исхода крайне малы. Даже если дейтроны вступают в ядерную реакцию, она почти наверняка завершается рождением ядра трития и протона или же возникновением нейтрона и ядра гелия-3, причем вероятности этих превращений примерно одинаковы. Если внутри палладия действительно идет ядерный синтез, то он должен порождать большое число нейтронов вполне определенной энергии (около 2,45 МэВ). Их нетрудно обнаружить либо непосредственно (с помощью нейтронных детекторов), либо косвенно (поскольку при столкновении такого нейтрона с ядром тяжелого водорода должен возникнуть гамма-квант с энергией 2,22 МэВ, который опять-таки поддается регистрации). В общем, гипотезу Флейшмана и Понса можно было бы подтвердить с помощью стандартной радиометрической аппаратуры.
Однако из этого ничего не вышло. Флейшман использовал связи на родине и убедил сотрудников британского ядерного центра в Харуэлле проверить его «реактор» на предмет генерации нейтронов. Харуэлл располагал сверхчувствительными детекторами этих частиц, но они не показали ничего!
Создателями первого в мире термоядерного реактора на холодном синтезе являются профессор университета Болонии Серджио Фокарди Андреа Росси и соавтор, а также владелец уже зарегистрированного на устройство патента. В соответствии с их теорией вместо «простейшего» (но до сих не осуществимого на практике) ядерного синтеза с участием легких изотопов водорода, в реакторе происходит слияние ядер никеля и водорода. В качестве «побочных» продуктов образуется медь и излишки энергии, которая по утверждению создателей в 6 раз превосходит все энергозатраты реактора.
Согласно представленным расчетам 1кг никеля достаточно, чтобы обеспечить беспрерывную выработку 12,4 кВт в течении 14 месяцев, что собственно и позволит получать электричество по очень привлекательной себестоимости 1 цент/кВтчас.
Существует предположение, что сведения о неограниченном источнике энергии замалчивают, так как это приведет к окончанию энергетической зависимости любого из государств. Если развить технологию холодного ядерного синтеза автомобили на двигателях внутреннего сгорания и многие другие сферы человеческой деятельности связанные с сжиганием природного топлива канут в лету. Для исследований требуются вложения, но электричество для большинства людей станет практически бесплатным! Экологического кризиса можно избежать в связи с использованием ХЯС (отпадает необходимость сжигать природное топливо, абсолютно все можно перевести на электрическую энергию). Исчезнет проблема озоновой дыры, глобального потепления и огромных потерь самого ценного газа – кислорода.[3]
Литература
1. Левин А. И. Популярная механика. 2011. № 8. с.38-59.
2. http://www.membrana.ru/particle/213.
Воронежский государственный технический университет
УДК 621.892.5
К.А. Журавский, А.В. Петров, Г.Г. Тимошенко
ПЕРСПЕКТИВНЫЕ МЕТОДЫ НЕРАВНОМЕРНОГО РАСПРЕДЕЛЕНИЯ ФЕРРОМАГНИТНЫХ ПРОВОДЯЩИХ ЧАСТИЦ В РАДИОПОГЛОЩАЮЩИХ МАТЕРИАЛАХ
В статье рассматривается перспективный метод дифференцированного распределения радиопоглощающих свойств материалов по объему покрытия с целью уменьшения эффективной площади рассеяния
Развитие системы ПВО, основанная на радиоэлектронных средствах обнаружения и наведения оружия привело к необходимости разработки самолетов с низкой эффективной площадью рассеяния (ЭПР).
Важным фактором, обеспечивающим малую эффективную площадь рассеяния, является применение радиопоглощающих материалов (РМ), преобразующих энергию радиолокационного излучения в тепловую энергию в результате взаимодействия с электромагнитным излучением.
Поглощающие покрытия содержат специальные поглощающие компоненты (графит, порошки ферритов и пр.), а структура покрытий обеспечивает снижение отражений от границы раздела сред (воздух — покрытие). Различие между собственно материалами (РПМ) и покрытиями (РПП) до некоторой степени условно и предполагает, что первые входят в состав конструкции объекта, а вторые — как правило, наносятся на его поверхности. Условность разделения связана и с тем обстоятельством, что любой радиопоглощающий материал является не только материалом, но микроволновым устройством-поглотителем. Способность материала поглощать высокочастотное излучение зависит от его состава и структуры. РПМ и РПП не обеспечивают поглощения излучения любой частоты, напротив, материал определенного состава характеризуется лучшей поглощающей способностью при определенных частотах. Не существует универсального поглощающего материала, приспособленного для поглощения излучения радиолокационной станции (РЛС) во всем частотном диапазоне.
Существует, по меньшей мере три типа РПМ: резонансные, нерезонансные магнитные и нерезонансные объёмные материалы. Резонансными или частотнонастроенными РПМ обеспечивается частичная или полная нейтрализация отраженного от поверхности поглотителя излучения частью его, прошедшей по толщине материала. Эффект нейтрализации значителен при толщине поглотителя, равной одной четверти длины волны излучения. В этом случае, отраженные поверхностью поглотителя волны находятся «в противофазе».
Резонансные материалы наносятся на отражающие поверхности объекта маскировки. Толщина РПМ соответствует четверти длины волны излучения РЛС. Падающая энергия высокочастотного излучения отражается от внешней и внутренней поверхностей РПМ с образованием интерференционной картины нейтрализации исходной волны. В результате происходит подавление падающего излучения. Отклонение ожидаемой частоты излучения от расчётной приводит к ухудшению характеристик поглощения, поэтому данный тип РПМ эффективен при маскировке от излучения РЛС, работающей на стандартной, неизменяемой моночастоте.
Нерезонансные магнитные РПМ содержат частицы феррита, распределенные в эпоксидном пластике или в покрытии. Поскольку нерезонансные магнитные РПМ рассеивают энергию высокочастотного излучения по большой поверхности, результатом является тривиальное повышение ее температуры. Иными словами уменьшение ЭПР производится за счет ухудшения ИК сигнатуры объекта. Основное преимущество нерезонансных магнитных РПМ состоит в их широкополосности — эффективности поглощения излучения в широком диапазоне частот. Напротив, эффективность резонансных РПМ ограничена узким диапазоном расчётных частот излучения /3/.
Нерезонансные объёмные РПМ обычно используются в виде относительно толстых слоев, поглощающих большую часть подводимой энергии до подхода и возможного отражения волны от металлической задней пластины. Принцип работы основан на использовании как диэлектрических, так и магнитных потерь, последнее — за счет добавления соединений феррита. В некоторых случаях используется введение графита в пенополиуретановую матрицу.
Противолокационная окраска рассеивает электромагнитное излучение за счет электропроводности и ослабляет интенсивность отражения от «электромагнитных горячих точек» на поверхности самолета. Однако, высокая электропроводность обшивки самолета приводит к возникновению вторичного излучения, источником которого могут быть головки заклепок, острые кромки и выступающие антенны.
Наносимые на различные элементы самолета радиопоглощающие покрытия отличаются от тех, которые применялись 10-15 лет тому назад. Современные покрытия имеют переменную по профилю толщину, сложную структуру с меняющимися значениями диэлектрической и магнитной проницаемостей как по толщине (нормально к поверхности), так и вдоль поверхности обшивки.
Создание веществ с произвольным законом поведения магнитной проницаемости связано с некоторыми дополнительными ограничениями.
Оптимизация ЭПР какого-либо фрагмента самолета изменением диэлектрической и магнитной проницаемости вещества, распределением его толщины по поверхности фрагмента требует разработки технологий, которые в дальнейшем воспроизведут требуемые параметры.
Для нанесения покрытий используются совершенно разные технологии /1/. Большая часть поверхности самолета покрывается методом лакокрасочных технологий. Несмотря на кажущуюся простоту, эта технология наиболее ответственная, поскольку от ее качества зависит вклад в ЭПР одного из основных рассеивающих элементов самолета - его воздухозаборника, кроме того, нарушение адгезии покрытия в воздухозаборнике может привести к аварии самолета. Многослойные радиопоглощающие покрытия напыляются с помощью как роботизированных систем в серийном производстве самолетов, так и ручным способом при создании экспериментальных образцов техники.
Для упрощения технологии нанесения покрытий предлагается не изменять его толщину, а дифференцированно распределять радиопоглощающие свойства по объему. Для этого в ряде случаев улучшить радиопоглощающие покрытия, можно используя ферромагнитные проводящие частицы очень малого размера, неравномерно распределенные как по площади, так и по глубине залегания. Распределение частиц предлагается производить после нанесения покрытия, до момента его затвердевания воздействуя на частицы силами электростатического поля. В электрическом поле на диэлектрики и проводники действуют силы. Их называют пондеромоторпыми силами, т. е. силами, действующими на весомые тела. Первопричиной возникновения пондеромоторных сил являются электрические заряды, сообщаемые телам. Однако сообщение зарядов телам осложняется появлением поляризационных зарядов и упругих деформаций в диэлектриках и проводниках. Пондеромоторные силы, действуют на границе раздела двух диэлектриков с разными диэлектрическими проницаемостями. Управление движением ферромагнитных проводящих частиц очень малого размера возможно изменением конфигурации электростатического поля. Максвеловские силы обусловленные воздействием электрополя на жидкий диэлектрик на границе раздела двух диэлектриков, что приводит жидкость в движение вдоль электродов, в результате чего в межэлектродной зоне возникает система вихрей /2/. Вихри с максимальной частотой вращения возникают у торцов фокусирующих элементов. Частицы, попадающие в подобную систему, также принимают участие в циркуляции и, как правило, имеют тенденцию сохранять свое положение в том вихре, в который они попадают при входе в систему. Это свойство обеспечивает создание работоспособной конструкции, позволяющей транспортировать частицы вдоль фокусирующей системы вплоть до выхода из нее.
Исследование
параметров электрополя в электростатических
системах сводится к изучению характеристик
напряженности электрополя Е
и измерению градиента напряженности
электрополя grad![]() в рабочей зоне устройства.
в рабочей зоне устройства.
Напряженность поля зависит, прежде всего, от разности потенциалов, подводимых к электродам, формы электродов, их взаимного расположения.
Величина градиента напряженности поля будет
![]()
где:![]() Еn+1
и Еn
– значения напряженности в произвольных
точках, между которыми имеется
Еn+1
и Еn
– значения напряженности в произвольных
точках, между которыми имеется
![]() ,
отстоящих друг от друга на расстоянии
Δ
,
отстоящих друг от друга на расстоянии
Δ![]() .
.
Течение жидкости, как правило, возникает в зоне искривления электростатического поля.
Максвеловские силы обусловленны воздействием электрополя на жидкий диэлектрик на границе раздела двух диэлектриков, что приводит жидкость в движение вдоль электродов, в результате чего в межэлектродной зоне возникает система вихрей.
Вихри, расположенные ближе к периферии фокусирующей зоны, характеризуются активным движением масс жидкости, поскольку напряженность поля в этой части системы максимальна.
На внесенные ферромагнитные проводящие частицы также действуют пондеромоторные силы, приводящие их в движение.
В случае неоднородного поля имеет место пондеромоторная сила:
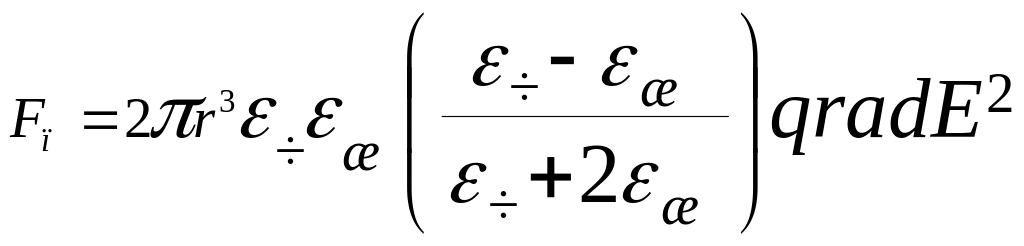
где:
r
- радиус частицы м;
![]() -
диэлектрическая проницаемость частицы
и жидкости соответственно.
-
диэлектрическая проницаемость частицы
и жидкости соответственно.
Особенностью конструкции является то, что практически во всех точках проходного канала, по которому движутся частицы, электрополе неоднородно. Неоднородность поля обусловлена формой и взаимным расположением криволинейных электродов. Расстояние между электродами изменяется не линейно при приближении от периферии к центральной части устройства.
Таким образом силы электрического взаимодействия внешнего электрополя и частиц зависят от заряда частиц, их расположения, диэлектрической проницаемости частиц и среды, параметров электрополя.
 Траектория
движения жидкости не стационарна и
изменяется со временем. На рисунке 1
представлена фотография натурной модели
элементарной ячейки устройства с вязкой
жидкостью обогащенной окисью хрома до
наложения электростатического поля. А
на рисунке 2 представлена та же ячейка,
но через несколько секунд после наложения
разницы потенциалов 3 кВ.
Траектория
движения жидкости не стационарна и
изменяется со временем. На рисунке 1
представлена фотография натурной модели
элементарной ячейки устройства с вязкой
жидкостью обогащенной окисью хрома до
наложения электростатического поля. А
на рисунке 2 представлена та же ячейка,
но через несколько секунд после наложения
разницы потенциалов 3 кВ.
 Рис.
1. Элементарная ячейка с топливом, Рис.
2. Элементарная ячейка с
Рис.
1. Элементарная ячейка с топливом, Рис.
2. Элементарная ячейка с
загрязненным окисью хрома до топливом, загрязненным окисью
наложения электростатического поля хрома после наложения
электростатического поля
При подаче разности потенциалов на электроды в ячейках возникает интенсивное движение жидкости, увеличивающееся по мере увеличения напряжённости поля. Вихри, вызванные этим движением, захватывают всю проточную зону канала устройства, а скорость движения жидкости под действием “электрического ветра“, может превышать скорость движения, вызванную прокачкой жидкости через устройство. Движение жидкости направлено из зон с малой напряженностью в зоны, где напряженность наибольшая. Такими свойствами обладают зоны у кромок электродов в центральной части устройства.
Вследствие условия неразрывности начинается движение по восполнению дефицита массы жидкости. Причём, вход жидкости в ячейку осуществляется в периферийной зоне, где напряжённость Е и её градиент qrad E имеют меньшие значения из - за максимального расстояния между электродами. Визуальные наблюдения и анализ виртуальной модели позволяет сделать следующие заключения о механизме работы ячейки: если частица несёт значительный заряд, то, войдя в устройство, она направляется к электроду по кратчайшему пути. Если частица несёт незначительный заряд, то электрические силы, действующие на неё, существенно меньше сил вязкого трения и гидродинамического сопротивления среды. Частицы с незначительным зарядом вовлекаются в движение вместе с жидкостью по кольцевой траектории и проносятся вдоль электрода.
Таким образом, воздействуя электростатическим полем определенной конфигурации на покрытия с ферромагнитными частицами можно изменять его радиопоглощающие свойства в нужных направлениях.
Литература
1. Иванов Е.Г. Новые авиационные материалы и технологии.// М.: ВАТУ – 2008. - 97 с.
2. Леонов В.В. Исследование явления электрического ветра и применение его для перекачивания жидких диэлектриков.// Вестник Приазовского государственного технического университета – 2011. – Вып. №1/2011(13)
3. http//vpk.name/blog/fundamentalnye _ i _ prikladnye _ problemy _ stelstehnologii/
Военный учебно-научный центр Военно-воздушных сил
“Военно-воздушная академия”, г. Воронеж
УДК 547:61
Д.С. Минаков, А.Н. Корнеева, В.В. Корнеева
Анаболические стероиды
В статье рассматривается влияние анаболических стероидов на организм человека, их положительные и отрицательные свойства
Анаболические стероиды (греч. "anabolein" - "наращивать") - это фармакологические препараты, которые имитируют действие мужского полового гормона - тестостерона и дигидротестостерона, поэтому они обладают андрогенным ("andros" и "genein", что переводится как "делать мужчиной" или "омужествлять")эффектом, то есть действуют по типу мужского полового гормона. Основное свойство этих препаратов - усиление процесса обмена и усвоения тех веществ, которые идут на построение тканей живого организма [1]. Способствуют фиксации кальция в костной ткани. Активизируют минеральный обмен, задерживая в организме фосфор и серу, ускоряют синтез протеина внутри клеток, что приводит к выраженной гипертрофии мышечной ткани (анаболизм), увеличивают вес благодаря приросту мышечной массы, в результате чего они нашли широкое применение в бодибилдинге, прежде всего с целью увеличения мышечной массы и силовых показателей [2].
Изначально они использовались исключительно в медицинских целях, когда требовалась дополнительная стимуляция анаболических процессов в организме человека. Однако, очень скоро эти особенности стероидов заинтересовали спортсменов. Началась эра использования стероидных анаболических средств в спортивной практике. Клинические испытания на людях начались в 1937 году. Первое упоминание анаболического стероида в истории силовых видов спорта датируется 1938 годом. Активное применение в спорте началось в 1960 г. в США и хранилось в строжайшей тайне. Вскоре анаболики начали применять в Европе.
Сейчас анаболики используют многие, известные всему миру спортсмены. Как в Европе, так и в США были проведены тщательные исследования по изучению совместного действия спортивной тренировки и анаболических стероидов [3]. В 1976 году анаболические стероиды были запрещены международным олимпийским комитетом, на этом заканчивается история их легального применения в спорте, а через 10 лет после этого были разработаны специальные тесты для определения анаболических стероидов в моче.
Механизм действия анаболических стероидов не похож на действие пептидных гормонов. Попадая в кровь, молекулы стероидов разносятся по всему телу, где они реагируют с клетками скелетных мышц, сальными железами, волосяными мешочками, определенными участками мозга и некоторыми эндокринными железами. Анаболические стероиды растворимы в жирах, поэтому могут проникать через мембрану клеток, состоящую из жиров; внутри клетки анаболические стероиды взаимодействуют с андрогенными рецепторами ядра и цитоплазмы. Активированные андрогенные рецепторы передают сигнал внутрь клеточного ядра, в результате чего изменяется экспрессия генов или активируются процессы, которые посылают сигналы другим частям клетки [4]. В результате этого происходит стимуляция синтеза всех видов нуклеиновых кислот и запускается процесс образования новых молекул белка. Эффект анаболических стероидов на рост мышечной массы обусловлен следующими механизмами: ускорение синтеза белка, снижение времени восстановления, уменьшение влияния катаболических гормонов (кортизола и др.), смещение дифференцировки клеток в сторону мышечных, уменьшая образование жировых клеток, ускорение метаболических реакций, за счет чего происходит распад жира [5].
Эффекты анаболических стероидов делятся на две основные категории: анаболические и андрогенные.
Анаболические эффекты: Значительный прирост мышечной массы (5-10 кг в месяц), увеличение силовых показателей, увеличение выносливости и производительности, увеличение числа эритроцитов крови, укрепление костной ткани, уменьшение жировых запасов.
Андрогенные эффекты: маскулинизация (процесс накопления вторичных половых признаков мужского пола у особи женского пола), вирилизация (процесс проявления мужских черт (тип телосложения, мужские черты лица, оволоcение, развитая мускулатура, тембр голоса и др.) у мужчин и женщин под влиянием гормонов), гипертрофия простаты, атрофия яичек, потеря волос на голове, и активация роста на лице и теле. На данный момент практически все анаболические стероиды обладают выраженными андрогенными эффектами [6].
Дополнительные эффекты: усиление аппетита, потеря чувства страха, повышение самоуверенности и самооценки, улучшение коммуникативных способностей, повышение полового влечения.
Побочные эффекты анаболических стероидов:
Во время курса: раздражительность или "стероидная ярость", повышение артериального давления, акне (угревая сыпь), повышение либидо, депрессия, задержка жидкости, повышение уровня холестерина, гинекомастия, маскулинизация у женщин, поражение печени, себорея, гипертрофия миокарда с развитием ишемии, остановка роста в молодом возрасте, выпадение волос [7].
После курса: снижение либидо, импотенция, привыкание, бесплодие, атрофия яичек (при передозировке и длительных курсах), депрессия.
Практически все побочные эффекты носят обратимый характер, за исключением случаев злоупотребления. Современные препараты практически не вызывают побочных эффектов и осложнений, если принимаются по инструкции.
Предотвратить побочные эффекты можно следующим образом: не превышать рекомендуемые дозы; не комбинировать несколько анаболических стероидов, если это не предусмотрено курсом; не превышать длительность курса; женщинам вообще не рекомендуется принимать анаболические стероиды, либо делать выбор из препаратов с высоким анаболическим индексом; не применять анаболические стероиды в возрасте младше 21 года; обязательно включать в курс PCT("Послекурсовая терапия" - комплекс препаратов и спортивных добавок, которые применяются в бодибилдинге и силовых видах спорта с целью минимизирования побочных эффектов и осложнений после цикла стероидных гормонов или прогормонов), это позволит существенно снизить или предотвратить многие побочные эффекты [8]. Данные рекомендации позволяют снизить частоту побочных эффектов до 1 % и ниже, а также сохранить набранную мышечную массу и результаты.
Применение стероидов в бодибилдинге приняло угрожающие размеры. Сегодня врачи и ученые делают резкие и необоснованные заявления, преувеличивая опасность стероидов и раздувая ее до вселенских масштабов. Такое искажение истины порочит лицо нашего спорта, якобы толкающего спортсменов на применение смертельных допингов. Посмотрим правде в глаза: 99,9 процентов ведущих бодибилдеров принимали и принимают стероиды [9]. В США андрогены вошли в обиход в конце 50-х годов. "Путевку в жизнь" им дал Джон Б. Зиглер, врач команды тяжелоатлетов. А ему о стероидах поведал врач команды СССР - советские тяжелоатлеты "вышли" на анаболики еще раньше. На сегодняшний день нет веских доказательств, которые бы подтвердили "смертельную" опасность стероидов [10]. Без сомнения, принимая стероиды, человек всегда рискует. Но прежде, чем делать выводы, надо точно определить степень этого риска. Честно говоря, риск погибнуть в автокатастрофе гораздо выше, чем от анаболиков. Но ведь это не значит, что надо запрещать автомобили или никогда не садиться за руль. Чтобы свести к минимуму побочные эффекты, врачи должны консультировать атлетов, принимающих стероиды. Тактика запугивания не делает чести медикам и ученым. Злоупотреблять стероидами недопустимо, но запретами мы ничего не добьемся. Самый лучший выход - открытый и честный разговор о реальных последствиях применения стероидов.
Литература
1. Hoberman JM, Yesalis CE (1995). "The history of synthetic testosterone". Scientific American 272 (2): 76–81. doi:10.1038/scientificamerican0295-76 (inactive 2010-01-05).
2. David K, Dingemanse E, Freud J, Laqueur L (1935). "Uber krystallinisches mannliches Hormon aus Hoden (Testosteron) wirksamer als aus harn oder aus Cholesterin bereitetes Androsteron". Hoppe Seylers Z Physiol Chem 233: 281
3. Taylor, William N (January 1, 2002). Anabolic Steroids and the Athlete. McFarland & Company. p. 181.
4. Justin Peters The Man Behind the Juice, Slate Friday, Feb. 18, 2005, Accessed 29 April 2008
5. Lavery DN, McEwan IJ (2005). "Structure and function of steroid receptor AF1 transactivation domains: induction of active conformations". Biochem. J. 391 (Pt 3): 449–64.
6. Singh R, Artaza J, Taylor W, Gonzalez-Cadavid N, Bhasin S (2003). "Androgens stimulate myogenic differentiation and inhibit adipogenesis in C3H 10T1/2 pluripotent cells through an androgen receptor-mediated pathway". Endocrinology 144 (11): 5081–8.
7. George P. Chrousos, The gonadal hormones and inhibitors, in Bertram G. Katzung (Ed.), Basic and Clinical Pharmacology, McGraw-Hill Professional, 2006, ISBN 0-07-145153-6, p. 674–676
8. Медицинская энциклопедия. М.: КРОН-ПРЕСС, 1999. 970 с.
9. Журнал «Здоровье», 1990 г., с испр.
10. “Железный мир”, 2011 г., №3 - "Анаболические стероиды и бодибилдинг"
Воронежский государственный технический университет
УДК 621. 367. 502.7
И. М. Винокурова, Д. Н. Бурдунюк
ОСОБЕННОСТИ ПЛАНИРОВАНИЯ РЕЖИМОВ ОБРАБОТКИ ЛЕГКОПАССИВИРУЮЩИХСЯ МЕТАЛЛОВ
В материалах статьи приводятся данные по определению методов расчета процессов анодной обработки
Для расчета параметров технологического процесса технолог должен иметь чертежи готовой детали и заготовки или карту операции, предшествующей ЭХО, данные о материале, его состоянии, о методе получения заготовок и технические условия на их поставку [1-6] (например, при получении труб с металлургических заводов).
Расчет выполняют в следующей последовательности:
1. Анализируют чертежи заготовки и находят наиболее приемлемый способ и схему обработки внутренней поверхности, при этом учитывают возможность использования имеющегося оборудования или его комплектующих.
2. Для выбранного способа обработку находят тип катодного устройства и выбирают или рассчитывают по приведенным методикам его основные параметры (зазор, длину и диаметр направляющих, рабочей части и др.). На основании таких материалов разрабатывают техническое задание на инструмент. При этом особое внимание уделяют обеспечению плавности движения электролита.
3. С учетом опыта создания оборудования для ЭХО внутренних поверхностей выбирают станок. Если необходимого оборудования не имеется, то разрабатывают заявку на его приобретение или выдают техническое задание на проектирование. При этом рассчитывают комплектующие изделия (насосы, ванны, источники питания, устройства для очистки электролита), а такие при необходимости находят диапазоны скоростей вращения деталей и поступательного перемещения электродов.
4. По марке обрабатываемого материала подбирают состав электролита и его температуру. Здесь следует иметь в виду, что по мере создания новых электролитов их состав будет изменяться и имеющиеся рекомендации следует корректировать с учетом результатов новых исследований.
5. Для выбранного электролита находят его электропроводность, потери напряжения в приэлектродных слоях. Кроме того, рассчитывают или выбирают по литературным данным электрохимический эквивалент сплава.
6. Для выбранного способа обработки с учетом результатов расчетов по пункту 5 находят, скорость съема материала и характеристики течения электролита (давление, подачу насоса).
7. По марке, структуре материала и виду заготовки для расчетного режима рассчитывают ожидаемую шероховатость поверхности и глубину микрорастравливаний. При необходимости корректируют режим обработки с позиций получения заданного качества поверхности. В последнем случае уточняют результаты расчетов по пункту 6.
8. С учетом исходных материалов находят минимальный припуск на обработку и проектируют заготовку с учетом особенностей ЭХО.
9. Определяют погрешность обработки и оценивают необходимость в последующей операции и припуске для нее.
10. По известному режиму обработки для различных участков детали устанавливают точность на концах и в местах перехода от одного сечения к другому. Оценивают целесообразность последующей операции на этих участках.
11. Находят наибольшую допустимую скорость подачи электрода и производительность процесса.
12. Для получениях параметров процесса уточняют размеры катодных устройств.
13. Оценивают изменение усталостной прочности детали при ЭХО по сравнению c прочностью, достигаемой при механической обработке, и с учетом условий эксплуатации изделия дают заключение о возможности использования ЭХО.
В источнике [3, 4], авторы показали необходимость увеличения давления на входе по мере роста плотности тока при стабильной длине зазора.
Авторы считают [5, 6], что границей образования "пробки" может служить часть канала, где пузырьковый режим течения газожидкостной смеси переходит в пленочный, т.е. образуется газовая "пробка" перекрывающая канал и останавливающая поток смеси (рисунок). Расчет может быть выполнен при условии, что газы имеют одинаковый (или близкий) диаметр пузырьков, их количество и степень заполнения растут равномерно, а движение жидкой среды между газами происходит по аналогии с фильтрами, при этом газ из смеси остается до начала положения "пробки", заполняет пространство между пузырьками, образуется газовый участок, который растет, тормозит движение "пробки" до ее полной остановки. После остановки потока процесс анодного растворения прекращается, газообразные продукты обработки со стороны Рвх сжимаются и уменьшают объем, давление в МЭЗ перед "пробкой" растет, а с противоположной стороны часть газов из "пробки" переходит в жидкость, которая по инерции движется по каналу, образуя зоны пониженного давления.
Активную роль, в разрушении "пробки" играет размыв ее струей газожидкостной смеси, поступающей в зазор при давлении Рвх.
Если давление Рвх достаточно для проталкивания "пробки", то ее разрушение произойдет достаточно быстро, т.к. после прекращения анодного процесса газу вновь не поступают к "пробке" со стороны движения потока, а ранее образовавшиеся пузырьками перешли в МЭЗ.
Большие расхождения с экспериментом (табл. 1) объясняются тем, что в расчетах вязкость газожидкостной среды принималась постоянной, хотя ее изменение достигает 300 %.
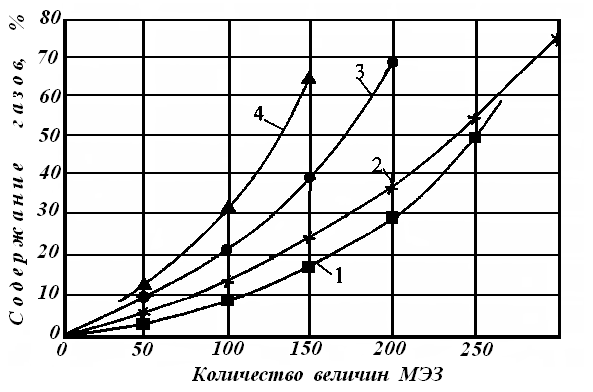
Содержание газов в смеси по длине канала при давлении на входе в МЭЗ
1 - 0,8 МПа; 2 - 0,4 МПа; 3 - 0,2 МПа; 4-0,1 МПа
Таблица 1
Сравнение расчетных и экспериментальных скоростей потока на выходе из
канала
Расстояние от обрабатываемой поверхности, мм
|
Скорость потока, м/с
|
Расхождение, %
|
|
Расчетная
|
Экспериментальная
|
||
0
|
~0
|
~0
|
~0
|
0,02
|
-12,3
|
10
|
181
|
0,04
|
-10,2
|
22
|
316
|
0,06
|
2
|
12
|
500
|
0,08
|
3
|
3
|
0
|
0,10
|
5,1
|
6
|
17,6
|
0,2
|
9,2
|
10
|
8,7
|
Таблица 2
Погрешность профиля при глубинном шлифовании
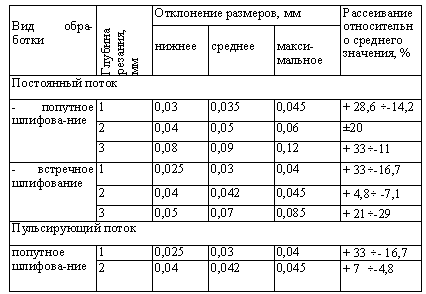
После выхода из зоны обработки поток достаточно быстро перемешивается и его скорость на расстоянии более 70 - 80 мкм подчиняется расчетным зависимостям. Влияние пульсирующей подачи электролита на точность обработки приведено в табл. 2.
Погрешность обработки возрастает по мере увеличения припуска, поэтому для особо точных работ требуются подачи по глубине, измеряемые сотыми долями миллиметра. Наибольший эффект для снижения погрешности дает применение пульсирующего потока электролита при обработке сложнопрофильных поверхностей (лопаток турбин, рабочих профилей зубчатых колес, шлицев и др.), где наибольшая точность (в пределах допуска по чертежу) может быть достигнута при глубине припуска менее 0,01 мм на двойной ход и высоких скоростях продольного перемещения инструмента (более 5 м/мин).
Если анализ покажет необходимость введения в технологический процесс последующей операции, то на основании рекомендаций назначают припуск на окончательную обработку.
Опыт практического использования предлагаемой методики показал, что она обеспечивает точность расчетов порядка 20 %. В ряде случаев это удовлетворяет требованиям производства. При необходимости получения большей точности или повышения достоверности результатов целесообразно выполнить дополнительные эксперименты и уточнить полученный диапазон режимов. Использование методики резко ускоряет темпы внедрения технологического процесса в производство, сокращает затраты на опытные работы и заготовки, стоимость которых может исчисляться тысячами рублей.
Литература
1. Электрохимическая размерная обработка. Проблемы и решения/ Г.Н. Зайдман // Электрохимическая размерная обработка. 1991. № 1. С. 3-14.
2. Саушкин Б. П. Электрохимическая обработка изделий из титановых сплавов / Б. П. Саушкин, Ю. Н. Петров, А. З. Нистрян, А. В. Маслов // Кишинёв. Штиница. 1988. 200 с.
3. Мандрыкина И. М. Исследование взаимосвязи термокине-тических и электрохимических параметров при импульсных режимах обработки титановых сплавов. Дис… Воронеж. 1998. 210 с.
4. Шалимов Ю. Н. Оптимизация электрохимического процесса обработки алюминиевой фольги в производстве конденсаторов / Ю. Н. Шалимов, И. М. Мандрыкина, Ю. В. Литвинов Воронеж: Изд-во
5. Смоленцев В. П. Технология электрохимической обработки внутренних поверхностей. Москва. Машиностроение. 1978. 176 с.
6. Газизулин К. М. Электрохимическая размерная обработка крупногабаритных деталей в пульсирующих рабочих средах: Научное издание. Воронеж: Воронежский государственный университет, 2002. 243 с.
Воронежский государственный технический университет
УДК 665.6/7+621.643+666.9.019.3
В.П. Горшунова, Б.А. Спиридонов, М.К. Карташов, А.С. Соколов
О ВОЗМОЖНОСТЯХ ПРИМЕНЕНИЯ КОМПОЗИЦИОННЫХ
МАТЕРИАЛОВ В НЕФТЕГАЗОВОМ КОМПЛЕКСЕ
В статье даны сведения о композиционных материалах с неметаллической матрицей, а также рассмотрены возможности использования композитов для получения покрытий трубопроводов
Функционирование транспортных и нефтегазопромысловых трубопроводов происходит в жестких условиях, поскольку в зависимости от назначения они подвержены различным нагрузкам (внутреннему давлению, осевым растягивающим или сжимающим напряжениям, давлению грунта засыпки и подвижных средств, перепадам температур). Основная причина аварий на промысловых трубопроводах – внутренняя коррозия, на транспортных – внешняя коррозия.
Одно из направлений повышения надежности трубопроводов – внедрение новых изоляционных материалов и современных технологий их нанесения. В последние годы для повышения прочностных свойств и износостойкости полимерных материалов и покрытий применяют их армирование наноструктурными наполнителями.
Общие сведения о композиционных материалах. Композиционные материалы (композиты) состоят из химически разнородных компонентов, нерастворимых друг в друге и связанных между собой в результате адгезии. Основой композитов является пластическая матрица, которая связывает наполнители, определяет форму изделия, его монолитность, теплофизические, электро- и радиотехнические свойства, герметичность, химическую стойкость, а также распределение напряжений между наполнителями.
В качестве матрицы применяют металлы (алюминий, магний, их сплавы), полимеры (эпоксидные, фенолформальдегидные смолы, полиамиды), керамические, углеродные материалы.
Наполнители чаще всего играют роль упрочнителей, воспринимают основную долю нагрузки и определяют модуль упругости и твердость композита, а иногда также фрикционные, магнитные, теплофизические и электрические свойства. Наполнителями служат тонкая диаметром несколько микрометров проволока из высокопрочной стали, вольфрама, титана, а также стеклянные, полиамидные, углеродные, боридные волокна и волокна на основе нитевидных кристаллов оксидов, карбидов, боридов, нитридов и др.
Композиты получают пропиткой наполнителей матричным раствором, нанесением материала матрицы на волокна плазменным напылением, электрохимическим способом, введением тугоплавких наполнителей в расплавленный материал матрицы, прессованием, спеканием. Остановимся подробнее на композитах с неметаллической матрицей.
Композиционные материалы с неметаллической матрицей. Композиционные материалы с неметаллической матрицей нашли широкое применение. В качестве неметаллических матриц используют полимерные, углеродные и керамические материалы. Из полимерных матриц наибольшее распространение получили эпоксидная, фенолоформальдегидная и полиимидная матрица. Угольные матрицы, коксованные или пироуглеродные получают из синтетических полимеров, подвергнутых пиролизу. Матрица связывает композицию, придавая ей форму. Упрочнителями служат волокна: стеклянные, углеродные, борные, органические, на основе нитевидных кристаллов (оксидов, карбидов, боридов, нитридов и др.), а также металлические (проволоки), обладающие высокой прочностью и жесткостью.
Содержание упрочнителя в ориентированных материалах составляет 60–80 об.%, в неориентированных (с дискретными волокнами и нитевидными кристаллами) – 20–30 об.%. Чем выше прочность и модуль упругости волокон, тем выше прочность и жесткость композиционного материала. Свойства матрицы определяют прочность композиции при сдвиге и сжатии и сопротивление усталостному разрушению.
Карбоволокниты (углепласты) представляют собой композиции, состоящие из полимерного связующего (матрицы) и упрочнителей в виде углеродных волокон (карбоволокон).
Связующими служат синтетические полимеры (полимерные карбоволокниты); синтетические полимеры, подвергнутые пиролизу (коксованные карбоволокниты); пиролитический углерод (пироуглеродные карбоволокниты).
Образующийся при пиролизе кокс имеет высокую прочность сцепления с углеродным волокном. В связи с этим композиционный материал обладает высокими механическими и изоляционными свойствами, стойкостью к термическому удару.
Бороволокниты представляют собой композиции из полимерного связующего и упрочнителя — борных волокон.
Бороволокниты отличаются высокой прочностью при сжатии, сдвиге и срезе, низкой ползучестью, высокими твердостью и модулем упругости, тепло- и электропроводностью. Ячеистая микроструктура борных волокон обеспечивает высокую прочность при сдвиге на границе раздела с матрицей.
Органоволокниты представляют собой композиционные материалы, состоящие из полимерного связующего и упрочнителей (наполнителей) в виде синтетических волокон. Такие материалы обладают малой массой, сравнительно высокими удельной прочностью и жесткостью, стабильны при действии знакопеременных нагрузок и резкой смене температуры. Для синтетических волокон потери прочности при переработке небольшие; они малочувствительны к повреждениям.
В органоволокнитах значения модуля упругости и температурных коэффициентов линейного расширения упрочнителя и связующего близки. Происходит диффузия компонентов связующего в волокно и химическое взаимодействие между ними. Структура материала бездефектна. Пористость не превышает 1–3% (в других материалах 10–20%). Отсюда стабильность механических свойств органоволокнитов при резком перепаде температур, действии ударных и циклических нагрузок. Ударная вязкость высокая (400–700 кДж/м2). Недостатком этих материалов является сравнительно низкая прочность при сжатии и высокая ползучесть (особенно для эластичных волокон).
Перспективы использования композиционных покрытий. В Московском «Объединенном центре исследований и разработок» начата работа, направленная на создание и внедрение нанокомпозиционных покрытий на основе полиолефинов, модифицированных наночастицами углерода и кремния. Благодаря сочетанию в различных комбинациях составляющих материала и вариации толщины слоев могут быть достигнуты высокие твердость, прочность, химическая стабильность, низкий коэффициент трения и хорошая износостойкость покрытий. Цель данной работы – оценка перспективности многослойного покрытия на основе полиэтилена и углеродных наночастиц (УНЧ).
Поставлена задача: создать на основе полиэтилена покрытия, превосходящего современное заводское покрытие по следующим технологическим показателям: повышенные на десятки процентов защитные и теплотехнические свойства; меньшая влагоемкость; меньшая влагоемкость; высокие прочность и изностойкость; расширенный температурный диапазон эксплуатации; сниженный за счет замены полиэтилена на наполнитель на 40% удельный расход сырья (этилена) на тонну готовой продукции (компаунда).
Актуальность разработки обусловлена огромным потенциальным рынком сбыта новой продукции, включающим нефтяную, газовую, нефтегазоперерабатывающую, химическую и энергетическую отрасли и ужесточающимися требованиями к качеству защитных покрытий трубопроводов. Ежегодная потребность только нефтяной промышленности в трубах с покрытием составляет выше 80 тыс. км [1,2].
В трубной промышленности [3] за последние пять лет также наблюдался устойчивый рост производства труб с полимерным покрытием заводского нанесения.
Ассортимент труб с покрытием из полиолефинов довольно широк. Перспективы связываются с увеличением объемов выпуска труб большого диаметра (ТБД) с антикоррозионным покрытием. За последние 1–2 года наблюдался огромный спрос на ТБД с покрытием [4, 5].
Кроме того, спрос на новый материал для покрытий диктуется тем, что многие трубопроизводящие компании мира стремятся попасть на рынок России. В связи с этим от отечественных предприятий потребуется высокая конкурентоспособность, которая может быть достигнута как за счет повышения качества, так и за счет внедрения новых разработок.
Эксперты считают, что созданные с использованием нанотехнологий материалы поднимут на новый уровень качество труб с антикоррозионным покрытием. Это повысит их конкурентоспособность, увеличит срок эксплуатации и изменит физико-химические свойства покрытий. Это обстоятельство немаловажно в связи со строительством нефтегазопроводов в сложных климатических условиях Крайнего Севера, пустынь и территорий с большими и резкими колебаниями температур. Кроме того, созданное с использованием нанотехнологий антикоррозионное покрытие нового типа ориентировано на соответствие международным экологическим нормам. Все это позволяет сделать вывод о том, что актуальность и перспективность разработки несомненна.
Как отмечено в ряде публикаций по наноматериалам [6,7], углеродные нанотрубки (УНТ) и углеродные нановолокна (УНВ) как наполнители полимеров способны повысить электропроводность, увеличить теплопроводность, теплостойкость, температуру воспламенения; придать антистатические свойства; улучшить механические характеристики; увеличить адгезионную прочность и расширить температурный диапазон применения (от -60 до 250°С); обеспечить устойчивость к воздействию агрессивных рабочих сред.
В публикациях сообщалось о весьма ощутимых эффектах от введения нанотрубок в полимерные волокна [8]. Добавление фуллеренов приводит к повышению механических свойств, радиационной стойкости, стабильности полимеров при «жесткой» эксплуатации.
Следует отметить, что эти выводы касаются не полиэтилена, а других полимерных материалов. Для выяснения, насколько сохранятся эти свойства в пленке полиэтилена, требуется дополнительное исследование.
Анализ работ [7, 8] показал, что введение УНВ в сверхвысокомолекулярный полиэтилен (СВМПЭ) повышает механическую стойкость материала, но только при строго определенных соотношениях основы и наполнителя. Вопреки ожиданиям, частицы наполнителя не распределены равномерно по объему матрицы, а располагаются преимущественно по границам глобул, проявляясь в виде нитевидных образований.
При введении 2 вес.% УНВ эти образования наглядно проявляются на поверхности скола и имеют преимущественную продольную ориентацию. Это не изменяет характер надмолекулярного строения полимера – волокнистую структуру. Увеличение доли УНВ до 10 вес.% приводит к формированию весьма неоднородной надмолекулярной структуры. Введение наночастиц углерода в полимерную матрицу меняет механические характеристики полимерных материалов.
Установлено, что прочность образцов с УНВ при растяжении повышается, но при этом в два раза снижается относительное удлинение. Отмечено, что значительное увеличение объемной доли наполнителя приводит к снижению прочности полимерных материалов; увеличению тенденции к хрупкому разрушению.
Установлено, что введение УНТ приводит к изменению проводящих свойств полимеров.
Волокнистые структуры с высоким коэффициентом отношения длина/диаметр увеличивают количество электрических контактов и обеспечивают более однородный путь.
Следует отметить, что наиболее перспективные результаты были получены в исследованиях по керамическим наполнителям. Введение керамических наполнителей в СВМПЭ приводит к увеличению износостойкости по сравнению с покрытием из чистого СВМПЭ в 5–20 раз. Однако даже в этом случае износостойкость покрытий из модифицированного СВМПЭ сопоставима с износостойкостью защищаемого металла (Ст3) за счет низкого коэффициента трения при невысоких удельных нагрузках.
Максимальную стойкость имеют покрытия с добавкой 10 об.% глинозема: не обнаружено разрушения материала покрытия, сохранилась адгезия к подложке. Покрытия с меньшим содержанием добавок (3 об.%) частично или полностью отслаиваются. Испытания на химическую стойкость проводили на образцах с покрытием, которые погружали в емкость со щелочной средой (раствор NaOH 140 г/л) и помещали в термический шкаф. Длительность испытаний составила 6 ч; диапазон температур 20–95°С. Термоусадку определяли регистрацией изменения размеров покрытий до и после кипячения в воде в течение 1 ч.
Введение наноструктурных наполнителей влияет также на термо- и огнестойкость полимеров. Установлено, что покрытия из чистого СВМПЭ, а также с невысоким содержанием керамических наполнителей (до 2%) подвержены необратимой термической усадке при нагреве выше 80°С, что является причиной отслоения покрытий. Добавка 10 об.% глинозема в СВМПЭ сдерживает термоусадку покрытий, в результате чего сохраняется их адгезия к подложке после нагрева.
Термоусадка является причиной отслоения и растрескивания покрытий с невысоким содержанием добавок (3 об.%) при испытаниях на термостойкость. Испытанные покрытия выдерживали не более трех термоциклов. Покрытия, содержащие 10 об.% глинозема, показывают термостойкость в 20 и более циклов.
Ранее установлено, что гибкие УНТ по-иному прилипают к поверхностям, чем более крупные структуры из-за Ван-дер-вальсовой силы притяжения между отдельными атомами. Обнаружено, что УНТ отделяются от поверхности рывками. Наблюдаются скачки в силе отрыва, когда УНТ сначала отрываются от поверхности, а потом цепляются за нее.
Для достижения требуемых качеств композитного материала на основе полиэтилена следует учесть ориентированную укладку УНТ и обеспечение оптимальной прочности связи матрица-наполнитель.
Важен выбор метода ориентированной укладки УНТ: растягивание, использование сдвигающих усилий, ориентирование в электрическом или магнитном полях, матричный синтез, использование капиллярных сил.
Еще один вопрос, который возникает при создании полимерных покрытий на основе полиэтилена, модифицированного углеродными наночастицами, это необходимость изменения химической природы их поверхности.
Такая функциализация будет способствовать увеличению прочности связи трубка-матрица, обеспечит разделение сростков УНТ на отдельные трубки и улучшит однородность распределения УНТ в матрице.
Примером могут служить данные по введению в эпоксидную смолу 0,5% двухслойных УНТ, функциализованных амином, в результате чего повысилась прочность на 10, жесткость на 15 и трещиностойкость на 43%. Однако аналогичные данные по полиэтилену отсутствуют. Здесь необходимы дополнительные исследования.
Литература
1. Басиев К.Д., Бигулаев А.А., Кодзаев М.Ю. Механо-коррозионные процессы в грунтах и стресс-коррозия в магистральных газопроводах. – Вестник ВНЦ, 2005, №1.
2. Завизенов К.В. Обзор некоторых аспектов производства труб для нефтяной промышленности. – Территория НЕФТЕГАЗ, 2004, №10. – 25с.
3. Низьев С.Г. Защита трубопроводов от коррозии с использованием современных изоляционных покрытий заводского и трассового нанесения. – Территория Нефтегаз, 2004, №6, с. 3.
4. Низьев С.Г., Семенченко В. Заводские полиэтиленовые покрытия – надежная защита трубопроводов от коррозии. – Нефтегазовая вертикаль, 2008, №12, с. 2.
5. Ушанов С. и др. Рынок внутренней изоляции труб. – Нефтегазовая вертикаль, 2002, №11, с. 88–89.
6. Раков Э.Г. Нанотрубки и фуллерены. – М.: Логос, 2006.
7. Раков Э.Г. Методы получения углеродных нанотрубок. – Успехи химии, 2000, т. 69, № 1, с. 41–59.
8. Елецкий А.В. Упрочнение полимеров однослойными углеродными нанотрубками. //www.nanometer.ru –2007, № 9.
Воронежский государственный технический университет
УДК 593.194
Ю. Н. Босикова, Б.А. Спиридонов
ВОЗМОЖНОСТИ ПРИМЕНЕНИЯ УГЛЕРОДНЫХ НАНОТРУБОК
В РАДИОТЕХНИКЕ
В статье приведен анализ литературных данных по структуре, свойствам и применению углеродных нанотрубок
Многие из перспективных направлений в материаловедении, нанотехнологии, наноэлектронике, прикладной химии связываются в последнее время с фуллеренами, нанотрубками и другими похожими структурами, которые можно назвать общим термином углеродные каркасные структуры. Углеродные каркасные структуры - это больши молекулы, состоящие исключительно из атомов углерода[1].
В 1985 году Роберт Керл, Гарольд Крото и Ричард Смолли открыли принципиально новое углеродное соединение – фуллерен, уникальными свойствами. В 1996 году им была присуждена Нобелевская премия. Основой молекулы фуллерена является углерод - этот уникальнейший химический элемент, отличающийся способностью соединяться с большинством элементов и образовывать молекулы самого различного состава и строения. Известно, что углерод имеет два основных аллотропных состояния -графит и алмаз.
В 1991 году японский профессор Сумио Иидзима обнаружил длинные углеродные цилиндры, получившие названия нанотрубок[2].
Открытие углеродных нанотрубок относится к наиболее значительным достижениям современной науки. Эта форма углерода по своей структуре занимает промежуточное положение между графитом и фуллереном. Однако многие свойства углеродных нанотрубок не имеют ничего общего ни с графитом, ни с фуллереном. Это позволяет рассматривать и исследовать нанотрубки как самостоятельный материал, обладающий уникальными физико-химическими характеристиками.
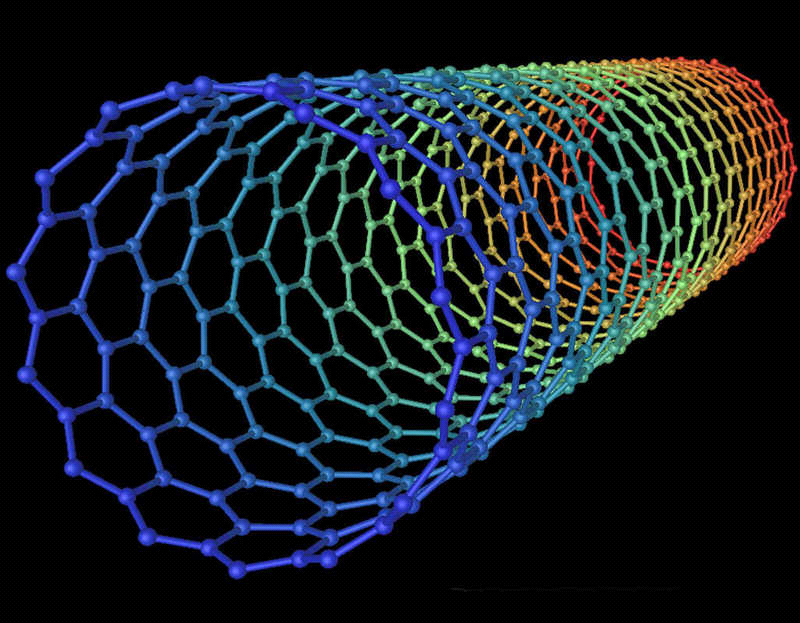
Рис.1. Однослойная нанотрубка
Исследования углеродных нанотрубок представляют значительный фундаментальный и прикладной интерес. Фундаментальный интерес к этому объекту обусловлен, в первую очередь, его необычной структурой и широким диапазоном изменения физико-химических свойств в зависимости от хиральности (рис.1). К проблеме исследования фундаментальных свойств углеродных нанотрубок вплотную примыкает проблема прикладного использования. Решение этой проблемы, в свою очередь, от создания способов дешевого получения углеродных нанотрубок в больших количествах. Эта проблема пока исключает возможность крупномасштабного применения этого материала. Однако такие свойства нанотрубок, как сверхминиатюрные размеры, хорошая электропроводность, высокие эмиссионные характеристики, высокая химическая стабильность при существующей пористости и способность присоединять к себе различные химические радикалы, позволяют надеяться на эффективное применение нанотрубок в таких областях, как измерительная техника, электроника и наноэлектроника, химическая технология и др.
Нанотрубка – это молекула из более миллиона атомов углерода, представляющая собой трубку с диаметром около нанометра и длиной несколько десятков микрон. В стенках трубки атомы углерода расположены в вершинах правильных шестиугольников. Нанотрубки в 50-100 раз прочнее стали и имеют в шесть раз меньшую плотность!
Уровень деформации у нанотрубок вдвое выше, чем у обычных углеродных волокон. Они напоминают по своему поведению не ломкие соломинки, а жесткие резиновые трубки.
Наиболее распространенными методами синтеза нанотрубок являются электродуговой метод, лазерная абляция и химическое осаждение из газовой фазы (CVD).
Нанотрубки, являются прочным материалом, как на растяжение, так и на изгиб. Под действием механических напряжений, превышающих критические, нанотрубки не "рвутся", а перестраиваются.
Как показали эксперименты, открытая нанотрубки обладает капиллярными свойствами. Чтобы открыть нанотрубку, надо удалить верхнюю часть – крышечку. Один из способов удаления заключается в отжиге нанотрубок при температуре 8500 C в течение нескольких часов в потоке углекислого газа. В результате окисления около 10% всех нанотрубок оказываются открытыми.
Наряду с металлами углеродные нанотрубки могут заполняться газообразными веществами, например водородом в молекулярном виде. Эта способность имеет практическое значение, ибо открывает возможность безопасного хранения водорода, который можно использовать в качестве экологически чистого топлива в двигателях внутреннего сгорания. В настоящее время разработаны технологии по внедрению внутрь нанотрубок цепочек из фуллеренов с уже имеющимися в них атомами гадолиния.
В зависимости от конкретной схемы сворачивания графитовой плоскости (хиральности), нанотрубки могут быть как проводниками, так и полупроводниками электричества. Электронные свойства нанотрубок можно целенаправленно менять путем введения внутрь трубок атомов других веществ.
Примером нанотрубок является создание первого наномасштабного мотора на основе многостенных нанотрубок. Углеродная нанотрубка выполняет своего рода роль оси, на которой монтируется ротор. На основе нанотрубки возможно создание микроскопических весов. (рис.2)

Рис.2. Микроскопические весы на нанотрубках
Существует также применение в наноэлектронике - создание полупроводниковых гетероструктур, т.е. структур типа металл/полупроводник или стык двух разных полупроводников.
В процессе роста углеродной нанотрубки в ней создается структурный дефект (рис.3) (заменяется один из углеродных шестиугольников на пятиугольник и семиугольник). Тогда одна часть нанотрубки будет металлической, а другая – полупроводником.
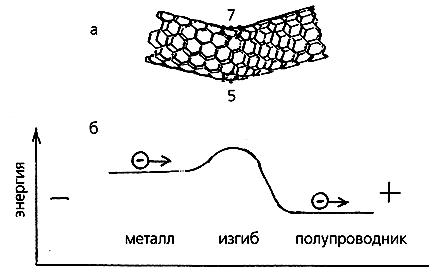
Рис.3. Влияние дефекта семиугольник-пятиугольник на геометрию нанотрубки (а)и энергию подвижных электронов(б)
Необычные электрические свойства нанотрубок делают их одним из основных материалов наноэлектроники [3,4]. Уже сейчас созданы опытные образцы полевых транзисторов на основе одной нанотрубки: прикладывая запирающее напряжение в несколько вольт, ученые научились изменять проводимость однослойных нанотрубок на 5 порядков (рис.4)
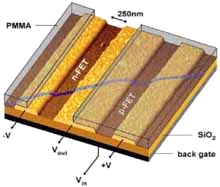
Рис.4. Транзистор p - типа на основе углеродных нанотрубок
Наноаккумуляторы – это аккумуляторы, использующие технологию нанопластин (менее 100 нм). Для сравнения, традиционные литиево-ионная технология использующая такие материалы, как оксиды лития с кобальтом или марганцем, чьи частицы имеют размер 5-20 мкм. Их основными преимуществами являются: более быстрое время зарядки аккумулятора, чем у литиево-ионных аналогов,
более сильное создаваемое напряжение и значительно увеличенная плотность заряда, а также небольшая масса и повышенный срок эксплуатации.
Разработано несколько применений нанотрубок в компьютерной индустрии. Например, по оценкам специалистов, нанотехнологии позволят создать микропроцессоры, которые будут содержать около 1 миллиарда транзисторов и смогут работать на частоте до 20 гигагерц при напряжении питания менее 1 вольта. Помимо этого, созданы и опробованы прототипы тонких плоских дисплеев, работающих на матрице из нанотрубок.
. Углеродные нанотрубки могут найти применение их в качестве детонаторов для подрыва боезарядов. Экспериментально установлено, что черные углеродные нанотрубки взрываются при свете вспышки, поскольку чрезвычайно эффективно поглощают свет. Световая энергия превращается в тепловую, которая не может быстро диссипироваться вдоль сборки нанотрубок, при этом взрываются только одностеночные нанотрубки. Первоначальный хлопок происходит вследствие нагрева кислорода внутри нанотрубок и между ними, что приводит к возникновению ударной волны.
Литература
1. Лозовик. Ю.Е. Образование и рост углеродных наноструктур –фуллеренов, наночастиц, нанотрубок и конусов/ Ю.Е.Лозовик, .А.М. Попов//УФН.-1997.-Т.167,№7.-с.751-774.
2. Золотухин И.В. Углеродные нанотрубки и нановолокна: учебное пособие/И.В. Золотухин, Ю.Е. Калинин. Воронеж: ГОУВПО «Воронежский государственный технический университет», 2006, 228с. УДК 593.194
3. Балабанов. Ю.Е. Нанотехнологии. Наука будущего/В.И. Балабанов. – М; ЭКСМО, 2009. 256с.
4. Гусев А.И. Наноматериалы, наноструктуры, нанотехнологии.– 2-е изд., исир.-14.; ФИЗМАТЛИТ, 2007. – 416с. – ISBN 978-5-9221-0582-8.
Воронежский государственный технический университет
УДК 537.2
О.Н. Болдырева
технология направленного изменения
характеристик адгезионных соединений
Рассматриваются пути направленного изменения характеристик адгезионных соединений с использованием различных групп модификаторов
Ускорители действуют по различным механизмам, интенсифицируя либо межфазные процессы взаимодействия субстратов с адгезивами (модификаторы адгезионного типа), либо внутрифазные процессы в последних ( модификаторы когезионного типа). Снижение энергетического барьера на границе раздела контактирующих фаз должно способствовать росту прочности и долговечности адгезионных соединений.
Одним из направлений реализации такого подхода является введение в состав адгезивов компонентов с пониженной поверхностной энергией, например содержащих атомов фтора и кремния. Это согласуется данными модификации цианакрилатных композиций соответст-вующими продуктами, не способными к самостоятельной полимеризацией. К числу таких продуктов принадлежат, например, линейные или циклические фторзамещенные β-дикетоны. Добавка к этил α-циана-крилату незначительных количеств трифторацитилацетона обеспечивает существенное повышение адгезионной способности состава (рис.1)
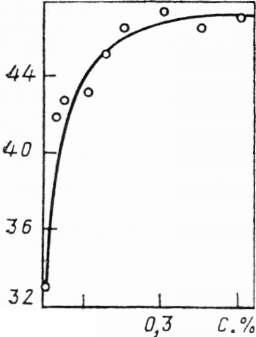
Рис.1. Зависимость сопротивления сдвигу адгезионных соединений стали от концентрации трифторацетилацетона
Подобный эффект обеспечивает также модификация 0,3-5 % перфторалкилкарбоновыми кислотами, алкильными замести-телями в молекулах которых являются радикалы алифатического (C3F7―C11F23) и ароматического (от C3F5OC6H4 до C9F19OC6H4) рядов. Наличие таких добавок позволяет применить цианакрилатные адгезивы для крепления практически любых металлов ( вплоть до меди, олова, серебра, золота и их сплавов), стекол и полимеров ( за исключением фторсодержащих). Для этих же целей могут быть использованы и кремнийсодержащие модификаторы, например, 0,01―5% метилдифенилсиланола, полидиметил-, дигидроксиполидиметил- и полифенилвинилсилоксанов, улучшающих смачиваемость адгезивом субстратов. Исключение из их состава гидроксильных групп позволяет использовать цианакрилатные композиции для соединения пористых металлов.
Эффективными модификаторами α-цианакрилатов когезионного типа должны служить акрилаты и диены. Действительно, добавка к этил-α-цианакрилату 5% глицидилметакрилата увеличивает сопротивление сдвигу выдержанных в воде в течение 10 суток адгезионных соединений сплава алюминия с 8,5 до 10,5 МПа; несколько более активен циклопендатиен, 1 % которого обеспечивает увеличение сопротивления сдвигу до 9,5 МПа.
Эффективность действия подобных добавок связана с их реакционной способностью по отношению к α-ци-анакрилатам, что подтверждается данными по модификации последних моно- и дизамещенными алкил-, алокси- и венил-замещенными кремнийсодржащими изоцианатами.
Наиболее перспективны модификаторы когезонного типа, интенсифицирующее процесс склеивания по механизму ускорения анионной полимеризации α-цианакрилатов. К их числу должны принадлежать ионные соединения, дассоциирующие на ониевый катион К и анион А. из общих соображений ясно, что в качестве К целесообразно использовать щелочные и щелочноземные металлы, поскольку они весьма склонны к гидрадации, снижая pH, а в качестве А – ионы сильных кислот вплоть до галогеноводородных. Справедливость такого вывода подтверждена результатами исследования нитратов, гало-генидов, перхлоратов, периодатов, тетрафторборатов, пер-фторфосфонатов, перфторарсенатов, трифторацетатов, ме-тилсльфатов, n-толуолсульфонатов, трифторметилсульфона-тов, хроматов и роданидов. Эти соли применяют в виде водных, этанольных или изопропанольных растворов.
Установлена линейность взаимосвязи параметров: продолжительность полимеризации этил-α-цианакрилата, включающего стандартные ингибиторы (0,0038% сернистого ангидрида и 0,04% гидрохинона) при 343 К увеличивается с 1,5 до 115 ч в интервале CH2O= 0.02―0.45%. Указанный ниже предел считают критическим, а на практике предпочитают не увеличивать концентрацию воды в α-цианакрилатах выше 0,013―0,026%.
Кроме того, наличие воды в композициях, иногда жела-тельное для ускорения их отверждения, может приводить к расслаиванию адгезивов. Поэтому в качестве гидроксилсодер-жащих добавок целесообразно использовать одно-, двух- и трехосновные спирты, например глицерин, 1,1,6-гексантриол в количествах 0,001―3%.
Сочетание ускорении полимеризации с повышением ад-гезионной способности цианакрилатных клеев - может быть обеспечен с помощью добавок, имеющих в своём составе ато-мы неопределенными электронными парами. Примером по-добных продуктов полифункционального действия является N,N-фениленбисмалиемид, введение 2% которого в этил-α-цианакрилат увеличивает сопротивление адгезионных соеди-нений стали сдвигу при 394К через 1, 24, и 48 ч в 3,1, 1,9 и 2,4 раза соответственно. Типичным представителям этой группы модификаторов следует считать также третичные амины али-фатического, ароматического и гетероциклического рядов, содержащие гидроксильные группы.
Аналогично действие и других добавок, содержащих группы с различными гетороатомами, например
= N―C = S и ―S―C = N.
׀ ׀
Более активны линейные и циклические бораты: введение в этил-α-цианакрилат 0,1% триэтилбората обеспечивает склеивание стили в течение 10 с и возрастание ударной прочности изделий в 5 раз. Эффективность действия модификаторов общей формулы AX(O)nXBX(O)nXA, где А-алкильные, ацильные группы либо кислород- или серусодержащие гетероциклы:
\ \
B = ― CH2CH2 ―, C = O; X = ―O―, ―S―, N―CH3;
/ /
n=1- 40 обусловлена соответствием их химической природы.
Ингибиторами анионной полимеризации α-циано-крилатов могут быть кислоты, обладающие дегидратирующим действием. Избыточное содержание воды в этих мономерах отрицательно сказывается на прочности (рис.2) и долговечности (рис.3) адгезионных соединений.
Влияние большинства протонных кислот сводится к замедлению процесса поляризации молекул α-цианакрилатов, чем и объясняется их применение в качестве ингибиторов. Исключение составляют лишь наиболее сильные кислоты – соляная, фтористоводородная, фосфорная.
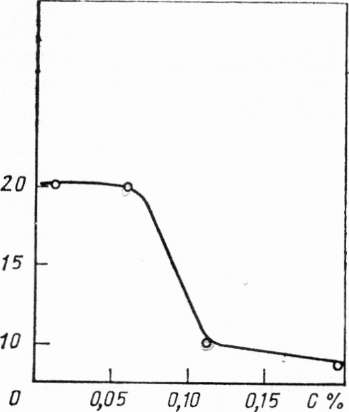
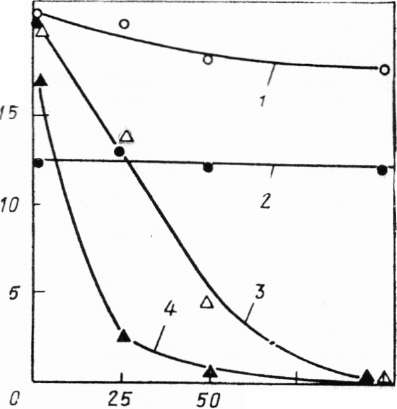
Рис. 2. Зависимость сопротивления сдвигу адгезинных соединений сплава алюминия Д16 при 323К от концентрации воды в метил-α-цианакрилате
Рис.3. Влияние концентрации воды в метил и n-третбутил α-цианакрилатах (темные точки) на кинетику изменения сопротивления сдвигу адгезионных соединений сплава алюминия Д16
(/, 2 — 0,008 %,3, 4 — 0,056 %)
Переход к бифункциональным модификаторам например к бистриметилсилилсульфату, увеличивает стабильность метил α-цианакрилата вдвое по сравнению с применением исходной метансульфоновой кислоты при 350К Подобные соединения могут иметь не только линейное, но и циклическое строение, когда
R + R' = С —C 6 H4-x R"x; R" = —NO2, —CyH2y+ 1,—OCyH2y+1; | |
O O
х = 0 — 3; у =1 - 4 Поэффективности к ним приближаются образующиеся при взаимодействии сульфурилдинзоцианата с карбоновыми кислотами органосульфамиды
RC (О) N (Н)—SO2—N (Н)С (O)OR, в молекулах которых R = — СхН2x+1 , —CF3, —CCI3, —С6Н5; х = 1—8. Действие даже наиболее сильных кислот типа серной может быть про-мотировано продуктами, гидролизуемыми в среде ингиби-тора. К их числу принадлежат, например, таннины, образу-ющие в сернокислотных растворах смесь галловой эллаговой и преимущественно дубильной кислот. Введение в этил-α-цианакрилат 0,1 % последней из них, содержащей следы гид-ролизующего агента, повышает сопротивление адгезионных соединений стали сдвигу с 13,9 до 19,5 МПа
Ангидриды многоосновных кислот способны дополни-тельно повышать температуростойкость адгезивов: введение в изопропил-α-цианакрилавсего 0,5 % ангидрида бензофено-тетракарбоновой кислоты повышает сопротивление адгезионных соединений стали сдвигу при 423 К с 1,7 до 16,5 МПа через 1 ч и с 3,7 до 13,3 МПа через 5 ч.
Диоксид серы широко используется в большинстве технологических процессов синтеза α-цианакрилатов. Достаточный эффект ингибирования анионной полимеризации данных мономеров обеспечивают незначительные его количества — от 5-10-5[381] до 3• 10-3 % Даже при минимальной концентрации сернистого ангидрида этил-а-цианакрилат сохраняет стабильность при 333 К в течение 50 сут, однако за более длительный срок прочность адгезионных соединений закономерно уменьшается вследствие удаления ингибитора из мономеров (рис.3). Действие этого ингибитора промотируют любые сильные кислоты с рH от 7 до 12, например фосфоновые, фосфористые, что используется при защите соответ-ствующими растворами внутренних поверхностей полиэтиленовых емкостей для хранения α-цианакрилатных клеев их доступные азотсодержащие производные — окси- и фенилзамещенные, фосфазены.
Близкий эффект обеспечивает применение в качестве промоторов фторированных спиртов, отличающихся от незамещенных повышенной степенью кислотности. Их вводят в композиции в несколько больших количествах. Так, при концентрации 0,002 % трифтометилэтанол практически равноценен по активности мегансульфоновой кислоте. Наиболее оправдано усиление ингибирующих свойств диоксида серы его различными источниками, прежде всего сульфонами в качестве ингибиторов анионной полимеризации цианакрилатов предложен новый класс продуктов - эфиры, способные к включению различных молекул во внутреннюю полость макроциклов. Подобные эффекты в принципе известны для защиты других соединений, однако в данном случае для сокращения требуемой скорости отверждения адгезива необходимо обеспечить пониженную стойкость лиганда. С учетом этого требования, а также для соблюдения соответствия геометрических размеров молекул рекомендуют использовать 1,1-диметилсилан в количестве 0,5 %.
Поскольку в состав макроциклических продуктов могут быть введены самые различные заместители, их следует рассматривать как перспективные модификаторы цианакрилатных адгезивов.
Важной группой наполнителей являются мелкодисперсные металлы, введение которых в α-циана-крилаты сообщает адгеивам токопроводимость. Для этой цели используют хром, платину, золото, но чаще всего серебро.
Так, наполнение метил- и этил-α-цианакрилатов короткими металлическими волокнами повышает удельное объемное электрическое сопротивление адгезивов до 104 Ом/см, не изменяя скорости образования и прочности адгезионных соединений. Адгезионную способность Так, наполнение метил- и этил-α-цианакрилатов короткими металлическими волокнами повышает удельное объемное электрическое сопротивление адгезивов до 104 Ом/см, не изменяя скорости образования и прочности адгезионных соединений. Адгезионную способность металлических порошков повышают их кислотным травлением металлических порошков повышают их кислотным травлением
Диэлектрические характеристики цианокрилатных клеев регулируют наполнением не только металлами, но и техни-
ческим углеродом. При этом возникает та же проблема дегидратации поверхности наполнителя. В данном случае для связывания воды, способствующей полимеризации
α-цианокрилатов, рекомендуют использовать трихлорид или трифторид бора.
Итак, модификация α-цианокрилатов позволяет направленно регулировать их характеристики (вплоть до специфичных, типов огнестойкости, которым можно обеспечивать введением 0,0001—0,05% полифеноксифосфазенов.
Адгезионные свойства различных α-цианакрилатных клеев весьма близки друг к другу. В этом убеждает сопоставление основных характеристик наиболее распространенных зарубежных и отечественных адгезивов. Действительно, несмотря на различие в химической природе заместителей в эфирной группе и вспомогательных добавок, α-цианакрилатные клеи различаются лишь вязкостью и скоростью отверждения и в несколько большей степени — температурным интервалом эксплуатации. Следовательно, их рациональный выбор обусловлен главным образом требованиями долговечности конкретных изделий и определяются технологией и режимами применения клеевых композиций.
Литература
1. Привалко В.П Молекулярное строение и свойства полимеров. Химия, 1986.- 134 с.
2. Вакула В.А., Притыкин А.М. Физическая химия полимеров. М: Химия, 1984.- 222 с.
3. Подстригач Я.С. Введение в механику поверхностных явлении в деформируемых твердых телах. Киев, 1995.– 200 с.
4. Прыткин Л.М., Кардашов Д.А., Вакула В.А. Мономерные клеи. М.: Химия, 2008.- 176 с.
Воронежский государственный технический университет
УДК 502
И. А. Ходякова, Т. А. Бондарева, И. М. Винокурова
Проблема эвтрофикации и пути ее решения
Рассматриваются вопросы биологического загрязнения водоемов и методы воздействия на эвтрофикацию
В результате использования воды для хозяйственно-бытовых и промышленных нужд образуется большое количество сточных вод, содержащих минеральные и органические соединения. Загрязнение минеральными соединениями обычно представлено в виде песка, частиц глины, руды, шлака, минеральных солей, растворов кислот, щелочей и других веществ.
Органическое загрязнение по своему происхождению подразделяется на растительное и животное. Растительные органические соединения — это остатки растений, плодов, овощей, злаков, бумаги и т. д. Загрязнением животного происхождения могут быть физиологические выделения людей и животных, остатки погибших животных, клеевые вещества.
К биологическому загрязнению относится загрязнение различными микроорганизмами, например грибами, мелкими водорослями и бактериями (как сапрофитами, так и паразитами). Это загрязнение поступает в водоем в основном с бытовыми сточными водами и со стоками таких промышленных предприятий, как бойни, кожевенные заводы, фабрики первичной обработки шерсти, меховые, предприятия микробиологической промышленности. Кроме того, на поверхности водоема могут появляться плавающие вещества. Попадающее в водоем загрязнение вызывает изменение физических и органолептических свойств воды: прозрачности, цветности, запаха и привкуса. Изменяется и химический состав воды, так как в ней появляются вещества, изменяющие активную реакцию воды и увеличивающие содержание органических и неорганических соединений. Загрязнение органического происхождения требует для своего окисления большого количества кислорода, что, в свою очередь, уменьшает содержание растворенного в воде кислорода. Изменяются количество и виды микроорганизмов, а иногда появляются и болезнетворные.
В водоемы сбрасываются отходы городских предприятий, фекально-хозяйственные сточные воды, атмосферные осадки и смываемые ими различные загрязняющие вещества.
Эвтрофикацией называется процесс ухудшения качества воды из-за избыточного поступления в водоем так называемых «биогенных элементов», в первую очередь соединений азота и фосфора. Эвтрофикация — нормальный природный процесс, связанный с постоянным смывом в водоемы биогенных элементов с территории водосборного бассейна. Однако в последнее время на территориях с высокой плотностью населения или с интенсивно ведущимся сельским хозяйством интенсивность этого процесса увеличилась многократно из-за сброса в водоемы коммунально-бытовых стоков, стоков с животноводческих ферм и предприятий пищевой промышленности, а также из-за смыва избыточно внесенных удобрений.
Механизм воздействия эвтрофикации на экосистемы водоемов следующий.
1. Повышение содержания биогенных элементов в верхних горизонтах воды вызывает бурное развитие растений в этой зоне (в первую очередь фитопланктона, а также водорослей – обрастателей) и увеличение численности питающегося фитопланктоном зоопланктона. В результате прозрачность воды резко снижается, глубина проникновения солнечных лучей уменьшается, и это ведет к гибели донных растений от недостатка света. После отмирания донных водных растений наступает черед гибели прочих организмов, которым эти растения создают места обитания или для которых они являются вышерасположенным звеном пищевой цепи.
2. Сильно размножившиеся в верхних горизонтах воды растения (особенно водоросли) имеют намного большую суммарную поверхность тела и биомассу. В ночные часы фотосинтез в этих растениях не идет, тогда как процесс дыхания продолжается. В результате в предутренние часы теплых дней кислород в верхних горизонтах воды оказывается практически исчерпанным, и наблюдается гибель обитающих в этих горизонтах и требовательных к содержанию кислорода организмов (происходит так называемый «летний замор») см. рисунок.

Вертикальное изменение концентрации кислорода при одинаковой температуре в озерах:
a) – олиготрофных; б – эвтрофиных
3. Отмершие организмы рано или поздно опускаются на дно водоема, где происходит их разложение. Однако, как мы отметили в пункте 1, донная растительность из-за эвтрофикации погибает, и производство кислорода здесь практически отсутствует. Если же учесть, что общая продукция водоема при эвтрофикации увеличивается (см. пункт 2), между производством и потреблением кислорода в придонных горизонтах наблюдается дисбаланс, кислород здесь стремительно расходуется, и все это ведет к гибели требовательной к кислороду донной и придонной фауны. Аналогичное явление, наблюдающееся во второй половине зимы в замкнутых мелководных водоемах, называется «зимним замором».
4. В донном грунте, лишенном кислорода, идет анаэробный распад отмерших организмов с образованием таких сильных ядов, как фенолы и сероводород, и столь мощного «парникового газа» (по своему эффекту в этом плане превосходящего углекислый газ в 120 раз), как метан. В результате процесс эвтрофикации уничтожает большую часть видов флоры и фауны водоема, практически полностью разрушая или очень сильно трансформируя его экосистемы, и сильно ухудшает санитарно-гигиенические качества его воды, вплоть до ее полной непригодности для купания и питьевого водоснабжения (таблица).
Общие характеристики олиготрофных и эвтрофных озер
|
Олиготрофные |
Эвтотрофные |
Глубина |
Глубокие |
Мелкие |
Содержание кис-лорода в гиполи-мнионе летом |
Содержится |
Не содержится |
Водоросли и цианобактерии |
Высокое видовое разнообразие при низких популяционной плотнос-ти и продуктивности; часто доминируют зеленые водоросли |
Низкое видовое разно-образие при высоких популяционной плот-ности и продуктивнос-ти; часто доминируют цианобактерии |
Водорослевое цветение |
Редко |
Часто |
Поток питательных веществ через автотрофов |
Слабый |
Сильный |
Продуктивность животных |
Низкая |
Высокая |
Рыба |
Часто доминируют лососевые и сиговые |
Часто доминируют малоценные виды |
При экологической оценке гидроэкосистемы одним из наиболее информативных объектов изучения являются донные отложения. Аккумулируя загрязнения, которые поступают в водоём на протяжении продолжительного периода, донные отложения являются индикатором экологического состояния территории, своеобразным интегральным показателем уровня загрязненности.
Донные отложения представляют собой неразрывное единство сложного комплекса минералов и водного раствора, который пропитывает отложения. Именно этот водный раствор физически и химически объединяет совокупность дискретных зёрен, минеральных фаз и органических остатков в целостную систему. Благодаря нему, через его посредство осуществляется многостороннее взаимодействие её частей. В нём и на поверхностях его раздела с твердыми частицами протекают разнообразные химические реакции, происходит перенос и перераспределение растворенных компонентов. В водном растворе и на поверхности зерен живет донная микрофлора, которая осуществляет важное влияние на протекание химических процессов в донных отложениях и жизнедеятельность организмов зообентоса.
При накоплении донных отложений (заилении) изменяются морфометрические показатели водоёмов, химические и биологические процессы. Процессы, которые происходят в донных отложениях и придонном пласте воды приводят к изменениям состава воды, а также её оптических свойств.
Это приводит к коренному изменению экологического состояния водотоков, которое, в частности, обусловлено формированием в них протяжных и комплексных по составу геохимических аномалий, которые наиболее полно проявляются в современных русловых отложениях. Образование техногенных отложений обусловлено изменением условий формирования твердого стока рек и поступлением в водные объекты значительных масс твердого материала, который имеет специфические геохимические свойства.
В геологических масштабах времени водоемы постепенно обогащаются биогенами и заполняются поступающими с суши наносами. Таким образом, их эвтрофикация становится составной частью естественного процесса, называемого сукцессией. Люди своей деятельностью значительно ускоряют этот процесс. За несколько десятилетий они приводят к изменениям, которые в природных условиях проходили бы тысячи лет, поэтому разделяют антропогенную и естественную эвтрофикацию.
Существует два основных подхода для борьбы с эвтрофикацией:
1. Борьба против ее симптомов: развития водорослей и (или) снижения уровня растворенного кислорода;
2. Устранение ее причины: чрезмерное поступление наносов и биогенов.
Часто используют 1-й способ, но успех сомнителен и дорогостоящий. Например, для устранения нежелательных растений в водоемах успешно применяют гербициды. Еще в 70-х и 80-х годах в пруды и озера сброшены тысячи тонн химикатов, оказалось, что они не всегда помогают. Если сбросить в водоем количество химикатов, достаточное для уничтожения водорослей, то все живое в нем погибнет. Если же понизить концентрацию гербицидов, то в первую очередь, появятся планктонные водоросли. Для поддержания в водоеме содержания растворенного кислорода на достаточно высоком уровне часто используют аэрацию (систему механической подачи воздуха). При аэрации может также сократиться содержание в воде фосфатов, т.к. они переходят в нерастворимую форму. Однако аэрация, особенно крупных водоемов требует значительных энергетических затрат. Поэтому 2-й способ борьбы с эвтрофикацией более эффективен, для него необходимо выявить источники притока наносов и биогенов, а затем применить экономические эффективные методы контроля за ними. Источником наносов является почвенная эрозия. Биогены, например, нитраты, фосфаты и калий ионы, прикрепляются к частичкам глины и гумуса и сопутствуют наносам.
Меры борьбы с эвтрофикацией: противоэрозионные и биолого-технические мероприятия по защите склонов водоемов, контроль за отходами на стройплощадках и в горном деле, охрана болот, запрещение использования фосфатных детергентов, усиление очистки канализационных стоков.
Литература
А.С. Маршалкович, М.И. Афонина, М.И. "Экология ", Москва, 2009. 220 с.
Материалы конференции памяти Н.Н. Воронцова, Изд. отд. УНЦДО 2001 "Эволюция, экология, биоразнообразие". 160 с.
Воронежский государственный технический университет
УДК 630. 42
О.Н. Болдырева

 осударственный
технический университет”, 2013
осударственный
технический университет”, 2013