
- •Методическое руководство
- •Предисловие
- •1. Скорость химических реакций. Химическое равновесие
- •2. Спецификация теста по теме “Скорость химических реакций. Химическое равновесие”
- •3. Варианты теста Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Библиографический список
- •394026 Воронеж, Московский просп., 14
- •Методическое руководство
Вариант 6
А 1. При повышении температуры с 30°С до 60°С скорость реакции увеличится в
исходных данных недостаточно для
получения ответа
1) 1,5 раза 2) 150 раз 3) 6 раз 4) 9 раз 5)
А 2. Повышение давления в системе
![]()
![]() приведет к
приведет к
1) увеличению концентрации ;
2) увеличению концентрации
![]() ;
;
3) смещению равновесия влево (←);
4) сохранению равновесия системы;
5) смещению равновесия вправо (→).
А 3. Скорость прямой реакции
![]() при повышении давления в 2 раза увеличится
в
при повышении давления в 2 раза увеличится
в
1) 4 раза 2) 24 раза 3) 48 раз 4) 128 раз 5) 144 раза
А 4. Константа равновесия реакции
![]()
![]() соответствует выражению
соответствует выражению
1)
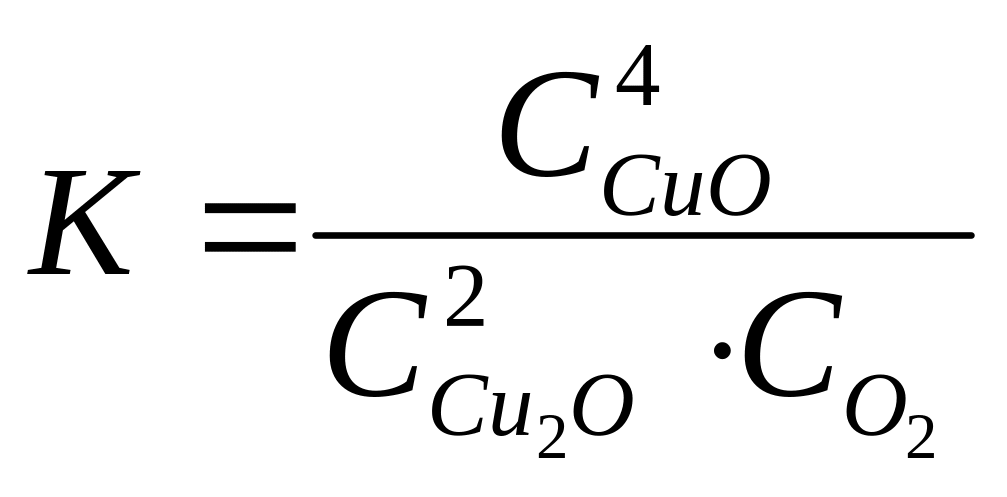 2)
2)
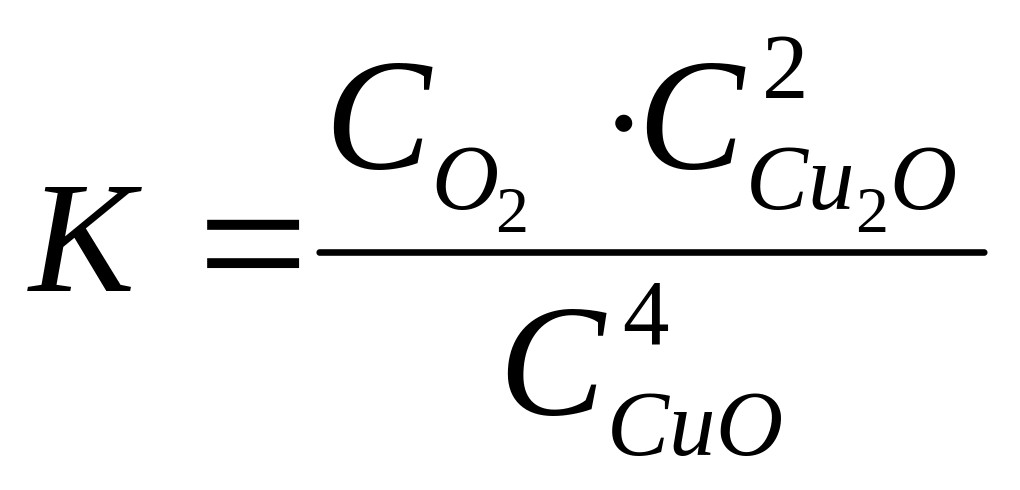 3)
3)
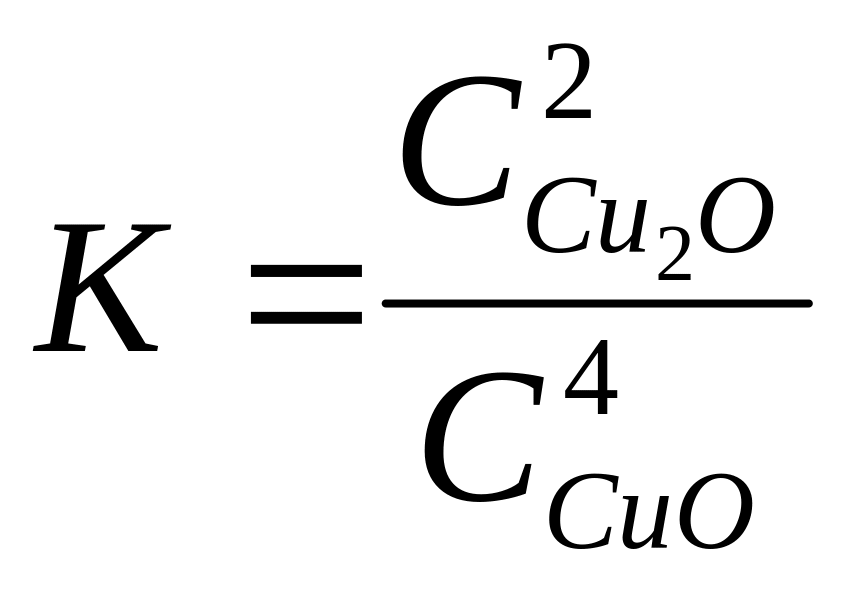
4)
![]() 5)
5)
![]()
А
5. Константа равновесия гомогенной
газообразной реакции
![]()
![]() при некоторой температуре равна 1. В
состоянии равновесия концентрации
веществ составили:
при некоторой температуре равна 1. В
состоянии равновесия концентрации
веществ составили:
![]()
![]() Начальная концентрация монооксида
углерода (моль/л) равна:
Начальная концентрация монооксида
углерода (моль/л) равна:
1) 0,01 2) 0,02 3) 0,03 4) 0,04 5) 0,05
Вариант 7
А 1. При повышении температуры на 40°С скорость реакции увеличилась в 256 раз. Температурный коэффициент скорости реакции ( ) равен
1) 2 2) 4 3) 6 4) 8 5) 16
А 2. Реакция, в которой повышение давления и понижение температуры вызовут смещение равновесия в одну сторону это
1
)
![]()
![]()
2
)
![]()
![]()
3
)
![]()
![]()
4
)
![]()
![]()
![]()
5
)
![]()
А 3. Скорость реакции
![]()
![]() при увеличении объема в 4 раза изменится
при увеличении объема в 4 раза изменится
1) уменьшится в 4 раза
2) увеличится в 4 раза
3) не изменится
4) увеличится в 16 раз
5) уменьшится в 16 раз
А 4. Математическое выражение скорости прямой реакции
имеет вид
1)
![]() 2)
2)
![]() 3)
3)
![]()
4)
![]() 5)
5)
![]()
А 5. В гомогенной газообразной реакции
![]()
![]() в состоянии равновесия концентрации
веществ равны
в состоянии равновесия концентрации
веществ равны
![]() Начальная концентрация
Начальная концентрация
![]() (моль/л) равна
(моль/л) равна
исходных данных недостаточно для
получения ответа
1) 10 2) 3) 7,7 4) 9 5) 11
Вариант 8
А 1. Скорость реакции уменьшится при
понижении температуры от 120°С до 80°С
при![]() в
в
1) 24 раза 2) 81 раз 3) 12 раз 4) 64 раза 5) 120 раз
А 2. Повышение температуры в системе
![]()
![]() приведет к
приведет к
1) увеличению концентрации
![]() ;
;
2) увеличению концентрации ;
3) смещению равновесия влево (←);
4) уменьшению концентрации
![]() ;
;
5) сохранению концентрации .
А 3. Скорость прямой реакции
при изменении концентрации
с 2 до 6 моль/л, а концентрации
![]() с 3 до 1 моль/л, изменится
с 3 до 1 моль/л, изменится
1) увеличится в 32 раза
2) увеличится в 36 раз
3) увеличится в 10 раз
4) увеличится в 8 раз
5) увеличится в 3 раза
А 4. константа равновесия реакции
![]()
![]() соответствует выражению
соответствует выражению
1)
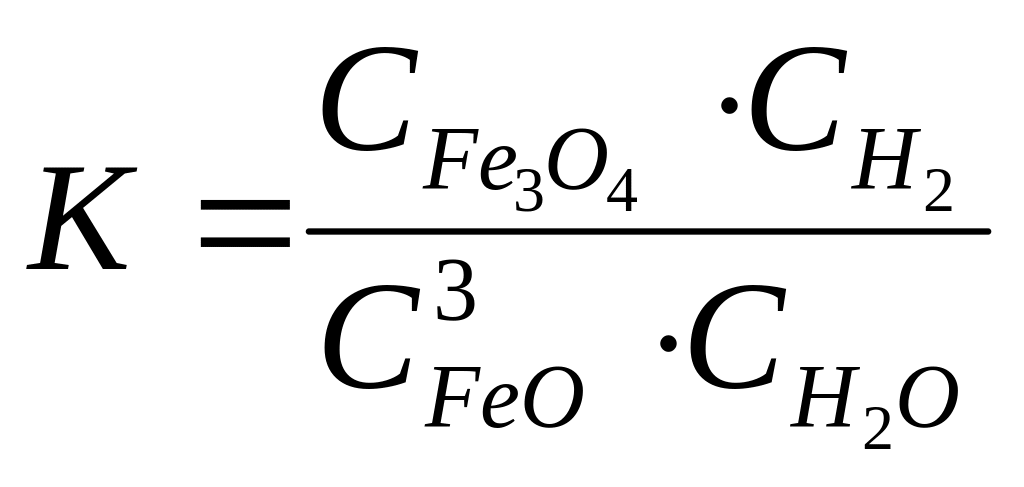 2)
2)
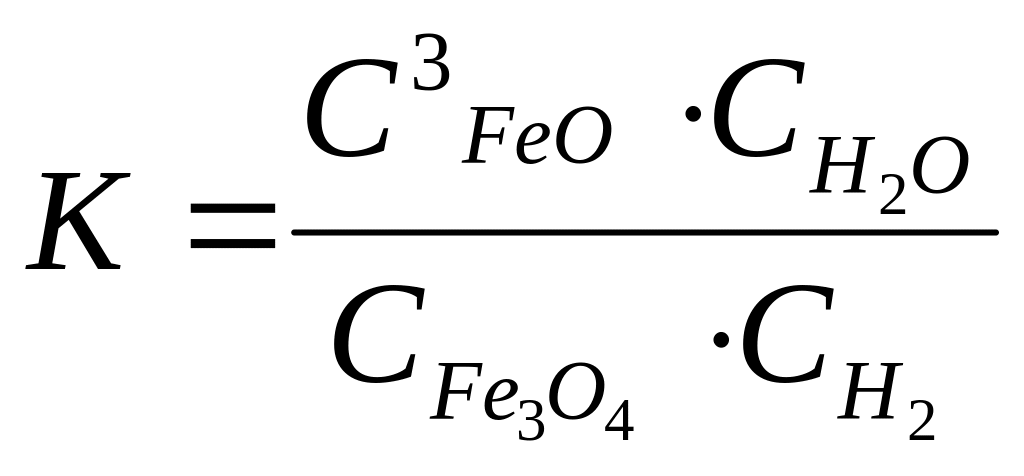 3)
3)

4)
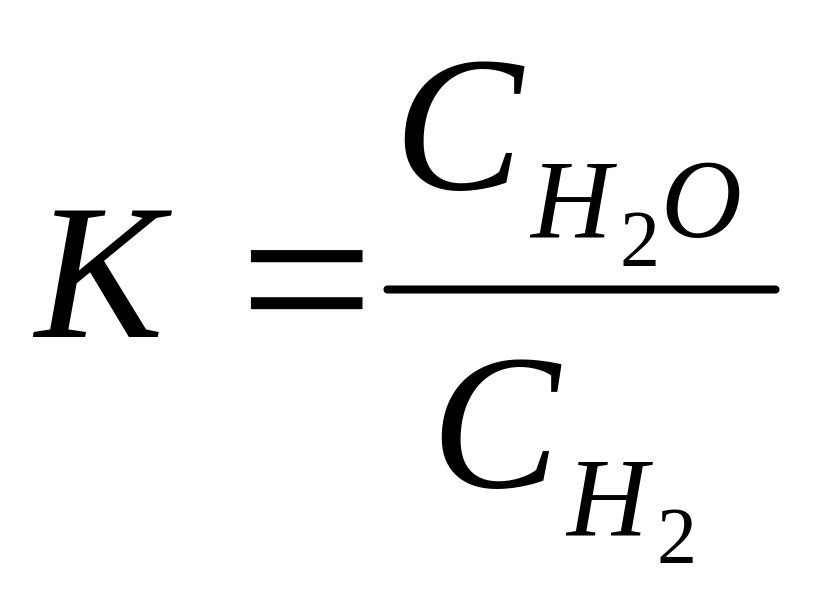 5)
5)
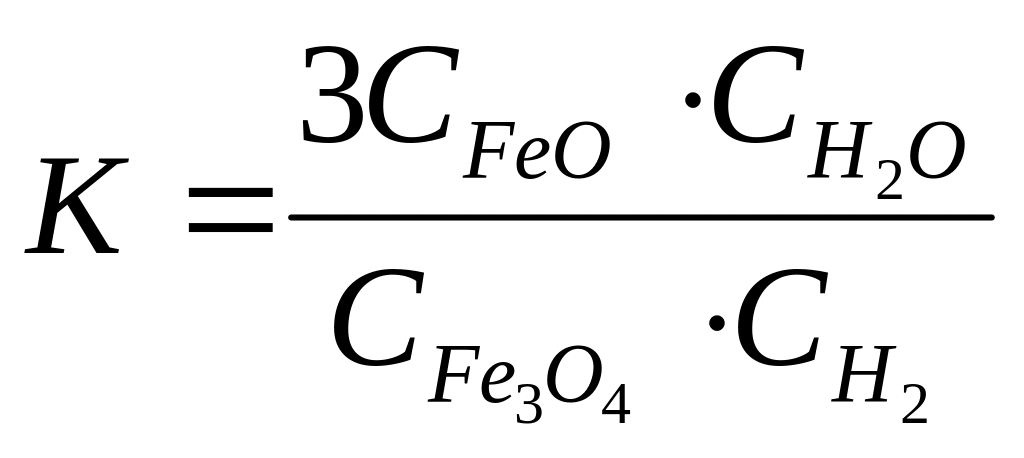
А 5. В состоянии равновесия в реакции
![]()
![]() концентрации равны
концентрации равны
![]() Исходная концентрация
(моль/л)
равна
Исходная концентрация
(моль/л)
равна
1) 8 2) 17 3) 1 4) 29 5) 49
