
- •Аналитическая химия
- •Авторский коллектив:
- •Рецензенты:
- •Введение
- •Глава 1 основы качественного анализа
- •1.1. Качественный анализ неорганических веществ
- •1.1.1. Аналитическая классификация катионов
- •1.1.2. Аналитическая классификация анионов
- •Вопросы для самоподготовки
- •Задачи для самостоятельного решения
- •Глава 2 количественный химический анализ
- •2.1. Сущность и характеристика
- •Гравиметрического метода анализа
- •2.1.1. Операции гравиметрического анализа
- •2.1.2. Отбор средней пробы и подготовка её к анализу
- •2.1.3. Расчет навески для анализа и взвешивание
- •2.1.4. Вскрытие навески
- •2.1.5. Устранение влияния мешающих компонентов
- •2.1.6. Осаждение определяемой составной части вещества в виде малорастворимого соединения
- •2.1.6.1. Механизм образования осадков
- •2.1.6.2. Влияние условий осаждения на структуру осадка
- •2.1.6.3. Причины загрязнения осадков
- •2.1.6.4. Старение осадков
- •2.1.7. Фильтрование и промывание осадков
- •2.1.7.1. Правила фильтрования
- •2.1.7.2. Промывные жидкости
- •2.1.7.3. Высушивание, прокаливание осадков
- •2.1.7.4. Техника получения гравиметрической формы и ее взвешивание
- •2.1.8. Расчет количества определяемого вещества
- •2.1.9. Метрологическая оценка результатов анализа
- •Математическая обработка результатов количественного анализа
- •Влияние отдельных ошибок на конечный результат
- •Значащие цифры
- •Определение гигроскопичной воды Материалы, оборудование и реактивы
- •Порядок выполнения работы
- •Определение SiO2 в силикате
- •Материалы, оборудование и реактивы
- •Порядок выполнения работы
- •Определение оксида серы so3
- •Материалы, оборудование и реактивы
- •Порядок выполнения работы
- •Определение полуторных оксидов Al2o3, Fe2o3, TiO2
- •Материалы, оборудование и реактивы
- •Порядок выполнения работы
- •Вопросы для самоподготовки
- •Задачи для самостоятельного решения
- •2.2. Сущность и характеристика титриметрического метода анализа
- •2.2.1. Стандартизация растворов титрантов
- •2.2.2. Основные приемы титрования
- •2.2.3. Расчеты в титриметрическом анализе Химический эквивалент
- •Расчет результата прямого титрования при разных способах выражения концентрации раствора
- •Расчет результата в методах обратного титрования
- •2.2.4. Кривые титрования
- •2.2.5. Основные методы титриметрического анализа
- •2.2.6. Кислотно-основное титрование
- •2.2.6.1. Рабочие растворы
- •2.2.6.2. Кривые титрования и выбор индикатора
- •100,0 Мл 0,1 н hCl 0,1 н раствором NaOh
- •100,0 Мл 0,1 м уксусной кислоты 0,1 м раствором NaOh
- •2.2.7. Комплексонометрическое титрование
- •Синий цвет
- •Посуда, приборы, реактивы
- •Порядок выполнения работы
- •2.2.8. Титрование по методу осаждения
- •2.2.8.1. Аргентометрия
- •2.2.8.2. Кривые титрования и способы обнаружения конечной точки титрования
- •Порядок выполнения работы
- •2.2.9. Окислительно-восстановительное титрование
- •2.2.9.1. Перманганатометрия
- •2.2.9.2. Способы обнаружения конечной точки титрования
- •Вопросы для самоподготовки
- •Задачи для самостоятельного решения
- •Глава 3 спектральные методы анализа
- •3.1. Принципы аналитической оптической спектроскопии
- •3.2. Основные узлы и приборы для аналитической оптической спектроскопии
- •3.3. Молекулярная абсорбционная спектроскопия
- •3.3.1. Основной закон светопоглощения - закон Бугера-Ламберта-Бера
- •Таким образом
- •3.3.1.1. Ограничения и условия применения закона Бугера-Ламберта-Бера
- •3.3.1.2. Аппаратура в молекулярной абсорбционной спектроскопии
- •3.4. Молекулярная спектроскопия в инфракрасном диапазоне (икс)
- •3.4.1. Задачи, решаемые инфракрасной спектроскопией
- •Лабораторная работа № 7
- •Цель работы
- •Теоретическая часть
- •Посуда, приборы, реактивы
- •Порядок выполнения работы
- •Вопросы для самоподготовки
- •Задачи для самостоятельного решения
- •Концентрация Оптическая
- •Глава 4 электрохимические методы анализа
- •4.1. Потенциометрические методы
- •4.1.1. Методы проведения потенциометрического анализа
- •4.1.2. Потенциометрическое титрование
- •Посуда, приборы, реактивы
- •Порядок выполнения работы
- •4.2. Кулонометрический анализ
- •4.2.1. Установка для кулонометрического титрования
- •4.3. Кондуктометрические методы анализа
- •4.3.1. Прямая кондуктометрия
- •4.3.2. Кондуктометрическое титрование
- •Выполнение кондуктометрических измерений с помощью учебно-лабораторного комплекса «Химия»
- •Посуда, приборы, реактивы
- •Порядок выполнения работы
- •Вопросы для самоподготовки
- •Задачи для самостоятельного решения
- •Глава 5 хроматографические методы анализа
- •5.1. Хроматографические параметры
- •5.2. Обработка хроматограмм
- •5.3. Жидкостная хроматография
- •5.4. Газовая хроматография
- •5.5. Тонкослойная хроматография (тсх)
- •5.5.1. Параметры тонкослойной хроматографии
- •5.5.2. Количественные характеристики эффективности разделения в тсх
- •Посуда, приборы и реактивы
- •Порядок выполнения работы
- •Посуда, приборы и реактивы
- •Порядок выполнения работы
- •Вопросы для самоподготовки
- •Задачи для самостоятельного решения
- •Глава 6 микроскопические методы исследования
- •6.1. Принцип работы и конструкция сзм NanoEducator
- •6.2. Техническая спецификация оборудования NanoEducator
- •Посуда, приборы и реактивы
- •Порядок выполнения работы
- •Вопросы для самоподготовки
- •Заключение
- •Библиографический список Основная литература
- •Дополнительная литература
- •3 94006 Воронеж, ул. 20-летия Октября, 84
Глава 5 хроматографические методы анализа
Хроматография - метод разделения смесей газов, жидкостей, растворенных веществ путем сорбции в динамических условиях. В простейшем варианте разделение происходит при прохождении потока анализируемой смеси через колонку, содержащую сорбент. Вследствие различной сорбируемости компонентов смеси достигается их разделение по высоте сорбента при повторяющихся циклах сорбция-десорбция.
Классификация хроматографических методов. Известно несколько подходов к классификации методов хроматографии с использованием различных признаков:
по средам, в которых проводится разделение (жидкостная, газожидкостная, газовая);
по механизму разделения (молекулярная или адсорбционная, ионообменная, осадочная, комплексообразовательная, окислительно-восстановительная);
по форме проведения процесса (колоночная, капиллярная, хроматография на бумаге и в тонком слое);
по способу проведения процесса (фронтальная, вытеснительная, проявительная).
В табл. 5.1 хроматографические методы классифицированы по подвижным и неподвижным фазам, форме проведения процесса и механизму разделения.
Каждый хроматографический метод по мере развития сопровождался возникновением новых вариантов. Например, адсорбционная и распределительная хроматография осуществляются на колонках, фильтровальной бумаге, в тонком слое сорбента, нанесенном на стеклянную пластинку; колонки могут иметь различную форму и конструкцию. В зависимости от этих факторов различают следующие варианты: колоночная, хроматография на бумаге, хроматография в тонком слое.
Таблица 5.1
Классификация хроматографических методов
Методы хроматографии |
Подвижная фаза |
Неподвижная фаза |
Форма проведения |
Механизм разделения |
Газоадсорбционная |
газ |
твердая |
колонка |
адсорбционный |
Газожидкостная |
газ |
жидкость |
колонка |
распределительный |
твердожидкостная |
жидкость |
твердая |
колонка |
адсорбционный |
жидкостно-жидкостная |
жидкость |
жидкость |
колонка |
распределительный |
ионообменная |
жидкость |
твердая |
колонка |
ионный обмен |
Гель-хроматография |
жидкость |
жидкость |
колонка |
по размерам молекул |
Хроматография в тонком слое |
жидкость |
твердая |
тонкий слой |
адсорбционный |
Хроматография в тонком слое |
жидкость |
жидкость |
тонкий слой |
распределительный |
Хроматография на бумаге |
жидкость |
жидкость |
бумага |
распределительный |
5.1. Хроматографические параметры
В зависимости от контекста под хроматографией понимается наука, процесс или метод.
К основным хроматографическим параметрам относят нижеперечисленные понятия.
Хроматография – наука о межмолекулярных взаимодействиях и переносе молекул или частиц в системе несмешивающихся и движущихся относительно друг друга фаз.
Хроматография – процесс дифференцированного многократного перераспределения веществ или частиц между несмешивающимися и движущимися относительно друг друга фазами, приводящий к обособлению концентрационных зон индивидуальных компонентов исходных смесей этих веществ или частиц.
Хроматография – метод разделения смесей веществ или частиц, основанный на различии в скоростях их перемещения в системе несмешивающихся и движущихся относительно друг друга фаз.
Аналит – определяемый компонент пробы, в случае аналитической жидкостной хроматографии – это определяемый сорбат.
Аналитическая хроматография - хроматография, используемая для качественного анализа смеси и (или) количественного определения отдельных компонентов смеси.
Время удерживания вещества, TR – время пребывания исследуемого вещества в хроматографе.
Высокоэффективная жидкостная хроматография (ВЭЖХ) – колоночная хроматография, в которой применяют сорбенты с размером частиц 3 - 10 мкм, в результате чего резко возрастает эффективность хроматографического разделения.
Мертвый объем, Vм – объем подвижной фазы ПФ между точкой ввода пробы и точкой ее обнаружения. Мертвый объем включает в себя свободный объем колонки, объемы устройства ввода пробы (дозатора), детектора, а также объемы коммуникаций между ними.
Модификатор – растворитель, входящий в состав ПФ, который для выбранного варианта жидкостной хроматографии обладает большей элюирующей силой, чем базовый растворитель (разбавитель).
Колонка – трубка, наполненная сорбентом, в объеме которого осуществляется хроматографическое разделение смеси веществ.
Константа распределения вещества, Кс – отношение объемных концентраций вещества (или определенной его формы) в неподвижной и подвижной фазах в условиях равновесия.
Коэффициент асимметрии As – отношение двух отрезков, образуемых на горизонтальной линии, проведенной на высоте 10 % от основания пика, при ее пересечении с вертикалью, опущенной из вершины пика. При этом берется отношение «тыльного» отрезка к «фронтальному» (рис. 5.1).
AS=A/B (5.1)
Неподвижная фаза (НФ) – твердый сорбент, на котором осуществляется дифференцированное удерживание и разделение компонентов смеси.
Нормально-фазовая хроматография (НФХ) – жидкостная хроматография, в которой неподвижная фаза более полярна, чем подвижная.
Обращенно-фазовая хроматография – жидкостная хроматография, в которой неподвижная фаза менее полярна, чем подвижная. Это вариант распределительной жидкостной хроматографии, в котором используют сорбенты с привитыми неполярными группами и полярные ПФ.
Объем удерживания вещества, VR – объем ПФ, затрачиваемой на элюирование пробы вещества. VR определяют между точкой ввода пробы и точкой, при которой регистрируется максимум сигнала детектора.
Подвижная фаза (ПФ) - поток жидкости, перемещающий компоненты разделяемой смеси вдоль неподвижной фазы. Этим термином обозначают так же одно- и многокомпонентные растворители, применяемые для создания потока жидкости.
Разрешение пиков, Rs – расстояние между максимумами выбранных соседних пиков, деленное на полусумму их ширин у основания (выраженных в одних и тех же единицах измерения)
Rs=2(tR2-tR1)/(Wb1+Wb2) (5.2)
Разбавитель – базовый растворитель для выбранного варианта ЖХ, обладающий минимальной элюирующей силой среди компонентов, входящих в состав ПФ.
Свободный объем, Vo – часть объема колонки, не занятая сорбентом.
Селективность хроматографической системы – избирательность, способность к специфическим взаимодействиям подвижной и неподвижной фазы с молекулами сорбата, обладающими определенными структурными признаками, приводящая к разной скорости перемещения концентрационных зон индивидуальных компонентов.
Сорбат – вещество, удерживаемое сорбентом, компонент хроматографически разделяемой смеси.
Сорбент – твёрдое вещество, жидкость или их смеси, способные поглощать или удерживать растворенные вещества и используемые в хроматографии в качестве неподвижной фазы.
Хроматограмма – записанная во времени функция концентрации определяемых веществ в ПФ на выходе из колонки.
Хроматограмма – наглядное изображение результатов разделения компонентов исходной смеси в планарной хроматографической системе (в тонком слое сорбента, на бумаге и т.д.).
Хроматографическая система – совокупность несмешивающихся и движущихся относительно друг друга фаз с развитой межфазной границей (поверхностью). По нашему мнению, в хроматографическую систему следуют включить и сорбат, так как при его отсутствии нет хроматографического процесса.
Хроматографический тракт – путь, по которому происходит перемещение ПФ от резервуара для элюента, через насос, дозатор, предколонку, колонку, детектор и приемник элюата, соединенных друг с другом посредством фитингов и капилляров.
Фактор удерживания (коэффициент емкости), k – безразмерная величина, характеризующая удерживание вещества и равная отношению чистого объема удерживания к свободному объему колонки
k = VN/Vo. (5.3)
Фактор удерживания k можно определить как частное от деления массы вещества в НФ на массу вещества в ПФ
k= mНФ/mПФ (5.4)
Величина k связана с коэффициентом распределения К в данной системе (отношение концентраций сорбата в НФ к его концентрации в ПФ) и свободной энергией сорбции ΔG
k =Kβ = βe-(ΔG/RT) , (5.5)
где β – фазовое отношение колонки.
Элюент – жидкость, используемая в качестве подвижной фазы.
Элюирующая сила (способность) – свойство подвижной фазы вступать в такие межмолекулярные взаимодействия с компонентами хроматографической системы, которые способствуют десорбции хроматографируемых соединений, более быстрому перемещению концентрационных зон индивидуальных компонентов исходных смесей.
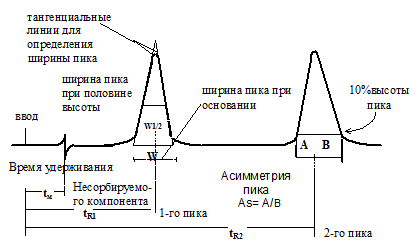
Р ис.
5.1.
Основные хроматографические параметры:
ис.
5.1.
Основные хроматографические параметры:
tM – время удерживания несорбируемого соединения; tR1 и tR2 – абсолютные времена удерживания компонентов 1 и 2, tW1 и tW2 – ширина пика у основания, выраженная в единицах времени; а и В – отрезки, образуемые на горизонтальной линии, проведенной на высоте 10 % от основания пика,
при ее пересечении с вертикалью, опущенной из вершины пика
Элюотропный ряд – серия чистых или смешанных растворителей, приведенных в порядке возрастания их элюирующей способности в выбранной хроматографической системе.
