
Методическое пособие 508
.pdf
4. Математическое выражение второго закона термодинамики для бесконечно малого изменения состояния в обратимом и необратимом процессах в изолированной системе имеет вид:
dS
1) |
обратимый процесс |
0 |
; |
dS
0
, необратимый процесс
2)обратимый процесс dS dHT , необратимый процесс dS dHT ;
3)обратимый процесс dS TQ , необратимый процесс dS TQ ;
4) обратимый процесс dS TQ , необратимый процесс dS TQ .
5. Для графического расчѐта теплоты испарения жидкости при заданной температуре используется следующий график и расчѐтная формула:
1) |
|
|
|
|
|
|
2) |
|
|
|
|
|
|
P |
|
|
|
|
|
ln |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
α |
|
|
||
|
|
|
|
α |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
tg RT2 |
T |
|
Hèñï |
Rtg |
1 |
|
|||
|
исп |
|
T |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
60 |
|
|
|
|
|
|
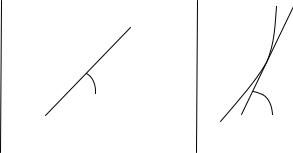
3) |
|
|
|
4) |
P |
|
|
||||||
lnP |
|
|
|
|
|
|
|
||||||
|
|
α |
|
|
|
|
|
|
|
α |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Hисп RTtg |
1 |
1 |
|
|
|
Hисп tg |
RT2 |
T |
||||
|
|
|
T |
|
|
|
|
||||||
|
T |
|
P |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||
6. Давление насыщенного пара над твѐрдым телом зависит от температуры так:
1)при увеличении температуры может и расти, и падать в зависимости от природы вещества;
2)не зависит от температуры;
3)растѐт при увеличении температуры;
4)падает при увеличении температуры.
ВАРИАНТ 5
1. Величина G процесса при переходе от начального состояния к конечному, если его сначала провести обратимо, а затем необратимо, изменяется так:
1)сначала растѐт, а затем падает;
2)увеличивается;
3)не изменяется;
4)уменьшается.
2. Повышение температуры влияет на изменение изобар- но-изотермического потенциала G в ходе химической реакции следующим образом:
1) с ростом температуры G реакции всегда падает; 61
2) в зависимости от природы реакции и интервала температур G реакции может расти, падать или не меняться с ростом температуры;
3) с ростом температуры G реакции всегда растѐт; 4) G реакции не зависит от температуры.
3.Изменение энтропии системы не происходит при обратимом протекании следующего процесса:
1) изотермического;
2) изобарического;
3) адиабатического;
4) изохорического.
4.Изменение энтропии процесса равно работе этого процесса в следующих случаях:
1) в процессах, протекающих в изолированной системе; 2) никогда не равна работе, так как энтропия – не термо-
динамический потенциал; 3) всегда равно работе, так как энтропия – характеристи-
ческая функция; 4) в обратимых процессах.
5.Изменение температуры плавления с ростом давления
таково:
1) может расти, а может падать, характер зависимости определяется природой вещества;
2) растѐт;
3) падает; 4) в области малых давлений растѐт, а в области высоких
давлений падает.
6.Уравнение зависимости теплоты испарения ртути от температуры (в Дж/моль) имеет следующий вид, если зависимость давления насыщенного пара ртути от температуры можно выразить уравнением
62
lg P |
3276 |
0,652lgT 9,9 |
|||||
T |
|||||||
|
|
|
|
|
|
||
1) |
Hисп 9,9 0,781T |
; |
|
||||
2) |
Hисп 8276 |
0,652 |
; |
||||
T |
|
||||||
|
|
|
|
|
|
||
3) |
Hисп 6500 1,29T |
; |
|
||||
:
4) Hисп 62600 5,41T .
ВАРИАНТ 6
1. В условиях постоянства температуры и объѐма в качестве критерия самопроизвольного протекания процесса следует выбрать термодинамический потенциал:
1)внутреннюю энергию U ;
2)энергию Гиббса G ;
3)энергию Гельмгольца F ;
4)энтальпию H .
2. Зависимость изобарно-изотермического потенциала от давления в дифференциальной форме (при условии, что температура остаѐтся постоянной и система не совершает никакой работы, кроме работы расширения) имеет следующее математическое выражение:
1) |
|
G |
S ; |
|
|
||
|
|
P T |
|
2) |
|
G |
S ; |
|
|
||
|
|
P T |
|
3) |
|
G |
V ; |
|
|
||
|
|
P T |
|
4) |
|
G |
V . |
|
|
||
|
|
P T |
|
63

3. Между некоторым исходным состоянием I и конечным состоянием II осуществляются два перехода. Один из них протекает обратимо, другой – необратимо. Известны тепловые
эффекты этих процессов
Qобр. и Qнеобр. , причѐм,
Qобр.
Qнеобр.
.
Соотношение между изменением энтропии процессе имеет вид:
S
в том и другом
1)Sобр. Sнеобр. ;
2)Sобр. Sнеобр. ;
3)соотношение между может быть различным в зависимости от конкретных условий протекания процесса;
4)Sобр. Sнеобр. .
4. Равновесная система состоит из трѐх частей, каждая из которых обладает определѐнной энтропией. Энтропия системы
вцелом имеет вид:
1)S 3 S1 S2 S3 ;
S1 S2 S3 ;
2)S S1 S2 S3 ;
3)S S1 S2 S3 ;
4)S S1 S2 S3 .
3
5. Изменение температуры плавления вещества при повышении давления, если имеется зависимость давления насыщенного пара над твѐрдым веществом от температуры (в виде уравнения P f (T) или графика в координатах P T ), можно
рассчитать:
1) путѐм дифференцирования уравнения или по графику найти величину dTdP , так как обратная величина есть зависимость температуры плавления от давления;
64
2)температура плавления не зависит от давления, поэтому достаточно определить еѐ при любом давлении;
3)по этим данным рассчитать нельзя, необходимо знать теплоту плавления и значения плотностей жидкой и твѐрдой фаз;
4)по этим данным рассчитать нельзя, нужны данные о зависимости теплоѐмкостей твѐрдой и жидкой фаз от температуры.
6. Под давлением 26,6·103 Н/м2 циклогексан и этилацетат кипят при одинаковой температуре. При нормальном давлении температура кипения циклогексана выше температуры кипения этилацетата на 3,6 º, так как:
1)теплота испарения циклогексана больше теплоты испарения этилацетата;
2)молекулярная масса циклогексана меньше молекулярной массы этилацетата;
3)изменение температуры мало, возможно, это – ошибка эксперимента;
4)теплота испарения этилацетата больше теплоты испарения циклогексана.
ВАРИАНТ 7
1. Зависимость энергии Гельмгольца F от температуры при постоянном объѐме имеет вид:
1) |
|
|
dF |
|
S ; |
|
при росте температуры уменьшается, |
|
|
||||
|
|
|
dT V |
|
||
2) |
dF |
0 |
; |
|
|
|
не зависит от температуры, |
|
|
|
|||
|
dT V |
|
|
|
|
|
3) |
при росте температуры увеличивается, |
dF |
|
S ; |
||
|
|
|||||
|
|
|
|
dT |
V |
|
|
65 |
|
|
|
|
|
4) при росте температуры может и увеличиваться, и уменьшаться, что зависит от природы вещества,
dF |
|
|
|
dT V |
|
nRT
.
2. Максимальная работа в системе совершается за счѐт убыли изобарно-изотермического потенциала G , если соблюдаются условия:
1)в обратимом процессе при постоянных температуре и
объѐме;
2)в обратимом процессе при постоянных давлении и температуре;
3)в необратимом процессе при постоянных объѐме и температуре;
4)в необратимом процессе при постоянных давлении и температуре.
3. Изменение энтропии при изотермическом сжатии n молей газа в идеальном состоянии рассчитывается по формуле:
1)S nRlnV2 ;
V1
2)S nCP V2 ; V1
3)S nRT ln V1 ;
V2
4)S nCV lnV2 .
V1
4. Рассчитать изменение термодинамических функций
( S , G, F , U , H ) для необратимых процессов, используя уравнение для обратимых процессов, можно:
66

1)в изотермических процессах
2)в изобарических процессах
3)в адиабатических процессах
4)в случае, если начальные и конечные состояния в необратимом и обратимом процессах одинаковы, то есть, необратимый процесс можно заменить одним или несколькими обратимыми процессами.
5. Из уравнения Клапейрона - Клаузиуса следует, что давление насыщенного пара над жидкостью и твѐрдым телом растѐт при увеличении температуры, так как:
1)S 0 и V 0;
2)S 0 и V 0;
3)H 0 и V 0;
4)H 0 и V 0.
6. Кривая зависимости давления насыщенного пара жидкости от температуры начинается и заканчивается точками:
1)начало кривой – температура кристаллизации, конец – температура кипения;
2)начало кривой – температура кипения, конец – критическая температура;
3)начало кривой – тройная точка, конец – критическая температура;
4)начало кривой – тройная точка, конец – температура кипения.
ВАРИАНТ 8
1. Математическое соотношение между изменением энтропии и теплотой необратимого процесса имеет вид:
1) dSнеобр. QTнеобр. ;
67

|
|
Q |
|
|
2) |
dSнеобр. |
необр. |
; |
|
T |
|
|||
3) |
|
|
|
|
TdSнеобр. Qнеобр. |
|
|||
|
|
Q |
|
|
4) |
dSнеобр. |
необр. |
. |
|
T |
|
|||
|
|
|
|
|
0
;
2. Изохорно-изотермический потенциал в процессе изотермического сжатия изменяется так:
1) не меняется;
2) уменьшается;
3) увеличивается; 4) ответить на поставленный вопрос нельзя, не зная, ка-
кой газ сжимается.
3. Основной смысл второго закона термодинамики:
1)второй закон термодинамики решает задачу о направлении и пределах самопроизвольного протекания процесса;
2)второй закон термодинамики утверждает, что тепло может переходить от тела более холодного к телу более горячему;
3)второй закон термодинамики позволяет рассчитать максимальную работу процесса;
4)второй закон термодинамики позволяет рассчитать энергетический баланс процесса.
4. Уравнение, связывающее изменение энергии Гельмгольца F , температурный коэффициент этого изменения и изменения внутренней энергии в ходе термодинамического процесса при постоянной температуре, имеет вид:
68

1) |
F |
2) |
F |
3) |
F |
U
U
U
T S ; |
|
|
F |
; |
|
T |
|
|
T V |
|
|
|
F |
|
T |
T |
|
|
V |
|
;
4) |
|
F |
|
U F T |
T |
. |
|
|
|
V |
|
5. Графическая зависимость теплоты испарения от температуры имеет вид:
1) ΔHисп |
2) ΔHисп |
3) ΔHисп |
4) ΔHисп |
T T T T .
6. Кривая зависимости давления насыщенного пара жидкости от температуры начинается точками:
1)начало – абсолютный нуль температуры, конец – критическая температура;
2)начало – абсолютный нуль температуры, конец – тройная точка;
3)начало – тройная точка, конец – критическая темпера-
тура;
4)начало – тройная точка, конца эта кривая не имеет, так как при всех температурах давление насыщенного пара растѐт при увеличении температуры.
69
