
- •Методические указания
- •Исследование процесса водородного восстановления кремния из тетрахлорида кремния методом численного
- •Теоретические сведения
- •1.1. Равновесный выход конденсирующегося элемента
- •1.2. Компонентный состав и базисные реакции в системе
- •1.4.Константа равновесия химической реакции.
- •1.4. Вычисление константы равновесия кр химической
- •1.5. Система уравнений химического равновесия
- •2. Лабораторные задания
- •3. Требования к отчёту
- •4. Контрольные вопросы
- •1.1. Методы получения монокристаллов из расплавов
- •1.2. Упрощающие предположения, принимаемые при теоретическом описании процессов направленной
- •1.3. Уравнения материального баланса примесного
- •1.4. Однократная зонная перекристаллизация
- •1.5. Многократная зонная перекристаллизация.
- •1.6. Механизмы переноса примеси в жидкой фазе
- •1.7. Уравнение Бартона– Прима – Слихтера для расчёта
- •1.8.Распределение нелетучей примеси по длине
- •2. Лабораторные задания
- •3.Требования к отчёту
- •4. Контрольные вопросы
- •Библиографический список
- •394026 Воронеж, Московский просп., 14
1.5. Система уравнений химического равновесия
Мы рассматриваем многофазную систему, в которой возможно одновременное протекание нескольких химических реакций, и хотим найти давления компонент парогазовой фазы в состоянии равновесия. Систему уравнений, из которых можно определить эти давления, принято называть системой уравнений химического равновесия. В соответствии с выбором компонентного состава системы неизвестных давлений пять. Давлением паров атомов кремния в расчёте пренебрегаем (см. /1,4/)
Первые три уравнения этой системы можно получить, записав выражения для констант равновесия базисных реакций (12) – (14)
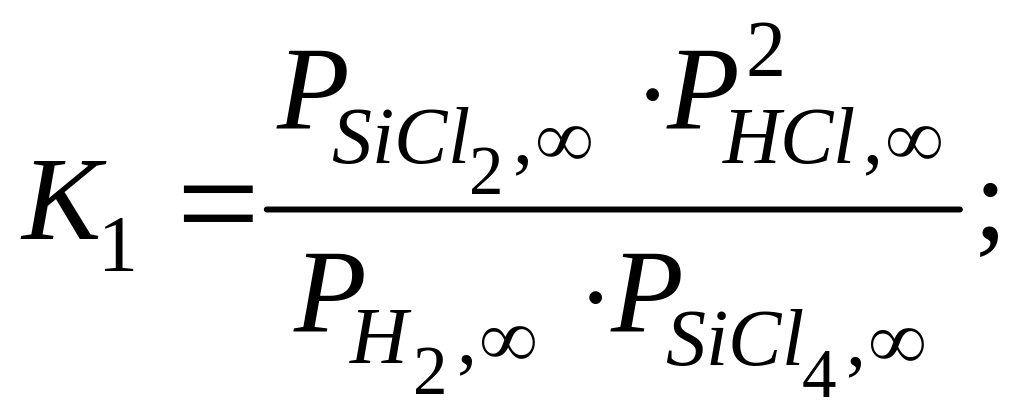 (32)
(32)
 (33)
(33)
 (34)
(34)
Здесь через Pi обозначены безразмерные отношения парциальных давлений газообразных компонент к давлению P0 , принимаемому за стандартное. В данном случае за стандартное удобно принять давление P0 = 1атм. Следовательно, величины Pi численно равны искомым парциальным давлениям, выраженным в атмосферах.
В качестве четвёртого берём уравнение, выражающее условие постоянства давления в системе Р0
![]() (35)
(35)
Будем считать, что уравнение (35) далее будет приведено к безразмерной форме путём деления обеих его частей на Р0 = 1 атм.
Поскольку известно, что атомы хлора и
водорода в данной системе не входят в
состав конденсированной фазы, то
отношение их гипотетических давлений
должно оставаться неизменным. Обозначим
(![]() )0
= 4PSiCl4,0/2PH2,0
через 2М и запишем условие материального
баланса неконденсирующихся атомов в
виде
)0
= 4PSiCl4,0/2PH2,0
через 2М и запишем условие материального
баланса неконденсирующихся атомов в
виде
 (36)
(36)
Будем считать, что и (36) будет далее приведено к безразмерной форме путём деления числителя и знаменателя левой части на Р0=1 атм.
В итоге будет получена система пяти уравнений относительно пяти безразмерных неизвестных Pi, численно равных равновесным парциальным давлениям компонент парогазовой фазы, выраженным в атмосферах. Для её решения необходимы значения констант равновесия базисных химических реакций при температуре процесса водородного восстановления и значение параметра М, задающего состав исходной смеси как отношение парциальных давлений исходного кремнийсодержащего вещества и водорода. Полное давление в системе Р0 равно по условию одной атмосфере, и потому правая часть (35) равна единице. Следует также отметить, что успех численного решения системы уравнений химического равновесия существенно зависит от удачного выбора начального приближения для искомых величин Pi.
2. Лабораторные задания
2.1. После изучения теоретического введения ознакомьтесь со всем блоком лабораторных заданий и материалом приложений. Согласуйте с преподавателем состав Вашего индивидуального лабораторного задания. Определите рациональную с Вашей точки зрения систему обозначений для всех величин, которые предстоит использовать в расчётах. Спланируйте свои дальнейшие действия.
2.2. Расчёт температурной зависимости констант равновесия базисных химических реакций процесса водородного восстановления кремния из тетрахлорида кремния. (Для выполнения задания рекомендуется воспользоваться программой Mathсad).
2.2.1. Используя справочные термодинамические данные, приведённые в приложении 1, рассчитайте по формуле (31) температурную зависимость приведённой энергии Гиббса для всех реактантов выбранных базисных химических реакций процесса водородного восстановления кремния из его тетрахлорида в интервале температур от 1000К до 1500К. Результаты представьте в форме таблицы. Шаг по температуре согласуйте с преподавателем. Позаботьтесь при этом о рациональном выборе обозначений.
2.2.2. Используя справочные термодинамические данные, приведённые в приложении 1, введите на рабочее поле программы Mathсad энтальпии образования всех реактантов выбранных базисных химических реакций в стандартных состояниях при Т=0К из элементов, взятых из их стандартных состояний при Т=0К. Позаботьтесь при этом о рациональном выборе обозначений.
2.2.3. Используя результаты пунктов 2.2.1 и 2.2.2, рассчитайте по формуле (30) температурную зависимость натурального логарифма констант равновесия КР всех рассматриваемых базисных химических реакций. Результаты представьте в табличной форме для того же температурного интервала и с тем же шагом, что и в п.2.2.1.
2.2.4. Используя результаты выполнения п.2.2.3, постройте графики зависимости lnКР(Т) от обратного значения абсолютной температуры для всех рассматриваемых базисных химических реакций в том же температурном интервале, что и в п.2.2.1.
2.3. Расчёт температурной зависимости равновесных парциальных давлений компонент паровой фазы для процесса водородного восстановления кремния из его тетрахлорида при атмосферном давлении. (Для выполнения задания рекомендуется воспользоваться программой Mathсad).
2.3.1. Введите на рабочее поле программы Mathсad систему уравнений химического равновесия (31) – (36) для процесса водородного восстановления кремния из его тетрахлорида при атмосферном давлении. Значение параметра М, характеризующего состав исходной смеси, согласуйте с преподавателем.
2.3.2. Используя результаты выполнения п.2.2, путём численного решения системы уравнений химического равновесия для процесса водородного восстановления кремния из его тетрахлорида найдите значения равновесных парциальных давлений компонент парогазовой фазы в атмосферах для того же температурного интервала и с тем же шагом, что и в п.2.2.1. Результаты представьте в табличной форме и в виде графиков зависимости от температуры равновесных парциальных давлений компонент парогазовой фазы, измеренных в атмосферах. По оси давлений рекомендуется выбрать логарифмический масштаб.
2.3.3. Сравните результаты п.2.3.2. с результатами аналогичных расчётов, приведённых в /4/, и сформулируйте выводы.
2.4.Расчёт температурной зависимости равновесного выхода кремния в процессе его водородного восстановления из тетрахлорида кремния. (Для выполнения задания рекомендуется воспользоваться программой Mathсad).
2.4.1. Используя результаты п.2.3.2., рассчитайте в соответствии с формулой (10) температурную зависимость равновесного выхода кремния в процессе его водородного восстановления из тетрахлорида кремния при атмосферном давлении для заданного в п.2.3.1 состава исходной смеси. Результаты представьте в форме таблицы и графика.
2.4.2. Повторите вычисления пунктов 2.3.2 и 2.4.1 для нескольких значений параметра М, характеризующего состав исходной смеси. Набор этих значений согласуйте с преподавателем. Охарактеризуйте зависимость от температуры и состава исходной смеси равновесного выхода кремния в процессе его водородного восстановления из тетрахлорида кремния.
2.4.3. Используя результаты п.п. 2.4.1-2.4.2, определите, при каких температурах в исследованном интервале равновесный выход кремния достигает максимума при заданных составах исходной смеси. По массовому расходу тетрахлорида кремния, указанному преподавателем, найдите по формуле (11) максимальную производительность реактора в квазиравновесном приближении для всех исследованных составов исходной смеси.
2.5. Сформулируйте выводы по результатам численного эксперимента.
