
- •Лекция № 53-54 углеводы
- •Моносахариды
- •1.1. Строение и классификация
- •Стереоизомерия
- •Цикло-оксо-таутомерия
- •Конформационное строение
- •1.2. Химические свойства
- •Восстановление
- •Окисление
- •П олучение гликоновых кислот
- •Взаимопревращения в щелочном растворе между альдозами, эпимерами по с-2, называют эпимеризацией. Получение гликаровых кислот
- •Окисление виц-диольной группировки
- •Получение сложных эфиров
- •Получение производных по карбонильной группе. Образование озазонов
- •Наращивание цепи по методу Килиани-Фишера
- •Д еградация по Руффу
- •Дисахариды
- •2.1. Строение
- •2.2. Химические свойства
- •3. Полисахариды
Взаимопревращения в щелочном растворе между альдозами, эпимерами по с-2, называют эпимеризацией. Получение гликаровых кислот
П ри
действии разбавленной азотной кислоты
окисляется оба конца углеродного скелета
альдоз и образуются гликаровые
кислоты.
ри
действии разбавленной азотной кислоты
окисляется оба конца углеродного скелета
альдоз и образуются гликаровые
кислоты.
При образовании гликаровых кислот, как и в случае глицитов, происходит «уравнивание» функциональных групп на концах цепи и из некоторых альдоз образуются мезо-соединения.
Окисление кетоз азотной кислотой протекает с расщеплением С-С связей.
Окисление виц-диольной группировки
Моносахариды содержат виц-диольную группировку, которая претерпевает окислительное расщепление под действием иодной кислоты или тетраацетата свинца.
HOCH2(CHOH)nCHO + (n+1) HIO4 (n+1) HCOOH + HCHO + (n+1) HIO3
Р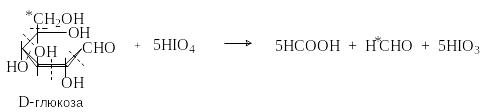 еакция
протекает количественно. По составу
продуктов и количеству израсходованной
иодной кислоты получают ценную информацию
о строение моносахаридов и их производных.
еакция
протекает количественно. По составу
продуктов и количеству израсходованной
иодной кислоты получают ценную информацию
о строение моносахаридов и их производных.
Получение гликозидов
Циклические формы моносахаридов содержат несколько групп ОН, одна из которых – гликозидный (полуацетальный) гидроксил, отличается повышенной склонностью к реакциям нуклеофильного замещения.
И звестно,
что в присутствии кислотных катализаторов
полуацетали реагируют со спиртами. При
этом происходит нуклеофильное замещение
полуацетального гидроксила и образуются
полные ацетали.
звестно,
что в присутствии кислотных катализаторов
полуацетали реагируют со спиртами. При
этом происходит нуклеофильное замещение
полуацетального гидроксила и образуются
полные ацетали.
А налогично
реагирует гликозидный гидроксил в
альдозах и кетозах. Спиртовые ОН группы
при этом не затрагиваются. Продукты
замещения гликозидного гидроксила
называют гликозидами
(гликопиранозидами
или гликофуранозидами
в зависимости
от размера цикла). Например, при пропускании
через раствор D-глюкозы в метаноле
газообразного HCl образуется смесь
метилглюкозидов, соответствующих разным
таутомерным формам D-глюкозы (двум
пиранозным и двум фуранозным). В условиях
термодинамического контроля в реакционной
смеси преобладают более стабильные
метилпиранозиды.
налогично
реагирует гликозидный гидроксил в
альдозах и кетозах. Спиртовые ОН группы
при этом не затрагиваются. Продукты
замещения гликозидного гидроксила
называют гликозидами
(гликопиранозидами
или гликофуранозидами
в зависимости
от размера цикла). Например, при пропускании
через раствор D-глюкозы в метаноле
газообразного HCl образуется смесь
метилглюкозидов, соответствующих разным
таутомерным формам D-глюкозы (двум
пиранозным и двум фуранозным). В условиях
термодинамического контроля в реакционной
смеси преобладают более стабильные
метилпиранозиды.
Метил--D-глюкопиранозид большей термодинамической стабильностью, чем -аномер (аномерный эффект) и поэтому образуется в большем количестве. Гликозиды существуют только в циклической форме, поэтому - и -аномеры гликозидов не могут спонтанно переходить друг в друга в результате таутомерных превращений. Гликозиды не имеют свободной альдегидной группы и являются невосстанавливающими сахарами.
К ак
полные ацетали гликозиды гидролизуются
в условиях кислотного катализа и
устойчивы в разбавленных растворах
щелочей. Механизм кислотного гидролиза
включает протонирование гликозидного
кислорода, расщепление гликозидной С-О
связи с образованием гликозил-катиона,
который затем атакуется молекулой воды.
ак
полные ацетали гликозиды гидролизуются
в условиях кислотного катализа и
устойчивы в разбавленных растворах
щелочей. Механизм кислотного гидролиза
включает протонирование гликозидного
кислорода, расщепление гликозидной С-О
связи с образованием гликозил-катиона,
который затем атакуется молекулой воды.
Расщепление гликозидной связи важно с биологической точки зрения, поскольку многие природные соединения являются гликозидами. Широко используется ферментативный гидролиз гликозидов, преимущество которого заключается в его специфичности. Определенные ферменты гидролизуют только - или только -гликозидные связи., что может быть использовано для установления конфигурации гликозидной связи.
М олекулу
гликозида рассматривают как состоящую
из двух частей – сахарной части и
агликона:
олекулу
гликозида рассматривают как состоящую
из двух частей – сахарной части и
агликона:
В качестве агликона в природных гликозидах могут выступать спирты, фенолы, стероиды, сами моносахариды. Перечисленные агликоны связаны с сахарной частью через атом кислорода, поэтому такие гликозиды называют О-гликозидами. В природе широко распространены N-гликозиды, в которых агликонами являются азотистые основания. К ним относятся нуклеозиды – структурные единицы нуклеиновых кислот.
Получение простых эфиров
М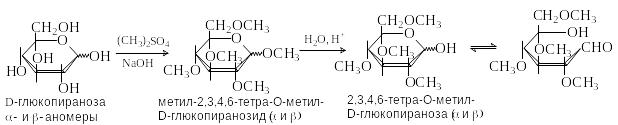 етиловые
эфиры по спиртовым группам ОН получают
действием на моносахариды диметилсульфата
в водном растворе щелочи или метилиодида
в присутствии оксида серебра. Эти методы
являются модификациями синтеза
Вильямсона. При этом в реакцию вступает
и гликозидный гидроксил. Простые эфиры
по спиртовым группа устойчивы к гидролизу,
в то время как гликозидная связь легко
расщепляется в кислой среде.
етиловые
эфиры по спиртовым группам ОН получают
действием на моносахариды диметилсульфата
в водном растворе щелочи или метилиодида
в присутствии оксида серебра. Эти методы
являются модификациями синтеза
Вильямсона. При этом в реакцию вступает
и гликозидный гидроксил. Простые эфиры
по спиртовым группа устойчивы к гидролизу,
в то время как гликозидная связь легко
расщепляется в кислой среде.
П риведенная
последовательность реакций (метилирование,
затем гидролиз) используется для
определения размера цикла в моносахаридах.
Неметилированной остается группа ОН,
которая участвовала в образовании
циклического полуацеталя. Окисление
образовавшейся тетраметил-D-глюкозы
азотной кислотой в жестких условиях
дает сначала кетокислоту, а затем
триметоксиглутаровую и диметоксиянтарную
кислоты.
риведенная
последовательность реакций (метилирование,
затем гидролиз) используется для
определения размера цикла в моносахаридах.
Неметилированной остается группа ОН,
которая участвовала в образовании
циклического полуацеталя. Окисление
образовавшейся тетраметил-D-глюкозы
азотной кислотой в жестких условиях
дает сначала кетокислоту, а затем
триметоксиглутаровую и диметоксиянтарную
кислоты.
Состав продуктов окисления указывает на то, что кетогруппа, а, следовательно, и свободная гидроксигруппа находились в положении 5. Это означает, что цикл был пиранозным.
