
- •Вопрос 110 Молекулярная структура миофибрилл. Структура и функции основных белков миофибрилл миозина, актина, тропомиозина, тропонина.
- •Вопрос 111 Биохимические механизмы мышечного сокращения и расслабления. Роль ионов кальция и других ионов в регуляции мышечного сокращения.
- •Вопрос 112 Саркоплазматические белки. Миоглобин, его строение и функции. Карнозин и анзерин. Особенности энергетического обмена в мышцах; роль креатинфосфата.
- •Вопросы 113 и 114
- •Вопрос 115 Медиаторы нервной системы: ацетилхолин, катехоламины, серотонин, γ-аминомасляная кислота, глицин, глутамат, гистамин. Физиологически активные пептиды мозга.
Вопрос 110 Молекулярная структура миофибрилл. Структура и функции основных белков миофибрилл миозина, актина, тропомиозина, тропонина.
Саркомер – структурно-функциональная единица поперечнополосатой мышечной
ткани. Из саркомеров состоят миофибриллы.
Миофибриллы – пучки белков, располагающиеся вдоль клетки. Они построены из
белковых нитей (филаментов) двух типов – толстых и тонких.
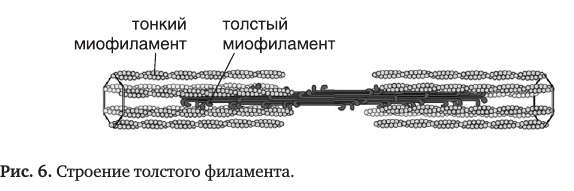
1. Миозин – образует толстые нити миофибрилл. Его молекула содержит 2
идентичные тяжелые ППЦ и 4 легкие цепи.
Каждая тяжелая цепь с С-конца имеет конформацию α-спирали, они скручены
друг с другом; эта часть молекулы имеет форму палочки. Противоположные концы каждой цепи (N-концы) имеют глобулярную форму и образуют “головку” молекулы. И к ним нековалентно присоединены по 2 легкие цепи.
Функции моизина:
Катализирует гидролиз АТФ, что используется для сокращения мышцы.
Каталитический активный центр локализован в головках молекулы миозина.
В физиологических условиях палочкообразные хвосты молекул миозина могут
соединяться друг с другом продольно, образуя пучки; головки выступают на поверхности пучка, выстраиваясь вокруг него по спирали.
В области М-линии пучки стыкуются «хвост к хвосту». Так получаются
миозиновые нити саркомера, каждая из которых содержит около 400 молекул миозина.
В состав актиновых нитей входят белки:
Актин (сократительная функция)
Тропомиозин и тропонин (регуляторная функция).
2. Актин – небольшой глобулярный белок тонких нитей – G-актин (глобулярный
актин), молекулы которого могут нековалентно соединяться, образуя фибриллярный актин – F-актин. Форма молекул F-актина напоминает две нитки бус, скрученные друг с другом.
В мышечных клетках весь актин находится в форме F-актина. К F-актину могут
присоединяться головки миозина, причем на каждой молекуле G-актина в F-актине есть центр связывания миозина. В результате такого взаимодействия в сотни раз увеличивается АТФазная активность миозина. Актомиозин – соединение F-актина с миозином
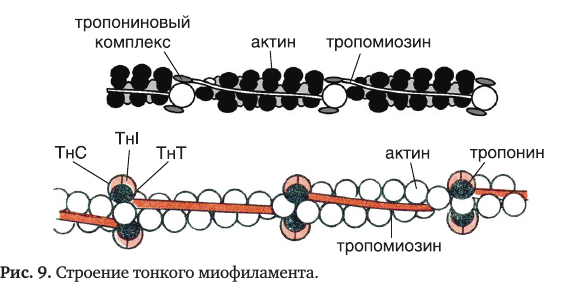
3. Тропомиозин – фибриллярный белок, имеет вид α-спирали и располагается
вблизи ленты F-актина. В тонкой нити на 1 молекулу тропомиозина приходится 7 молекул G-актина. Располагается тропомиозин в желобке между двумя спиралями G-актина. Соединяется тропомиозин “конец-в-конец”, цепочка непрерывная. Молекула тропомиозина закрывает активные центры связывания актина поверхности глобул актина.
4. Тропонин – имеет глобулярную форму; построен из трех разных субъединиц –
тропонин Т, тропонин С и тропонин I. Он нековалентно связан с тропомиозином и с актином; на каждую молекулу тропомиозина приходится одна молекула тропонина.
Тропонин Т (ТнТ) – отвечает за связывание тропонина с тропомиозином, через
ТнТ конформационные изменения тропонина передаются на тропомиозин.
Тропонин С (ТнС) – Ca-связывающая субъединица, содержит 4 участка для
связывания кальция, по строению похожа на белок кальмодулин.
Тропонин I (ТнI) – ингибиторная субъединица – это ненастоящий ингибитор, он
только создает пространственное препятствие, мешающее взаимодействию актина и миозина в момент, когда ТнС не связан с Са2+.
Содержание миозина, актина, тропомиозина и тропонина в миофибриллах
равно примерно 55, 25, 15 и 5 %.
