
- •2. Оксалоацетат превращается в фосфоенолпируват
- •Вопрос 66 Гликоген, биологическое значение. Биосинтез и мобилизация гликогена. Регуляция синтеза и распада гликогена.
- •Синтез гликогена (гликогеногенез)
- •Распад гликогена (гликогенолиз)
- •Регуляция метаболизма гликогена
- •Регуляция метаболизма гликогена в печени
- •1. В постабсорбтивном периоде инсулин-глюкагоновый индекс снижается, и
- •Для схемы с глюкагоном и адреналином (действие через аденилатциклазную систему)
- •2. В период пищеварения преобладает влияние инсулина, так как инсулин-
- •Регуляция метаболизма гликогена в мышцах
- •Вопрос 67 Уровень глюкозы крови как гомеостатический параметр внутренней среды организма. Роль инсулина, глюкагона, адреналина, аденилатциклазной и инозитолфосфатной систем в регуляции уровня глюкозы.
- •Вопрос 68 Наследственные нарушения обмена моносахаридов и дисахаридов: галактоземия, непереносимость фруктозы и дисахаридов. Гликогенозы и агликогенозы.
- •1.1. Галактоземия, вызванная дефектом галактозо-1-фосфатуридилтрансферазы
Вопрос 65
Биосинтез глюкозы (глюконеогенез) из аминокислот, глицерина и молочной кислоты; регуляция глюконеогенеза. Биотин, роль в образовании оксалоацетата. Взаимосвязь гликолиза в мышцах и глюконеогенеза в печени (цикл Кори).
Глюконеогенез – синтез глюкозы из веществ не углеводной природы. Протекает в
основном в печени и менее интенсивно в корковом веществе почек, а также слизистой оболочки кишечника
Биороль: поддержание уровня глюкозы в крови при длительном голодании и
интенсивных физических нагрузках
Субстраты:
Лактат – продукт анаэробного гликолиза, он образуется при лююых состояниях организма в эритроцитах и работающих в мышцах
Глицерол – образуется при гидролизе жиров, в период голодания или при длительной физической нагрузке
Некоторые аминокислоты – образуются при распаде мышечных белков
Пункты включения субстратов в глюконеогенез:
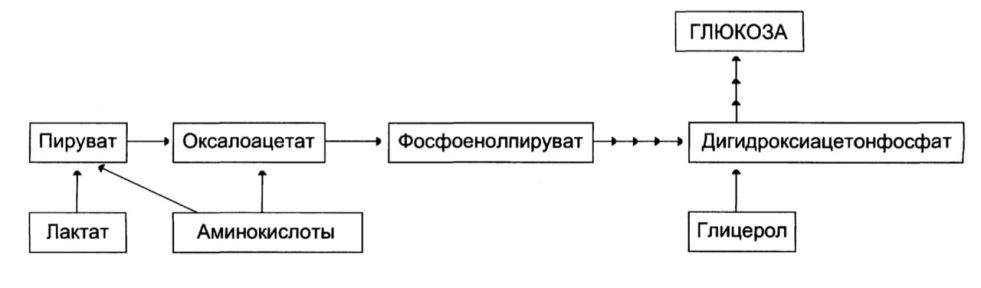
Реакции глюконеогенеза: большинство протекает за счет обратимых р. гликолиза и катализируется теми же ферментами. Но 3 реакции необратимы и протекают по другому пути с др. ферментами.
Гликолиз протекает в цитозоле
Часть реакций глюконеогенеза протекает в митохондриях
В глюконеогенезе 3 термодинамически не обратимые реакции, вместо них протекают 4 других реакции (на общ. схеме выделены)
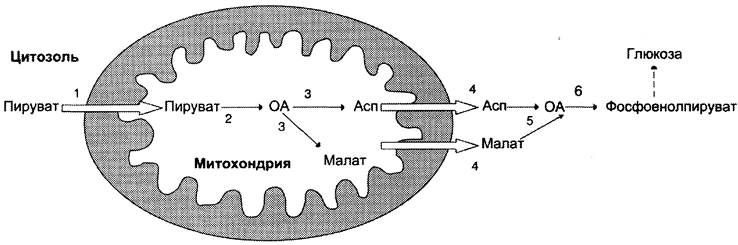
1. Образование фосфоенолпирувата из пирувата: первая реакция происходит
в митохондриях, при которой пируват, транспортируется в матрикс митохондрий и там карболизируется с образованием оксалоацетата.
Фермент: пируваткарбоксилаза (кофермент – биотин)

Дальнейшие превращения происходят в цитозоле: оксалоацетат может
проходить через митоходондриальную мембрану только в виде малата или аспартата.
Поэтому в митохондриальном матриксе оксалоацетат восстанавливается с обр.
малата (обратная р. цитратного цикла). Малат проходит через митохондр. мембрану с помощью спец. переносчиков в цитозоль
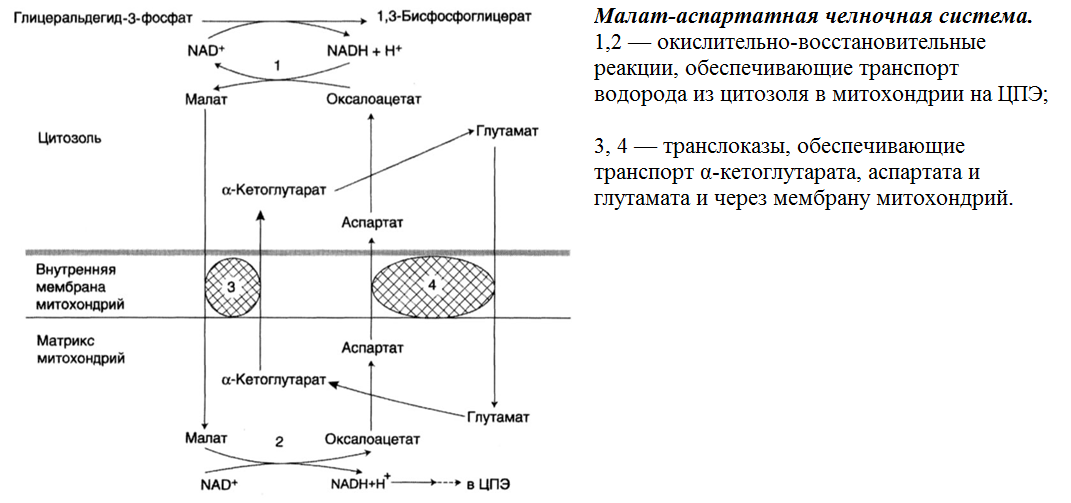
Оксалоацетат также может транспортироваться из митохондрий в виде аспартата в
ходе малат-аспартатного челночного механизма
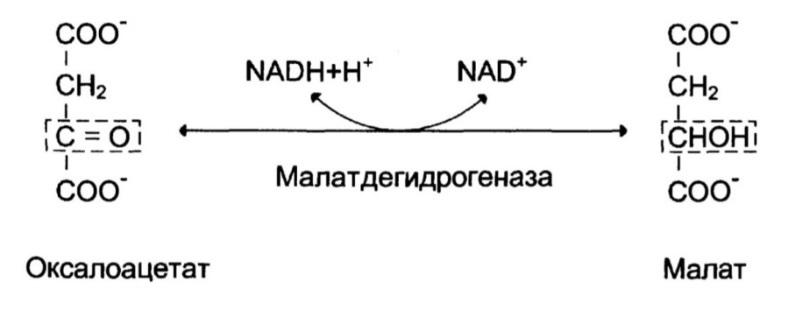
В цитозоле малат при помощи малатдегидрогеназы (NAD+-зависимой) вновь
превращается в оксалоацетат
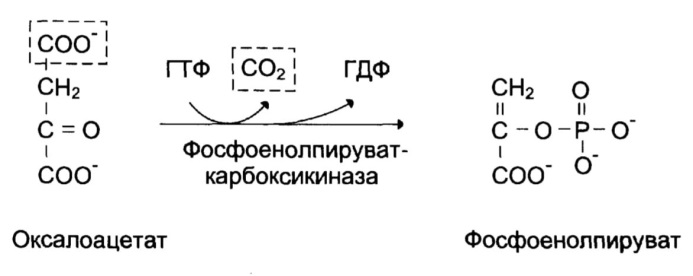
2. Оксалоацетат превращается в фосфоенолпируват
Фермент: фосфоенолпируваткарбоксикиназа
Суммарная схема до этого момента:
Далее все реакции (вплоть до образования фруктозо-1,6-бисфосфата) протекают в
цитозоле и катализируются гликолитическими ферментами
3. Гидролиз фруктозо-1,6-бисфосфата с обр. глюкозо-6-фосфата
Фермент: фруктозо-1,6-бисфосфатаза
4. Гидролиз глюкозо-6-фосфата с обр. глюкозы
Фермент: глюкозо-6-фосфатаза
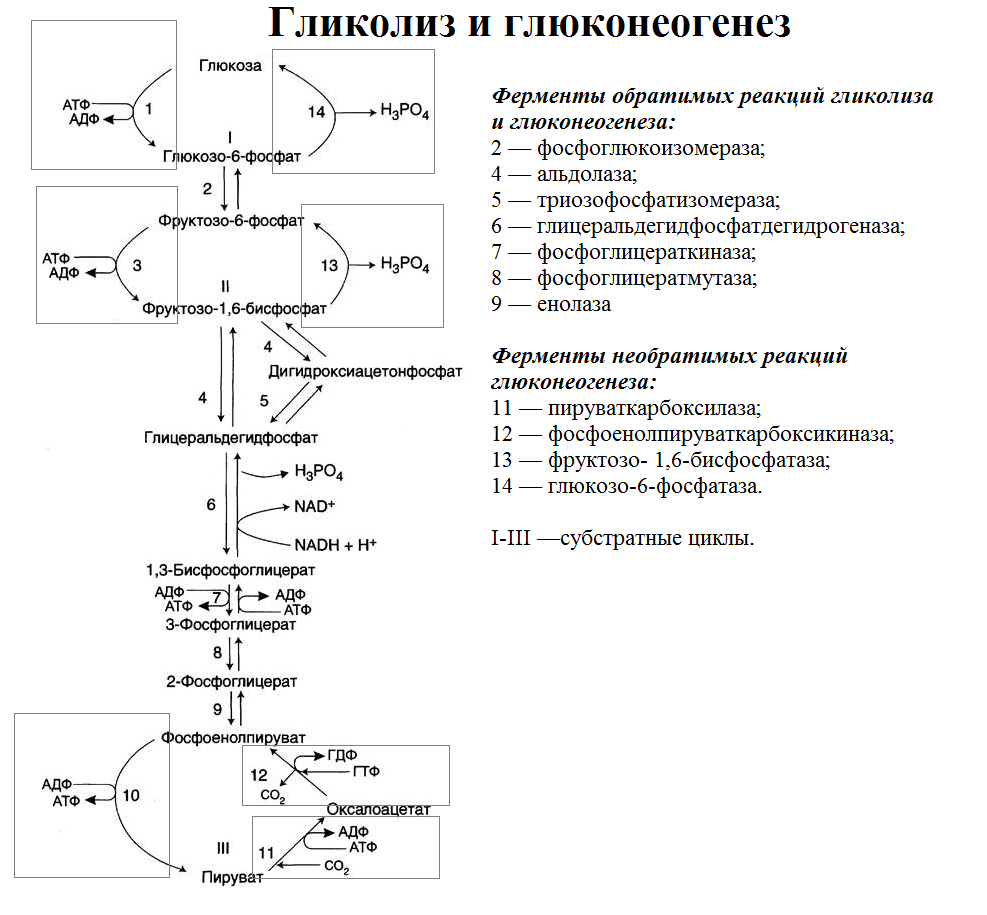
Образовавшаяся свободная глюкоза выходит из клетки в кровь.
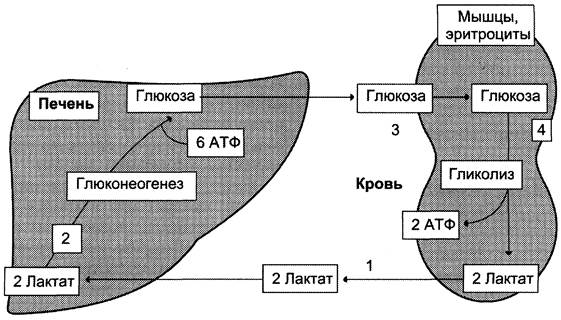
Синтез глюкозы из лактата или цикл Кори: лактат, образовавшийся в
интенсивно работающих мышцах или в клетках с преобладающим анаэробным способом катаболизма глюкозы, поступает в кровь, а затем в печень.
В печени отношение NADH/NAD+ ниже, поэтому лактатдегидрогеназная р.
протекает в обратном направлении -= образуется пируват.
Далее пируват включается в глюконеогенез, а образовавшаяся глюкоза поступает в
кровь и поглощается скелетными мышцами.
Цикл Кори выполняет 2 важнейшие функции:
Обеспечивает утилизацию лактата;
Предотвращает накопление лактата и, как следствие этого, опасное снижение рН
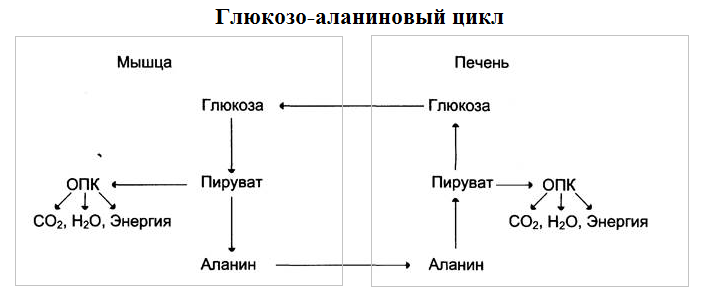
Синтез глюкозы из аминокислот или глюкозо-аланиновый цикл:
гликогенные АК – те, что при катаболизме превращаются в пируват или
метаболиты цитратного цикла, могут рассматриваться как потенциальные предшественники глюкозы и гликогена
Оксалоацетат (обр. аспарагиновой кислоты), явл. промежуточным продуктом как
цитратного цикла, так и глюконеогенеза.
При расщеплении мышечных белков образуются АК, многие из которых
превращаются сразу в пируват или сначала в оксалоацетат, а затем в пируват.
Пируват же превращается в аланин, приобретая аминогруппу от других аминокислот
Аланин из мышц переносится кровью в печень, где снова преобразуется в пируват,
который частично окисляется и частично включается в глюконеогенез.
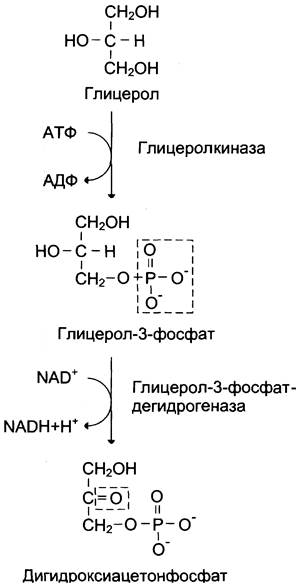
Синтез глюкозы из глицерола: глицерол обр. из ТАГ в жировой ткани
Использовать глицерол могут только те ткани, в которых имеется фермент
глицеролкиназа (печень, почки). Этот АТФ-зависимый фермент катализирует превращение глицерола в глицерол-3-фосфат
При включении глицерол-3-фосфата в глюконеогенез происходит его
дегидрирование NAD-зaвисимой дегидрогеназой с образованием дигидроксиацетонфосфата, который далее превращается в глюкозу.
РЕГУЛЯЦИЯ ГЛЮКОНЕОГЕНЕЗА
Переключение с гликолиза на глюконеогенез и обратно происходит с участием
инсулина, глюкагона и осуществляется с помощью:
Аллостерической регуляции ферментов
Фосфорилирования/дефосфорилирования
Индукции/репессии синтеза ключевых ферментов,
катализирующие необратимые стадии
«Субстратные» циклы – парные комбинации процессов синтеза и распада
метаболитов. Название означает объединение реакций синтеза и распада субстрата.
Изменение в печени гликолитического направления на глюконеогенез и обратно
при смене абсорбтивного состояния на постабсорбтивное или при голодании происходит главным образом в результате регуляции активности ферментов, катализирующих реакции субстратных циклов. Эти циклы обозначены цифрами I, II, III
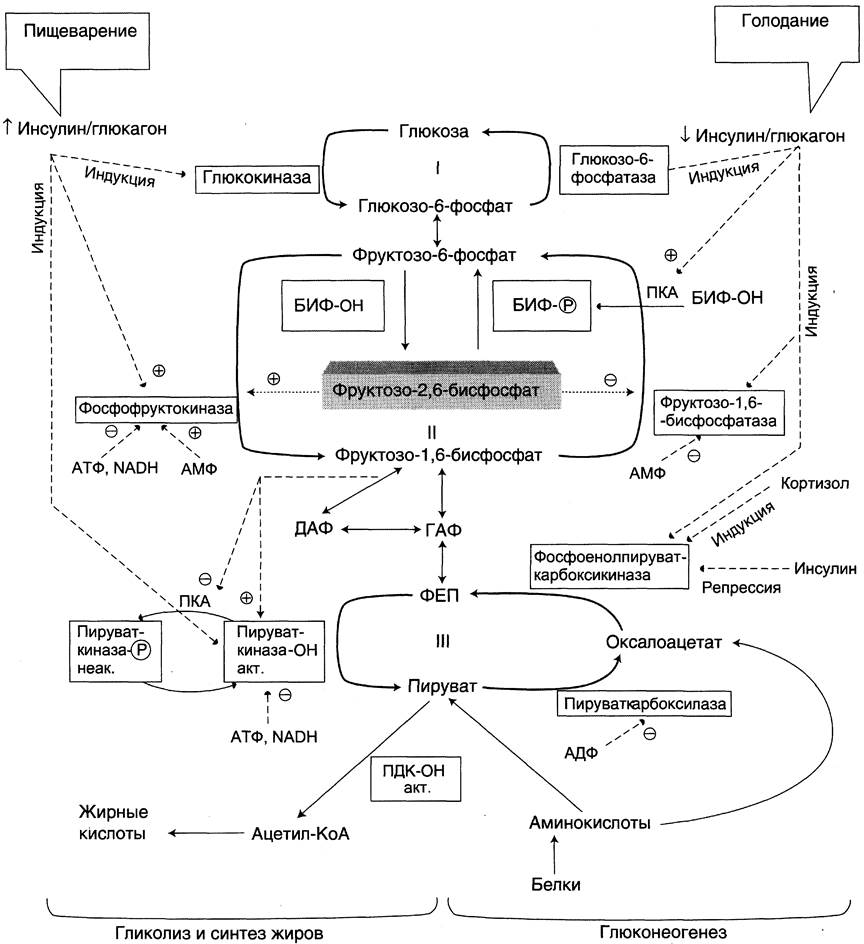
Направление реакций первого субстратного цикла:
Регулируется главным образом концентрацией глюкозы. При пищеварении
концентрация глюкозы в крови повышается. Активность глюкокиназы – максимальна.
Вследствие ускоряется гликолитическая реакция образования глюкозо-6-фосфата.
Инсулин тожн индуцирует синтез глюкокиназы и ускоряет тем самым
фосфорилирование глюкозы. Поскольку глюкокиназа печени не ингибируется глюкозо-6-фосфатом (в отличие от гексокиназы мышц), то основная часть глюкозо-6-фосфата в абсорбтивном периоде направляется на синтез гликогена и по гликолитическому пути.
Направление реакций второго субстратного цикла
Зависит от активности фосфофруктокиназы и фосфатазы фруктозо-1,6-бисфосфата.
Их активность зависит от концентрации фруктозо-2,6-бисфосфата.
Фруктозо-2,6-бисфосфат – метаболит, образующийся из фруктозо-6-фосфата и выполняющий только регуляторные функции.
Образование фруктозо-2,6-бисфосфата путём фосфорилирования
фруктозо-6-фосфата катализирует бифункциональный фермент (БИФ).
Превращение фруктозо-2,6-бисфосфата в фруктозо-6-фосфат не явл. обратимым
процессом. Само бразование фруктозо-2,6-бисфосфата требует затрат АТФ, а при образовании фруктозо-6-фосфата из фруктозо-2,6-бисфосфата гидролитически отщепляется неорганический фосфат.
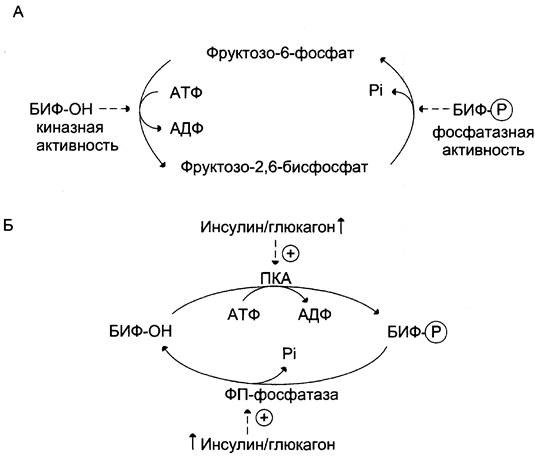
В реакции фосфорилирования фруктозо-6-фосфата фермент БИФ киназную
активность, а при дефосфорилировании образованного фруктозо-2,6-бисфосфата –
фосфатазную (поэтому и называется «бифункциональный)
Киназная активность БИФ проявляется, когда фермент находится в
дефосфорилированной форме (БИФ-ОН) – она характерна для абсорбтивного периода, когда инсулин/глюкагоновый индекс высокий
Фосфатазная активность БИФ – при низком инсулин-глюкагоновом индексе,
характерном для периода длительного голодания, тогда происходит фосфорилирование БИФ, и он функционирует как фосфатаза.
Результат: снижение количества фруктозо-2,6-бисфосфата.
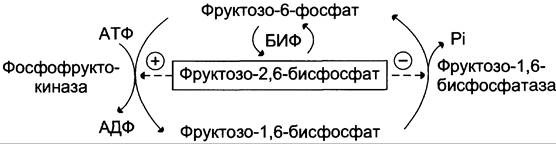
Регуляторное влияние фруктозо-2,6-бисфосфата в том, что он аллостерически:
Активирует фосфофруктокиназу (фермент гликолиза).
Ингибирует фруктозо-1,6-бисфосфатазу (фермент глюконеогенеза)
Итак, в абсорбтивном периоде уровень фруктозо-2,6-бисфосфата повышается, что
приводит к активации фосфофруктокиназы и ускорению гликолиза.
Результат уменьшения кол-ва фруктозо-2,6-бисфосфата в постабсорбтивном
периоде – снижение активности фосфофруктокиназы, замедление гликолиза и переключение гликолиза на глюконеогенез.
Направление реакций третьего субстратного цикла
Основная роль принадлежит пируваткиназе, фосфорилированная форма которой
неактивна, а дефосфорилированная – активна
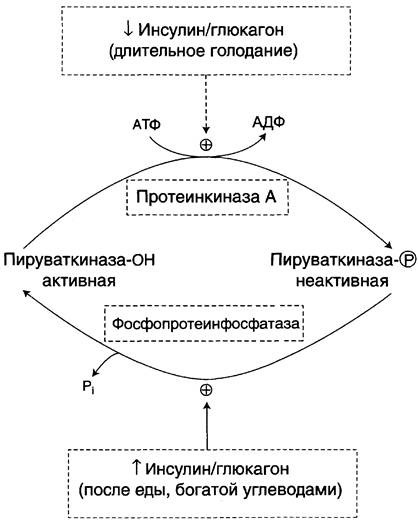
В период пищеварения инсулин активирует фосфопротеинфосфатазу, которая
дефосфорилирует пируваткиназу = пируваткиназа активна
Также инсулин в печени стимулирует синтез пируваткиназы и
репрессирует синтез фосфоенолпируваткарбоксикиназы.
Следовательно, гликолитическая реакция фосфоенолпируват → пируват
ускоряется при пищеварении.
В постабсорбтивном состоянии, под влиянием глюкагона, который
опосредованно через цАМФ-зависимую протеинкиназу фосфорилирует и инактивирует пируваткиназу, эта реакция замедляется
При длительном голодании глюкагон ускоряет глюконеогенез: э
то достигается не только путём фосфорилирования пируваткиназы и снижением скорости гликолиза, но и тем, что глюкагон стимулирует синтез ферментов глюконеогенеза: фосфоенолпируваткарбоксикиназы, фруктозо-1,6-бисфосфатазы и глюкозо-6-фосфатазы.
Координация скорости реакции II и III субстратных циклов достигается с помощью
фруктозо-1,6-бисфосфата – продукта II субстратного цикла (гликолитическое направление), который является аллостерическим активатором пируваткиназы.
В период пищеварения вследствие ускорения начальных стадий гликолиза
концентрация фруктозо-1,6-бисфосфата повышается, что приводит к дополнительной активации пируваткиназы.
