
Дополнительные учебные материалы / Болевой шок
.pdfПатофизиология болевого шока
1. Общие сведения
Термин «шок» появился в медицине достаточно давно. Как свидетельствуют Г.С.Мазуркевич и А.И.Тюкавин (Шок, СПб, 2004) его появлению мы обязаны консультанту армии Людовика XV хирургу Henry Francois le Dran, который в своей книге, посвященной проблемам военнополевой хирургии и изданной в 1737 году, применил термин «secousse» (удар, толчок). В дальнейшем при переводе этой книги на английский язык и изданной в 1743 году это французское слово было переведено как «shock» (шок) и с тех пор вошло в медицинскую и обиходную лексику.
Если первоначально шок рассматривался почти исключительно как результат тяжелых травматических повреждений организма и, в первую очередь, как результат военно-полевой травмы (о чем и свидетельствуют труды уже упомянутого выше французского хирурга и известные работы Н.И.Пирогова), то в последующем появились описания шока ожогового, шока при воздействии на организм электрического тока, шока, возникающего при тяжелой патологии внутренних органов. Более того, понятие «шок» в сочетании с определением «гуморальный» стало применяться по отношению к аллергическим состояниям («анафилактический шок») и тяжелым последствиям переливания несовместимой крови («гемотрансфузионный шок»). В соответствующей медицинской литературе помимо понятия «сепсис» мы часто встречаемся с термином «эндотоксиновый или септический шок», а состояние обезвоживания организма трактуется как «ангидремический шок». Для тяжелых психических потрясений нередко стало употребляться словосочетание «психогенный шок». Отсутствие четко очерченных границ между зонами таких патологических состояний как шок и коллапс, шок и стресс не прибавляет ясности в понимании интимных механизмов развития шока, хотя и стресс, и коллапс в той или иной степени проявляются при развитии шока различной этиологии.
Чрезмерное, по нашему мнению, расширение понятия «шок» и распространению его на патологические состояния самой различной этиологии не позволяет дать единого, всеобъемлющего определения этой патологии. В самом деле, еще в 1960 году в своей статье «О классификации шоков» И.К.Ахунбаев и Г.А.Френкель привели 119 определений этого патологического состояния. Единого подхода патологов и клиницистов к этой проблеме нет и до настоящего времени. С этой точки зрения нам кажется вполне справедливым высказывание Бэллингера: "Шок - это понятие, хотя и не совсем научное, но, взамен этого, - весьма полезное в клинической практике». Поэтому, отдавая должное необходимости рассмотреть и описать в
2 первую очередь именно те виды шока, которые наиболее часто встречаются в клинической
практике, характеризуются стремительным развитием и грозят пациентам фатальным исходом, мы в данном разделе учебника решили остановиться на рассмотрении этиологии, патогенеза и принципов патогенетической терапии болевого шока.
2.Определение понятия «болевой шок»
Болевой шок – это угрожающее жизни пациента патологическое состояние, возникающее в результате воздействия на организм сверхсильного патогенного раздражителя, исходящего из внешней или внутренней среды организма и вызывающего глубокие изменения нервно-рефлекторных и нейрогуморальных механизмов регуляции, ведущие к тяжелым расстройствам гемодинамики, дыхания и обмена веществ
В приведенном определении болевого шока следует обратить внимание на следующие моменты:
-во-первых, болевой шок – это результат воздействия на организм разрушительного патогенного раздражителя, вызывающего (за исключением, может быть, некоторых видов болевого шока эндогенного происхождения) чрезвычайно объемные повреждения тканей и органов;
-во-вторых, именно эти объемные повреждения и порождают мощнейший поток ноцицептивной импульсации и развитие болевого синдрома;
-в-третьих, развившийся болевой синдром и тяжелый психогенный стресс в относительно короткий промежуток времени приводят к резкому изменению и нарушению практически всех регуляторным механизмов, как нервно-рефлекторных, так нейрогуморальных;
-в-четвертых, именно эти регуляторные нарушения и приводят к тяжелейшим расстройствам гемодинамики, дыхания и обмена веществ, что, в результате, является причиной возникновения «шоковых органов» и синдрома полиорганной недостаточности.
Исходя из этого определения, болевого шока мы представляем и описание основных его патогенетических механизмов: болевого синдрома, нарушений макро- и микроциркуляции, гипоксии, токсемии, извращения метаболических процессов и образования шоковых органов.
Излишне говорить о том, что болевой шок требует немедленного врачебного вмешательства, так как в противном случае скорость развития патологии и обширность повреждающего воздействия неизбежно приводят к трагическому исходу.
Следует упомянуть и еще об одном обстоятельстве. Именно для болевого шока наиболее характерно наличие двух стадий его развития – эректильной и торпидной, классическое описание которых было дано еще нашим великим соотечественником Н.И.Пироговым. Однако, если внимательно рассматривать патогенез различных видов болевого шока, мы можем обнаружить, что патологические изменения, характерные для торпидной стадии, проявляются
3 уже в ходе развития стадии эректильной. В результате, далеко не всегда можно четко
отграничивать эти стадии друг от друга, да и само понятие о комплексной терапии болевого шока не обязательно должно учитывать эту четкую стадийность. Поэтому, когда в дальнейшем мы рассматриваем принципы патогенетической терапии болевого шока, мы рекомендуем обращать внимание, прежде всего, на возможность врача вмешаться в развитие того или иного патогенетического механизма и прервать патологические круги, а не на то, на какой стадии развития шока это вмешательство происходит.
3. Из истории изучения шока
Выше уже указывалось, что с шоком, как с последствием чрезвычайно тяжелых, прежде всего – травматических, повреждений организма первыми пришлось реально столкнуться военным хирургам, которые уже тогда, в XVIII веке, считали, что основной причиной возникновения шока является сильнейшее болевое возбуждение. Именно боль и вызванный ею «паралич» нервной системы (Н.И.Пирогов описывал шок как «общее окоченение тела – травматический торпор или ступор») долгое время считались основным и единственным патогенетическим механизмом шока. Этого мнения, наряду с Пироговым, придерживались, например, Купер (1824) и Тауэрс (1826).
Развитие медицинской науки в XIX и XX веках, появление возможности моделировать различные виды шока у экспериментальных животных и при этом регистрировать изменения, которые претерпевают при шоке те или иные системы организма, позволило физиологам и патологам выявить и другие патогенетические механизмы шоковых состояний. Так H.Fisher (1870) и Mapother (1879), а также A.Malcolm(1905) показали, что на различных стадиях развития шока значительно изменяется состояние кровообращения, возникает как массивная вазодилатация, так и вазоконстрикция определенных сосудистых сетей. В результате, к концу XIX века многие исследователи считали резкое падение артериального давления основной причиной развития шока.
Приблизительно в это же время появились исследования, в которых одним из основных патогенетических механизмов шока описывали токсемию организма, возникающую в результате поступления в кровь продуктов размозженных мышц и тканей (Munde, 1879; Schmidt, Mulcheim, 1889; E.Quenu, 1919). Практически одновременно с этими исследованиями, в 1909 году, Y.Henderson выдвинул теорию акапнии, объясняющую, по его мнению, патогенез травматического шока. Он считал, что гипервентиляция, возникающая как результат возбуждения после полученной травмы, способствует вымыванию углекислоты из крови, что, в свою очередь, резко снижает возбудимость дыхательного центра и приводит к последующей гипоксии организма и ацидозу.
4 Инструментальные возможности, которые получили в свое распоряжение патологи и
клиницисты в ХХ веке, позволили выявить чрезвычайно важную роль нарушений микроциркуляции органов и тканей, возникающие в процессе развития шока (B.Zweifach, R.Chambers, Shorr, 1950 – 1974; А.М.Чернух, 1975). В результате обобщения экспериментальных и клинических данных ко второй половине ХХ века удалось сформулировать положение о «шоковых органах» и, в дальнейшем, учение о полиорганной недостаточности – как о феномене, сопровождающим многие терминальные состояния, в том числе – и шок.
Разбирая в дальнейшем основные патогенетические механизмы шока, мы убедимся, что многие из описанных выше теорий шока являются составными частями патогенеза этого сложного и чрезвычайно опасного для жизни явления.
3. Этиология болевого шока
Все этиологические факторы, способные вызвать развитие болевого шока, можно разделить на две большие группы: экстремальные, повреждающие факторы, исходящие из внешней среды (факторы «экзогенного болевого шока»), и повреждающие факторы, появление которых обусловлено патологией органов и систем организма, возникающей в результате определенных заболеваний (факторы «эндогенного болевого шока»).
К экзогенным факторам болевого шока можно отнести механическую травму, ожоговую травму, поражение организма электрическим током, воздействие на организм сильных кислот и щелочей и многие другие экстремальные факторы внешней среды, способные разрушающе воздействовать на организм. Следует отметить, что во многих случаях мы сталкиваемся с комбинированным одновременным воздействием нескольких экзогенных шокогенных факторов. Например, механической травме может сопутствовать обширные ожоги, раздавливание мягких тканей (краш-синдром), массивное кровотечение. Такая комбинация шокогенных факторов, возникающая достаточно часто при техногенных и геологических катастрофах, безусловно, будет значительно отягощать состояние пострадавшего человека, и вызывать самые тяжелые формы протекания болевого шока.
Эндогенные факторы, вызывающие развитие болевого шока, возникают при ряде патологических состояний, характеризующихся обширными повреждениями внутренних органов (например, кардиогенный шок при массивном инфаркте миокарда, шок при прободной язве желудка, шок, сопровождающий развитие острого панкреатита и т.п.).
Развитие болевого шока в значительной степени определяется состоянием реактивности организма, подвергнувшегося воздействию того или иного шокогенного фактора. Иначе говоря, на развитие шока влияют такие составляющие реактивности организма, как пол, возраст, конституция, наследственность. Проявления реактивности могут как осложнять развитие

5 патогенетических механизмов болевого шока, так и способствовать относительно благоприятному протеканию этой тяжелой патологии.
4. Патогенез болевого шока
Патогенез болевого шока – это сложная комбинация взаимосвязанных и влияющих друг на друга патогенетических механизмов. Среди них можно выделить:
-развитие болевого синдрома и формирование в ЦНС патологических алгических систем;
-изменения системной гемодинамики и микроциркуляции;
-токсемию, энергодефицит и извращение метаболических процессов;
-образование «шоковых органов».
Рассмотрим более подробно каждый из этих патогенетических механизмов.
4.1. Болевой синдром и формирование в ЦНС патологических алгических систем
Развитие болевого синдрома начинается немедленно после воздействия на организм повреждающего (шокогенного) фактора. Повреждение тканей и органов вызывает мощный поток ноцицептивной импульсации, исходящей из затронутых повреждением экстеро- и интерорецепторов, нервных проводников, нервных сплетений. В дальнейшем, по ходу развития шока, к этому потоку присоединяется ноцицептивная импульсация, вызываемая гипоксией тканей, возникшей сначала из-за макроциркуляторных расстройств кровообращения (централизация кровообращения), а затем и из-за расстройств микроциркуляции. Интенсивное болевое возбуждение порождает мощный, но быстро истощающийся психогенный стресс, на пике развития которого концентрация адреналина в крови может повышаться в 6 и более раз, а норадреналина – в два раза. Непрекращающийся и до определенного этапа развития шока усиливающийся приток ноцицептивной афферентации вызывает с одной стороны разрушение стресс-лимитирующих систем мозга 1), а с другой – приводит к развитию недостаточности тормозных нейрональных механизмов: сначала первичной, а затем и вторичной. При этом развитие первичной недостаточности тормозных систем связана с энергетическим истощением нейронов, а вторичная порождается дополнительным притоком ноцицептивной импульсации уже не столько от поврежденных органов и тканей, сколько благодаря массивной гипоксии, охватывающей организм, лишенный нормальной микроциркуляции.
1)В настоящее время описаны (Ф.З.Меерсон, М.Г.Пшенникова, 1988) три стресс-лимитирующие системы:
ГАМК-ергическая, бензодиазепиновая и опиоидергическая. ГАМК-ергическая система реализует свой стресслимитирующий эффект за счет осуществления пресинаптического торможения нейронов, а также за счет пресинаптической блокады выхода нейромедиаторов и, тем самым, блокады передачи возбуждения. Бензодиазепиновая стресс-лимитирующая система основывает свое действие на потенциировании бензодиазепином эффектов ГАМК-ергической системы. Третья стресс-лимитирующая система - опиоидергическая действует благодаря морфиноподобному анальгезирующему воздействию эндогенных опиоидных пептидов.
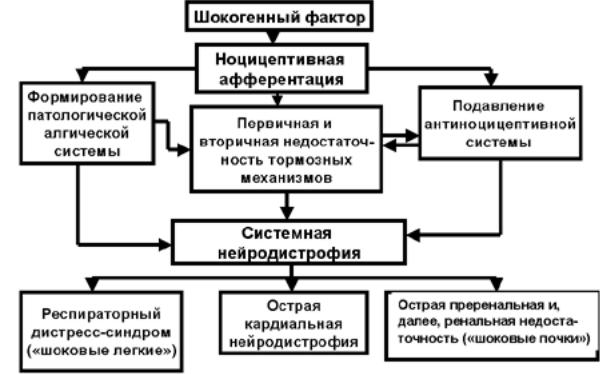
6 И тот, и другой эффекты длительного болевого возбуждения приводят к образованию в
различных отделах ЦНС генераторов патологически усиленного возбуждения, которые по мере развития этой патологии образуют патологические алгические системы (Г.Н.Крыжановский, 1993). Образовавшиеся патологические алгические системы реализуют себя не только расстройствами центральной регуляции функций, но и проявляют свое действие на периферии в виде системных нейродистрофических процессов, повреждающих жизненно важные органы – сердце, легкие, почки. Сведения о патогенезе этих повреждений будут представлены в последующем материале. Схема патогенеза шокового болевого синдрома изображена на Рис.1.
Рис. 1. Схема патогенеза шокового болевого синдрома (по В.Ю.Шанину)
4.2. Изменения системной гемодинамики и микроциркуляции
Как уже было указано ранее, возникновение болевого синдрома при шоке приводит к развитию мощного психогенного стресса, благодаря чему в крови резко возрастает (в несколько раз) концентрация катехоламинов и вазопрессина, выработка которого значительно увеличивается в результате стимулирующего воздействия катехоламинов на нейрогипофиз.
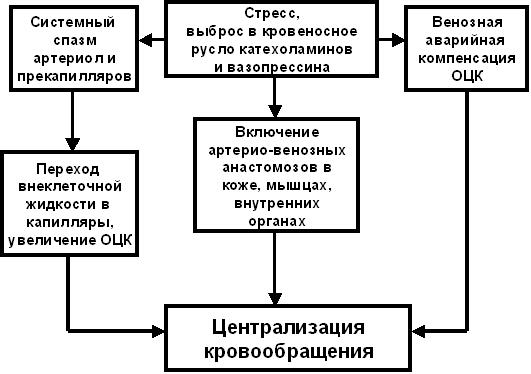
На этой стадии развития шока можно проследить несколько серьезных изменений макроциркуляции, направленных на обеспечение в этой критической ситуации кровоснабжения жизненно важных органов: головного мозга, сердца и, в определенной степени, легких за счет централизации кровообращения (Рис.2.).
7
Рис. 2. Механизмы централизации кровообращения при болевом шоке. Пояснения в тексте.
Так, под влиянием катехоламинов и вазопрессина происходит системный спазм артериол, прекапилляров и венул. С одной стороны это приводит к ускорению кровотока в капиллярном русле, уменьшению гидростатического давления в капиллярах и переходу части внеклеточной жидкости в капилляры, а с другой – спазм венул, имеющих достаточно развитую адренергическую иннервацию, так же выводит в кровеносное русло дополнительные объемы крови. В результате на критическом этапе развития шока увеличение ОЦК и подъем артериального давления определенное время способны поддерживать практически нормальное кровоснабжение головного мозга и сердца.
Дополнительным фактором, обеспечивающим централизацию кровообращения, служит открытие артерио-венозных анастомозов в большинстве внутренних органов, скелетной мускулатуре и коже. Естественно, что при этом кровоснабжение большинства органов и тканей резко ухудшается, в них начинает развиваться гипоксия, гиперкапния и ацидоз. Так, например, почечный кровоток во время развития этой стадии шока снижается более чем в пять раз (С.А.Селезнев и др., 1974). Однако для организма в целом по-прежнему важнейшей задачей остается обеспечение кровоснабжения тех органов, без нормальной деятельности которых его существование просто невозможно.
Централизация кровообращения, предохраняющая на некоторое время жизненно важные органы от повреждающего воздействия шока, по мере его развития приводит все к большему
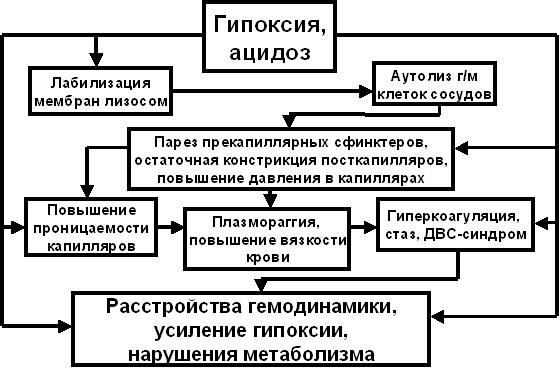
8 циркуляторному и энергетическому «обкрадыванию» и голоданию большинства внутренних
органов и скелетной мускулатуры. В результате в организме начинают нарастать гипоксия и ацидоз. Эти явления в начале сказываются на микроциркуляции наиболее обойденных кровоснабжением органов, а затем и всего организма в целом, не исключая сердечную мышцу и головной мозг (Рис.3.).
Рис. 3. Схема расстройств микроциркуляции при болевом шоке Пояснения в тексте
Возрастающая гипоксия весьма отрицательно сказывается на состоянии микроциркуляторного русла, однако, прежде всего она резко повышает проницаемость стенок капилляров. Во-первых, этому способствует повышение концентрации углекислоты и молочной кислоты, и, как следствие этого явления, дегрануляция тучных клеток и освобождение из них гистамина и серотонина. Во-вторых, проницаемость капилляров повышается благодаря увеличению концентрации кининов, разрушение которых киназами тормозится в условиях гипоксии. Дополнительный вклад в повышение капиллярной проницаемости вносят эйкозаноиды и некоторые другие цитокины, например, фактор некроза опухолей, так же активирующиеся в условиях гипоксии и ацидоза.
Одновременно с развитием этих событий повышается и внутрикапиллярное давление, так как посткапиллярные сфинктеры значительно менее чувствительны к гипоксии, чем сфинктеры прекапиллярные, парез которых возникает на самых ранних стадиях развития гипоксии.
9 Гипоксия вызывает лабилизацию лизосомальных мембран, и лизосомные протеолитические
ферменты, повреждающие многие элементы сосудистой стенки, повреждают так же и гладкую мускулатуру артериол, что служит еще одним фактором, обеспечивающим резкое расширение микроциркуляторного русла и рост давления в капиллярах. В результате суммации этих процессов резко возрастает плазмораггия, повышается вязкость крови, и создаются благоприятные условия для развития стаза и гиперкоагуляции крови, вплоть до развития ДВСсиндрома.
Так возникает порочный гипоксический регуляторный круг, инициированный первичной гипоксией, обусловленной централизацией кровообращения и потенцированный тотальными микроциркуляторными расстройствами. В том случае, если на этом этапе развития шока не предпринимаются радикальные лечебные мероприятия, гипоксия и ацидоз неизбежно приводят к критическим нарушениям метаболизма, возникновению шоковых органов и полиорганной недостаточности.
4.3. Развитие токсемии, энергодефицита и извращение метаболических процессов
Тотальное нарушение микроциркуляции усугубляет в организме, подвергнувшемуся воздействию болевого шока, развитие гипоксии. При этом, с одной стороны, нарастающий энергодефицит смещает энергопродуктивные процессы в сторону гликолиза и липолиза, а с другой, остающийся избыток катехоламинов вызывает разобщение процессов окисления и фосфорилирования и, тем самым, еще более увеличивает энергодефицит (Рис.4.).
Усиление перекисного окисления липидов (ПОЛ) способствует образованию избытка свободных радикалов и снижает антиоксидантную защиту клеток органов и тканей. Это не только приводит к разрушению клеточных мембран и гибели клеток путем некроза, но и стимулирует апоптоз. Другим фактором, способствующим развитию апоптоза, является повышенная продукция оксида азота (NO), а также ряда цитокинов (например, фактора некроза опухолей альфа).
К повреждению клеточных мембран и аутолизу клеток приводит и выход лизосомальных ферментов в результате гипоксической лабилизации мембран этих клеточных органелл. Клеточный энергодефицит нарушает работу натрий-калиевого насоса, клетки теряют ионы калия, в них проникают ионы натрия, а вслед за ними и вода. Набухание и последующая деструкция митохондрий еще более разобщают процессы окисления и фосфорилирования, энергодефицит становится необратимым.
В конечном итоге, каскад патологических процессов приводит к необратимым разрушениям органов и тканей, образованию «шоковых органов» и полиорганной недостаточности.

10
Рис. 4. Роль токсемии и энергодефицита в патогенезе болевого шока. Пояснения в тексте ПОЛ – перекисное окисление липидов; ПОН – полиорганная недостаточность
Термин «полиорганная недостаточность» или «синдром полиорганной недостаточности - СПОН» прочно утвердился в медицинской литературе в начале 80-х годов прошлого века, когда клиницисты вообще, и реаниматологи, в частности, убедительно показали, что выпадение функций трех или более органов и систем пациента, как правило, ассоциируется с крайне неблагоприятным исходом.
В большинстве случаев СПОН представляет собой тяжелую неспецифическую стрессреакцию организма в ответ на мощное экзогенное воздействие, сопровождающееся недостаточностью двух или более его функциональных систем с преобладанием симптомов той или иной органной дисфункции. Развитие СПОН носит характер стремительно развивающейся, обвальной патологии органов и систем организма, в основе которой, как правило, лежит серьезное расстройство микроциркуляции, развитие острого респираторного дистресссиндрома, печеночной и почечной недостаточности, резкого нарушения функции сердечнососудистой системы.
Чрезвычайно важным патологическим фактором, значительно осложняющим течение СПОН, является развитие синдрома гиперметаболизма (аутоканнибализма) организма. По своей сути гиперметаболические изменения должны были бы нести защитный характер, привлекая на
