
Биологически активные органические соединения
.pdf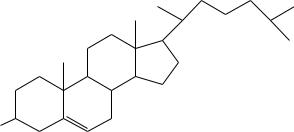
HO |
Холестерин |
цикл А |
цикл В |
В холестерине пятичленный цикл связан с углеводородным радикалом, содержащем 8 атомов углерода.
Если гидроксильная группа не связана с остатком высшей жирной кислоты, такое соединение принято называть холестерин свободный (ХС), если гидроксигруппа этерифицирована, то холестерин этерифицированный.( ХЭ )
ХС присутствует совместно с ФЛ в |
мембранах клеток, ХЭ входит в состав сложных |
белков крови липопротеинов (ЛП ) и |
из них поступает в цитоплазму клеток.В |
мембранах клеток, за исключением мембран эритроцитов, холестерин этерифицированный не содержится.
В организме человека холестерин превращается в стероидные гормоны, витамин Д и желчные кислоты. С нарушением обмена холестерина связано тяжелое заболевание
атеросклероз. Растительные стерины не вызывают развитие атеросклероза.
Холестерин дает множество цветных реакций, которые позволяют провести его качественное обнаружение и количественное определение. Чаще всего применяют реакцию Сальковского: образец, содержащий холестерин, обрабатывают хлороформом, добавляют концентрированную серную кислоту. Хлороформный слой окрашивается в красный цвет, а кислотный слой флуоресцирует зеленым цветом.
4.3 Принципы создания липотропных лекарственных препаратов
Эмульгирующая способность липидов нашла применение в создании транспортных форм для лекарств. Биоактивное вещество включают в состав липосомы.
Липосома представляет собой пузырькообразную частицу, которая состоит из множества замкнутых фосфолипидных бислоев, разделенных водными промежутками.
Липосомы бывают моноламеллярные (однослойные) и мультиламеллярные |
|
|||
(многослойные). В процессе приготовления |
липосом в их внутреннее |
водное |
||
пространство включаются те вещества, которые присутствовали в растворе. |
В состав |
|||
липосом |
можно включать водорастворимые |
антигены, лекарственные препараты, |
||
гормоны, |
витамины, фрагменты нуклеиновых |
кислот. Липосомы |
проходят через |
|
липидные слои мембраны и переносят внутрь клетки содержащиеся в них вещества вещества, которые иначе не смогли бы преодолеть барьер мембраны..
4.4 Строение и химический состав мембран клеток
В 1972 г. С. Дж Синджер и Г.Л. Николсон предложили модель молекулярной организации мембраны, которая получила название жидко-мозаичной модели. . Структурной основой является липидный бислой, в котором углеводородные цепи высших карбоновых находятся в жидкокристаллическом состоянии. В этот вязкий слой включены молекулы белков, которые могут достаточно свободно перемещаться в
61
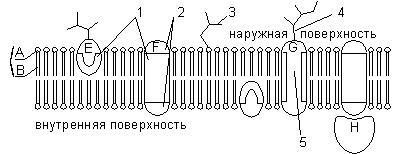
мембране и молекулы свободного неэтерифицированного холестерина.. Белки подразделяют на два типа: периферические и интегральные. Периферические белки достаточно легко отделяются от мембраны и связаны с ней за счет полярного и ионного взаимодействия. Интегральные белки располагаются внутри мембраны, имеют на своей поверхности большие гидрофобные участки, для их выделения необходимо разрушение мембраны. Модель С. Дж Синджера и Г.Л. Николсона не является окончательной (в науке редко бывают «неприкасаемые» истины) , она уточняется и разрабатывается в современных исследованиях (рисунок ).
Рис. Строение мембраны:
А — гидрофильная головка фосфолипида; В — гидрофобные хвостики фосфолипида; 1 — гидрофобные участки белков Е и F; 2 — гидрофильные участки белка F; 3 — разветвленная олигосахаридная цепь, присоединенная к липиду в молекуле гликолипида (гликолипиды встречаются реже, чем гликопротеины); 4 — разветвленная олигосахаридная цепь, присоединенная к белку в молекуле гликопротеина; 5 — гидрофильный канал (функционирует как пора, через которую могут проходить ионы и некоторые полярные молекулы).
Жидкокристаллическое состояние мембраны обозначают термином «текучесть». Биологические и физико-химические свойства мембран ухудшаются при появлении транс-изомеров полиненасыщенных кислот, продуктов окисления двойных связей в составе этих кислот, при частичном гидролизе фосфолипидов и белков. В тоже время перечисленные превращения входят в обязательный комплекс изменений, связанных с процессами адаптации к меняющимся условиям среды существования организма.
Дисциплинарный модуль 4 Обмен белков, аминокислот, нуклеотидов в организме человека
Для успешного усвоения этой темы необходимо
Знать
-классификацию белков по составу, строению третичной структуры, биологической ценности для организма человека, -заменимые и незаменимые аминокислоты,
- особенности химического и пространственного строения (стереоизомерию) аминокислот , присутствующих в организме человека и продуктах питания, физические свойства,
-химические свойства аминокислот, определяющие их биологическую активность in vivo. -физические и химические свойства биоактивного вещества мочевины, конечного продукта обмена аминокислот в организме -физические и химические свойства , явление таутомерии азотистых оснований пуринового и пиримидинового ряда, мочевой кислоты.
-структурные формулы нуклеозидов, нуклеотидов,
Уметь
62
- записать структурные формулы изучаемых аминокислот, мочевины, азотистых оснований, нуклеозидов и нуклеотидов, образованных азотистыми основаниями.
-составить схемы реакций декарбоксилирования, переаминирования (трансаминирования) -написать реакцию окислительного дезаминирования глутаминовой кислоты
Ключевые слова к теме:
Аденин, аминокислота, амфотерность, буферный раствор, витамин В6, гипоксантин, гуанин, дезаминирование, декарбоксилирование, изоэлектрическая точка, ксантин, мочевина, мочевая кислота, нуклеозид, нуклеотид, окислительное дезаминирование, основание Шиффа (азометин), пептид (полипептид), пептидная группа, переаминирование (трансаминирование), стереоизомер, стереоряд, тимин, урацил, цитозин, энантиомер.
5.1 Номенклатура, классификация природных аминокислот (Примечание. Общий список природных аминокислот, структурные формулы представлены на стр. 17-20)
Аминокислоты - большой класс органических соединений. характерным признаком которых является наличие в составе молекулы двух функциональных группкарбоксильной и аминогруппы. Особую группу составляют природные аминокислоты. Их условно можно разделить на 2 группы:
- аминокислоты , которые участвуют в образовании пептидов и белков. Для них характерно только а- строение и все принадлежат к L – стереоряду.
- аминокислоты, которые обладают биологической активностью, но не являются мономерами природных полимеров белков и пептидов.
Природные а –L - аминокислоты – мономеры полипептидов и белков.
Обычно выделяют около 20 природных аминокислот , из которых образуется все множество природных белков растительного и животного происхождения.
Единый генетический код природы определяет единство аминокислотного состава белков.
Номенклатура природных аминокислот: применяются тривиальные названия.
Природные аминокислоты классифицируют по нескольким признакам:
1) биологическому : в отношении обмена веществ в организме человека различают два вида аминокислот
заменимые( синтезируются в клетках человека) :
аланин, аргинин, аспарагиновая кислота, глицин, глутаминова кислота, гистидин, пролин, серин, тирозин, цистеин,
незаменимые( не синтезируются в клетках человека, должны поступать с продуктами питания) :
валин, изолейцин, лейцин, лизин, метионин, треонин, триптофан, фенилаланин Для детей дополнительно незаменимыми являются аргинин и гистидин.
2) химическому , который связан со строением и составом радикала 3) физикохимическому, в основу которого положены кислотноосновные свойства:
различают нейтральные , кислые , основные аминокислоты.
5.2 Особенности пространственного и структурного строения
Природные аминокислоты относятся к L – стереоряду и имеют а- строение (это означает, что обе функциональные группы - амино- и карбоксильная - связаны с общим атомом углерода, который всегда оптически активный (за исключением глицина – аминоуксусной кислоты). Исследованию пространственного строения природных аминокислот посвящены фундаментальные работы Э.Фишера, П. Каррера.
63
R –C*H – COOH |
COOH |
NH2 - СН2- СООН |
| |
| |
глицин |
NH2 |
NH2 - *C – H |
|
|
| |
|
RL – стереоряд
5.3Химические свойства аминокислот in vivo
Физические, химические, кислотно-основные свойства природных аминокислот
обсуждались на стр.4 - 8 (Модуль1).
5.3.1 Декарбоксилирование
Общая реакция для всех природных а- аминокислот , в которой участвуют ферменты декарбоксилазы при участии витамина В6. Образуются вещества с выраженной биологической активностью – биогенные амины.
R – CH – COOH |
фермент декарбоксилаза |
|
||
|
| |
————> |
R – CH2 - NH2 |
+ CO2 |
|
NH2 |
В6 |
биогенный амин |
|
|
Аминокислота |
|
|
|
Синтез важнейших биоактивных соединений |
связан с декарбоксилированием серина, |
|||
глутаминовой кислоты, |
гистидина , 5-окситриптофана, диоксифенилаланина ( в |
|||
последнем случае образуется вначале дофамин, затем норадреналин и адреналин) |
||||
СН2 - СНСООН ———> НО - СН2 – СН2 |
- NH2 + СО2 |
|
||
| |
| |
аминоэтанол( коламин) |
|
|
OH |
NH2 |
|
|
|
серин
Аминоэтанол является предшественником в синтезе холина и медиатора ацетилхолина. Аминоэтанол и холин входят в состав фосфолипидов: аминоэтанол – кефалина, холинлецитина.
фермент глутаматдекарбоксилаза
НООССН2 -СН2 -СН-СООН |
———> НООССН2 -СН2 -СН2 -NH2 + CO2 |
| |
γ -аминомасляная кислота ( ГАМК) |
NH2 |
|
глутаминоая кислота |
|
4-Аминобутановая кислота (γ -аминомасляная кислота , ГАМК) - медиатор торможения ц.н.с.. применяется как лекарственный препарат( аминалон, гаммалон ). У экспериментальных животных недостаток витамина В6 сопровождается дефицитом образования нейромедиаторов и проявляется возникновением судорог, напоминающих эпилепсию .
5.3.2 Дезаминирование
Различают два вида дезаминирования : неокислительное и окислительное.
64
Неокислительное дезаминирование
Различают несколько видов неокислительного дезаминирования:
*элиминирование аминогруппы – получается непредельная кислота
*гидролитическое – аминокислота превращается в гидроксикислоту
*восстановительное – образуется насыщенная аминокислота
*трансаминирование (переаминирование). Представляет собой основное направление обмена аминокислот в организме человека.
Трансаминирование (переаминирование)
Эта чрезвычайно важная реакция, которая протекает во всех тканях организма человека, но особенно активно в печени, почке, миокарде, сводится к взаимопревращению двух различных аминокислоты и кетокислотыобразуются новая аминокислота и новая кетокислота. В результате трансаминирования вступают в обмен веществ аминокислоты, поступающие в составе белков, синтезируются заменимые кислоты.
R1 - CH –COOH |
+ R2 – C- COOH |
———> R 2 - CH –COOH |
+ R1 – C- COOH |
|
| |
| | |
<——— |
| |
| | |
NH2 |
О |
|
NH2 |
О |
аминокислота (1) |
кетокислота( 1) |
|
аминокислота(2) |
кетокислота( 2) |
Наиболее важные пары :
аланин + щавелевоуксусная кислота <=== > ПВК + аспарагиновая кислота аланин + а -кетоглутаровая кислота <===> ПВК + глутаминовая кислота аспарагиновая кислота+ а –кетоглутаровая <=== >ЩУК + глутаминовая
кислота кислота В составе катализаторовферментов обязательно присутствует витамин В6
Элиминирование аминогруппы Реакция характерна для бактерий и грибов. Для примера можно привести превращение
аспарагиновой кислоты в фумаровую
|
Н |
СООН |
НООС- СН2-СН-СООН ———> |
> С = С < |
+ NH3 |
| |
НООС |
Н |
NH2 |
фумаровая кислота( транс-бутендиовая) |
|
Окислительное дезаминирование
Рассмотрите внимательно еще раз схему трех наиболее важных реакций
трансаминирования. |
В двух из них участвует |
а-кетоглутаровая кислота, а образуется |
глутаминовая. Для |
непрерывности процесса |
необходимо превратить обратно |
глутаминовую кислоту в а -кетоглутаровую. В клетках организма человека это происходит путем реакции окислительного дезаминирования.
В организме человека только глутаминовая кислота участвует в обратимой реакции окислительного дезаминирования, схема которой приведена ниже.
НООС-СН2-СН2 -СН-СООН |
+ НАД + —> НООС-СН2-СН2-С-СООН + НАДН + Н+ |
| |
| | |
NH2 |
NH |
65

глутаминовая кислота иминоглутаровая
Далее иминоглутаровая кислота подвергается гидролизу , образуется кетоглутаровая
кислота и аммиак |
|
НООС-СН2-СН2-С-СООН + НОН |
—> НООС-СН2-СН2-С-СООН + NH3 |
| | |
| | |
NH |
О |
|
а-кетоглутаровая кислота |
5. 4 Строение витамина В6 и механизм реакции с его участием
Каталитическая роль витамина В6 в реакциях декарбоксилирования и транстаминирования аминокислот сводится к образованию промежуточного соединения - азометина (основания Шиффа) (реакция нуклеофильного присоединенияэлиминирования воды). Витамин В6 существует в трех активных формах. В реакции декарбоксилирования участвует пиридоксамин, а в переаминировании - амино- и альдегидная.
|
|
|
CH2OH |
|
|
|
CHO |
|
|
|
CH2NH2 |
|||
HO |
|
|
|
CH2OH |
HO |
|
|
|
CH2OH |
HO |
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
||||||
H3C |
|
|
|
|
H3C |
|
|
|
|
H3C |
|
|
|
|
|
N |
|
N |
|
N |
|||||||||
Пиридоксин |
Пиридоксаль |
Пиридоксамин |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||
Витамин В6
Все 3 формы витамина — бесцветные кристаллы, хорошо растворимые в воде. Активны в виде фосфорных эфиров – пиридоксальфосфата , пиридоксаминофосфата
R - OH + АТФ ———> R – OРО3 Н2 + АДФ
активный витамин В6
Схема реакции переаминирования |
|
||
|
|
- НОН |
изомеризация |
R1 - CH –COOH |
+ В6 – СН = О < =======> R1 |
- CH –COOH < =======> |
|
| |
|
|
| |
NH2 |
|
|
N=СН - В6 |
аминокислота |
пиридоксальфосфат |
азометин ( 1) |
|
|
+ НОН |
|
|
R1 - C –COOH |
< =======> |
R1 - C –COOH + В6 – СН2 - NH2 |
|
| | |
гидролиз |
| | |
|
N — СН2 - В6 |
О |
|
|
азометин( 2) |
|
кетокислота |
пиридоксаминфосфат |
Аминокислота реагирует с пиридоксальфосфатом - альдегидной формой витамина В6 . Образуется азометин(1), который изомеризуется в азометин (2). После гидролиза образуется кетокислота и аминоформа витамина В6пиридоксаминфосфат. Пиридоксаминфосфат реагирует с новой кетокислотой, реакция проходит в обратном направлении в соответствии со схемой через образование азометина (2), затем азометина(1) . Кетокислота в итоге превращается в аминокислоту, а витамин В6 вновь возвращается в альдегидную форму.
5.5 Медико - биологическое значение аминокислот
66
Кроме участия в биосинтезе белков, аминокислоты выполняют множество других самостоятельных функций.
1. участвуют в биосинтезе нейромедиаторов и гормонов:
-из аминокислоты серина образуется медиатор парасимпатической нервной системы ацетилхолин
-из фенилаланина или тирозина образуется медиатор симпатической нервной системы
норадреналин и гормоны адреналин, тироксин. - из глутаминовой кислоты синтезируется ГАМК
2.аминокислоты глицин, глутаминовая обладают нейромедиаторными функциями
3.аспарагиновая кислота необходима в синтезе азотистых оснований нуклеиновых кислот( аденина, гуанина, урацила, тимина, цитозина)
4.глутаминовая и аспарагиновая кислоты участвуют в обезвреживании аммиака
5.аминокислота метионин передает свою активную метильную группу для образования тимина., холина, адреналина.
6.в условиях углеводного голодания из аминокислот в организме человека синтезируется глюкоза.
Поэтому аминокислоты используются в качестве лекарственных препаратов: глутаминовая, метионин, глицин, цистеин, триптофан.
5.6 Строение, физмко-химические свойства мочевины.
Мочевинатвердое кристаллическое вещество, игольчатые кристаллы, холодящее на вкус.Растворима в воде, одно – и многоатомных спиртах. При комнатной температуре растворяется 104 г в 100 г воды.
Мочевина – конечный продукт обмена пищевых белков, белков организма и аминокислот. Содержится во всех биологических жидкостях организма, стабилизирует структуры белков, нуклеиновых кислот, участвует в поддержании постоянства значения рН внутренней среды организма. Выделяется в составе мочи в количестве до
30 г/ сутки. Мочевина NH2 - CO - NH2 - однокислотное основание. |
|
|
||
По современным данным протон присоединяется к атому кислорода и |
положительный. |
|||
заряд равномерно распределяется (делокализуется) между четырьмя атомами. |
|
|||
R- С=О |
NH2 -C - NH2 + НNO3 —> NH2 -C - NH2 |
|
||
| |
|| |
|| |
. NO3 |
- |
NH2 |
O |
+ ОН |
|
|
амид |
мочевина ( карбамид) |
соль нитрат мочевины |
|
|
|
хорошо растворима |
плохо растворима |
|
|
|
в воде |
|
|
|
Под действием фермента уреазы, которая присутствует у большинства микроорганизмов, в бобовых растениях, при нагревании с серной кислотой гидролизуется до аммиака и углекислого газа.
(NH2)2 CО + Н2О —> 2 NH3 + CО2
Мочевина обладает комплексообразующими свойствами, способна к образованию клатратов – соединений включения, участвует в стапбилизации третичной структуры белков и сложных надмолекулярных соединений, например, мембран клеток. Входит в состав гигиенических средств, зубных паст, кремов.
5.7 Азотистые т основанияпроизводные пиримидина (урацил, тимин, цитозин)
67
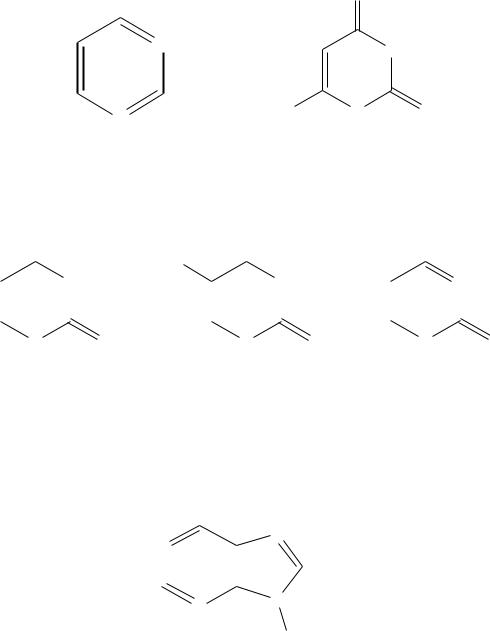
Пиримидин (1,3 - диазин) – гетероароматическое соединение. слабое основание (оба атома азота сохраняют основные свойства)
Производные пиримидина , содержащие в цикле гидрокси- и аминогруппывходят в состав нуклеиновых кислот, и их называют пиримидиновые азотистые основания. К ним относятся урацил, тимин, цитозин.
В клетке исходным соединением в синтезе пиримидиновых азотистых оснований является оротовая кислота–2,6–диоксопиримидин-4-карбоновая кислота.(4- карбоксиурацил). После декарбоксилирования в составе нуклеозида образуется урацил, а из него тимин( путем метилирования) и цитозин.
O
|
N |
|
NH |
|
|
|
|
N |
HOOC |
N |
O |
|
H |
|
Пиримидин
Оротовая кислота
|
|
|
O |
|
|
|
|
|
|
|
O |
|
|
|
|
NH2 |
|
||||
|
|
|
|
NH |
|
H3C |
|
|
|
|
|
|
NH |
|
|
N |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
O |
|
|
|
|
|
N |
|
O |
|
N |
O |
|||||||
|
|
H |
|
|
|
|
|
|
H |
|
|
|
H |
|
|||||||
|
|
Урацил |
|
|
|
|
Тимин |
|
|
|
Цитозин |
|
|||||||||
2,4-диоксопиримидин 2,4- диоксо-5-метилпиримидин |
2 –оксо -4-аминопиримидин |
||||||||||||||||||||
5.8 Азотистые основанияпроизводные пурина( аденин, гуанин) |
|
||||||||||||||||||||
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
7 |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
1 N |
|
|
N |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
8 |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
4 |
|
|
N 9 |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3
H
пурин
Пуринконденсированное гетероароматическое соединение, в составе которого два гетероциклических соединения: пиримидин и имидазол. Обратите внимание на правило
68
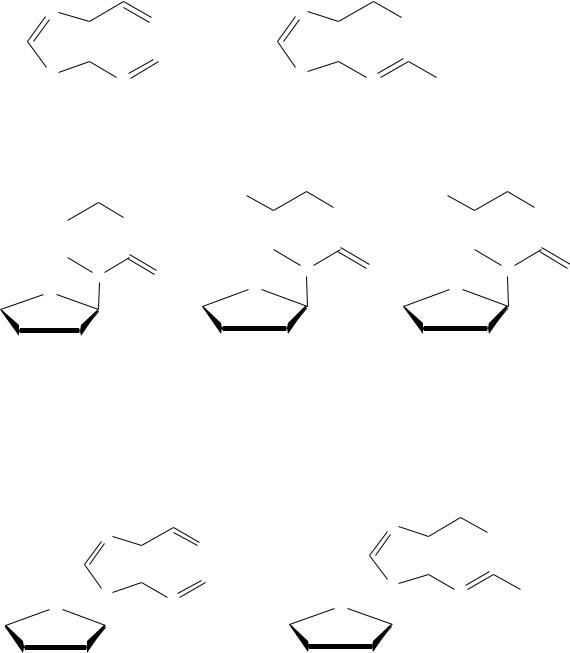
нумерации атомов. Атом водорода может занимать два положения: |
у атома N9 |
и у |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
атома N7 ( устанавливается равновесие между двумя изомерами) |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||
В |
составе нуклеиновых кислот ДНК и РНК обнаружены два соединения, производные |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
пурина: аденин и гуанин. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
NH |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
N |
N |
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
аденин |
|
|
|
|
|
|
|
|
|
|
|
|
|
гуанин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
6-аминопурин |
|
|
|
|
|
|
|
|
|
|
|
2-амино-6-оксопурин |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH |
|
|
|
|
|
H3C |
|
|
|
|
|
|
NH |
|
|
|
|
|
|
|
H3C |
|
|
|
|
|
|
|
|
|
NH |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
N |
O |
|
|
|
CH2OH |
|
|
|
|
|
|
N |
O |
||||||||||||||||||
CH2OH |
|
|
|
N |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
H |
H |
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
H |
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
H |
|
|
|
H |
|
|
|
|
|
H |
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
H |
|
||||||||||||||||||||
|
|
|
OH |
OH |
|
|
|
|
|
OH |
|
|
OH |
|
|
|
|
|
|
|
OH |
|
|
|
|
H |
|
|||||||||||||||||||||||||||||||
|
|
|
|
Уридин |
|
|
|
|
|
|
|
|
|
|
|
|
Тимидинрибозид |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Тимидин |
|
||||||||||||||||||||||||
В |
природных нуклеозидах, |
|
|
содержащих |
|
аденин, |
|
|
|
гуанин , гипоксантин и другие |
||||||||||||||||||||||||||||||||||||||||||||||||
пуриновые соединения, |
|
всегда образуется |
|
|
N9 -β- гликозидная связь |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
NH |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
NH2 |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
CH2OH |
|
|
|
|
N |
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
H |
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
OH |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
OH |
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Аденозин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Дезоксигуанозин |
|
|||||||||||||||||||
5.9 Нуклеотиды
Нуклеотидыфосфорные эфиры нуклеозидов.
Их химический состав: азотистое основание( А.О.) + пентоза + фосфорная кислота
69
Фосфорные эфиры образуются с участием |
гидроксильных групп пентоз . Места |
||||
положения фосфорноэфирных |
групп принято обозначать, |
используя обозначение ( ' ) , |
|||
например: 5' , 3 ' |
|
|
|
|
|
Предварительная краткая информация: нуклеотиды играют |
чрезвычайно важную роль в |
||||
жизнедеятельности клетки. |
|
|
|
|
|
Классификация нуклеотидов |
|
|
|
|
|
Нуклеотиды, |
состоящие из |
одной молекулы |
А.О, пентозы, фосфорной кислоты, |
||
называются |
мононуклеотидами. Мононуклеотиды могут содержать одну молекулу |
||||
фосфорной кислоты , две или |
три молекулы фосфорной кислоты, соединенных друг с |
||||
другом. |
|
|
|
|
|
Комбинация из двух мононуклеотидов называется динуклеотидом. В |
составе |
||||
динуклеотида |
обычно присутствуют разные азотистые основания или одно другое |
||||
циклическое соединение, например, витамин.. |
|
|
|
||
Особую роль в биохимических процессах играют циклические мононуклеотиды. |
|
||||
Номенклатура |
мононуклеотидов. |
|
|
|
|
К названию нуклеозида добавляют в зависимости от количества фосфатных остатков, « монофосфат », « дифосфат », « трифосфат », с указанием их места положения в цикле пентозыцифровое обозначение места со значком ( ' ) ,
Положение фосфатной группы в положении (5') является наиболее распространенным и типичным, поэтому его можно не указывать ( АМФ, ГТФ, УТФ, дАМФ и т.д.) Остальные положения обозначаются обязательно ( 3'- АМФ, 2'- АМФ , 3'- дАМФ )
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
N |
|
|
N |
||
|
|
|
|
|
|
||||
|
CH2OPO3H2 |
|
N |
|
|
||||
|
|
|
|||||||
|
|
|
|
|
|
||||
|
|
|
N |
||||||
|
|
|
|
|
|||||
|
|
O |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
H |
H |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
H |
|
|
H |
|
|
|
|
||
|
OH |
OH |
|
|
|
|
|||
5'-аденозинмонофосфат (5'- АМФ или АМФ )
Мочевая кислота
Поступающие в организм пуриновые соединения (в составе пищи, лекарственных препаратов – аденин, гуанин, кофеин, теофиллин, теобромин) и синтезированные в организме в конечном итоге превращаются в мочевую кислоту. Азотистые основания, поступившие с пищевыми продуктами, не используются для синтеза нуклеотидов и нуклеиновых кислот
Схема обмена азотистых оснований :
70
