

Характеристика металлов VIII В группы
В побочной подгруппе VIII группы периодической системы 9 элементов: железо, кобальт, никель, рутений, родий, палладий,
осмий, иридий, платина.
Сходные между собой элементы этой подгруппы образуют горизонтальные группировки, так называемые триады.
Железо, кобальт и никель образуют триаду железа, или
семейство железа.
Остальные элементы VIII группы составляют семейство платиновых металлов, которое включает триады палладия и
платины.
По своим свойствам эти семейства существенно различаются между собой.
Атомы элементов триады железа имеют на внешнем энергетическом уровне по 2 электрона, которые они легко отдают в химических реакциях.

Триада железа
Однако они могут отдавать электроны и с Зd-орбиталей второго снаружи уровня.
Поэтому в своих устойчивых соединениях эти элементы проявляют степени окисления +2 и +3.
Образуют оксиды состава RO и R203 (R – элемент). Им соответствуют гидроксиды состава R(OH)2 и R(OH)3.
Для элементов триады (семейства) железа характерна особенность присоединять нейтральные молекулы, например оксид углерода (II), оксид азота (II).
Кобальт и никель менее реакционноспособны, чем железо.
При обычной температуре они устойчивы к коррозии на воздухе, в воде и в различных растворах.
Разбавленные соляная и серная кислоты легко растворяют
железо и кобальт, а никель – лишь при нагревании. Концентрированная азотная кислота все три металла
пассивирует.

Триада железа
Металлы семейства железа при нагревании взаимодействуют с кислородом, парами воды, галогенами, серой, фосфором, кремнием, углем, бором.
Наиболее устойчивыми являются соединеняя железа (III), кобальта (II) и нииеля (II).
Железо, кобальт и никель в ряду стандартных электродных потенциалов расположены до водорода, платиновые металлы – после.
Поэтому первые распространены в природе в виде соединений (оксиды, сульфиды, сульфаты, карбонаты), в свободном состоянии встречаются редко – в виде железных метеоритов.

Триада железа
Платиновые металлы встречаются только в свободном состоянии.
По распространенности в природе за железом следует никель, а затем кобальт.
Соединения элементов семейства железа в степени окисления +2 очень сходны между собой.
В состоянии высших степеней окисления проявляют окислительные свойства.
Железо, кобальт, никель и их сплавы –важные материалы современной техники.
Но наибольшее значение имеет железо.
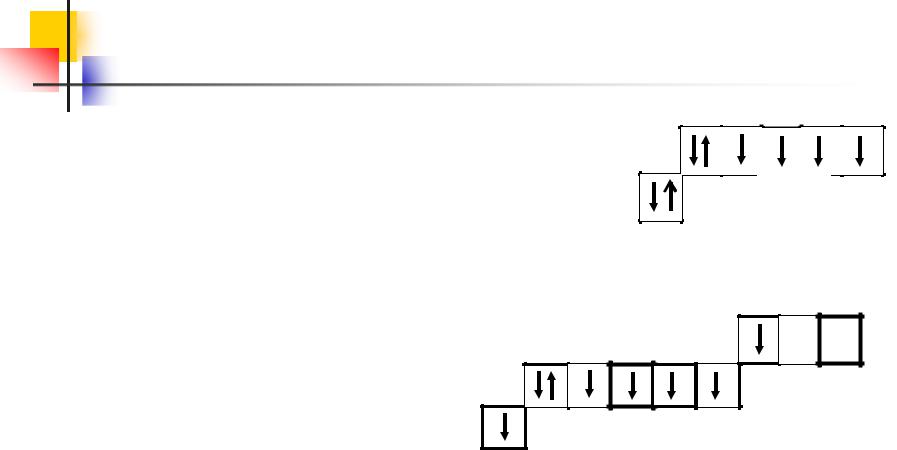
Железо
Запишем электронно-графическую формулу
 атома железа в нормальном состоянии:
атома железа в нормальном состоянии:
26 Fe 1s2 2s2 2 p6 3s2 3 p6 4s2 3d 6 |
|
3d |
|
в возбужденном состоянии: |
4s |
В' = 4 |
|
26 Fe* 1s2 2s2 2 p6 3s2 3 p6 4s13d 6 4 p1 |
|
|
|
|
4p |
3d |
В' = 6 |
4s |
|
Степени окисления железа в соединениях: Fe2+, Fe3+, Fe6+.

Нахождение в природе
Содержание железа в земной коре составляет 4÷5 % по массе и оно встречается в виде минералов:
Магнитный железняк (магнетит) – Fe3O4
(FeO·Fe2O3);
Красный железняк (гематит) – Fe2O3;
Бурый железняк (сидерит) – 2Fe2O3 3Н2О;
Шпатовый железняк - FeСO3;
Железный колчедан (пирит) – FeS2.

Нахождение в природе
В свободном состоянии железо находится только в метеоритах.
Количество железных руд в России
составляет более половины мировых запасов.
Самые крупные месторождения руд в Керчи, Кривом Роге, вблизи Курска, на Урале, в Кузбассе и т.д.

Получение
Промышленным способом получают
сплавы железа. Это чугун и сталь.
Современная схема получения стали состоит из доменного и сталеплавильного процессов.
Химические реакции, лежащие в основе производства чугуна
В ходе доменного процесса из руды
получают чугун – сплав железа с углеродом.

Получение
В домну послойно загружают кокс и агломерат (обогащенную руду и флюсы).
Флюс (CaF2) добавляют к руде, чтобы понизить температуру плавления руды.
Снизу домны подают кислородное дутье (воздух, обогащенный кислородом)
и кокс сгорает: С О 15000 С СО .
+ 2 → 2 ↑
0
СО2 +С 1500 С→СО ↑.

Получение
Угарный газ СО восстанавливает оксиды железа из руды в верхней части домны:
Fe2O3 +CO 450−5000 C →Fe3O4 +CO2 ↑;
0
Fe3O4 +CO 600 C →FeO +CO2 ↑;
0
FeO +CO 700 C →Fe +CO2 ↑;
FeO +C >7000 C →Fe +CO2 ↑.

Получение
Одновременно с железом идет из руды
восстанавливаются:
SiO2 +C >13000 C →Si +CO ↑.
MnO +C >13000 C →Mn +CO ↑.
Са3 (РO4 )2 +C >13000 C →Р+СаО+CO ↑.
шлак

Получение
Шлак состоит из силикатов, алюмосиликатов, пустой породы и флюсов.
Из домны выходит колошниковый газ:
25% СО, СО2, N2. Его сжигают для предварительного нагревания вдуваемого в печь воздуха.
Снизу домны выпускают чугун – сплав железа с углеродом, где углерода
4÷5 % по массе.

Получение
В состав чугуна входят:
Fe – 93 %,
C – 4-5 %;
Mn – 1-3 %;
P – 0.02-2.5 %;
Si – 0.5-2 %;
S (FeS) – 0.005-0.1 %.

Получение
Доменный процесс – восстановительный.
Восстановителями являются монооксид углерода (СО) и кокс (С).
Метод получения чугуна –
пирометаллургия (карботермия).
В зависимости от условий кристаллизации различают чугун серый и белый.

Получение
В сером чугуне углерод присутствует в виде пластинок графита.
Серый чугун используют в литейном производстве.
Белый чугун содержит весь углерод в виде цементита (Fe3C). Он хрупок и его используют в сталеплавильном переделе.

Химические реакции, лежащие в основе  сталеплавильного производства
сталеплавильного производства
Существует несколько способов переработки чугуна в сталь:
мартеновский, конвертерный и электросталеплавильный.
Все процессы выплавки стали основаны
на окислении углерода и примесей в
чугуне кислородным дутьем
(воздухом, обогащенным кислородом) и
удалении их в газовую фазу и в шлак .

Химические реакции, лежащие в основе сталеплавильного производства
С +О2 →СО ↑; СО+О2 →СО2 ↑;
Si +О2 → SiO2 ;
Мn +О2 → MnO;
Р+О2 → Р2О5 ;
Р2О5 +СаО →Са3 (РO4 )2 СаО;
в шлак
FeS +CaО →CaS + FeO.

Химические реакции, лежащие в основе  сталеплавильного производства
сталеплавильного производства
Присутствие фосфора придает стали
хрупкость.
В присутствии серы раскаленный металл дает трещины при механической обработке.
Содержание углерода в стали не должно превышать 2,14 %.
При выплавке специальных марок стали добавляют легирующие элементы:
Cr, Ni, Mn, V, Mo, …
Разработан непрерывный процесс
производства стали.

Получение
Чистое железо получают при термическом разложении
пентакарбонила железа (жидкость бледно-желтого цвета):
Fe(CO)5 t →Fe +5CO ↑.

Физические свойства
Железо – металл серебристо-белого цвета.
Легко подвергается коррозии, ржавеет. Образующиеся при этом оксиды
рыхлые и не защищают металл от дальнейшего окисления.
Fe +O2 + H2O → FeO Fe2O3 H2O.
Железо обладает магнитными свойствами, легко
куется, прокатывается в листы.

Физические свойства
В зависимости от температуры кристаллизации железо имеет
несколько модификаций:
αFe →βFe →γFe →σFe . |
||
7690 C |
9100 C |
14100 C |
Железо в обычных условиях это
Магнитными свойствами обладает лишьαFe .

Физические свойства
Для железа:
температура плавления –Тпл =15360 С;
плотность – ρ = 7,9 г/ см3 ;
стандартный электродный
ϕFe0 2+ = − 0.44 B.
Fe

Химические свойства
Главное свойство всех металлов – отдавать электроны:
Fe −ne = Fen+.
1. Отношение к кислороду.
Железо легко окисляется кислородом воздуха уже при комнатной температуре
Fe +О2 → Fe3O4 (Fe2O3 FeO).

Химические свойства
2. Отношение к воде.
Железо вытесняет водород из воды:
Fe + H2O >5000 C →Fe3O4 + H2 ↑.
1 |
Fe −2e = Fe2+ |
о-ие, в-ль |
|
2Fe −6e = 2Fe3+ |
|||
|
|
||
4 |
2H + +2e = H2 ↑, в−ие, о− ль. |
||
Так получают водород в промышленности.

Химические свойства
3. Отношение к неметаллам . Галогены окисляют железо на свету:
Fe +Cl2 = FeCl2 .
хлорид железа (II)
Другие неметаллы окисляют железо при нагревании :
Fe +C t →Fe3C.
карбид железа (II), цементит

Химические свойства
Fe + Si t →Fe3Si,
силицид железа (II)
Fe + H2 t →FeH2 .
гидрид железа (II)
4. Железо восстанавливает менее активные металлы из растворов их
солей: |
2+ |
|
2+ |
↓ +Cu0 . |
|
Cu SO |
+ Fe0 = Fe SO |
|
4 |
4 |
|

Химические свойства
5. Отношение к щелочам.
Со щелочами железо не взаимодействует.
Fe + NaOH ≠
6. Отношение к кислотам.
а) железо вытесняет водород из неокислительных кислот:
Fe + HCl → FeCl2 + H2 ↑
1 Fe0 −2e = Fe2+, о−ие
1 2H + +2e = H2 ↑, в−ие

Химические свойства
б) концентрированные окислительные кислоты при комнатной температуре
пассивируют железо, но при нагревании
железо растворяется, проявляя степень окисления +3:
Fe + H |
|
+6 |
O |
+ Fe (SO ) |
. |
||||
2 |
SO4 конц. t → S 0 + H |
||||||||
|
|
|
2 |
|
2 |
4 |
3 |
|
|
1 |
|
SO42− +6e +8H += S 0 +4H2O, в−е; |
|
|
|||||
|
|
|
|||||||
1 |
|
2Fe0 −6e = 2Fe3+, о−е. |
|
|
|
|
|||
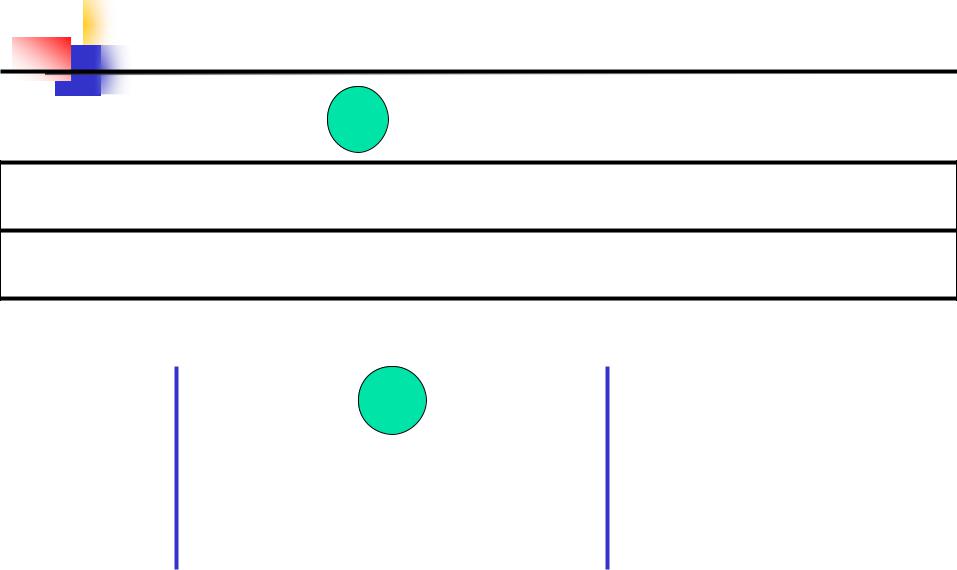
6. Взаимодействие металлов  с кислотами
с кислотами
Ca Na Mg Al Mn Zn Fe Co Ni Sn Pb H Sb Bi Cu Hg Ag Au
НNO3 конц
NO2
Н2SO4 конц
|
Н2S |
S |
SO2 |
НNO3 разб
NH4+ |
N2 |
N O |
NO |
|
|
2 |
|

Химические свойства
|
|
|
|
|
+4 |
|
+5 |
|
|||||
H NO3 конц.+Fe t → N О2 |
+ H2O + Fe(NO3 )3. |
|||||
|
3 |
|
NO3− +e |
+2H + = NО2 + H2O, в−е, |
||
|
|
|||||
|
1 |
|
Fe0 −3e = Fe3+, о−е. |
|
||
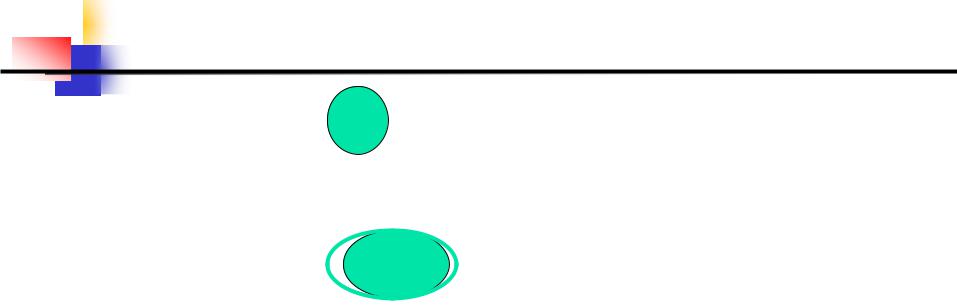
6. Взаимодействие металлов  с кислотами
с кислотами
Ca Na Mg Al Mn Zn Fe Co Ni Sn Pb H Sb Bi Cu Hg Ag Au
|
|
НNO3 |
конц |
|
|
|
|
NO2 |
|
|
|
|
|
Н2SO4 конц |
|
||
Н2S |
|
S |
|
SO2 |
|
|
|
НNO3 |
разб |
|
|
NH4+ |
N2 |
|
|
N O |
NO |
|
|
|
|
2 |
|
|
|
|
|
|
|

Химические свойства
|
|
|
|
|
|
|
|
|
|
+5 |
|
+Fe → N 0 |
+ H |
O |
+ Fe(NO ) |
. |
|||
|
|
H NO |
3 разб |
||||||
|
|
|
|
2 |
2 |
|
3 2 |
|
|
3 |
|
2 NO3−+10e +12H + = N2 +6H2O, в−е, |
|
||||||
|
|
||||||||
10 |
|
Fe0 −3e = Fe3+, о−е. |
|
|
|
|
|||
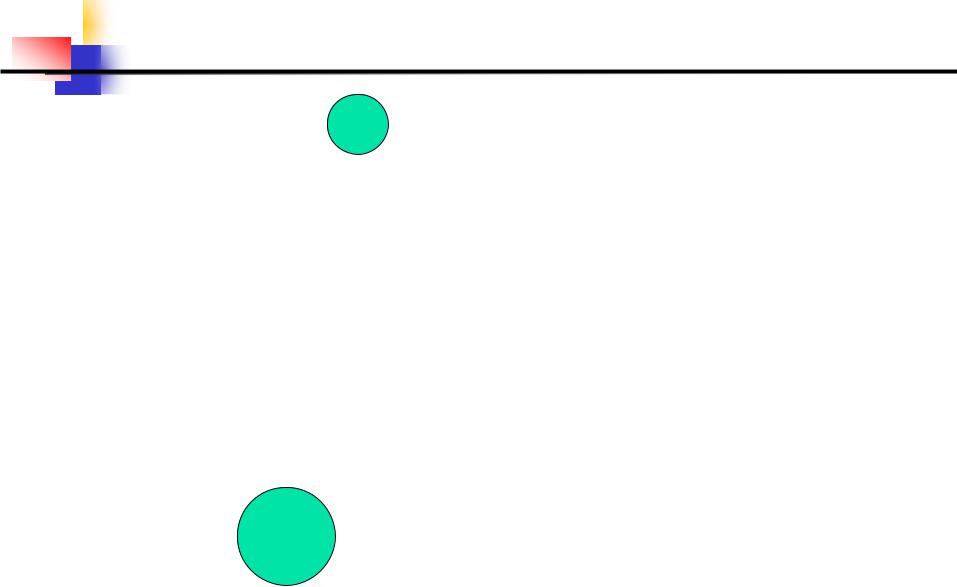
6. Взаимодействие металлов  с кислотами
с кислотами
Ca Na Mg Al Mn Zn Fe Co Ni Sn Pb H Sb Bi Cu Hg Ag Au
|
|
НNO3 |
конц |
|
|
|
|
NO2 |
|
|
|
|
|
Н2SO4 конц |
|
||
Н2S |
|
S |
|
SO2 |
|
|
|
НNO3 |
разб |
|
|
NH4+ |
N2 |
|
|
N O |
NO |
|
|
|
|
2 |
|
|
|
|
|
|
|

Применение
Железный век пришел на смену
бронзовому во втором тысячелетии
до нашей эры.
Железо – основной конструкционный металл.
90 % производства металлов составляют железо и сплавы на его
основе, которые называют черными металлами.
Применение – самостоятельно!!!

Соединения железа: Fe2+
FeO – осно׳вный оксид.
Получение:
Fe +O2 800°C→FeO,
Fe3O4 +CO 600°C →FeO +CO2 ↑.
Свойства:
FeO +2HCl = FeCl2 +H2O,
FeO +2H+ = Fe2+ +H2O,
FeO + NaOH ≠.

Свойства соединений Fe2+
Свойства окислительновосстановительные:
Fe(OH )2 +O2 + H2O → Fe(OH )3.
4Fe (OH )2 − e + OH − = Fe (OH )3 , о − ие, в − ль,
1O2 + 2 H 2O + 4e = 4OH − , в − ие, о − ль.
Вывод: Fe(OH)2 – восстановитель.

Свойства соединений Fe2+
Соли Fe2+ получают взаимодействием железа с неокислительными
кислотами:
Fe +2HCl → FeCl2 + H2 ↑,
1 |
|
Fe −2е = Fe2+, о−ие, в− ль. |
||||||||||
|
||||||||||||
1 |
|
2H |
+ + |
2е |
= |
H |
2 |
↑ |
− |
ие, о |
− |
ль. |
|
||||||||||||
|
|
|
|
, в |
|
|
||||||
Fe + H2 SO4 разб |
= FeSO4 + H2 ↑. |
|||||||||||

Свойства соединений Fe2+
Соли Fe2+ подвергаются гидролизу:
слабый сильная
FeSO4 (Fe(OH )2 и H2 SO4 ).
FeSO4 =Fe2 + + SO42 −
H +OH −
Fe2+ + HOH = FeOH + + H +, рН<7 2FeSO4 +2H2O = (FeOH )2 SO4 + H2 SO4 .

Свойства соединений Fe2+
Соли Fe2+ – сильные восстановители:
+2 |
+7 |
|
+3 |
+2 |
|
FeSO4 |
+ KMnO4 |
+ H2 SO4 |
→ Fe2 (SO4 )3 |
+MnSO4 |
+ H2O. |
5 2Fe2+ −2е = 2Fe3+, о−ие, в− ль,
2MnO4− +5е +8H + = Mn2+ +4H2O, в−ие, о− ль.
Применение солей: FeSO4·7H2O – железный купорос применяют в производстве чернил , красок и для борьбы с вредителями растений.

Свойства соединений Fe2+
Качественная реакция на Fe2+ ̶это взаимодействие с красной кровяной солью К3[Fe(CN )6 ] :
3FeSO4 +2К3[Fe(CN )6 ] = Fe3[Fe(CN)6 ]2 ↓ +3K2 SO4 .
3Fe2+ +2 [Fe(CN )6 ]3− = Fe3[Fe(CN )6 ]2 ↓.
турнбулевая синь

Соединения железа: Fe3+
 Fe2O3 – слабо амфотерный оксид,
Fe2O3 – слабо амфотерный оксид,
встречается в природе – красный железняк.
Получение: Fe +O2 → Fe2O3.
Свойства:
|
Fe2O3 +6HCl = 2FeCl3 +3H2O. |
||||
|
Fe O +6H + |
= 2Fe3+ +3H |
O. |
|
|
|
2 |
3 |
2 |
|
|
|
|
1000 |
−14000 C |
|
+ H2O. |
Fe2O3 + NaOH →NaFeO2 |
|||||
НFeO2 |
– железистая |
феррит |
|
||
|
кислота |
натрия |
|
||

Соединения железа Fe3+
Fe2O3 – обнаруживает амфотерные свойства только при спекании.
Fe O + FeO t →Fe(FeO ) |
. |
|||
2 |
3 |
2 |
2 |
|
НFeO2 |
феррит железа II |
|||
Fe3O4 отличается повышенной устойчивостью и встречается в природе в виде минерала
магнетита, обладает полупроводниковыми и магнитными свойствами.

Соединения железа Fe3+
Fe2O3 – это коричневая краска, железный сурик.
Ферриты обладают магнитными свойствами и высоким электрическим сопротивлением.
Их используют в технике связи, счетнорешающих устройствах, в автоматике и телемеханике.

Свойства соединений Fe3+
Fe(OH)3 – слабо амфотерный гидроксид.
Получение:
Fe 2 (SO4 )3 + 6 NaOH = 2Fe(OH )3 ↓ +3Na 2 SO4 , Fe 3+ + 3OH − = Fe(OH )3 ↓ .
Свойства кислотно-основные:
2 Fe (OH ) 3 + 6 HCl = 2 FeCl 3 + 3 H 2 O , Fe (OH ) 3 + 3 H + = Fe 3 + + 3 H 2 O .
Fe (OH ) 3 + NaOH t → NaFeO 2 + 2 H 2 O .

Свойства соединений Fe3+
Соли Fe3+ получают взаимодействием металла
с окислительными
кислотами (см. эту тему выше).
Соли Fe3+ легко подвергаются гидролизу и при определенных условиях
(увеличении температуры и уменьшении концентрации) гидролиз идет до конца с образованием (FeOH)3 – осадка бурого цвета .

Свойства соединений Fe3+
Поэтому соли Fe2 (SO4 )3 9Н2Ои FeСl3
используют в качестве каогулянтов при очистке
воды:
слабый сильная
Fe 2 ( SO 4 )3 ( Fe (OH )3 и H 2 SO 4 ).
Fe 2 ( SO 4 )3 = 2 Fe 3+ + 3SO 42 −
H +OH −
Fe 3+ + HOH = FeOH 2 + + H + , pН < 7, Iступень
Fe 2 (SO 4 )3 + 2 H 2 O = 2 FeOHSO 4 + H 2 SO 4 .

Свойства соединений Fe3+
После увеличения температуры и разведения гидролиз идет по II-ой ступени:
FeOH 2+ + НОН = Fe(OH )+2 + H +, pН < 7,
FeOHSO4 + H2O = (Fe(OH )2 )2 SO4 + H2 SO4 .
После увеличения температуры и разведения гидролиз идет по III-ей ступени:
Fe(OH )+2 + НОН = Fe(OH )3 ↓ +H +, pН < 7,
(Fe(OH )2 )2 SO4 +2H2O = 2Fe(OH )3 ↓ +H2 SO4 .

Свойства соединений Fe3+
Осадок Fe(OH)3 увлекает с собой все
механические примеси, содержащиеся в воде.
Чаще всего Fe3+ в ОВР – окислитель.
+3 |
−1 |
+2 |
|
+ KCl + I 0 . |
FeCl |
+ KI → FeCl |
2 |
||
3 |
|
|
2 |
|
2 Fe3+ +1е = Fe2+, в−ие, о− ль,
1 2I − −2е = I2 , о−ие, в− ль.

Свойства соединений Fe3+
Качественная реакция на Fe3+ ̶это взаимодействие с роданидом аммония:
NH4CNS :
Fe2 (SO4 )3 +6NH4CNS =
2Fe(CNS)3 +3(NH4 )2 SO4 .
кроваво-красный цвет

Свойства соединений Fe6+
|
|
|
|
Если нагреть Fe2O3 c нитратом и |
|
|
||||||
|
|
|
|
|
|
|||||||
|
|
|
|
|
||||||||
|
|
|
|
|
||||||||
+3 |
гидроксидом калия то получаем: |
|
|
|||||||||
|
|
|
+5 |
+6 |
|
+3 |
+ H |
O. |
||||
|
Fe О + КОH + |
КNО |
t →K |
FeO |
+ KNO |
|||||||
2 |
3 |
3 |
2 |
|
4 |
2 |
2 |
|
||||
|
|
|
|
|
+3 |
|
+6 |
|
|
|
|
|
|
|
|
|
|
1 2Fe −6e = 2 Fe, о−ие, в− ль, |
|
|
|||||
+5 +3
3N +2е = N, в−ие, о− ль.
К2FeO4 – феррат калия, соль железной кислоты Н2FeO4.

Свойства соединений Fe6+
Железная кислота и соответствующий ей
ангидрид FeO3 не выделены в
свободном виде.
Все ферраты – сильнейшие окислители.
Железо – жизненно важный элемент. В
крови человека 14,5 % её веса
приходится на долю гемоглобина – красного пигмента эритроцитов, содержащих железо.

Кобальт
В природе распространен мало: содержание его в земной коре составляет около 0,004 % (масс).
Чаще всего кобальт встречается в соединении с мышьяком в виде минералов 'кобальтовый шпейс
CoAs2 и кобальтовый блеск CoAs.
Кобальт – твердый, тягучий, похожий на железо блестящий металл.
Как и железо, он обладает магнитными свойствами. Вода и воздух на него не действуют.
В разбавленных кислотах кобальт растворяется значительно труднее, чем железо.
Кобальт применяется главным образом в сплавах, которые используются в качестве жаропрочных и жаростойких материалов, для изготовления постоянных магнитов и режущих инструментов.

Кобальт
Жаропрочный и жаростойкий сплав виталлиум содержит 65 % Со, 28 % Сг, 3 % W и 40 % Мо.
Этот сплав сохраняет высокую прочность и не поддается коррозии при температурах до 800 – 850°С.
Твердые сплавы стеллиты, содержащие 40 60 % Со, 20 – 35 % Сг, 5 – 20% W и 1 – 2 % С, применяются для изготовления режущего инструмента.
Кобальт входит также в состав керамикометаллических твердых сплавов – керметов.
Соединения кобальта придают стеклу темно-синюю окраску (вследствие образования силиката кобальта).

Кобальт
Такое стекло, истолченное в порошок, употребляется под названием «шмальты» или «кобальта» в качестве синей краски.
Радиоактивный изотоп 60Со применяется в медицине как источник Ɣ-излучения («кобальтовая пушка»).
Кобальт образует оксид кобальта (II) СоО и оксид кобальта (III), или окись кобальта, Со2O3, которым соответствуют гидроксиды Со(ОН)2 и Со(ОН)3.
Этим соединениям отвечают два ряда солей, но соли кобальта (III) нестойки и легко переходят в соли кобальта (II).
Известен также смешанный оксид СO3О4 (или
СоО·Со2О3).

Кобальт
Соли кобальта (II) в безводном состоянии обычно синего цвета, а их водные растворы и кристаллогидраты имеют розовый цвет.
Хлорид кобальта (II) образует розовые кристаллы состава СоСl2·6Н2O.
Фильтровальная бумага, пропитанная раствором этой соли и потом высушенная, может служить грубым гигроскопом (указателем влажности), так как в зависимости от содержания влаги в воздухе принимает разные оттенки цветов – от синего до розового.
Гидроксид кобальта (II) Со(ОН)2 получается при действии щелочи на растворы солей кобальта (II).

Кобальт
Вначале выпадает осадок синей основной соли, который при кипячении жидкости переходит в
розовый гидроксид Со(ОН)2.
Со(ОН)2 при прокаливании дает оксид кобальта (II) СоО серо-зеленого цвета.
Соединения кобальта (II) окисляются с большим трудом, чем соединения железа (II).
Так, гидроксид кобальта(II) окисляется на воздухе в темно-бурый гидроксид кобальта (III) Со(ОН)3
гораздо медленнее, чем происходит аналогичное превращение гидроксидов железа.

Кобальт
Однако в присутствии сильных окислителей, например гипохлорита натрия, окисление Со(ОН)2 в Со(ОН)3 протекает быстро:
2Co(OH)2 + NaClO +H2O = 2Co(OH)3 + NaCl.
При действии на гидроксид кобальта (III) кислородсодержащих кислот соли кобальта (III) не образуются, а выделяется кислород и получаются соли кобальта (II), например:
4Co(OH)3 +4H2SO4 = 4CoSO4 +10H2O +O2 ↑.
Из соляной кислоты гидроксид кобальта(III) выделяет хлор:
2Co(OH)3 +6HCl = 2CoCl2 +Cl2 ↑ +6H2O.

Кобальт
Таким образом, соединения Со (III) менее устойчивы, чем соединения железа (III) и проявляют более сильно выраженную окислительную способность.
Для кобальта (III) очень характерна его способность к комплексообразованию.
Комплексные соединения кобальта (II) хотя и известны, но очень неустойчивы.
В комплексных солях кобальт может входить как в состав катиона, так и в состав аниона, например,
[Со(NH3)6]Сl3 и К3 [Co(NO2)6].
Координационное число кобальта равно шести.

Никель
Подобно кобальту, встречается в природе преимущественно в виде соединений с мышьяком или серой.
Таковы, например, минералы купферникель NiAs,
мышьяково-никелевый блеск NiAsS и др.
Никель более распространен, чем кобальт (около 0,01 % (масс.) земной коры).
Металлический никель имеет серебристый цвет с желтоватым оттенком, очень тверд, хорошо полируется, притягивается магнитом.
Он характеризуется высокой коррозионной стойкостью – устойчив в атмосфере, в воде, в щелочах и ряде кислот.

Никель
Активно растворяется никель в азотной кислоте.
Химическая стойкость никеля обусловлена его склонностью к пассивированию – к образованию на поверхности оксидных пленок, обладающих сильным защитным действием.
Главная масса никеля идет на производство различных сплавов с железом, медью, цинком и другими металлами.
Присадка никеля к стали повышает ее вязкость и стойкость против коррозии.
Сплавы на основе никеля можно разделить на жаропрочные, магнитные и сплавы с особыми свойствами.

Никель. Сплавы
Жаропрочные сплавы никеля используются в современных турбинах и реактивных двигателях,
где температура достигает 850 – 900 °С.
Таких температур сплавы на основе железа не выдерживают.
К важнейшим жаропрочным сплавам никеля относятся
нимоник, инконель, хастеллой.
В состав этих сплавов входит свыше 60 % никеля, 15
– 20 % хрома и другие металлы.
Производятся также металлокерамические жаропрочные сплавы, содержащие никель в качестве связующего металла.
Эти сплавы выдерживают нагревание до 1100°С.

Никель. Сплавы
Широко применяются для изготовления элементов
электронагревательных устройств сплавы типа нихрома, простейший из которых содержит 80 % никеля и 20 % хрома.
Из магнитных сплавов никеля особое значение приобрел пермаллой, содержащий 78,5 % никеля и 21,5 % железа.
Он обладает очень высокой начальной магнитной проницаемостью, что обусловливает его интенсивную
намагничиваемость даже в слабых полях.
К сплавам никеля с особыми свойствами принадлежат
монельметалл, никелин, константан, инвар, платинит.

Никель. Сплавы
Монель-металл (сплав никеля с 30 % меди) широко используется в химическом аппаратостроении, так как по механическим свойствам он превосходит никель, а по коррозионной стойкости почти не уступает ему.
Никелин и константан тоже представляют собой сплавы никеля с медью.
Они обладают высоким электрическим сопротивлением, почти не изменяющимся с температурой, и используются в электроизмерительной аппаратуре.
Инвар (сплав 36 % никеля и 64 % железа) практически не расширяется при нагревании до 100°С и применяется в электрорадиотехнике и в химическом машиностроении.

Никель
Сплав никеля с железом – платинит – имеет коэффициент расширения такой же, как у стекла и используется для впаивания вводов металлических контактов в стекло.
В сравнительно небольших количествах никель расходуется для покрытия им других металлов.
Мелко раздробленный никель применяется в качестве катализатора при многих химических процессах.
Из чистого никеля изготовляют лабораторную посуду.
Соединения никеля очень сходны с соединениями кобальта.
Подобно кобальту, никель образует оксид никеля (II) NiO и оксид никеля (III) Ni2O3 и соответствующие им гидроксиды.

Никель
Однако известен только один ряд солей никеля, в которых он находится в степени окисленности +2.
Гидроксид никеля (II) Ni(ОН)2 выпадает в виде светло-зеленого осадка при действии щелочей на растворы солей никеля.
При нагревании он теряет воду и переходит в серозеленый оксид никеля (II) NiO.
В отличие от гидроксидов железа(II) и кобальта(II), гидроксид никеля (II) кислородом воздуха не окисляется.
В этом проявляется более высокая устойчивость к окислению соединений никеля (II) по сравнению с аналогичными соединениями железа и кобальта.
Соли никеля большей частью имеют зеленый цвет.

Никель
Из них наибольшее применение имеет сульфат никеля NiSO4·7H2O, образующий красивые
изумрудно-зеленые кристаллы.
Гидроксид никеля (III) Ni(OH)3 имеет черно-
бурый цвет и образуется при действии щелочей на соли никеля в присутствии сильных окислителей.
По свойствам он подобен гидроксиду кобальта (III), но обладает еще более выраженными
окислительными свойствами.
Никель (II) образует много комплексных солей.

Никель
С оксидом углерода никель дает летучий
тетракарбонил никеля Ni(СО)4, разлагающийся при нагревании с выделением никеля.
На образовании и термическом разложении тетракарбонила никеля основан один из методов извлечения никеля из руд, а также способ получения высокочистого никеля.
Из соединений никеля важнейшее практическое значение имеет оксид никеля (III), применяемый при изготовлении щелочных кадмиево-никелевых или железо-никелевых аккумуляторов.

Аккумуляторы
Кадмиево-никелевые (условное обозначение КН) и железо-никелевые (ЖН) аккумуляторы весьма сходны между собой.
Основное их различие состоит в материале пластин отрицательного электрода: в аккумуляторах КН они
кадмиевые, а в аккумуляторах ЖН – железные.
Наиболее широкое применение имеют аккумуляторы
КН.
Щелочные аккумуляторы в основном выпускаются с ламельными электродами.
В них активные массы заключены в ламели – плоские коробочки с отверстиями.

Аккумуляторы
Активная масса положительных пластин заряженного аккумулятора в основном состоят из гидратированного оксида никеля (III) Ni2O3·Н2O или NiOOH.
Кроме того, в ней содержится графит, добавляемый для увеличения электропроводности.
Активная масса отрицательных пластин аккумуляторов КН состоит из смеси губчатого кадмия с порошком железа, а аккумуляторов ЖН – из порошка восстановленного железа.
Электролитом служит раствор гидроксида калия, содержащий небольшое количество LiOH.
Рассмотрим процессы, протекающие при работе аккумулятора КН.

Аккумуляторы
При разряде аккумулятора кадмий окисляется.
Cd +2OH− = Cd(OH)2 +2e.
a NiOOH восстанавливается:
2NiOOH +2H2O +2e = 2Ni(OH)2 +2OH−.
По внешней цепи при этом происходит перенос электронов от кадмиевого электрода к никелевому.
Кадмиевый электрод служит анодом и заряжен отрицательно, а никелевый – катодом и заряжен положительно.

Аккумуляторы
Суммарную реакцию, протекающую в аккумуляторе КН при его работе, можно выразить уравнением, которое получится при сложении двух последних электрохимических уравнений:
2NiOOH +2H2O +Cd = 2Ni(OH)2 +Cd(OH)2 .
ЭДС заряженного кадмиево-никелевого аккумулятора равна приблизительно 1,4 В.
По мере работы (разряда) аккумулятора напряжение на его зажимах падает.
Когда оно становится ниже 1 В, аккумулятор заряжают.

Аккумуляторы
При зарядке аккумулятора электрохимические процессы на его электродах «обращаются».
На кадмиевом электроде происходит восстановление металла:
Cd(OH)2 +2e = Cd +2OH−.
на никелевом – окисление гидроксида никеля (II):
2Ni(OH)2 +2OH− = 2NiOOH +2H2O +2e.
Суммарная реакция при зарядке обратна реакции, протекающей при разряде:
2Ni(OH)2 +Cd(OH)2 = 2NiOOH +2H2O +Cd.
