
Протекторная защита магистральных трубопроводов от коррозии
.pdfСПБГУАП группа 4736 https://new.guap.ru/i03/contacts
Почвенная коррозия
Под коррозией металлических трубопроводов понимается самопроизвольное разрушение их под действием различных факторов химического или электрохимического характера, определяемых окружающей трубопровод средой.
Химическая коррозия – самопроизвольное окисление металла под воздействием окружающей среды токонепроводящей среды. При этом продукты коррозии образуются непосредственно на участке поверхности металла, подвергающегося разрушению.
Электрохимическая коррозия – коррозия металлов в электолитах,
сопровождающаяся образованием электрического тока. При этом взаимодействие металла с окружающей средой разделяется на анодный и катодный процессы, протекающие на различных участках поверхности раздела металла и электролита.
Почвенная коррозия относится к электрохимической коррозии, однако ей присущи особенности:
1) связь влаги с окружающей средой:
-физико-механическая связь (свободная вода в порах грунта);
-физико-химическая связь (влага адсорбированная на поверхности грунта или металла);
-химическая (гидратированная) влага, входящая в химическое соединение Fe∙nH2;
2)неоднородность структуры и состава грунта, как в микро-, так и в макромасштабах;
3)почти полное отсутствие перемешивания твердой фазы грунта
(замедление процесса коррозии во времени);
4) неодинаковый доступ кислорода воздуха к поверхности металла.
Основные причины возникновения коррозионных элементов на
трубопроводе
СПБГУАП группа 4736 https://new.guap.ru/i03/contacts
Условия возникновения коррозии являются:
-наличие разнородности грунтовых участков, имеющих различные потенциалы;
-наличие разнородных грунтовых участков;
-наличие средств проводящих электрический ток.
Причины возникновения коррозионных элементов на трубопроводе:
1)микронеоднородность состава металла (присутствие механических примесей в металле труб).
2)Наличие окалины на поверхности металла (микронеоднородность состояния поверхности металла).
3)Наличие продольных и поперечных сварных швов, являющихся наиболее опасными участками в трубопроводах.
4)Различные напряженные состояния поверхности металла
(растянутые участки имеют менее отрицательный потенциал).
5)Различная глубина заложения трубопровода.
6)Чередование грунтов с различными физико-химическими свойствами.
7)Температура. С увеличением температуры происходит увеличение протекания анодных процессов, т.е. увеличивается скорость коррозии.
1.Условия применения и принцип действия протекторной защиты магистральных трубопроводов от коррозии
Протекторные установки предназначены:
-для защиты от почвенной коррозии участков большой протяженности, удаленных от источников электроснабжения, где нецелесообразно применение катодной защиты внешним током;
-на участках, защищенных СКЗ, - в местах неполной защиты, для обеспечения необходимого защитного потенциала;
СПБГУАП группа 4736 https://new.guap.ru/i03/contacts
-для защиты от почвенной коррозии патронок (кожухов) на переходах через железные и автомобильные дороги;
-на участках блуждающих токов – в качестве земляных микродренажей.
Протекторы также устанавливают на изолирующих фланцах для снятия анодных зон, на электрических перемычках при совместной защите подземных сооружений для устранения электрохимического взаимодействия между ними, для защиты металлических подземных емкостей и др.
Средний срок службы протектора – 5-10 лет.
Таким образом, положительные стороны данного способа ЭХЗ:
-эффективность;
-простота устройства;
-удобность эксплуатации;
-автономность.
Отрицательные стороны – снижение эффективности при значительном удельном сопротивлении грунта, окружающего протектор, и использование дефицитных материалов.
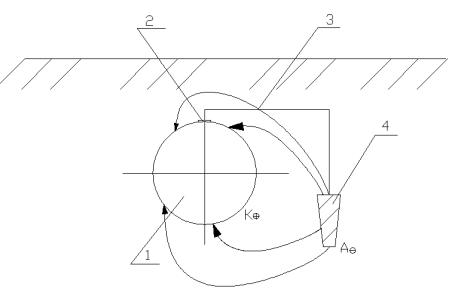
Рис.1. Принципиальная схема протекторной установки:
1 – трубопровод; 2 – точка дренажа; 3 – изолированный соединительный провод; 4 – протектор; А – анод; К – катод.
СПБГУАП группа 4736 https://new.guap.ru/i03/contacts
Протекторная защита трубопроводов основана на принципе работы гальванических пар. При защите подземных металлических объектов с помощью протекторных установок к трубопроводу подключают протектор
(анодный электрод), имеющий более низкий электрохимический потенциал,
чем потенциал металла трубы. Создаются условия, при которых трубопровод выступает в качестве катода, а электрод (протектор) в качестве анода, в
результате добиваются прекращения коррозионного разрушения трубопровода за счет интенсивного разрушения протектора.
При устройстве протекторной защиты к стальному трубопроводу подключают металлический протектор. В результате этого образуется гальванический элемент «труба-протектор», в котором трубопровод является катодом, протектор – анодом, а почва – электролитом.
Таким образом, протекторная защита имеет те же основы, что и катодная защита. Разница заключается в том, что необходимый для защиты ток создается крупным гальваническим элементом, поэтому протекторную защиту иначе называют защитой гальваническими анодами. При этом положительный полюс находится на защищаемой поверхности, а
отрицательный – на разрушаемом аноде, то есть в порядке, обратном порядку при катодной защите с наложенным током от внешнего источника.
2. Протекторные установки
2.1. Металлы и сплавы, применяемые для изготовления протекторов
Требования, предъявляемые к материалу протектора:
- материал протектора должен иметь более отрицательный потенциал,
чем потенциал трубопровода;
- на поверхности протектора не должны образовываться плотные окисные пленки (материал протектора должен иметь малую анодную поляризуемость);
СПБГУАП группа 4736 https://new.guap.ru/i03/contacts
-материал протектора должен иметь высокий КПД, т.к. происходит самокоррозия протектора;
-материал протектора должен иметь высокую удельную токоотдачу, то есть g → max [А∙час/кг];
-количество электроэнергии с единицы веса (токоотдача) должна быть максимальной при минимальной стоимости.
В качестве материалов протекторов используют алюминий, цинк и
магний, а так же сплавы на их основе.
|
|
|
Таблица 1 |
|
Физико-химические свойства металлов, |
|
|||
используемых в качестве протекторов |
|
|||
Показатели |
Магний |
Цинк |
алюминий |
|
Относительная молекулярная масса |
24,32 |
65,38 |
26,97 |
|
Валентность |
2 |
2 |
3 |
|
Электрохимический |
3,97 |
10,7 |
2,94 |
|
эквивалент, кг/(А∙год) |
||||
|
|
|
||
Токоотдача, (А∙час)/кг |
2200 |
820 |
2980 |
|
Равновесный электродный потенциал по нормальному |
-2,34 |
-0,76 |
-1,67 |
|
водородному электроду, В |
||||
|
|
|
||
2.1.1. Магниевые сплавы
Магний, относится ко второй группе периодической системы эле-
ментов Д. И. Менделеева. Металлы этой группы характеризуются относительно высокой химической и электрохимической активностью.
Интенсивность коррозии металлов этой группы во многом зависит от растворимости их гидроокисей. Более умеренная по сравнению с другими металлами коррозия магния в ряде случаев связана с плохой растворимостью окисных и гидроокисных пленок, образующихся на его поверхности.
Технический и даже чистый магний хорошо растворяется в водных растворах кислот, бурно выделяя водород и значительное количество тепла.
Так как гидроокись магния не обладает амфотерными свойствами, то скорость коррозии этого металла в водных растворах щелочей не увеличивается, а уменьшается.
СПБГУАП группа 4736 https://new.guap.ru/i03/contacts
Вводе магний корродирует медленно, причем скорость коррозии повышается с увеличением содержания в воде солей.
Внейтральных водных средах основным продуктом коррозии магния является гидроокись, в растворах же кислот образуются соли магния.
Наиболее растворимыми солями магния (по степени убывания растворимости) являются хлорид, бромид, иодид, сульфат, хромат и нитрат.
К плохо растворимым соединениям этого металла относятся сульфид,
карбонат, фторид, борат, фосфаты, гидроокись. Гидроокись магния осаждается из водного раствора при рН = 8—11 (в зависимости от концентрации ионов магния).
Потенциал магния в нейтральных водных электролитах и особенно в щелочных растворах оказывается более положительным, чем в кислотных растворах, т. е. растворение в кислых средах окисной пленки приводит к сдвигу электродного потенциала магния в область более отрицательных значений. Образование нерастворимых продуктов коррозии на металле частично или полностью тормозит анодную реакцию и этим смещает электродный потенциал магния в область более положительных значений.
Следовательно, поляризационные характеристики магниевого электрода в значительной мере зависят от состава окружающей среды. В
случае, когда к металлу поступают анионы хлора (С1-) или анионы серной кислоты (SO42-), образующие растворимые магниевые соли, анодная поляризация магниевого электрода оказывается небольшой. Ионы же,
образующие на поверхности магниевого электрода нерастворимые соединения, способствуют более сильной анодной поляризации. В
природных условиях такие анионы, как фтор (F-) и фосфорной кислоты
(РО43-), встречаются в небольших количествах.
Окисные и гидроокисные пленки, образующиеся на магниевом электроде, при наличии воды или влажного воздуха оказываются легко проницаемыми для ионов хлора и сульфат-ионов. По этой причине магниевые электроды не подвергаются сильной поляризации.
СПБГУАП группа 4736 https://new.guap.ru/i03/contacts
Продукты коррозии, образующиеся на протекторах, обогащаются анионами, находящимися в окружающей среде, поэтому вокруг протекторов создается токопроводящий слой, т. е. своеобразный активатор. Иногда такой слой оказывается более эффективным, чем искусственно созданный.
Стационарный потенциал магния примерно на один вольт оказывается положительнее его нормального потенциала. В нейтральных или слабощелочных электролитах сдвиг потенциала магниевого электрода в область более положительных значений зависит от наличия на его поверхности сплошной пленки, способствующей замедлению анодной реакции. Поэтому потенциал магниевого анода в водных электролитах зависит прежде всего от солевого состава и в меньшей степени от концентрации собственных ионов, которые и определяют стационарный потенциал магниевого электрода. Вещества, способствующие снятию окисной пленки или увеличивающие ее проницаемость, как правило,
облегчают течение анодной реакции и сдвигают потенциал в область более отрицательных значений. Наоборот, вещества, создающие защитную пленку,
тормозят анодную реакцию и сдвигают потенциал магниевого электрода в область более положительных значений. Первый случай наблюдается при наличии в среде ионов хлора Cl- и серной кислоты SO42-, способных легко проникать через пленку; второй случай — в щелочных средах или в при-
сутствии ионов, образующих нерастворимые соединения магния.
При подключении магниевого и других протекторов к защищаемой конструкции их потенциал меняется. При прочих равных условиях скорость растворения магниевых электродов пропорциональна плотности анодного тока. Чем больше отдача электрической энергии, приходящаяся на единицу веса протектора, тем интенсивнее его растворение. С увеличением плотности тока в растворах, содержащих гидроксильные, карбонатные, фторидные,
боратные или фосфатные ионы в значительных количествах, потенциал магниевого анода быстро понижается.
СПБГУАП группа 4736 https://new.guap.ru/i03/contacts
Высокая поляризация магниевых и других протекторов наблюдается в сухих почвах.
Таким образом, поведение магниевых протекторов во многом зависит от состава и концентрации в окружающей среде ионов различных солей, а
также от кислотности и щелочности среды, т. е. от концентрации водородных ионов и влажности почвы.
Несмотря на отмеченные положительные свойства магния как материала для протекторов, чистый магний все же не рекомендуется применять для изготовления протекторов из-за значительной самокоррозии этого металла.
Магниевые сплавы с добавками цинка имеют меньшую скорость самокоррозии. Введение в сплав алюминия позволяет также сместить потенциал протектора в область более отрицательных значений.
Наличие в протекторе примесей, особенно таких, как никель, железо и медь, имеющих сравнительно небольшое перенапряжение водорода, обычно способствует увеличению самокоррозии. Поэтому количество таких примесей должно быть минимальным.
Например, при исключении из магниевого сплава примесей железа КПД магниевого протектора может быть увеличен на 20%. Однако получение такого сплава связано с технологическими трудностями.
Марганец при определенных условиях может являться полезной примесью,
так как он способствует уменьшению вредного влияния железа,
содержащегося в сплаве протектора.
Литейные сплавы магния с цинком и алюминием, такие как МЛ-3 —
МЛ-6, могут быть использованы для изготовления протекторов. Однако более лучшими сплавами являются МЛ-4 и МЛ-5. Протекторы из них имеют значительный отрицательный электродный потенциал, небольшую поляризуемость, способность растворяться с образованием рыхлых продуктов коррозии, что и определяет высокую эффективность работы этих протекторов.
СПБГУАП группа 4736 https://new.guap.ru/i03/contacts
Магниевые протекторы МГА (ВНИИСТа) из сплава МЛ-5 широко применяют при защите магистральных трубопроводов и других конструкций от почвенной коррозии.
Вмагниевом сплаве сумма загрязнений должна быть не больше 0,6 %,
втом числе железа не больше 0,15 %. Стальной сердечник, устанавливаемый
вкокиль, должен иметь чистую поверхность, без следов окалины и коррозии.
К сплаву должно плотно прилегать не менее 80% поверхности сердечника. Это можно определять визуально при рассмотрении шлифов.
Поверхность протектора также должна быть чистой. В отливках не допускается трещин и флюсовых включений.
Вслучае длительного хранения протекторы подвергаются кон-
сервации.
Сернокислый магний и сернокислый натрий образуют легко растворимые соединения с продуктами растворения протектора, чем обеспечивают постоянство его потенциала и уменьшают сопротивление растеканию протектора.
Сернокислый магний и сернокислый натрий представляют собой соли,
растворимые в воде. Сернокислый кальций — мелкокристаллический порошок (либо строительный гипс или алебастр), в отличие от указанных двух солей, имеет значительно меньшую растворимость в воде, благодаря чему в заполнителе поддерживается постоянная концентрация сульфат-
ионов.
2.1.2. Алюминиевые сплавы
Алюминий относится к третьей группе периодической системы элементов Д. И. Менделеева. Известно, что его электрохимический потенциал в нейтральных и кислых электролитах небольшой, в щелочных же растворах, наоборот, значительный. На алюминиевом электроде не устанавливается потенциал, близкий к значению равновесного,
СПБГУАП группа 4736 https://new.guap.ru/i03/contacts
определяемого из термодинамических данных. Объясняется это тем, что алюминий в водных электролитах покрывается окисной пленкой. В
щелочных средах защитные окисные пленки на алюминиевом электроде не образуются вследствие их растворения, поэтому алюминий в этих условиях находится в активном состоянии.
Сравнительно небольшой молекулярный вес алюминия, а также его высокая валентность приводят к тому, что он оказывается способным отдать значительное количество электроэнергии на единицу его веса. Однако образование плотных окисных пленок па поверхности алюминиевого протектора с последующей поляризацией и смещением его потенциала примерно до потенциала незаполяризованной стальной конструкции пока не позволило применить протекторы из чистого алюминия. Поэтому были исследованы двойные сплавы на основе алюминия с добавкой цинка и тройные сплавы на основе алюминия с добавкой цинка и магния.
Алюминиевый сплав с добавками цинка даже в нейтральных электролитах имеет потенциал, смещенный в область более отрицательных значений. В щелочных средах потенциал такого сплава изменяется на небольшую величину.
Исследования показали, что такие сплавы имеют ряд преимуществ.
Так, например, испытания сплавов алюминия с 1 и 6,5% цинка показали, что в глинистой почве сплав алюминия с 6,5% цинка дает лучшие результаты по сравнению с первым сплавом. На единицу количества электрической энергии этого сплава требуется меньше по сравнению с другими сплавами и металлами. Сплав алюминия с цинком в глинистой среде имеет достаточно высокий отрицательный потенциал. Алюминиевые протекторы в среде из смеси песка, хлористого натрия и извести в первое время работы показывают высокую эффективность.
Преимуществом протекторов на основе алюминия с добавкой магния по сравнению с протекторами из чистого алюминия является то, что на их поверхности образуются менее устойчивые продукты коррозии. Добавка
