
- •Термодинамика и статистическая физика
- •Лекция № 4
- •Состояние системы детально охарактери- зованное на уровне каждой частицы
- •Детальное описание состояний макроскопи- ческих систем, ввиду колоссальности числа частиц в них, не
- •Основная задача статистической физики: найти наиболее
- •Элементарные сведения из теории вероятностей.
- •Статистические закономерности изучаются теорией вероятностей.
- •Если событие произойти не может, то его называют невозможным. Событие называют случайным, если
- •Математическое определение вероятности: вероятность какого-либо
- •По определению Лапласа,
- •События несовместимы, если появление одного из них исключает появление
- •Сумма вероятностей всех единственно возможных и несовместимых событий
- •Если события А и В независимы (их вероятности не зависят от того, произош-
- •либо зелёным, либо красным (событие А), равна по теореме сложения вероятностей:
- •Существует ещё одна интерпретация вероятности, применяющаяся в физике. Пусть в закрытом сосуде имеется
- •Важным понятием в теории вероятностей и её приложениях является понятие среднего значения. Пусть
- •Отношение n1 , т.е. отношение числа наб- людений при N которых величина x
- •Введём понятие отклонения результатов
- •Распространим полученные результаты на случай когда характеризующая систему ве- личина x может принимать
- •Вероятность того, что результат
- •Столбчатая диаграмма или гистограмма.
- •Гистограмма (столбчатая диаграмма) наг- лядно характеризует вероятность получения результатов измерений, заключающихся в различных
- •ФУНКЦИЯ РАСПРЕДЕЛЕНИЯ ВЕРОЯТНОСТЕЙ
- •Площадь столбика ширины dx равна ве- роятности того, что результат измерения окажется в
- •Зная функцию распределения f(x) , можно найти среднее значение результатов измере-
- •Аналогичные рассуждения дают, что сред-
- •Закон распределения Гаусса.
- •Гаусс (Gauss) Карл Фридрих (30.4.1777,
- •Закон распределения скоростей
- •друг друга всякие два противоположно направленные процесса. Скорости таких противоположно направленных процессов должны
- •Закон распределения скоростей Максвелла.
- •Скорости каждой молекулы будет соот-
- •Вследствие равноправности всех направ- лений движения расположение точек отно-сительно начала координат будет сферически
- •Молекулы движутся хаотически. Среди них есть и очень быстрые, и очень медленные. Благодаря
- •Мы будем искать число частиц ( n) скорости которых лежат в определён- ном
- •Ясно так же, что n должно быть
- •Таким образом, f(υ) – имеет смысл вероятности, то есть показывает, какова вероятность любой
- •Функция распределения Максвелла
- •В результате каждого столкно- вения проекции скорости молекулы испытывают случайное изменение на υx,
- •При этом, мы не можем ничего определенного сказать о точном значении скорости той
- •Максвелл Джеймс Клерк
- •Скорость – векторная величина. Для проекции скорости на ось х (x-
- •Видно, что доля молекул со скоростью
- •Приведённое выражение и график справедливы для распределения
- •Вероятность того, что скорость
- •Величина dnxyz не может зависеть от
- •Этот шаровой слой складывается из тех параллелепипедов, о которых говорилось выше.
- •Отсюда следует закон Максвелла
- •При dυ 1 получаем плотность вероятности, или функцию Максвелла
- •Выводы:
- •Распределение Максвелла характеризует распределение молекул по значениям кинетической энергии (то есть показывает, какова
- •Характерные скорости (наиболее вероятная, среднеквадратичная и средняя скорости молекул газа).
- •Из графика видно, что при «малых» υ , т.е.
- •НАИБОЛЕЕ ВЕРОЯТНАЯ СКОРОСТЬ
- •Величина скорости, на которую при- ходится максимум зависимости F( )
- •СРЕДНЯЯ СКОРОСТЬ
- •Средняя скорость υср
- •СРЕДНЯЯ КВАДРАТИЧНАЯ СКОРОСТЬ
- •Среднюю квадратичную скорость
- •Полезно знать, что
- •Зависимость функции распределения Максвелла от массы молекул
- •Из рис. можно проследить за измене-

Характерные скорости (наиболее вероятная, среднеквадратичная и средняя скорости молекул газа).
Рассмотрим, как изменяется с абсолютной величиной скорости число частиц, приходящихся на единичный интервал скоростей, при единичной концентрации частиц.
mυ2
F (υ) Ae 2kT υ2.

Из графика видно, что при «малых» υ , т.е. |
|||
при mυ2 |
|
, имеем F( ) ~ 2 ; затем F( ) |
|
|
|
|
|
|
2kT |
1 |
|
|
|
|
|
достигает максимума А |
и далее |
|
m 2 |
|
экспоненциально спадает |
F( ) ~ e |
2kT. |
||
|
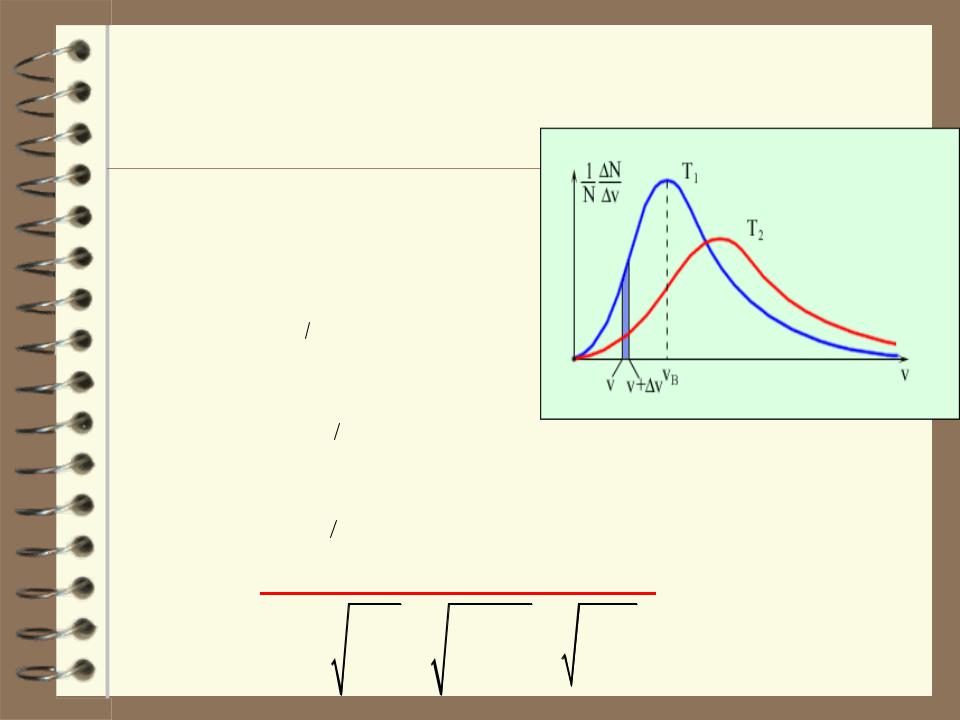
НАИБОЛЕЕ ВЕРОЯТНАЯ СКОРОСТЬ
Наиболее вероятной называют такую скорость молекул Vв, для которой F(V)
функция распределения F(V) при- |
Т1 < Т2 |
|||||||||
нимает максимальное значение, |
|
|||||||||
т.е. F΄(Vв)=0. |
|
|
|
|
|
|
|
|||
|
|
m0 |
3 2 |
2 |
|
m0V 2 |
|
|
||
F (V ) 4 |
|
|
V |
|
exp |
|
|
|
|
|
|
|
|
|
|||||||
|
|
2 kT |
|
|
|
2kT |
|
|
||
|
|
|
|
m |
|
|
|
3 2 |
|
|
|
|
m V 2 |
|
|
|
2 |
|
|
|
m V 2 |
|
2m V |
|
||
0 |
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
0 |
|
0 |
|
|
||||||
F (V ) 4 |
|
|
|
|
|
|
2V exp |
|
2kT |
|
V |
|
exp |
2kT |
|
2kT |
|
|
||||||||
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
2 kT |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
m0 |
|
|
3 2 |
|
|
m0V 2 |
|
|
m0V 2 |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
V exp |
|
2 |
|
|
|
|
|
|
|
||||||||||
F (V ) 4 |
|
|
|
|
|
|
|
|
|
|
|
|
; F (Vв ) 0 |
|
|
|||||||||||
|
|
2 kT |
|
|
|
|
2kT |
|
|
|
kT |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
V 2kT |
2kNAT 2RT . |
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
в |
m0 |
|
|
|
m0 NA |
|
|
M |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||

Величина скорости, на которую при- ходится максимум зависимости F( )
называют наиболее вероятной скоростью вер . Величину этой скорости находят из условия равенства нулю производной:
F ' dF( ) 0 d
|
|
|
|
|
|
|
|
υвер |
2kT |
|
2RT |
||
|
|
m |
|
|
|
|
|
|
|
|
|
|
|

СРЕДНЯЯ СКОРОСТЬ
Найдем среднюю скорость молекул Vc
с помощью функции распределения:
c
Vc VF(V )dV VF(V )dV |
|
|
|
0 |
0 |
|
|
|
m0 |
|
|
3 2 |
|
|
|
|
m0V 2 |
3 |
|
|
|
|
m0 |
|
|
3 2 |
|
|
|
m0V 2 |
|
2 |
|
2 |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
V |
|
|
|
|
|
|
|
|
4 |
exp |
|
|
|
|
V |
dV 2 |
|
|
|
|
|
exp |
|
|
|
|
V |
d(V |
|
). |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
c |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2kT |
|
|
|
|
|
|||||||
|
|
2 kT |
|
|
0 |
|
|
2kT |
|
|
|
|
|
2 kT |
|
0 |
|
|
|
|
|
|
|
|
|
||||||||||
|
|
m0V 2 |
|
|
|
|
|
V |
2 |
2kT |
|
|
|
|
|
|
|
|
2kT |
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
m0 |
|
|
|
d(V 2 ) |
m0 |
d |
|
|
|
|
||||||||||||||||||
|
|
2kT |
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
V 2 |
|
|
m0 |
3 2 e 2kT |
2kT d |
2 |
|
2kT e d |
|
8kT |
|
|
8RT . |
||||||||||||||||||||||
2 kT |
|
|
m |
|
|||||||||||||||||||||||||||||||
c |
|
|
|
|
|
|
m m |
|
|
|
|
|
m |
|
|
|
|
|
|
|
M |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
0 |
|
|
0 |
0 |
|
|
|
0 |
0 |
|
|
|
|
0 |
|
|
|
|
|
|
||||||

Средняя скорость υср
1
υср n 0 n F ( )d ,
где n F (υ)dυ dn – число молекул со
скоростью от υ до υ dυ . Если подставить сюда F(υ) и вычислить, то получим:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
υср |
|
8kT |
|
2,25kT |
|
|
|||
|
|
|
|
πm |
|
|
m |
|
|
||
или |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
υср |
8RТ |
|
2,25RT |
|
|
||||||
|
|
|
|
||||||||
|
|
|
|
πμ |
|
|
μ |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|

СРЕДНЯЯ КВАДРАТИЧНАЯ СКОРОСТЬ
Средней квадратичной скоростью молекул Vкв называется квадратный корень из среднего значения квадрата скорости
V V |
2 . |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кв |
c |
, то есть по теореме о равнораспределении энергии |
||||||||||||||||||
по степеням свободы: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
3kT |
|
3RT |
|
|
|
||||||||
m0 (V 2 )c |
|
3 |
kT |
|
V |
2 |
c |
|
3kT |
3RT |
|
|
V |
|
. |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
2 |
|
2 |
|
|
|
|
|
|
|
кв |
m0 |
|
M |
|
|
|
||||
|
|
|
|
|
|
|
m0 |
M |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Нахождении (V2)c с помощью функции распределения:
V |
|
c |
|
|
m0 |
3 2 |
|
|
|
m0V 2 |
4 |
|
3kT |
|
|
2 |
2 |
|
|
|
|
|
|||||||||
|
V |
F V dV 4 |
|
|
|
exp |
|
2kT |
V |
dV |
m0 |
. |
|||
|
|
|
|||||||||||||
|
|
|
0 |
|
2 kT |
|
0 |
|
|
|
|
|
|||
|
|
|
|
|
Vв :Vc :Vкв 2 : |
8 : 3. |
|
||||||||
Vв :Vc :Vкв 1:1,13:1,22.
вер

Среднюю квадратичную скорость
находят используя соотношение :
mυкв2 3 kT 2 2
|
|
|
|
|
|
|
|
υкв |
3kT |
|
3RT |
||
|
|
m |
|
|
|
|
|
|
|
|
|
|
|

Полезно знать, что
|
υ |
кв |
1,22 |
υср |
1,13; |
|
|
υвер |
|||
|
|
|
|||
|
υвер |
|
|||
F |
|
|
|
|
|
вер ср кв

вер ср кв
вер
