
3861
.pdfМинистерство образования и науки Российской Федерации Федеральное государственное бюджетное образовательное учреждение высшего образования
«Воронежский государственный лесотехнический университет имени Г.Ф. Морозова»
ЭКОЛОГИЯ ПОЛИМЕРНЫХ КОМПОЗИЦИОННЫХ МАТЕРИАЛОВ
Методические указания к лабораторным работам
для студентов по направлению подготовки 19.03.01 - Биотехнология, профиль – Промышленная экология
Воронеж 2017
2
УДК 630*81
Дмитренков, А.И. Экология полимерных композиционных материалов [Текст]: методические указания к лабораторным работам для студентов по направлению подготовки 19.03.01 - Биотехнология, профиль – Промышленная экология / А.И. Дмитренков, Л.А. Новикова, Л.И. Бельчинская; М-во образования и науки РФ, ФГБОУ ВО «ВГЛТУ». – Воронеж, 2017. – 40 с.
Печатается по решению учебно-методического совета ФГБОУ ВО «ВГЛТУ» (протокол № от г.)
Рецензент: канд. хим. наук, доцент кафедры неорганической химии и химической технологии ФГБОУ ВПО «ВГУИТ» Ю. С. Перегудов
Научный редактор канд. техн. наук, доц. А. И. Дмитренков
3
Оглавление
Введение………..………..………..………..………..………..………..………..……..……… |
3 |
Лабораторная работа № 1. Поликонденсация фенола с формальдегидом……………… |
4 |
Лабораторная работа № 2. Поликонденсация карбамида с формальдегидом………….. |
9 |
Лабораторная работа № 3. Глифталевые смолы …………………………………………. |
13 |
Лабораторная работа № 4. Крашение полимеров, красители (с элементами УИРС) …. |
16 |
Лабораторная работа № 5. Крашение древесины, красители (с элементами УИРС) …. |
20 |
Лабораторная работа № 6. Определение вязкости и молекулярной массы полимеров |
25 |
Лабораторная работа № 7. Определение содержания свободного формальдегида в |
30 |
карбамидных смолах ………………………………………………………………………… |
|
Лабораторная работа № 8. Определение степени набухания полимеров .…..…..…..…. |
32 |
Лабораторная работа № 9. Определение температуры размягчения по методу «кольцо-шар» |
33 |
Лабораторная работа №10. Качественные реакции на некоторые природные полимеры |
35 |
Лабораторная работа №11. Качественное определение растворимости полимеров…… 37
Библиографический список………………………………………………………………...... 40
Введение
Методические указания содержат лабораторные работы по курсу ―Экология полимерных композиционных материалов‖. При изучении данной дисциплины студент должен приобрести знания об особенностях строения и свойствах полимеров, методах получения природных синтетических и искусственных полимеров, усвоить понятие ―композиционный материал‖, знать состав композиций и назначение отдельных компонентов. В процессе выполнения лабораторных работ он должен освоить методы синтеза полимерных связующих для композиционных материалов, изучить их свойства, проанализировать взаимосвязь свойств и строения, сделать вывод и рекомендации о путях возможного применения композиционных материалов.
По объемам производства древесные композиционные материалы (ДКМ) занимают в мировой экономике одно из первых мест. Они включают в себя большую группу разнообразных по свойствам и методам производства материалов. К концу ХХ века мировое производство ДКМ в объемных единицах уже превосходило производство сталей, пластмасс и алюминия.

4
При самостоятельной подготовке студент должен составить конспект лабораторной работы, изучить теоретический материал по рекомендуемой литературе для получения допуска к лабораторной работе и ответить на вопросы по порядку выполнения опытов. После выполнения экспериментальной части студент должен записать в тетрадь свои наблюдения и выводы. По каждой лабораторной работе студент должен сдать отчет по теоретической части на оценку.
Лабораторная работа № 1 Поликонденсация фенола с формальдегидом
Цель работы: ознакомиться с методом синтеза и свойствами фенолоформальдегидных смол различной структуры: новолаков, резолов, резитов.
Поликонденсацией называется реакция образования высокомолекулярных соединений из низкомолекулярных (мономеров), содержащих не менее двух функциональных групп, способных реагировать друг с другом с выделением простых веществ (аммиака, воды, галоидоводорода и т.д.).
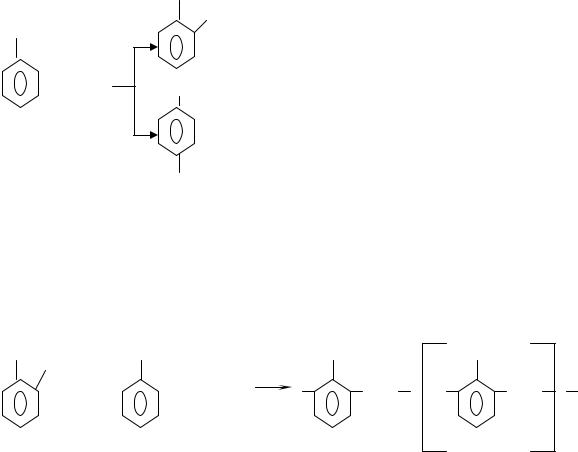
Поликонденсация фенола с формальдегидом в зависимости от условий (соотношение реагентов, типа катализаторов - кислых или щелочных) приводит к получению либо термопластичной смолы – новолака, либо термореактивной – резола, либо смолы сшитой структуры – резита. При избытке фенола (соотношение фенол : формальдегид = 1 : 0,8-0,9) в присутствии кислых катализаторов (соляная, серная, щавелевая кислоты) образуется линейная растворимая термопластичная смола с молекулярной массой 600-1200 у.е. – новолак.
5
На первой стадии взаимодействия фенола с формальдегидом происходит образование монометилольных производных фенола (фенолоспиртов). Процесс идет по типу электрофильного замещения атомов водорода в орто- и парапо- ложениях по фенольному гидроксилу:
|
OH |
|
CH2OH |
ОН |
|
+ CH2=О |
OH |
|
CH2OH |
орто-метилолфенол
пара-метилолфенол
Дальнейшая конденсация орто- и парафенолоспиртов с отщеплением воды дает линейный полимер.
OH |
OH |
OH |
OH |
|
CH2OH |
|
|
|
/ |
CH2 |
CH2 |
|
+ n |
+ n CH2=О -nH2O |
|
новолак n
Новолачная фенолоформальдегидная смола является термопластичным полимером. Она плавится при нагревании и затвердевает при охлаждении без изменения химической структуры полимера. Легкорастворима в различных растворителях.
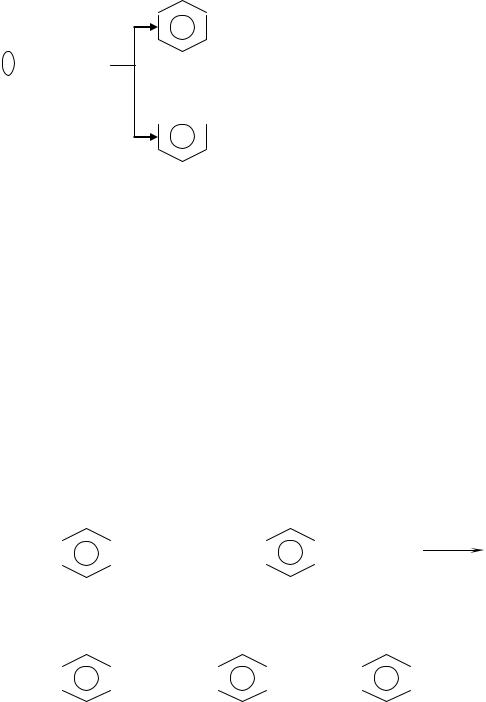
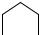
По-другому идет реакция в присутствии щелочных катализаторов. В щелочной среде (катализаторы – аммиак, едкий натр, едкий барий) при избытке формальдегида на начальной стадии образуется диметилольные производные фенола:
6
ОН
ОН |
НОСН2 |
СН2ОН 2,6-диметилолфенол |
|
|
|
 + 2СН2 =О
+ 2СН2 =О
ОН
 СН2ОН
СН2ОН
2,4 – диметилолфенол
СН2ОН
При нагревании диметилолфенолы конденсируются с выделением воды за счет гидроксида метилольных групп и подвижных атомов водорода бензольного кольца с образованием резола. При этом рост цепи может происходить линейно (с увеличением длины боковых ответвлений за счет свободных метилольных групп в n–положении по отношению к фенольному гидроксилу).
Полученная таким образом резольная смола является термореактивным полимером.
Термореактивные резольные смолы отверждаются, то есть превращаются в трехмерный пространственный полимер – резит при нагревании их до 802000С. Реакция идет с выделением воды за счет свободных метилольных групп.
|
|
|
ОН |
|
|
|
ОН |
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
n НОСН2 |
|
|
СН2ОН |
|
|
|
|
|
|
СН2ОН |
||||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
-n H2O |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СН2ОН |
|
|
|
|
|
||||||
|
|
|
ОН |
|
|
|
|
|
|
ОН |
|
|
|
|
|
|
ОН |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
…- |
|
|
|
|
|
СН2 |
|
|
|
|
|
|
|
|
СН2 |
|
|
|
|
|
|
|
|
СН2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
n |
|
|
|
|
|
|
|
|
m |
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
СН2ОН |
|
СН2ОН |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
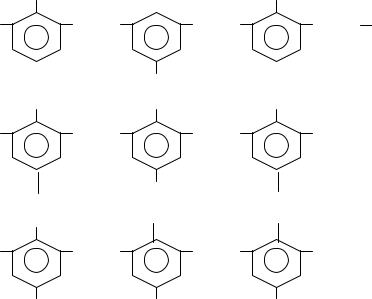
Резит может быть получен также из новолака при нагревании его в щелочной среде с дополнительной порцией формальдегида:
7
|
ОН |
|
|
|
ОН |
|
|
|
СН2 |
|
|
СН2 |
СН2 |
… + n СН2О |
|
|
|
ОН |
|
|
|
|
|
|
ОН |
СН2 |
… |
ОН |
|
|
|
|
СН2 |
|
|
СН2 |
… |
|
|
|
|
|
|
|
|
||
|
|
ОН |
|
|
|
|
|
|
СН2 |
ОН |
|
|
СН2 |
|
резит |
… |
СН2 |
|
|
СН2 |
СН2 |
… |
|
|
ОН |
СН2 |
… |
ОН |
|
|
|
Отверженная смола не разлагается при нагревании до 200 0С и не набухает в растворителях, обладает хорошими диэлектрическими свойствами, механической прочностью и твердостью, стойкостью к воздействию воды, растворителей и разбавленных кислот.
Фенолоформальдегидные смолы (ФФС) находят широкое применение в производстве различных видов пластмасс (фенопласты). Большие количества резольных смол применяют для производства слоистых пластиков из ткани и бумаги. ФФС – основа спиртовых лаков, политур, применяемых при отделке изделий из дерева. Для них характерна высокая скорость отверждения.
Резольные ФФС – используют для изготовления электроизоляционных и химически стойких лаков. Широкое применение нашли клеи на основе резольных фенолоформальдегидных смол в технологии деревообработки. Они используются для склеивания конструкций из древесины, металлов и пластмасс с древесиной, для изготовления фанеры. Клеи на основе резольных смол обладают высокими диэлектрическими показателями, водостойкостью, химической стойкостью.
Новолачные ФФС используются в качестве связующего при производстве пресспорошков, из которых изготавливаются различные строительные детали в виде арматуры, плит, труб.
8
Экспериментальная часть
Опыт 1.1. Получение новолачной ФФС
Помещают в пробирку 2,5 г фенола, 2 мл 40 % формалина, вносят кипятильный камешек. Нагревают смесь с холодильником до образования однородной жидкости и осторожно кипятят ее 1-2 мин. Затем вливают из пипетки или из другой пробирки 0,2 мл (несколько капель) концентрированной соляной кислоты (катализатор). При встряхивании горячая смесь начинает кипеть без подогревания через 1-2 мин. Жидкость мутнеет и внизу отслаивается тяжелое, непрозрачное масло. Если кипение прекращается, снова подогревают смесь на открытом огне 1-2 мин. Сливают верхний мутный слой и добавляют в пробирку примерно такой же объем воды, сливают воду, а смолу с остатками воды выливают на часовое стекло. Остывшую светло-сиреневую смолу снимают со стекла, высушивают в фильтровальной бумаге, снимают комочек и взвешивают. При хранении она постепенно твердеет и делается хрупкой тем быстрее, чем дольше продолжалось кипячение.
Опыт 1.2. Получение резольной ФФС
Помещают в пробирку 3 г фенола и 10 мл 40 % формалина. Смесь нагревают с холодильником на водяной бане до полного растворения фенола. Осторожно в слегка остывшую смесь вводят 3 мл концентрированного раствора аммиака (NH4OH – катализатор) и продолжают нагревание на горячей водяной бане (t = 80-90 0С) еще 10-15 мин. По окончании реакции происходит расслоение смеси на верхний водный слой и нижний слой (прозрачная желтокоричневая смола). Резольная смола образуется несколько медленнее новолачной и в меньшем количестве.
Водный слой сливают, смолу вливают в пробирку и проводят опыт 1.3.
Примечание: необходимо тщательно проводить нагрев, так как при недостаточной продолжительности нагревания смола в опытах 1.1, 1.2 получается липкой и почти не твердеет.
9
Опыт 1.3. Резит из резольной смолы
Часть полученной в опыте 1.2. смолы осторожно нагревают на открытом огне в сухой пробирке, держа пробирку горизонтально. При этом удаляется избыток воды, а смола при продолжительном нагревании вспучивается и затвердевает. Образуется неплавкий и нерастворимый резит.
Вопросы и задания
1.Какие вещества используются в качестве мономеров при поликонденсации? Приведите пример.
2.Что такое функциональность мономера? Чему равна функциональность фенола, формальдегида?
3.Что такое олигомеры?
4.Напишите реакцию поликонденсации фенола с избытком формальдегида в кислой среде, выделите элементарное звено. Назовите полученную смолу.
5.К чему приводит нагревание новолачной ФФС в присутствии формальдегида? Напишите реакцию.
6.Чем отличаются термореактивные полимеры от термопластичных?
7.Напишите реакцию образования новолачной смолы из n-крезола и формальдегида.
8.Какой из трех изомерных диоксибензолов наиболее активен в реакции конденсации с формальдегидом?
9.Напишите реакцию резорцина с формальдегидом:
а) в кислой среде, б) в щелочной среде. 10.Каковы особенности реакции поликонденсации?
11.Как проявляется ступенчатый характер поликонденсации при реакции фенола с формальдегидом?
Лабораторная работа № 2
Поликонденсация карбамида с формальдегидом
Цель работы: ознакомиться с особенностями синтеза карбамидоформальдегидных (мочевиноформальдегидных) смол, влиянием различных факторов на процесс поликонденсации.

10
Одной из важнейших реакции поликонденсации, нашедшей широкое техническое применение, является реакция карбамида (мочевины) с формальдегидом. Характер и скорость взаимодействия карбамида с формальдегидом в водном растворе зависят от условий реакции: катализатора, рН среды, температуры, соотношения исходных веществ, а также их концентрации в реагирующей среде. При этом влияние рН среды на молекулярную массу и структуру карбамидоформальдегидных смол (КФС) является определяющим. Рассмотрим влияние отдельных факторов на эту реакцию.
Влияние pH среды. В нейтральной или слабощелочной среде при температуре, не превышающей 40 оС в зависимости от соотношения карбамида и формальдегида образуется преимущественно моноили диметилолкарбамид. При молярном соотношении карбамида и формальдегида 1:1 образуется преимущественно монометилолкарбамид.
NH2 |
|
NHCH2OH |
|
NHCH2OH |
|
|
|
NH4OH |
|
NH4OH |
|
CO + |
CH2O |
CO |
+ |
CH2O |
CO |
|
|
|
|
|
|
NH2 |
|
NH2 |
|
|
NHCH2OH |
мочевина |
формаль- |
монометилол- |
|
формаль- |
диметилол- |
(карбамид) |
дегид |
мочевина |
|
дегид |
мочевина |
Метилолкарбамиды растворяются в воде и образуют вязкие растворы. При нагревании этих растворов при 100о в слабощелочной среде в присутствии NH4OH происходит поликонденсация монометилолкарбамида с отщеплением воды и образованием макромолекул линейного строения (полиметиленкарбамиды):
|
|
|
|
|
|
|
|
H-N-CH2OH H-N-CH2OH |
|
H-N-CH2-- |
N-CH2 |
–OH |
|||
|
|
NH4OH |
|
|
|
|
|
CO |
+ n CO |
|
CO |
|
CO |
|
+ n H2O |
|
|
100о |
|
|
|
|
|
NH2 |
NH2 |
|
NH2 |
|
NH2 |
|
n |
|
|
|
|||||
При рН 10 (сильнощелочная среда) образуются линейные олигомеры. Полученный полимер хорошо растворим в воде.
