

3.1 Исходные данные
Принятые исходные данные для расчета реактора представлены в таблице 3.1, состав сырья (бутен-изобутиленовой фракции) - в таблице 3.2, варианты заданий для расчета реактора синтеза МТБЭ - в таблице 3.3.
Таблица 3.1 – Исходные данные для расчета реактора
Параметр |
Единица |
Значение |
Температура процесса, t |
°С |
70 |
Давление процесса, Р |
МПа |
0,75 |
Количество дней работы установки |
- |
330 |
Производительность по МТБЭ, GМТБЭ |
т/год |
50000 |
Производительность по МТБЭ, GМТБЭ |
кг/ч |
6313,1 |
Конверсия изобутилена, ХИБ |
доля масс. |
0,95 |
Доля изобутилена на образование изооктилена, ХИБИО |
доля масс. |
0,005 |
Доля изобутилена на образование третбутанола, ХИБТБ |
доля масс. |
0,005 |
Соотношение метанол : изобутилен (мольное), К |
- |
4 |
Селективность процесса по изобутилену (на МТБЭ), S |
- |
0,99 |
Таблица 3.2 – Состав БИФ (бутен-изобутеновой фракции)
Компонент |
% масс. |
∑C3 |
0,5 |
Изобутан |
2 |
Н-бутан |
12 |
Бутен-1 + бутен-2 |
37 |
Изобутилен |
48,4 |
∑C5 |
0,1 |
Итого |
100 |
3.2Расчет процесса синтеза МТБЭ 3.2.1 Материальный баланс реактора
Обозначим количество изобутилена, поступающего в реактора как GИБ. Тогда количество конвертированного изобутилена составит
где ХИБ – конверсия изобутилена, доля масс. (таблица 3.1).
Количество образовавшегося МТБЭ составит:
где S – селективность процесса по изобутилену (на МТБЭ); ММТБЭ и МИБ – молекулярные массы МТБЭ и изобутена соответственно, г/моль.
31
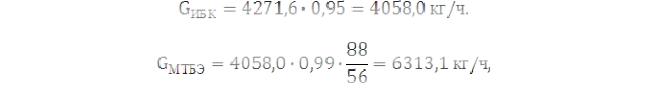
Таблица 3.3 – Варианты заданий для расчета реактора синтеза МТБЭ
Вариант |
Производительность |
Количество дней |
Температура |
|
реактора, т/год по МТБЭ |
работы |
процесса, °С |
||
|
||||
|
|
|
|
|
1 |
25000 |
325 |
60 |
|
2 |
27500 |
330 |
65 |
|
3 |
30000 |
335 |
70 |
|
4 |
32500 |
340 |
75 |
|
5 |
35000 |
325 |
80 |
|
6 |
37500 |
330 |
60 |
|
7 |
40000 |
335 |
65 |
|
8 |
42500 |
340 |
70 |
|
9 |
45000 |
325 |
75 |
|
10 |
47500 |
330 |
80 |
|
11 |
50000 |
335 |
60 |
|
12 |
52500 |
340 |
65 |
|
13 |
55000 |
325 |
70 |
|
14 |
57500 |
330 |
75 |
|
15 |
60000 |
335 |
80 |
|
16 |
62500 |
340 |
60 |
|
17 |
65000 |
325 |
65 |
|
18 |
67500 |
330 |
70 |
|
19 |
70000 |
335 |
75 |
|
20 |
72500 |
340 |
80 |
|
21 |
75000 |
325 |
60 |
|
22 |
77500 |
330 |
65 |
|
23 |
80000 |
335 |
70 |
|
24 |
82500 |
340 |
75 |
|
25 |
85000 |
325 |
80 |
|
26 |
87500 |
330 |
60 |
|
27 |
90000 |
335 |
65 |
|
28 |
92500 |
340 |
70 |
|
29 |
95000 |
325 |
75 |
|
30 |
97500 |
330 |
80 |
Подбираем значение GИБ таким образом, чтобы количество образовавшегося МТБЭ совпадало со значением, представленным в таблице 3.1. В ходе подбора определили, что GИБ = 4271,6 кг/ч. Таким образом,
Количество образовавшегося МТБЭ составит
32

что совпадает с табличным значением.
Количество непрореагировавшего изобутилена определяется по формуле
Количество углеводородной фракции, поступающей в реактор,
где 0,484 – содержание изобутилена в исходном сырье, доля мас. (таблица 3.2).








































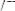


 .
.
Массовое соотношение метанол : изобутилен определится как





 )
)
где К – мольное соотношение метанол : изобутилен (табл. 3.1); ММЕТ – молекулярная масса метанола, г/моль.
Количество метанола на входе в реактор:
Количество метанола, пошедшего на образование МТБЭ:




































 .
.
Количество непрореагировавшего метанола на выходе из реактора:
Количество воды, пошедшей на образование третбутилового спирта:
где МВОДА – молекулярная масса воды, г/моль; ХИБТБ - доля изобутилена,
пошедшего на образование третбутанола, доля мас. (таблица 3.1).
Количество образовавшегося третбутанола:
где МТБ – молекулярная масса третбутанола, г/моль.
Количество образовавшегося изооктилена:
где ХИБИО – доля изобутилена, пошедшая на образование изооктилена, доля мас.
.
Материальный баланс реактора представлен в таблице 3.4.
33

Таблица 3.4 – Материальный баланс реактора
Компонент |
% масс. |
т/год |
т/сут |
кг/ч |
кг/с |
Приход |
|
|
|
|
|
∑C3 |
0,24 |
349,5 |
1,1 |
44,1 |
0,012 |
Изобутан |
0,95 |
1398,0 |
4,2 |
176,5 |
0,049 |
Н-бутан |
5,70 |
8387,9 |
25,4 |
1059,1 |
0,294 |
Бутен-1 + бутен-2 |
17,56 |
25862,6 |
78,4 |
3265,5 |
0,907 |
Изобутилен |
22,97 |
33831,1 |
102,5 |
4271,6 |
1,187 |
∑C5 |
0,05 |
69,9 |
0,2 |
8,8 |
0,002 |
Метанол |
52,50 |
77328,3 |
234,3 |
9763,7 |
2,712 |
Вода |
0,04 |
51,7 |
0,2 |
6,5 |
0,002 |
Итого |
100,0 |
147279,0 |
446,3 |
18595,8 |
5,166 |
Расход |
|
|
|
|
|
МТБЭ |
33,95 |
50000,0 |
151,5 |
6313,1 |
1,754 |
Непрореагировавший метанол |
40,16 |
59146,5 |
179,2 |
7468,0 |
2,074 |
Непрореагировавший изобутилен |
1,15 |
1691,6 |
5,1 |
213,6 |
0,059 |
∑C3 |
0,24 |
349,5 |
1,1 |
44,1 |
0,012 |
Изобутан |
0,95 |
1398,0 |
4,2 |
176,5 |
0,049 |
Н-бутан |
5,70 |
8387,9 |
25,4 |
1059,1 |
0,294 |
Бутен-1 + бутен-2 |
17,56 |
25862,6 |
78,4 |
3265,5 |
0,907 |
∑C5 |
0,05 |
69,9 |
0,2 |
8,8 |
0,002 |
Изооктилен |
0,11 |
160,7 |
0,5 |
20,3 |
0,006 |
Третбутанол |
0,14 |
212,4 |
0,6 |
26,8 |
0,007 |
Итого |
100,0 |
147279,0 |
446,3 |
18595,8 |
5,166 |
3.2.2 Тепловой баланс реактора
Суть теплового баланса реактора заключается в определении количества несбалансированного тепла, образующегося в ходе процесса и в расчете количества водяного конденсата, необходимого для снятия избытка тепла процесса синтеза МТБЭ. Количество вносимого в реактор или уносимого из реактора тепла определится по формуле
где Gi – расход i-го компонента, кг/с; Сpi – теплоемкость i-го компонента, кДж/(кг·град); ti – температура, °С.
Для углеводородных компонентов сырья и продуктов реакции теплоемкость определим по формуле
где 



 – относительная плотность нефтепродукта. Значение
– относительная плотность нефтепродукта. Значение 


 определим по формуле
определим по формуле
34

где 


 - относительная плотность нефтепродукта при 20 °С. Является справочной величиной.
- относительная плотность нефтепродукта при 20 °С. Является справочной величиной.
Значения плотностей углеводородных компонентов сырья представлены в таблице 3.5.
Таблица 3.5 – Плотности углеводородных компонентов сырья
Компонент |
Плотность, ρ420 |
Плотность, ρ1515 |
∑C3 |
0,5100 |
0,5162 |
Изобутан |
0,5573 |
0,5633 |
Н-бутан |
0,5789 |
0,5847 |
Бутен-1 + бутен-2 |
0,5945 |
0,6002 |
Изобутилен |
0,595 |
0,6007 |
∑C5 |
0,6262 |
0,6317 |
Диизобутилен |
0,7149 |
0,7199 |
Значения теплоемкости метанола, третбутанола и МТБЭ являются справочной величиной.
Потери тепла в реакторе принимаются равными 1 % от входящего тепла. Реакция синтеза МТБЭ протекает с выделением тепла. Тепловой эффект
реакции определяется по формуле
где НПРОД и НС – теплоты образования продуктов реакции и исходного сырья соответственно, кДж/моль.
Ввиду малой доли побочных реакций в ходе процесса их влиянием на тепловой эффект пренебрегаем. Теплоты образования метанола, изобутилена и МТБЭ приведены в таблице 3.6.
Таблица 3.6 – Теплоты образования компонентов
Компонент |
|
МТБЭ |
Метанол |
Изобутилен |
|
|
|
|
|
Теплота образования, |
кДж/моль |
-291 |
-201 |
-16,92 |
Таким образом, согласно реакции, по которой протекает процесс, тепловой эффект реакции составит
Мольное количество образовавшегося МТБЭ составит
Таким образом, количество тепла, выделившееся в ходе синтеза МТБЭ составит
Тепловой баланс реактора представлен в таблице 3.7.
Из таблицы 3.7 видно, что разность входящего и уходящего тепла равняется
35
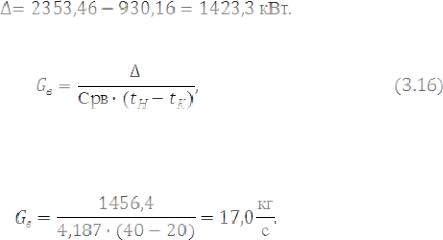
Количество воды, необходимой для снятия избытка тепла процесса, вычисляется по формуле:
где Срв – теплоемкость воды, принимается равной 4,187 кДж/(кг·К); tН и tК – начальная и конечная температура соответственно охлаждающей воды, °С; принимаем соответственно 20 и 40 °С.
Подставляя значения, получим
Таблица 3.7– Тепловой баланс реактора
Компонент |
Расход, |
Температура, °С |
Теплоемкость, |
Количество тепла, |
|
кг/с |
кДж/(кг·град) |
кДж/с |
|||
Приход |
|
|
|
|
|
∑C3 |
0,012 |
70,00 |
2,514 |
2,16 |
|
Изобутан |
0,049 |
70,00 |
2,406 |
8,26 |
|
Н-бутан |
0,294 |
70,00 |
2,362 |
48,64 |
|
Бутен-1 + бутен-2 |
0,907 |
70,00 |
2,331 |
148,02 |
|
Изобутилен |
1,187 |
70,00 |
2,330 |
193,54 |
|
∑C5 |
0,002 |
70,00 |
2,272 |
0,39 |
|
Свежий метанол |
0,638 |
70,00 |
2,610 |
116,51 |
|
Циркулирующий |
2,074 |
70,00 |
2,610 |
379,00 |
|
Вода |
0,002 |
70,00 |
4,187 |
0,53 |
|
Тепло реакции |
- |
- |
- |
1456,41 |
|
Итого |
5,166 |
|
|
2353,46 |
|
Расход |
|
|
|
|
|
МТБЭ |
1,754 |
70,00 |
2,511 |
308,20 |
|
Непрореагировавший |
2,074 |
70,00 |
2,610 |
379,00 |
|
метанол |
|||||
|
|
|
|
||
Непрореагировавший |
0,059 |
70,00 |
2,330 |
9,68 |
|
изобутилен |
|||||
|
|
|
|
||
∑C3 |
0,012 |
70,00 |
2,514 |
2,16 |
|
Изобутан |
0,049 |
70,00 |
2,406 |
8,26 |
|
Н-бутан |
0,294 |
70,00 |
2,362 |
48,64 |
|
Бутен-1 + бутен-2 |
0,907 |
70,00 |
2,331 |
148,02 |
|
∑C5 |
0,002 |
70,00 |
2,272 |
0,39 |
|
Изооктилен |
0,006 |
70,00 |
2,129 |
0,84 |
|
Третбутанол |
0,007 |
70,00 |
2,771 |
1,44 |
|
Потери |
- |
- |
- |
23,53 |
|
Итого |
5,166 |
|
|
930,16 |
|
|
|
36 |
|
|
3.2.3 Геометрические размеры реактора
Общий массовый расход сырьевой смеси равен (таблица 3.4) 18595,8 кг/ч. Объемный расход сырьевой смеси GОБ = 27,25 м3/ч. Требуемая объемная скорость подачи сырья в реактор синтеза составляет ω = 1,5 ч-1.
Таким образом, необходимый объем реакционной зоны вычисляется по формуле
|
V |
GoБ |
|
|
|||
|
|
|
|
||||
|
|
p |
w |
(3.17) |
|||
|
|
|
|
||||
V |
27,25 |
|
18,2м2 |
|
|||
|
|
|
|||||
p |
1,5 |
|
|
|
|
|
|
|
|
|
|
|
|
||
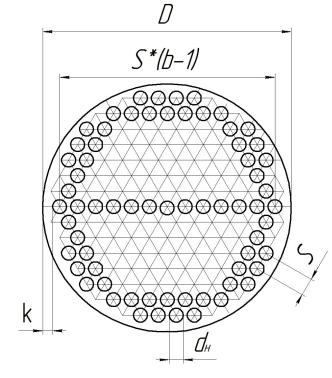
Принимаем шестиугольное расположение труб в реактор. Принимаем следующие параметры реактора:
-внутренний диаметр трубок dВН = 0,1 м;
-толщина стенок δ = 0,01 м;
-наружный диаметр трубок dН = 0,12 м;
-кольцевой зазор между крайними трубками и корпусом k = 0,01 м;
-длина трубок l = 6 м.
Схема размещения труб в решетке приведена на рисунке 3.2.
Рисунок 3.2 – Схема размещения труб в решетке реактора Объем одной трубки вычисляется по формуле
V |
3,14 d2 |
l. |
вн |
||
|
||
Tp |
4 |
(3.18) |
|
||
|
37 |
|
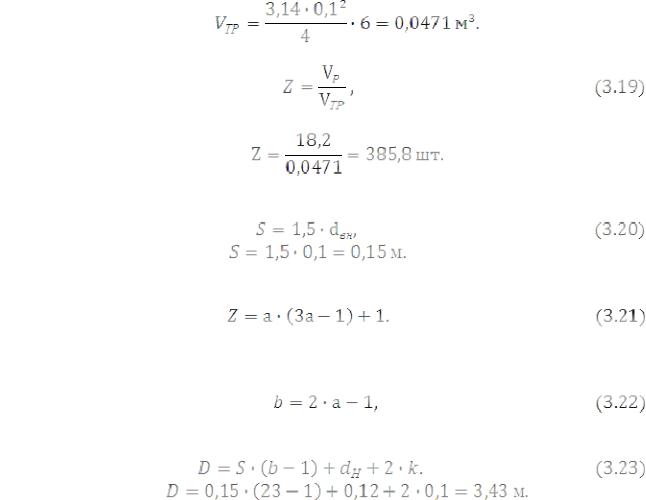
Необходимое количество трубок определяется по формуле
Примем с запасом количество трубок в реакторе равным Z = 400 штук. Шаг трубок определяется по формуле
Связь между числом трубок на стороне наибольшего шестиугольника (а) и общим числом трубок (Z) выражается соотношением
При количестве трубок Z = 400, а = 12,04, округляем до а = 12 шт. Число труб, расположенных на диагонали наибольшего шестиугольника,
определяется по формуле
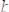





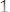










 .
.
Диаметр аппарата вычисляется по формуле
Принимаем стандартное значение диаметра D = 3,5 м.
Уточненное значение кольцевого зазора между крайними трубками и корпусом с учетом нового значения диаметра реактора составит k = 0,03 м.
Список литературы
1 Танатаров М.А., Ахметшина М.Н., Фасхутдинов Р.А. и др. Технологические расчеты установок переработки нефти: учеб. пособие для вузов. – М.: Химия, 1987. – 352 с.
3 Сарданашвили А. Г., Львова А. И. Примеры и задачи по технологии переработки нефти и газа.-2-е изд., - М.: Химия, 1980. – 256с.
5Кузнецов А.А., Кагерманов С.М. и др. Расчеты процессов и аппаратов нефтеперерабатывающей промышленности. – Л.: Химия, 1974. – 343 с.
6Дубовкин Н.Ф. Справочник по теплофизическим свойствам углеводородных топлив и их продуктов сгорания. – М.-Л.: Госэнергоиздат,
1962. – 288 с.
7Флореа О., Смигельский О. Расчеты по процессам и аппаратам химической технологии. – М.: Химия, 1971. – 448 с.
8Батунер Л.М. Процессы и аппараты органического синтеза и биохимической технологии. - Л., Химия, 1966. – 520с.
38
9 Варгафтик Н.Б. Справочник по теплофизическим свойствам газов и жидкостей. - М.: Физматгиз, 1963. – 708с.
10Козлов Б.И. Процессы алкилирования изомеризации и полимеризации
внефтепереработке. – М.: Химия, 1990. – 65 с.
11Ахметов С.А. Технология глубокой переработки нефти и газа. –Уфа:
Гилем 2002. – 672 с.
12Мириманян А.А., Вихман А.Г., Мкртпычев А.Л. Нефтепереработка и нефтехимия. – 2006. - №4. - С. 22-31.
13Интернет-ресурс www.chemistry.ssu.samara.ru
14Кузора И.Е., Томин В.П., Микишев В.А. и др. Технологии производства компонентов современных автомобильных бензинов // Химия и технология топлив и масел. – 2008. - №2. - С. 33.
15Стыценко В.Д., Лавриненко А.А., Надра В.А. и др. Перспективы улучшения экологических и эксплуатационных свойств моторных топлив // Химия и технология топлив и масел. – 2008. - №5. - С. 52.
16Ахметов С.А., Ишмияров М.Х., Кауфман А.А. Технология переработки нефти, газа и твердых горючих ископаемых: учеб. пособие. – СПб.: Недра, 2009. – 832 с.
17Капустин В.М., Кукес С.Г., Бертолусини Р.Г. Нефтеперерабатывающая промышленность США и бывшего СССР. – М.: Химия, 1995. – 304 с.
18Интернет-ресурс http://www.bmcompany.ru/ru/products/bioethanol/field_ of_application401.html. Высоко-кислородные добавки (оксигенаты) к топливу.
|
СОДЕРЖАНИЕ |
|
|
Введение |
1 |
1 |
Расчет процесса алкилирования изобутана олефинами |
2 |
2 |
Расчет процесса изомеризации углеводородов |
18 |
3 |
Расчет процесса синтеза метил-трет-бутилового эфира (МТБЭ) |
27 |
Редактор М.Е. Галина
Подписано в печать 01.-8.11. Бумага офсетная. Формат 60х84 1/16. Гарнитура «Таймс». Печать трафаретная. Усл. печ. л. 2,4. Уч.-изд. л. 2,2. Тираж 60. Заказ .
Издательство Уфимского государственного нефтяного технического университета Адрес издательства:
450062, Республика Башкортостан, г. Уфа, ул. Космонавтов, 1
39
