
- •Комплексные (координационные) соединения
- •Альфред Вернер (Werner A.) (12.XII.1866 - 15.XI.1919) Нобелевская премия по химии, 1913 г.
- •Составные части комплекса (кооординационной частицы)
- •Факторы, влияющие на состав комплексного соединения
- •Правило Сиджвика для определения состава комплексов
- •Правило Сиджвика (примеры)
- •Shriver and Atkins Inorganic Chemistry, 2010
- •Монодентатные лиганды образуют одну связь с комплексообразователем
- •Бидентатные лиганды образуют хелатные комплексы
- •Пентандион-2,4
- •Хелатные (клешневидные) комплексы с полидентатным лигандом – этилендиаминтетрауксусной кислотой
- •Жизненно важные комплексы хлорофил гемоглобин
- •Витамин В12
- •C.E. Housecroft, A.G. Sharpe. Inorganic chemistry, 2005 К. Сайто, С. Хаякава и др.
- •-комплексы
- •Классификация комплексных соединений
- •2. По природе лигандов
- •е) ацидокомплексы (лиганды – кислотные остатки неорганических и органических кислот)
- ••3. По составу внешней сферы
- •4. По внутренней структуре комплексных соединений:
- •в) полиядерные комплексы содержат два и более центральных атома
- •ИЗОМЕРИ
- •Изомерия комплексных соединений
- •[Cr(H2O)6]Cl3 фиолетовый [CrCl(H2O)5]Cl2·H2O светло-зеленый [CrCl2(H2O)4]Cl·2H2O темно-зеленый [CrCl3(H2O)3]·3H2O красный
- •Полимеризационные изомеры: (относят к
- •желтый
- •граневая
- •фиолетовый
- •Оптические изомеры способны вращать плоскость поляризации светового луча влево (L-изомер) или вправо (D-изомер).
- •Вращение плоскости поляризации плоско поляризованного света при прохождении
- •Примеры оптических изомеров комплексных соединений
- •Примеры названий комплексных соединений
- •Примеры названий комплексных соединений
- •Примеры названий комплексных соединений
- •Реакция Чугаева
- •1.Неорганическая химия: в 3 т. /Под ред. Ю.Д. Третьякова. — М.: Издательский центр
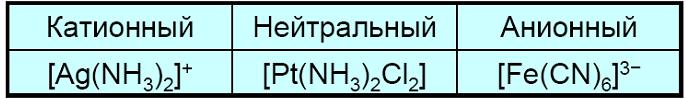
Классификация комплексных соединений
• 1. По знаку заряда комплексного иона
• |
а) катионные |
[Cu(NH |
) |
] SO |
; |
[Cr(H |
O) |
] Cl ; |
||
|
3 |
4 |
|
4 |
|
|
2 |
6 |
3 |
|
• |
б) анионные |
Ca[Cr(NH ) |
(SCN) |
]; |
|
|
||||
|
|
3 2 |
|
|
4 |
|
|
|
||
• в) нейтральные (соединения неионного характера) – [Rh(NH3)3Br3]
•г) соединения с комплексным катионом и комплексным анионом –
[Pt(NH3)4][PdCl6] .
2. По природе лигандов
а) аммиакаты (лиганды – NH3)
[Pt(NH3)6]Br2
б) аквакомплексы (лиганды – H2O)
[Ti(H2O)6]Cl3
в) гидроксокомплексы (лиганды – OH-)
Na[Sb(OH)6]
г) галогенидные (лиганды – F-, Cl-, Br-, I- ) Na3[AlF6]
д) карбонилы (лиганды –СО)
[Fe(CO)5]
е) ацидокомплексы (лиганды – кислотные остатки неорганических и органических кислот)
Na2[Ti(C2O4)3]
ж) цианидные (лиганды –CN-)
Na[Ag(CN)2]
2-
з) тиосульфатные (лиганды – S2O3)
Na3[Cu(S2O3)2]
и) смешаннолигандные комплексы –
[Pt(H2O)(NH3)6(OH)]NO3
•3. По составу внешней сферы
•а) комплексные кислоты
H2[SiF6]
• б) комплексные основания
[Cu(NH3)4](OH)2;
• в) комплексные соли
K2[HgI4].

4. По внутренней структуре комплексных соединений:
а) комплексы с монодентатными лигандами –
[Pt(NH3)6]Cl2 Na3[AlF6]
б) комплексы с полидентатными лигандами (хелатные комплексы)
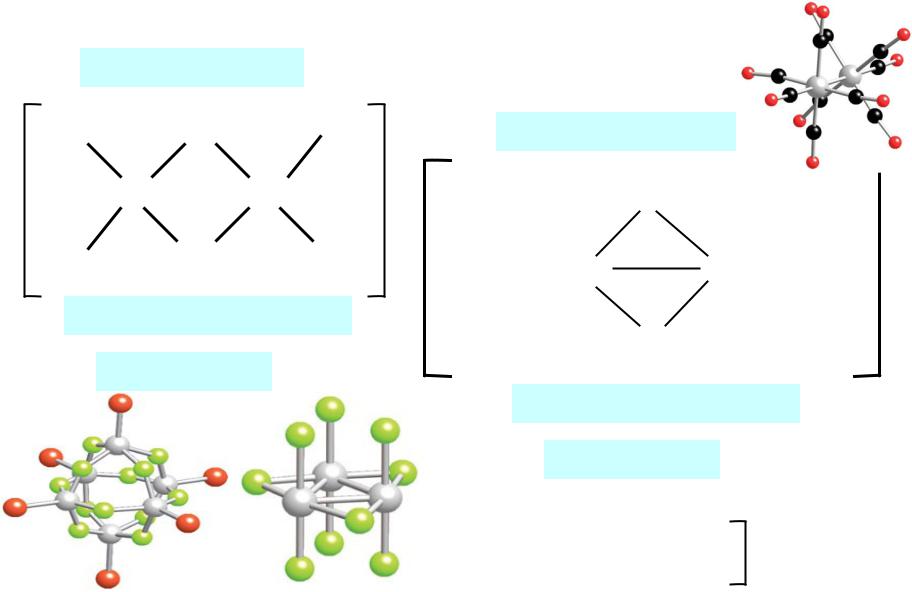
в) полиядерные комплексы содержат два и более центральных атома
Мостиковый
Cl Cl Cl
Al Al
Cl Cl Cl
КЧ 4
Кластер
[M6X12L6]2+ Re3Cl9
[(CO)5Mn – Mn(CO)5]
Смешанный тип
CO
(CO)3Co Co(CO)3
CO
КЧ 6
Кластер
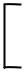 Cl4Re
Cl4Re ReCl4 2–
ReCl4 2– 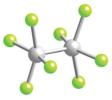

ИЗОМЕРИ
Я
Структурная
изомерия Стереоизомерия
Координационная |
Связевая |
Геометрическая |
Оптическая |
изомерия |
изомерия |
изомерия |
изомерия |

Изомерия комплексных соединений
Изомеры – химические соединения, одинаковые по составу и молекулярной массе, но различающиеся по строению и свойствам
[Pt(NH3)4SO4](OH)2 и [Pt(NH3)4(OH)2]SO4 pH 7 pH 7
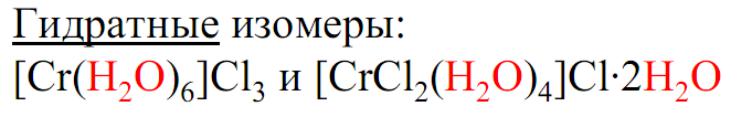
[Cr(H2O)6]Cl3 фиолетовый [CrCl(H2O)5]Cl2·H2O светло-зеленый [CrCl2(H2O)4]Cl·2H2O темно-зеленый [CrCl3(H2O)3]·3H2O красный
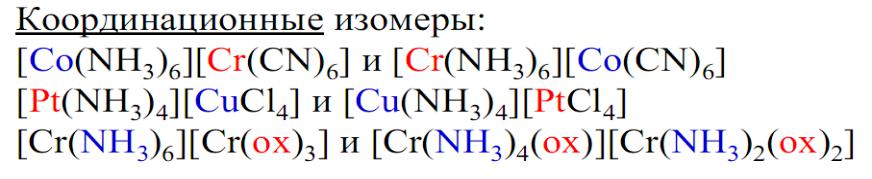
Полимеризационные изомеры: (относят к
изомерам условно, так как фактически являются
мономером |
и |
димером) |
[Co(NH3)3(NO2)3] |
и [Co(NH3)6][Co(NO2)6] |
|
Неэлектролит |
|
электролит |
[Pt(NH3)2Cl2] |
и [Pt(NH3)4][PtCl4] |
|
Неэлектролит |
|
электролит |
