
- •Строение атома
- •Ядерная модель атома
- •Постулаты Бора
- •Свет – электромагнитная волна
- •Виды излучений
- •Типы спектров
- •Спектральный анализ
- •Шкала электромагнитных волн
- •Инфракрасное излучение (тепловое)
- •Ультрафиолетовое излучение
- •Рентгеновские лучи
- •Модель атома водорода по Бору
- •Излучение атома водорода
- •Вынужденное излучение
- •Населенность уровней
- •Устройство рубинового лазера
- •Свойства лазерного излучения
- •Строение атомного ядра
- •Ядерные силы
- •Цепная реакция деления ядер урина
- •Неуправляемая цепная реакция
- •Управляемая цепная реакция
- •Радиоактивность
- •Виды радиоактивных излучений
- •Типы радиоактивного распада (правило смещения)
- •Закон радиоактивного распада
- •Экспериментальные методы регистрации заряженных частиц
- •Сцинтилляционный счетчик
- •Газоразрядный счетчик Гейгера
- •Получение радиоактивных изотопов
- •Биологическое действие радиоактивных излучений
- •Зарождение физики элементарных частиц
Свет – электромагнитная волна
Свет – это электромагнитная волна (λ = 4∙10−7 – 8∙10−7 м), которую излучает атом.
П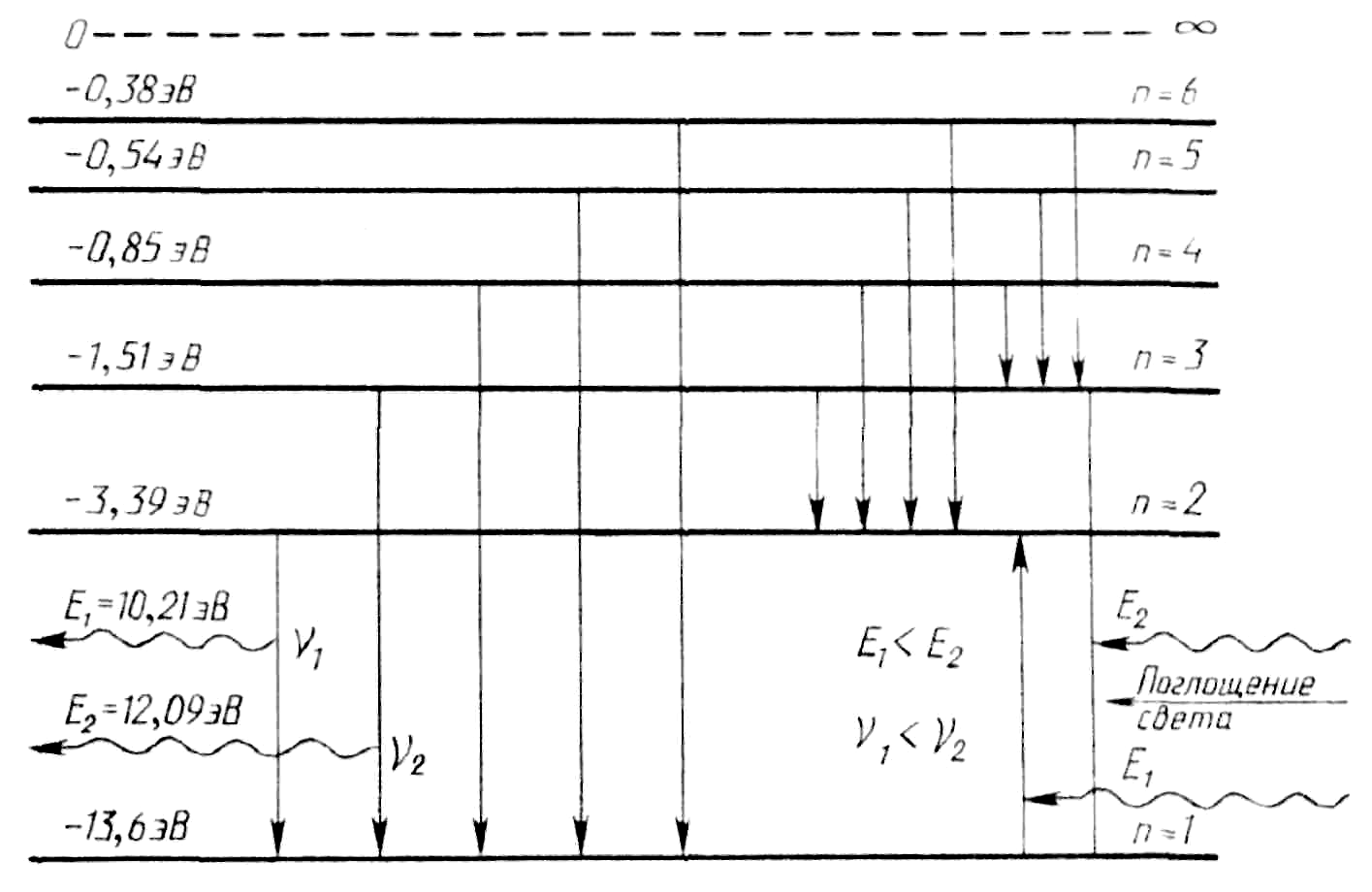 о
второму постулату Бора возможные частоты
излучения водорода равны:
о
второму постулату Бора возможные частоты
излучения водорода равны:
![]() ,
или
,
или
![]()
где R – постоянная Ридберга, равная 3,2∙1015 с−1, n и k – номера орбит.
Таким образом, источниками света являются возбужденные атомы и молекулы, свет генерируется при переходе атомов (молекул) из одного возбужденного состояния в другое, v генерируемого света пропорциональна ΔE, свет излучается и поглощается в виде квантов.
Виды излучений
Тепловое
При столкновении быстрых атомов (или молекул) друг с другом часть их кинетической энергии превращается в энергию возбуждения атомов, которые затем излучают свет (Солнце, лампа накаливания, пламя и др.).
Электролюминесценция
При разряде в газе электрическое поле увеличивает Ek электронов. Быстрые электроны возбуждают атомы в результате неупругого соударения с ними. Возбужденные атомы отдают энергию в виде световых волн (трубки для рекламных надписей, северное сияние и др.).
Катодолюминесценция
Свечение твердых тел, вызванное бомбардировкой этих тел электронами (электронно-лучевые трубки телевизоров).
Хемилюминесценция
Электроны возбуждаются от химических реакций (светлячки и другие живые организмы, бактерии, насекомые, многие рыбы).
Фотолюминесценция
П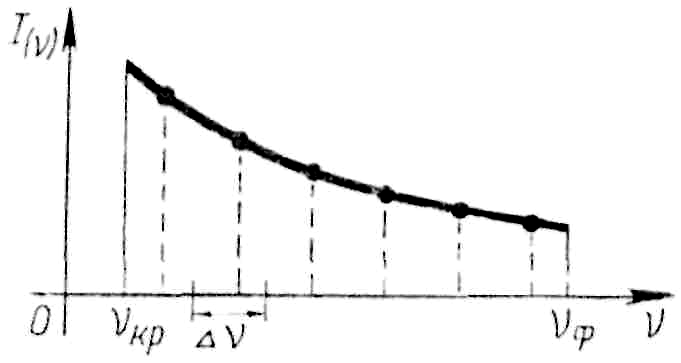 адающий
па вещество свет возбуждает атомы
вещества, после чего они излучают свет
(светящиеся краски).
адающий
па вещество свет возбуждает атомы
вещества, после чего они излучают свет
(светящиеся краски).
Распределение энергии в спектре
Все источники не дают свет строго определенной длины волны. Распределение излучения по частотам характеризуется спектральной плотностью интенсивности излучения Iν. Тогда интенсивность и излучения с небольшого спектрального интервала Δν равна IνΔν.
Распределение энергии в видимой части спектра электрической дуги.
Типы спектров
Спектры испускания
Совокупность частот (или длин волн), которые содержатся в излучении какого-либо вещества, называют спектром испускания. Они бывают грех видов.
Сплошной – эго спектр, содержащий все длины ноли определенного диапазона от красного с λк = 7,6∙10−7 м до фиолетового с λф = 4∙10−7 м. Сплошной спектр излучают нагретые твердые и жидкие вещества, газы, нагретые под большим давлением.
Л инейчатый
– это спектр, испускаемый газами, парами
малой плотности в атомарном состоянии.
Состоит из отдельных линий разного или
одного цвета, имеющих разные расположения.
Каждый атом излучает набор электромагнитных
воли определенных частот. Поэтому каждый
химический элемент имеем свой спектр.
инейчатый
– это спектр, испускаемый газами, парами
малой плотности в атомарном состоянии.
Состоит из отдельных линий разного или
одного цвета, имеющих разные расположения.
Каждый атом излучает набор электромагнитных
воли определенных частот. Поэтому каждый
химический элемент имеем свой спектр.
Полосатый – это спектр, который испускается газом в молекулярном состоянии.
Линейчатые и полосатые спектры можно получить путем нагрева вещества или пропускания электрического тока.
Спектры поглощения
С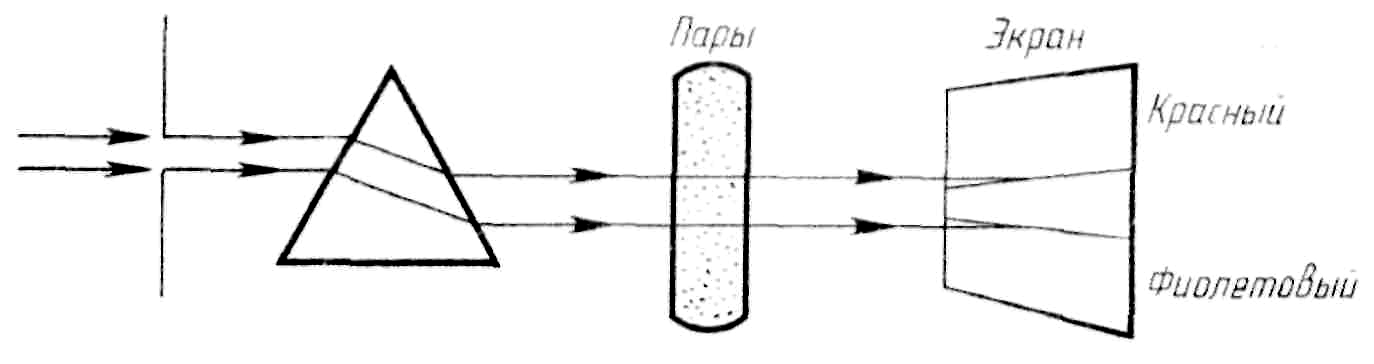 пектры
поглощения получают, пропуская свет от
источника, дающего сплошной спектр,
через вещество, атомы которого находятся
в невозбужденном состоянии.
пектры
поглощения получают, пропуская свет от
источника, дающего сплошной спектр,
через вещество, атомы которого находятся
в невозбужденном состоянии.
Спектр поглощения – это совокупность частот, поглощаемых данным веществом. Согласно закону Кирхгофа вещество поглощает те линии спектра, которые и испускает, являясь источником света.
Спектральный анализ
Исследование спектров испускания и поглощения позволяет установить качественный состав вещества Количественное содержание элемента в соединении определяется путем измерения яркости спектральных линий. Метод определения качественного и количественного состава вещества по его спектру называется спектральным анализом. Зная длины волн, испускаемых различными парами, можно установить наличие тех или иных элементов и веществе. Этот метод очень чувствителен, Можно обнаружить элемент, масса которого в пробе не превышает 10−10 г. Отдельные линии в спектрах различных элементов могут совпадать, но в целом спектр каждого элемента является его индивидуальной характеристикой. Спектральный анализ сыграл большую роль в науке. С его помощью был изучен состав Солнца и звезд.
В спектре Солнца (1814) были открыты фраунгоферовы темные линии.
Солнце – раскаленный газовый шар (Т ≈ 6000°С), испускающий сплошной спектр Солнечные лучи проходят через атмосферу Солнца, где Т ≈ 2000 – 3000 °С.
Корона поглощает из сплошного спектра определенные частоты, а мы на Земле принимаем солнечный спектр поглощения По нему можно определить, какие элементы присутствуют в короне Солнца.
О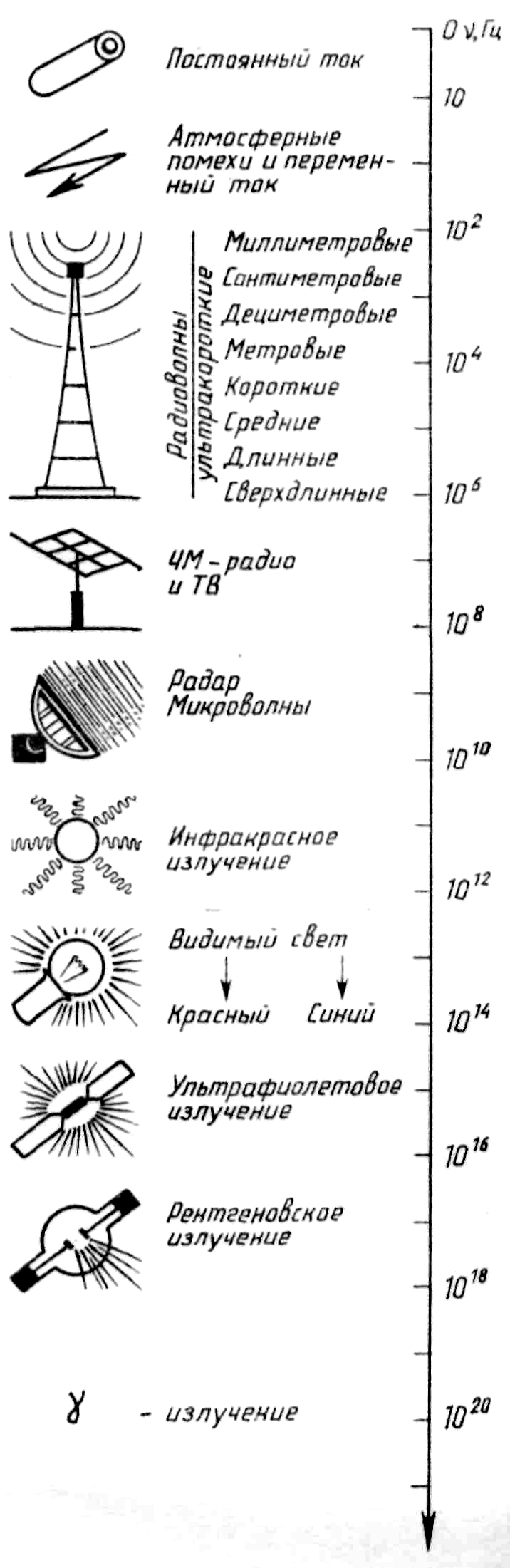 н
помог обнаружить все земные элементы,
а также неизвестный элемент, который
назвали гелий. Через 26 лет (1894) открыли
гелий на Земле. Благодаря спектральному
анализу открыто 25 элементов.
н
помог обнаружить все земные элементы,
а также неизвестный элемент, который
назвали гелий. Через 26 лет (1894) открыли
гелий на Земле. Благодаря спектральному
анализу открыто 25 элементов.
Благодаря сравнительной простоте и универсальности спектральный анализ является основным методом контроля состава вещества в металлургии и машиностроении. С помощью спектрального анализа определяют химический состав руд и минералов.
Спектральный анализ можно производить как по спектрам испускания, так и по спектрам поглощения.
Состав сложных смесей анализируется по молекулярном) спектру.
ОК-32
