
ВЭЯ ItSpdlll'm длипм ■
TNM Клиническая классификация Т — Первичная опухоль
ТХ — Недостаточно данных для оценки первичной опухоли
ТО — Первичная опухоль не определяется
Tis — Преинвазивная карцинома {carcinoma in situ)
Tl — Рак шейки матки, ограниченный маткой (распространение на тело учитывается)
Т1А — Инвазивная карцинома, диагностируется только микроскопически. Все опухоли, определяемые макроскопически, даже при поверхностном спространении, оцениваются Т1 В/стадия IB
Т1А1 — Инвазия стромы не более 3,0 мм в глубину и 7,0 мм по горизонтали Т1А2 — Инвазия стромы вглубь до 5,0 мм, горизонтальное распространив до 7,0 мм
Т1В — Клинически видимая опухоль, ограниченная шейкой, илимик-хжопическая опухоль больше Tl A2/IA2 Т1В1 — Клинически определяемая опухоль до 4,0см в наибольшем изме-
2нии
Т1В2 — Клинически определяемая опухоль более 4,0см в наибольшем змерении
Т2 — Опухоль шейки с распространением на матку, но без прорастания генки таза или нижней трети влагалища Т2А — Без инвазии параметрия Т2В — С инвазией параметрия
ТЗ — Рак шейки с распространением на стенку таза и/или вовлечением ижней трети влагалища, и/или приводит к гидронефрозу, или не функционирующей почке
ТЗА — Опухоль поражает нижнюю треть влагалища, но не распростра-[яется на стенку таза
ТЗВ — Опухоль распространяется на стенку таза и/или приводит к гид-юнефрозу или не функционирующей почке
Т4 — Опухоль распространяется на слизистую оболочку мочевого пузыря 1ли прямой кишки и/или распространяется далее малого таза
Примечание. Наличия буллезного отека недостаточно для классификации опухоли сак Т4.
N — Регионарные лимфатические узлы
Регионарными являются лимфатические узлы, расположенные около шейки и тела матки, подчревные (внутренние подвздошные, обтураторные), общие и наружные подвздошные, прекрестцовые и боковые сакральные
NX — Недостаточно данных для оценки состояния регионарных лимфатических узлов
N0 — Нет признаков поражения метастазами регионарных лимфатических узлов
N1 — Метастазы в регионарных лимфатических узлах М — Отдаленные метастазы
MX — Недостаточно данных для определения отдаленных метастазов
МО — Нет признаков отдаленных метастазов Ml — Имеются отдаленные метастазы
Группировка по стадиям
Стадия О
Стадия IA Стадия IA1 Стадия IA2 Стадия IB Стадия IB1 Стадия IB2 Стадия ПА Стадия ПВ Стадия III А Стадия IIIВ
Tis
Т1А
Т1А1
Т1А2
TIB
Т1В1
Т1В2
Т2А
Т2В
ТЗА
T1,T2,T3AN1
NO NO NO NO NO NO NO NO NO NO MO
MO MO MO MO MO MO MO MO MO MO
Стадия Стадия
IVA IVB
ТЗВ Т4
Любая Т
Любая N Любая N Любая N
МО МО Ml
В настоящее время основными методами лечения больных раком шейки матки являются хирургический, лучевой и комбинированный.
Хирургическое лечение проводят в основном у больных с ограниченными опухолями шейки матки. Для большинства больных с преинвазивным раком методом выбора является конусовидная электроэксцизия шейки матки. У больных с преинвазивным раком экстирпацию матки выполняют по следующим основным показаниям:
возраст старше 50 лет;
преимущественная локализация опухоли в шеечном канале;
распространенный анапластический вариант опухоли с врастанием в железы;
отсутствие в препарате после проведенной ранее конизации участков, свободных от преинвазивного рака (особенно по линии разреза);
техническая невозможность выполнить широкую электроэксцизию (коническая или укороченная шейка матки при сглаженных влагалищных сводах);
сочетание преинвазивного рака с миомой матки или опухолями придатков.
В случаях перехода преинвазивного рака на влагалищные своды показана экстирпация матки с верхней третью влагалища. Практически все больные преинвазивным раком шейки матки могут быть излечены.
Оперативное вмешательство широко используется и при лечении больных инвазивным раком шейки матки. Стандартным объемом операции является расширенная экстирпация матки (операция Вертгейма). Операция Вертгейма относится к числу наиболее серьезных онкологических вмешательств; нередко она осложняется повреждением мочевыводящих путей, возникновением так называемых лимфатических кист и лимфостаза.
комбинированный метод лечения состоит из двух компонентов: хирур-гского и лучевого, последовательность применения которых может быть
1Ичной.
"Оказаниями к комбинированному лечению являются: 1В стадия забо-ания (большая экзофитная опухоль; неблагоприятные прогностичес-: факторы; инвазия, превышающая 10 мм), II стадия в тех случаях, когда 'холь сочетается с беременностью и гинекологическими заболеваниями спалительный процесс придатков; опухоли матки и яичников), III ста-i с поражением регионарных лимфатических узлов (метастатический ва-iht), невозможность проведения сочетанного лучевого лечения, а также (истентность опухоли к облучению, выявленная при проведении лучевой >апии.
При IB стадии последовательность методов лечения не оказывает сущес-;нного влияния на его результативность. Между тем оперативное вмеша-тьство в качестве первого этапа лечения технически проще выполнимо и, ответственно, более эффективно.
Предоперационная лучевая терапия показана при больших экзофитных [ухолях (IB стадия); обоснованных подозрениях на метастазы в регионар-ле лимфатические узлы; некоторых вариантах II стадии рака шейки матки молодых женщин (переход опухоли на ближайшие к матке отделы парамет-шьной клетчатки или своды влагалища). Основными вариантами предо-фационной лучевой терапии являются следующие:
Дистанционное облучение первичного очага и зон регионарного мета-газирования в статическом или подвижном режиме. Разовые поглощенные озы составляют 2 Гр, суммарные — порядка 30 Гр. Операция выполняется ерез 12—14 дней после завершения облучения.
Дистанционное облучение тазовых лимфатических узлов через стати-еские поля, разовая очаговая доза в точках В — 4 Гр, суммарная — 16 Гр. \а первичный опухолевый очагдо и после дистанционного облучения про-юдят внутриполостное воздействие по 5—7 Гр в точке А за фракцию. Опера-шю проводят через 3—7 дней по окончании лучевой терапии.
Интенсивное концентрированное дистанционное облучение в под-зижном режиме, разовая очаговая доза — 5—6 Гр, суммарная — 20—24 Гр. Расширенную экстирпацию матки проводят на второй-третий день после эблучения.
Цель послеоперационного облучения — воздействие на опухолевые клетки, оставшиеся в зоне операции, а также на субклинические очаги поражения. Послеоперационную лучевую терапию осуществляют также у больных, имевших противопоказания к предоперационному облучению, при наличии глубокой инвазии опухоли и при метастазах в регионарные лимфатические узлы, выявленных при гистологическом исследовании удаленного препарата. Достоинством послеоперационного облучения является его целенаправленность, обусловленная четким представлением о распространенности опухолевого процесса.
Послеоперационную дистанционную лучевую терапию проводят с помощью источников высоких энергий (гамма-терапия, линейные ускорите-
ли электронов с энергией тормозного излучения 5—20 МэВ) в статическом или подвижном режиме. Разовые поглощенные дозы при этом обычно составляют 2 Гр, суммарные — 40—46 Гр.
При наличии неблагоприятных прогностических признаков (низкая диф-ференцировка опухоли, глубокая инвазия, распространение на тело матки, наличие метастазов в регионарных лимфатических узлах) послеоперационная дистанционная лучевая терапия дополняется профилактическим облучением стенок влагалища. При этом разовые дозы на глубине 0,5—1 см составляют около 5 Гр, суммарные — 30—35 Гр. Внутриполостное облучение проводят с ритмом два раза в неделю в дни, свободные от дистанционной лучевой терапии.
Самостоятельная сочетанная лучевая терапия является основным методом лечения, при этом почти у 75 % пациенток лучевая терапия — единственный метод лечения.
Эффективность лучевой терапии неуклонно повышается, что является результатом внедрения новых достижений ядерной физики и клинической дозиметрии, однако до сих пор 30—45 % больных раком шейки матки погибает от основного заболевания, а у 10—30% пациенток формируются лучевые повреждения, в первую очередь мочевого пузыря и прямой кишки.
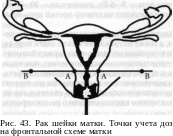
Проводят сочетанную лучевую терапию, включающую внутриполостное и дистанционное облучение. Главная цель внутриполостного лучевого воздействия — разрушение первичного опухолевого очага. Оптимальное распределение дозы от внутриполостного облучения достигается размещением источников в полости матки и овоидов в сводах влагалища (рис. 43). Доза при этом рассчитывается на опорную точку А, располагающуюся на 2см вверх от латерального свода влагалища и на 2 см вбок от оси цервикального канала. Точка В расположена в 5 см от центральной оси таза и анатомически соответствует группе запирательных лимфатических узлов.
Радиоактивные источники размещаются в аппликаторах, которые вводят в полость матки и влагалище. Аппликаторы могут представлять собой просто резиновую внутриматочную трубку и овоиды, вводимые в своды вла-
 галища,
либо специальные металлические или
пластиковые аппликаторы с современными
приспособлениями для последовательного
введения.
галища,
либо специальные металлические или
пластиковые аппликаторы с современными
приспособлениями для последовательного
введения.
Для внутриполостной лучевой терапии используются l37Cs и 60Со. Аппараты «Агат-В», «Агат-ВЗ», «Агат-ВУ» обеспечивают автоматизацию всего технологического цикла облучения на основе применения средств современной
эопроцессорной техники. Эти средства включают в себя систему ситуации, радиационного контроля, дистанционного компьютерного уп-ения полипозиционным перемещением высокоактивных источников, :же наблюдения за больным в процессе сеанса облучения, зависимости от активности источников методики внутриполостного об-ния проводят с низкой мощностью дозы (НМД), при которой мощность i в точке А составляет 50—70 сГр/ч; средней (СМД) — 15—20сГр/мини вы-
ш мощности дозы (ВМД) —более 200 сГр/мин. Физическая доза при пере-отНМДкСМДи ВМД соответственно уменьшается на 10—15%ина 35—
>, что позволяет достичь примерно равного биологического эффекта.
Суммарная очаговая доза от внутриполостного облучения в точках А за-
ит от стадии заболевания и мощности дозы ионизирующего излучения.
i использовании источников НМД у больных I стадии рекомендуется
водить СОД порядка 60—70 Гр, при II стадии — 70—75 Гр, при III ста-
[ - 80-90 Гр.
Дистанционное облучение проводят на зоны регионарного метастазиро-ия, на краевые отделы первичной опухоли, а в некоторых клинических уациях — на область первичного очага.
Источниками дистанционного облучения являются линейные ускори-и и гамма-терапевтические аппараты. Облучение осуществляют вста-шском или подвижном режимах. Разовые поглощенные дозы составляют •3 Гр, суммарные — 40—46 Гр.
При местно распространенном раке шейки матки дистанционное облу-
гие на первом этапе может проводиться с двух встречных открытых по-
\ до достижения суммарной очаговой дозы 20—30 Гр. Затем мочевой пу-
рь, прямая кишка и первичный очаг экранируются (формирующие блоки,
 ля
сложной конфигурации, мето-
ля
сложной конфигурации, мето-
ки 4-польного облучения) и доза
точку В доводится до 40—46 Гр
ис. 44). При проведении лучевой рапии у больных I—II стадии пер-[чный опухолевый очаг облучается )еимущественно за счет внутрипо->стных источников. В этих случа-с экранирование очага и смежных эганов проводится с самого начала Злучения.
Применение в качестве радио-одификатора метронидазола, рас-воренного в диметилсульфоксиде ЦМСО), позволило повысить пяти-етнюю выживаемость больных II тадии на 13 %, III стадии — на 23 %.
ДМСО проявляет свои протек-орные свойства, как при самостоя-ельном применении, так и в качестве растворителя метронидазола. Частота лучевых повреждений прямой кишки и мочевого пузыря при использовании ДМСО снижается в 4—6 раз. При этом удается полностью избежать тяжелых (язвенных или фистульных) лучевых повреждений.
При I стадии рака шейки матки 5-летняя выживаемость колеблется от 73 до 97,5 %. При II стадии, согласно статистическим данным, охватывающим результаты лечения в крупных клиниках мира, 5-летняя выживаемость больных в среднем составляет 48—50 %.
При III стадии злокачественного процесса 5-летняя выживаемость варьирует от 12,5—35 до 63—69,1 %, и при IV стадии — от 0 до 29,2 %.
