
- •Тау жыныстарын айналмалы бұрғылау қалай іске асырылады?
- •Таужыныстарын соққылап бұрғылау қалай іске асырылады?
- •Тау жыныстарын соққылап-бұрып бұрғылау.
- •Тау жыныстарын соқпа-айналымды бұрғылау.
- •Жарылғыш зат дегеніміз не?
- •Жарылыс реакциясының өту түрі.
- •Өнеркәсіптік жз-тар қандай қоспалардан тұрады?
- •Жарылыстың қандай түрлері болады?
- •Химиялық жарылыс д/з не?
- •Жз құрамдарына қоспалар қандай мақсатта қосылады?
- •Жз сипаттамаларын бағалау үшін қандай сынақ әдістері қолданылады?
- •Жарылғыш заттардың бризанттылығын анықтау.
- •Жарылғыш заттардың жұмыс істеуге қабілеттілігін анықтау.
- •Жз сезімталдығын анықтау.
- •Жарылғыш заттардың сапасын тексеру әдістері.
- •Құрғақ ұнтақталған жарылғыш заттар.
- •Құрамында суы бар жарылғыш заттар.
- •Жз оқтамдарын от арқылы қоздыру әдісінің ерекшеліктері.
- •От арқылы қоздыру әдісіндегі қолданылатын құралдар
- •Жарылғыш зат оқтамын электрлі-отты қоздыру әдісі.
- •Электрлі қоздыру әдісінің тиімділігі.
- •Электрлі қоздыру желісін жалғау әдістері.
- •Жз оқтамын дүмпіткіш пілте арқылы қоздыру әдісі.
- •Жарылғыш зат оқтамдары қандай белгілермен топталады?
- •Жарылыстан пайда болатын ұра көлемін қалай анықтауға болады?
- •Табан бойынша кедергі сызығы д/з не және оны қалай анықтайды?
- •Үйлер мен ғимараттарға байланысты зақымдану дәрежесі қалай белгіленеді?
- •Шпурлық оқтам д/з не, қолданылу орны.
- •Ұңғымалық оқтамды ашық кен жұмыстарында қолдану технологиясы.
- •Камералық оқтамдарды жербеті жағдайында қолдану әдісі.
- •Карьерлердегі ұңғымаларды қандай техникалармен оқтауға болады?
- •Камералық оқтамды дайындау үшін камераның көлемін қалай анықтайды?
- •Ұңғымаларды бос ауа аралықтарын қалдырып оқтаудың тиімділігі.
- •Ұңғымалар арақашықтығын қалай анықтайды?
- •Жерасты қазбаларының забойларында шпурлар қалай орналасады?
- •Шпурлардың тереңдігі қандай жағдайларға байланысты анықталады?
- •Бір аттыруға қолданылатын жз көлемі қалай анықталады?
- •Жарылғыш заттың меншікті шығыны д/з не?
- •Шпурларды пайдалану коэф?
- •Забойды қопаруға қолданылатын шпурлар саны қалай анықталады?
- •Электрлі қол бұрғыларының жұмыс принципі және қолданылатын орны.
- •Оттегілік баланс д/з не?
- •Оттегілік баланстың қандай түрлері болады?
- •Оттегілік балансты анықтауда аммиакты селитра қалай қолданылады?
- •Жарылыстан пайда болатын газдар қалай анықталады?
- •Нөлдік оттегілік баланс д/з не?
- •Жз жарылысынан пайда болатын газ көлемі қалай анықталады?
- •Жз жарылысынан пайда болатын қысымды қалай анықтауға болады?
- •Дүмпіткіш капсюль д/з не?
- •Отпілтенің құрылысы.
- •Тұтандырғыш түтік д/з не және ол қалай жасалады?
- •Электрлі-отты қоздыру жабдығы қалай жасалады?
- •Электрлі дүмпіткіш д/з не?
- •Лезде атылатын электрлі дүмпіткіштердің құрылысы.
- •Кідіріп атылатын электрлі дүмпіткіштердің ерекшеліктері.
- •Электрлі дүмпіткіштерге ток беретін құралдар.
- •Дүмпіткіш пілте құрылысы және қолданылатын орны.
- •Дүмпіткіш пілте аттыру желісін жалғау әдісі.
- •Жз оқтамын соққы толқынды қоздыру әдісі.
- •Соққы толқынды қоздыру әдісінің ерекшеліктері.
Жарылыстан пайда болатын газдар қалай анықталады?
Жарылыс болатын ортаның жағдайына байланысты жарылыстан пайда болатын газ құрамында улы заттар – көміртегі жəне азот тотықтары пайда болады
Жарылыстан пайда болатын газдардың нақты құрамын сəйкес тепе-теңдік константаларын қолдану арқылы есептеуге болады. Бірақ мұндай есептеулер, əсіресе, процестің бастапқы бөлімінде, яғни жарылыс газдарының температурасы мен қысымы жоғары кезде белгілі қиындықтар туғызады. Сондықтан жарылыс газдарының құрамын суыған күйіндегі химиялық талдаулар арқылы немесе тепе-теңдік процестерін ескере отырып, зерттеу қажет. Оларды анықтау үшін көбінесе, Ле-Шателье жəне Бринкли мен Уильсон əдістері қолданылады.
Ле-Шателье әдісі жарылыс газдарының максимальды көлемі принципіне негізделген, соған қоса көлемдер тең болған жағдайда басымдылық жоғары жылу бөлетін реакцияларға беріледі. Осы әдіс бойынша оттегілік балансы оң жарылғыш заттар үшін сутегінің Н2О-ға дейін және көміртегінің СО2-ге дейін толық тотығуын, сонымен қатар молекулярлық азот N2 және оттегі О2 пайда болады деп қабылдайды. Оттегілік балансы теріс жарылғыш заттар үшін реакция басымдылығын көміртегінің СО-ға дейін тотығуына береді. Егер мұндай жағдайда оттегі толық шығындалмаса, оның қалдығы тең мөлшерде СО-ны СО2-ге дейін және Н2-ні Н2О-ға дейін тотықтыруға жұмсалады.
Бринкли мен Уильсон әдісін, әдетте, жарылыс газдарының бастапқы құрамын анықтау үшін қолданады. Бұл әдіс энергетикалық жағынан барынша тиімді реакциялардың басымдылығын ескереді және сонымен қоса қайтымды реакциялардың да тепе-теңдігін ескеріп отырады. Соның әсерінен оттегілік балансы теріс жарылғыш заттар үшін жарылыс реакциясының соңғы процесі энергетикалық максимумнан ауытқиды. Оттегілік баланс оң немесе нөл болған кезде жарылыс реакциясының бағыты Ле-Шателье әдісіндегі сияқты қабылданады, яғни сутегі мен оттегі толық тотыққан газдар пайда болады, ол өз кезегінде максимальды жылу тиімділігін береді.
Нөлдік оттегілік баланс д/з не?
Егер ЖЗ құрамында жанғыш элементтерді толық тотықтыратын оттегі болса, онда – нөлдік оттегілік баланс деп аталады. Нөлдік оттегілік балансты, жарылғыш заттардың жарылысы кезінде негізінен су булары, көмір қышқылдары, еркін азот, алюминий тотығы және аз мөлшерде улы газдар бөлінеді. Сақтандырылмайтын ЖЗ нөлдік ОБқа ие.
Жз жарылысынан пайда болатын газ көлемі қалай анықталады?
Жарылыс газының көлемі жарылғыш заттың жұмыс істеуге қабілеттілігін сипаттайды. Газ көлемі қаншама көп болса, жарылыс қуаты механикалық жұмысқа бейім келеді.
Жарылыс газының көлемін Авогадро заңының негізінде анықтайды. Яғни, қалыпты жағдайда кез келген газдың 1 мольі 22,4 литрге тең болады. Бұл көлемді газдың мольдік көлемі деп атайды: Vm=22,4 л/моль н/е 22,4 м3/кмоль.
Жарылғыш заттың 1 мольінің жарылысы кезіндегі газ көлемі:
 ,
л/моль
,
л/моль
мұндағы ∑n – жарылыс газдарының барлық мольдерінің жиынтығының мөлшері.
1 г жарылғыш заттың жарылысынан бөлінетін газ көлемі – меншікті көлем деп аталады:
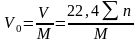 ,
л/г;
,
л/г;
мұндағы М – жарылғыш заттың мольдік массасы, г/моль.
1 кг жарылғыш зат атылған кезде газ көлемі 1000 есе жоғары болады да, өлшемі – м3/кг белгіленеді.
ЖЗ-тың жарылыс жылуын қалай анықтауға болады?
Жарылыс жылуы деп 1 кг жарылғыш заттың жарылысы кезіндегі бөлінетін жылу қуатының мөлшерін айтамыз.
Жарылыс жылуы – бұл дүмпу толқынының майданында жүретін бірінші реттік химиялық реакциялардың және реакция біткеннен кейінгі жарылыс өнімдерінің адиабатты кеңеюі кезінде жүретін екінші ретті реакциялардың жылу әсері.
Өзінен жылуды бөліп шығаратын реакцияларды – экзотермиялық деп атаймыз: С + О2 = СО2; ΔН = –393 кДж.
Егер реакция барысында қоршаған ортадан жылуды өзіне тартатын болса, онда эндотермиялық деп аталады: N2 + О2 = 2Н2О; ΔН = 180,8 кДж.
мұндағы ΔН – жылу әсері, кДж.
Жарылыс жылуын теориялық және тәжірибелік жолмен де анықтауға болады.
Жарылыс кезінде бөлінетін жылу мөлшері жарылыс жылуының жиынтығы мен жарылғыш заттың өз жылуының айырымына тең, яғни:
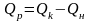 ,
кДж;
,
кДж;
мұндағы Qр – тұрақты қысым кезіндегі 1 моль ЖЗ-тың жарылыс жылуы, кДж;
Qк = n1q1 + n2q2 + ... – жарылыс газдарының пайда болуы кезіндегі жылу мөлшері, кДж;
n1, n2, ... – жарылыс газдарының мольдерінің мөлшері;
q1, q2, ... – жарылыстан бөлінетін әртүрлі газдардың жылу бөлу мөлшері, кДж;
Qн – 1 моль жарылғыш заттың жылу мөлшері, кДж.
ЖЗ-тың жарылыс температурасы қалай анықталады?
Газдардың температурасын келесі формуламен анықтауға болады:
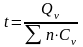 ;
;
мұндағы Qv – тұрақты көлем кезіндегі жарылыс жылуы, кДж/моль; Сv – жарылыстан бөлінетін барлық газдардың жылу сыйымдылығы
Жарылғыш заттың жарылыс температурасын білу арқылы, жарылғыш заттың түрін дұрыс таңдауға болады. Жарылыс температурасы 1800–45000С аралығында болуы мүмкін. Жарылыс жылуының жоғарылауы жарылғыш заттың құрамына, бөлінетін газдардың түріне, ылғалдылығына байланысты болады. Жарылғыш заттың құрамына алюминий ұнтағын қосатын болсақ, жарылыс температурасы жоғарылайды, ал инертті тұздар қосылатын болса, керісінше төмендейді.
