
- •Демидюк
- •ПРИНЦИПЫ ОЧИСТКИ БЕЛКОВ
- •ХНОЛОГИЯ БЕЛКОВЫХ ПРЕПАРАТ
- •ЛИТЕРАТУРА
- •БЕЛКИ СОСТОЯТ ИЗ АМИНОКИСЛОТ
- •ЙСТВА АМИНОКИСЛОТ ОЧЕНЬ РАЗНООБРАЗ
- •ПРОСТРАНСТВЕННАЯ ОРГАНИЗАЦИЯ БЕЛКОВ
- •ОВЫЕ МОЛЕКУЛЫ АМФИФИЛЬНЫ И АМФОТ
- •ИЗОЭЛЕКТРИЧЕСКАЯ ТОЧКА БЕЛКОВ
- •И СИЛЬНО РАЗЛИЧАЮТСЯ ПО РАЗМЕРУ И Ф
- •ЕТОДЫ ФРАКЦИОНИРОВАНИЯ БЕЛКО
- •ХРОМАТОГРАФИЯ
- •Осы и пчелы
- •йшая система для колоночной жидкостной хроматог
- •Обращенно-фазовая хроматография
- •Гидрофобная хроматография
- •Ионообменная хроматография
- •Катионо- и анионообменники
- •АНИОНИТЫ КАТИОНИТЫ
- •ивые титрования катионо- и анионообменни
- •Гель-проникающая хроматография
- •Материалы для ГПХ
- •ределение молекулярной массы методом Г
- •ффинная (биоспецифическая) хроматограф
- •еры взаимодействий в аффинной хроматогр
- •Лиганды с индивидуальной специфичностью
- •Лиганды с групповой специфичностью
- •3. Нуклеозид
- •4. Триазиновые красители
- •. Лиганды для протеаз
- •6. Олиго(dT) и полиуридировая кислота
- •Металлохелат аффинная хроматография
- •Металлохелат аффинная хроматография
- •Методы элюции
- •ЕТОДЫ ФРАКЦИОНИРОВАНИЯ БЕЛКО
- •ЕКТРОФОРЕТИЧЕСКИЕ МЕТОДЫ РАЗДЕЛЕН
- •Скорость движения идеализированной
- •Гель-электрофорез
- •Полиакриламидный гель
- •Агарозный гель
- •Агарозный и полиакриламидный гели
- •Вертикальный и горизонтальный электрофорез
- •Вертикальный электрофорез
- •Изоэлектрическое фокусирование
- •еление белков по размера с использованием
- •Гель-электрофорез: как это выглядит
- •ЕТОДЫ ФРАКЦИОНИРОВАНИЯ БЕЛКО
- •Центрифугирование –
- •Разделение осаждением
- •Диализ и ультрафильтрация
- •ЕТОДЫ ФРАКЦИОНИРОВАНИЯ БЕЛКО
- •СТРАТЕГИЯ ОЧИСТКИ БЕЛКОВ
- •ОСОБЕННОСТИ МЕТОДОВ РОМАТОГРАФИЧЕСКОГО РАЗДЕЛЕНИЯ СПОЛЬЗОВАНИИ ИХ ДЛЯ ОЧИСТКЕ БЕ
- •МЕЖДУ ЧЕТЫРЕХ ОГНЕЙ
- •ТКА РЕКОМБИНАНТНЫХ ВАРИАНТОВ ГЛУТАМИЛЭНДОПЕПТИ
- •ТЕЛЬЦА ВКЛЮЧЕНИЯ
- •чистка металлопротеазы термоактиномицет
- •Вопросы для
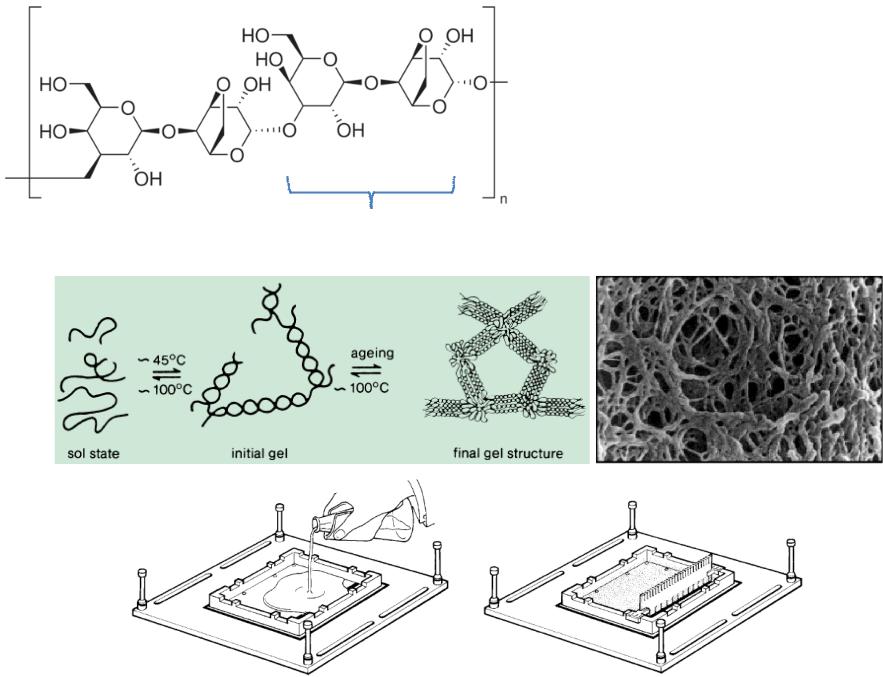
Агарозный гель
Агароза – полисахарид. Ее элементарным звеном служит дисахарид агаробиоза, в состав которого входит необычный сахар – 3,6- ангидро-L-галактоза.
Структура и формирование агарозного геля
Scanning EM image of agarose polymer
Заливка горячего |
Установка |
раствора агарозы |
«гребенки» |
в форму |
|
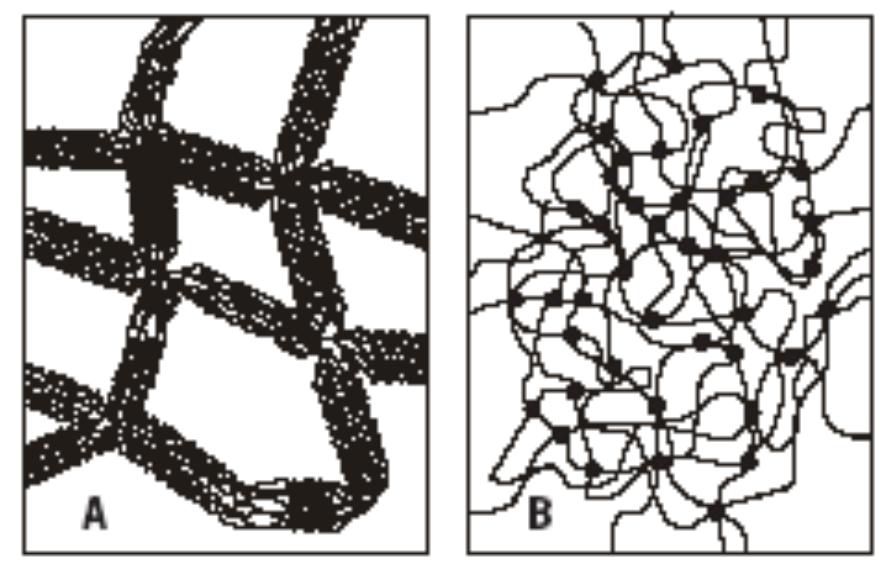
Агарозный и полиакриламидный гели
В агарозном геле |
В полиакриламидном геле |
формируются нековалентные |
полимерные цепи связаны |
водородные и гидрофобные |
ковалентными поперечными |
связи между протяженными |
сшивками (•) |
полисахаридными нитями |
|
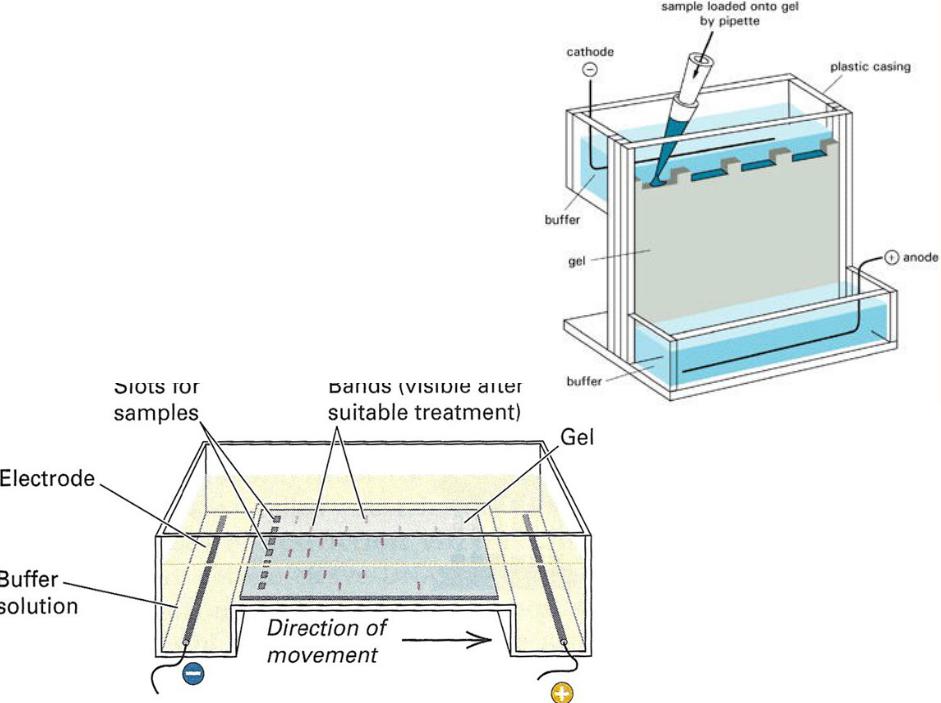
Вертикальный и горизонтальный электрофорез
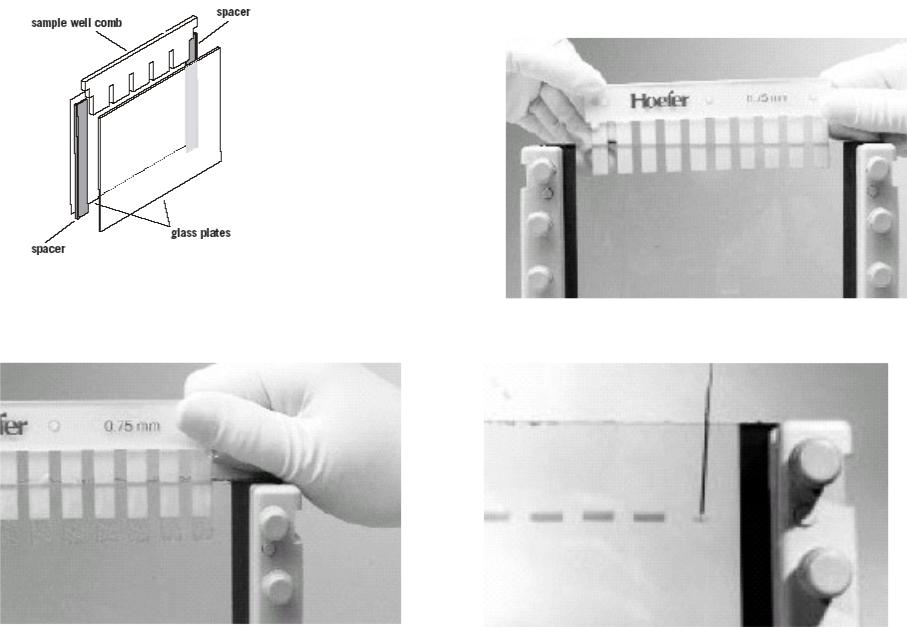
Вертикальный электрофорез
Формирование карманов и загрузка образцов
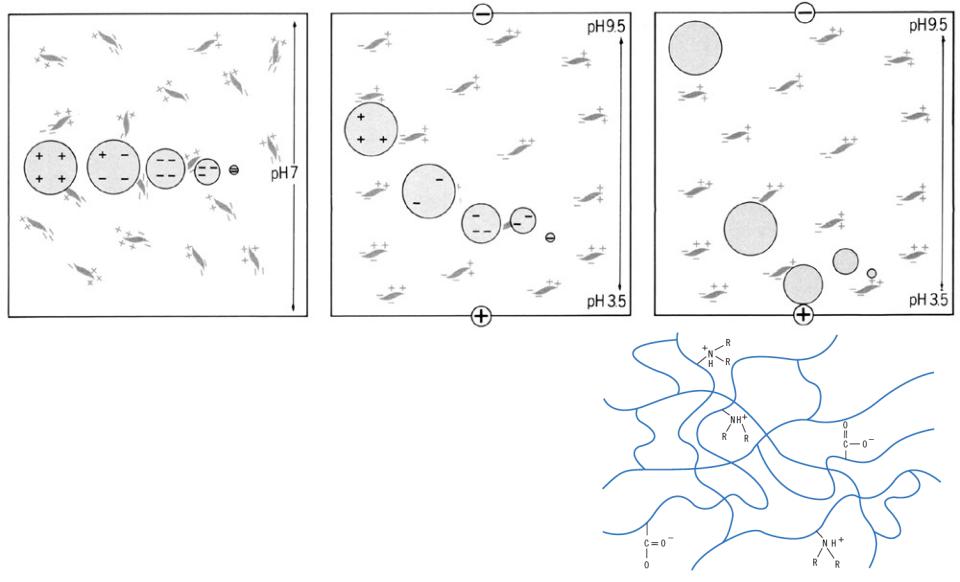
Изоэлектрическое фокусирование
отвечающих следующим требованиям:
•отсутствие взаимодействия с белками,
•низкая молекулярная масса,
•наименьшее возможное различие между рК и pI,
•хорошая электропроводность,
•наименьшее возможное поглощение света в области УФ-поглощения белков,
•равномерное распределение зон pI амфолитов,
•максимальноекие количество различных Коммерчес амфолиты для ИЭФзначений– рI.
смесь низкомолекулярных
полиаминополикарбоновых
В настоящее время для ИЭФ наиболее широко используются так называемые
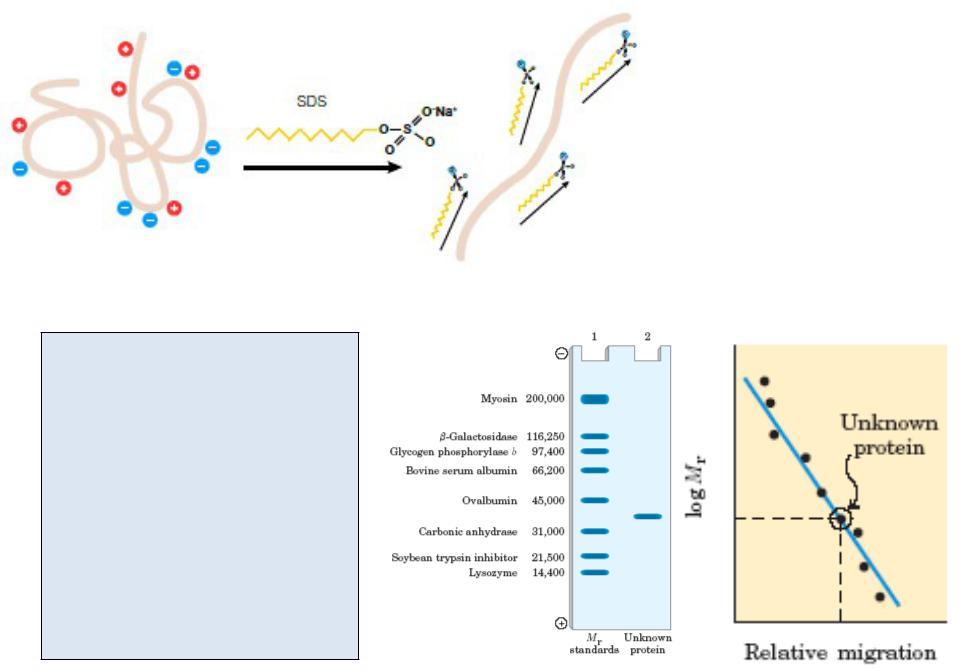
еление белков по размера с использованием
За счет гидрофобных взаимодействий додецилсульфат натрия (SDS, ДС-Na) примерно одинаково связывается с подавляющим большинством белков в соотношении около 1,4 мг ДС-Na на мг белка
Белки, обработанные ДС-Na, обладают одинаковым отношением масса/заряд и их подвижность при ЭФ в поддерживающей среде с эффектом молекулярного сита зависит только от размера молекулы.
Определение молекулярной массы белков при помощи SDS-электрофореза
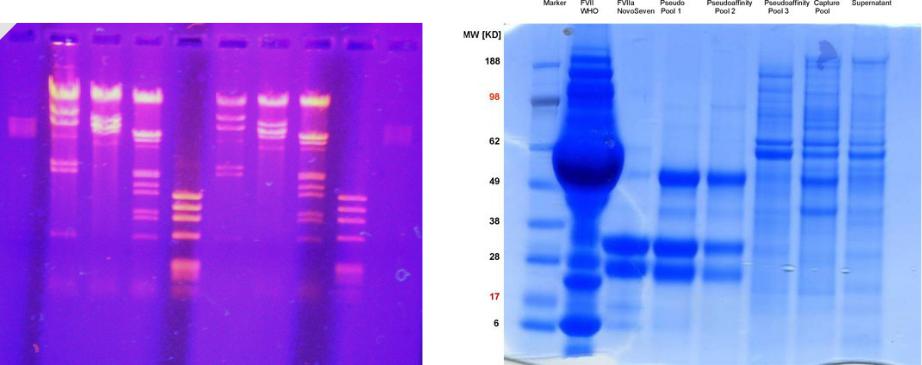
Гель-электрофорез: как это выглядит
Разделение ДНК в агарозном геле. |
Разделение белков в ПААГ с |
Гель окрашен бромистым этидием |
SDS. |
|
Гель окрашен Кумасси |
|
бриллиантовым синим |

ЕТОДЫ ФРАКЦИОНИРОВАНИЯ БЕЛКО
СВОЙСТВО
БЕЛКА
ЗАРЯД
ГИДРОФОБНО
СТЬ/ГИДРОФИ
ЛЬНОСТЬ
РАЗМЕР
МЕТОД РАЗДЕЛЕНИЯ
ХРОМАТОГРАФИ |
ЭЛЕКТОФОРЕ |
Я |
З |
ИОНООБМЕННАЯ |
ИЗОЭЛЕКТРОФ |
(ИОХ, IEX) |
ОКУ- |
[АФФИННАЯ (АХ, |
СИРОВАНИЕ |
AC)] |
(ИЭФ, IEF) |
ГИДРОФОБНАЯ |
|
(ГХ, HIC) |
|
ОБРАЩЕННО |
|
ФАЗОВАЯ (ОФХ, |
|
RPC) |
|
[АФФИННАЯ (АХ, |
|
AC)] |
|
ГЕЛЬПРОНИКАЮЩ |
С |
АЯ |
ДОДЕЦИЛСУЛЬ- |
(ЭКСКЛЮЗИОННАЯ |
ФАТОМ НАТРИЯ |
, ГПХ, SEC) |
(SDS-PAGE) |
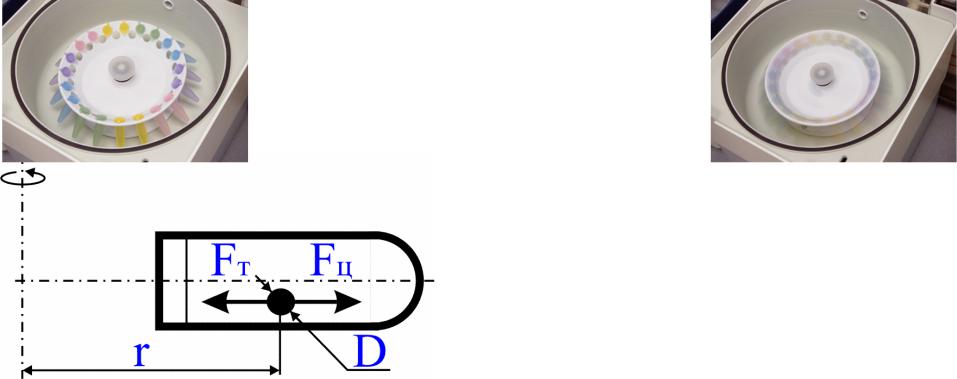
Центрифугирование –
фракционирование в поле центробежных сил
Fц – центробежная сила; Fт – сила трения |
|
D2 |
( с )N 2r |
|
|
v |
k |
||
|
|
с |
||
Выводы из зависимости: |
|
|
||
• |
При одинаковых плотностях частицы большего размера |
|||
|
оседают быстрее чем мелкие (D). |
|
|
|
• |
Скорость оседания (v) пропорциональна плотности частицы |
|||
|
(ρ), особенно сильно это проявляется когда плотность |
|||
|
частицы и среды (ρс) близки. |
|
|
|
• |
Скорость оседания пропорциональна квадрату числа |
|||
|
оборотов ротора (N). |
|
|
|
• |
Скорость оседания обратно пропорциональна вязкости среды |
|||
|
(ηс). |
|
|
|
• |
Скорость оседания пропорциональна расстоянию от оси |
|||
|
вращения (r). Это расстояние увеличивается по мере |
|||
|
оседания и следовательно возрастает скорость. Если это |
|||
|
почему-либо нежелательно следует создать градиент |
|||
Разделение осаждением
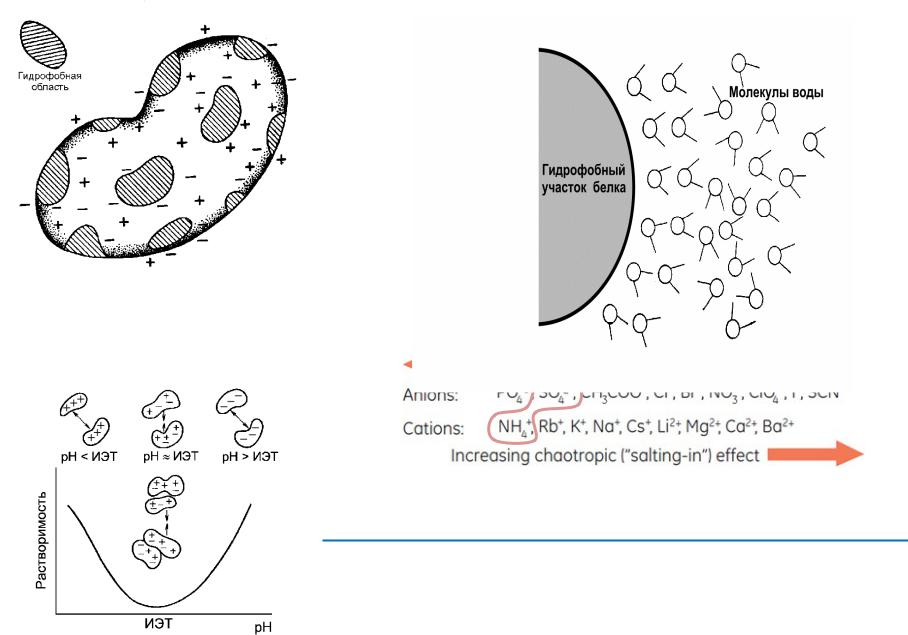
Распределение зарядов и гидрофобных областей на поверхности молекулы типичного белка
Изоэлектрическое осаждение
Ряд Гофмейстера – влияние ионов на растворимость белков
значениях pH, близких к
изоэлектрической точке
ОсаждениеДляорганическимиосаждения белрастковорителя
используют смешивающиеся с водой органические растворителями, такие как
ацетон, этанол или
