
- •Введение
- •Номенклатура фосфорорганических соединений
- •Классификация фосфорорганических соединений
- •Связи, образуемые атомом фосфора
- •Элементный фосфор и неорганические соединения фосфора
- •Получение органических производных фосфорной кислоты и их тиоаналогов
- •Синтез и свойства производных кислот фосфора с РН-связями
- •Производные кислот фосфора с трикоординированным атомом фосфора
- •Фосфины
- •Органические синтезы с участием производных кислот фосфора и фосфинов
- •Биологически активные производные кислот фосфора
- •Фосфорорганические инсектициды
- •Фитоактивные производные кислот фосфора
- •Производные кислот фосфора с фунгицидной активностью
- •Фосфорорганические соединения в фармакологии
- •Заключение
- •Литература
O |
|
|
|
|
|
|
|
|
O |
_ |
+ |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
Br |
|
P(OC2H5)3 |
||||||||||||||||
|
|
CH2Br |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
+ (C2H5O)3P |
|
|
|
|
|
|
|
|
CH2 |
||||||||||||||||
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
+ |
_ |
|
|
|
|
|
|
|
|
|
|
P(OC2H5)2 + C2H5Br |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
O |
|
P(OC2H5)3 |
Br |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Здесь приведено всего лишь несколько примеров, демонстрирующих синтетические возможности эфиров кислот трикоординированного фосфора. Многие из представленных в специальной литературе реакций, протекающих с образованием новых РС-связей через квазифосфониевые соединения, можно отнести к реакции Михаэлиса–Арбузова.
Фосфины
Важным в практическом отношении классом фосфорорганических соединений являются третичные фосфины. Фосфины отличаются от аминов тем, что у них более ярко выражена зависимость основности от заместителей. Так, например, фосфин РН3 представляет собой очень слабое основание, тогда как триметилфосфин сравним по силе с триметиламином. Достаточно сильным основанием является трифенилфосфин, образующий соли четвертичного фосфония в реакциях с алкилгалогенидами. Интересно также, что третичные фосфины с тремя разными заместителями могут быть разделены на оптические изомеры, поскольку инверсия их пирамидальной структуры идёт только при нагревании. В частности, стереоизомер метилпропилфенилфосфина медленно рацемизуется только при кипячении в толуоле. Алифатические фосфины токсичны, они имеют резкий неприятный запах и легко окисляются кислородом воздуха, многие низшие алкилированные фосфины на воздухе воспламеняется, но триарилфосфины достаточно устойчивы. Трифенилфосфин медленно окисляется на воздухе, для очистки его от образующегося при этом
76
трифенилфосфиноксида проводят перекристаллизацию из этанола или изопропанола.
Исходными продуктами для получения фосфинов служат галогениды кислот трикоординированного фосфора (трихлорид фосфора и соответствующие хлорфосфины). В реакции с металлорганическими соединениями атомы галогенов в этих соединениях могут замещаться на алкильные или арильные остатки. В качестве примера можно привести используемую в крупномасштабном производстве трёхкомпонентную реакцию, по которой из хлорбензола, трихлорида фосфора и металлического натрия получают трифенилфосфин:
PCl3 + 3 C6H5Cl + 6 Na |
|
P(C6H5)3 + 6 NaCl |
|
Понятно, что реакция протекает с промежуточным образованием фенилнатрия, который реагирует с трихлоридом фосфора. Один из способов получения фенилдихлорфосфина основан на термическом фосфорилировании бензола трихлоридом фосфора при температуре около 600 °С:
PCl3 + C6H6  C6H5PCl2 + HCl
C6H5PCl2 + HCl
В этих условиях можно также проводить диспропорционирование фенилдихлорфосфина с целью получения дифенилхлорфосфина по реакции:
2 C6H5PCl2  (C6H5)2PCl + PCl3
(C6H5)2PCl + PCl3
Термическое фосфорилирование метана используется для промышленного производства метилдихлорфосфина:
700oC
PCl3 + CH4  CH3PCl2 + HCl
CH3PCl2 + HCl
Ещё один промышленный способ получения метилдихлорфосфина основан на реакции трихлорида фосфора с метилхлоридом в присутствии эквивалентного количества безводного хлорида алюминия (реакция Клея–Киннера–Перрена,
1951-1952 гг.):
77

PCl3 + CH3Cl + AlCl3  [CH3PCl3]+AlCl4-
[CH3PCl3]+AlCl4-
Полученную высокоплавкую соль восстанавливают, например, порошковым алюминием и разлагают комплекс метилдихлорфосфина и хлорида алюминия хлоридом калия:
[CH PCl ]+AlCl - |
Al |
CH |
PCl |
.AlCl |
KCl |
CH PCl |
|
|
- KAlCl |
||||||
3 3 |
4 |
|
3 |
2 |
3 |
3 2 |
|
|
|
|
|
|
|
4 |
|
Образующиеся при этом примеси делают получаемый таким способом метилдихлорфосфин пирофорным.
В лабораторных условиях фенилдихлорфосфин и его производные по ароматическому остатку можно получать по реакции соответствующего замещенного бензола с трихлоридом фосфора в присутствии эквимолярного количества безводного трихлорида алюминия, например:
PCl |
+ C |
H |
CH |
+ AlCl |
|
CH C |
H |
PCl .AlCl |
+ HCl |
||
|
|||||||||||
3 |
6 |
5 |
3 |
3 |
3 |
6 |
4 |
2 |
3 |
||
Образующийся комплекс трихлорида алюминия и арилдихлорфосфина разлагают фосфорилхлоридом или сухим пиридином.
Пример получения третичного фосфина на основе метилдихлорфосфина с помощью магнийорганических соединений представлен синтезом метил-ди- трет-бутилфосфина, используемого в качестве лиганда для гомогенных катализаторов на основе металлов платиновой группы:
Cl |
|
|
|
CH3 |
|
|
C(CH3)3 |
||
CH3P |
+ 2 ClMg |
|
C |
|
CH3 |
|
CH3P |
+ 2 MgCl2 |
|
|
|
|
|||||||
|
|
|
|
||||||
Cl |
|
|
|
|
|
|
C(CH3)3 |
||
|
|
CH3 |
|
|
|||||
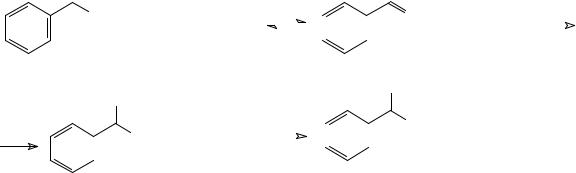
И всё же основной способ получения высших триалкилфосфинов, представлен взаимодействием фосфина с α-олефинами. В частности, широко используемый в металлокомплексном катализе трибутилфосфин получают из бут-1-ена и фосфина в присутствии генерирующих свободные радикалы катализаторов, реакция протекает не по правилу Марковникова:
78

R.
PH3 + CH2 CHC2H5  P(CH2CH2C2H5)3
P(CH2CH2C2H5)3
По этой схеме могут быть получены и другие третичные фосфины. Можно также получать третичные фосфины действием алкилгалогенидов
на соответствующие фосфиды щелочных или щелочноземельных металлов. Комплексные соединения трифенилфосфина и других фосфинов
используются в качестве лигандов в катализаторах на основе никеля и металлов платиновой группы в самых разных превращениях. Одним из первых комплексов этого ряда стало соединение Реппе Ni(CO)2(PPh3)2, катализирующее полимеризацию олефинов и ацетиленов. Гидрирование алкенов можно проводить в гомогенных условиях в присутствии катализатора Вилкинсона RhCl(P(С6Н5)3)3. Похожие катализаторы с трифенилфосфином в качестве лиганда, например, Rh(СО)(P(С6Н5)3)3, используют при гидроформилировании α-олефинов действием водорода и монооксида углерода. При этом значительно увеличивается выход альдегидов линейного строения.
Ещё одним важным аспектом применения металлокомплексных катализаторов стало использование асимметрических лигандов для проведения стереоселективных превращений. Одним из таких лигандов является 2,2′-бис-(дифенилфосфино)-1,1′- бинафтил (Бинап, BINAP). В основе асимметричности этого соединения лежит стерический фактор динафтилфосфиновых групп. Эти объёмные заместители не позволяют нафтильным остаткам находиться в одной плоскости. Они повёрнуты вокруг соединяющей их связи на угол около 90°. В результате этого получаются два пространственныхизомерапотипулевойи правой спирали:
P(C6H5)2 |
и |
P(C6H5)2 |
P(C6H5)2 |
P(C6H5)2 |
В качестве примера использования гомогенных металлокомплексных катализаторов с фосфиновыми лигандами в препаративной органической химии можно привести реакцию Сузуки:
79
