
- •Реферат
- •С одержание
- •П еречень сокращений и условных обозначений
- •В ведение
- •1 Литературный обзор с обоснованием метода производства
- •2 Физико-химические основы процесса
- •3 Характеристика сырья и готовой продукции
- •4 Описание технологической схемы
- •5 Аналитический контроль качества
- •6 Контроль и автоматизация процесса
- •6.1 Цели и задачи автоматизации
- •6.2 Анализ технологического процесса как объекта автоматизации
- •6.3 Выбор и описание функциональной схемы автоматизации
- •7 Материальный баланс
- •7.1 Исходные данные
- •7.2 Пересчет на часовую производительность
- •7.3 Расчет материального баланса реакционной стадии
- •7.4 Материальный баланс стадии горячей сепарации
- •7.5 Материальный баланс стадии холодной сепарации
- •7.6 Материальный баланс стадии стабилизации нестабильного гидрогенизата
- •7.7 Материальный баланс стадии дегазации дизельного топлива
- •7.8 Материальный баланс отвода жидкого нефтепродукта из шлемового продукта
- •7.9 Материальный баланс сепарации сырого углеводородного газа
- •7.10 Материальный баланс стадии абсорбции цвсг
- •7.11 Материальный баланс стадии сепарации цвсг после абсорбции
- •7.12 Материальный баланс стадии сепарации газовой фазы
- •7.13 Материальный баланс стадии отдува сероводорода от водного конденсата
- •7.14 Материальный баланс стадии абсорбции сухого углеводородного газа
- •7.15 Материальный баланс стадии очистки сероводородсодержащего газа
- •7.16 Материальный баланс стадии сепарации насыщенного раствора мдэа
- •7.17 Материальный баланс стадии смешения регенерированного раствора мдэа со свежим
- •8 Энергетический баланс
- •8.1 Энергетический баланс первого реактор а
- •8.2 Энергетический баланс второго реактора
- •9 Т ехнологический расчет реактора
- •9.1 Описание устройства реактора
- •9.2 Расчет основных технологических размеров реактора
- •9.3 Механический расчёт реактора
- •10.4 Расчет толщины изоляции стенок реактора
- •10 Подбор вспомогательного оборудования
- •11 Расположение оборудования на территории установки
- •11.1 Исходные данные для проектирования
- •11.2 Объемно-планировочные и архит ектурно-конструкторские решения
- •11.3 Служебно-производственное здание и его устройство
- •11.4 Снабжение энергоресурсами
- •11.5 Расположение оборудования
- •12 Безопасность и экологичность проекта
- •12.1 Вредные и опасные производственные факторы, присущие данному
- •12.2 Санитарно -гигиенические мероприятия
- •12.3 Техника безопасности
- •12.4 Пожарная безопасность
- •12.5 Экологичность проекта
- •12.6 Заключение
- •13 Организация и экономика производства
- •Заключение
- •Список литературы
2 Физико-химические основы процесса
Процесс гидроочистки основывается на реакции разложения органических соединений, содержащих серу, азот, кислород, в присутствии водорода и катализатора при температуре 320-400 оС и давлении 3-5 МПа (30-50 кгс/см2) с последующим их гидрированием.
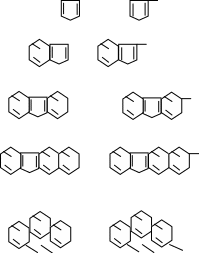
В керосиногазойлевых фракциях нефти содержатся классы серосодержащих соединений, перечисленные ниже в порядке уменьшения реакционной способности.
Таблица 2.1 – Классы серосодержащих соединений
Класс соединений |
Строение |
Меркаптаны (тиолы) |
R-SH |
Дисульфиды |
R-S-S-R |
Сульфиды |
R-S-R |
Тиофены
|
S S |
Бензотиофены
|
R
S S |
Дибензотиофены
|
R
S S |
Бензонафтотиофены
|
R
S S |
Бензо дибензотиофены
|
R S S |
В процессах гидрообессеривания протекают следующие основные реакции: сама реакция гидрообессеривания приводит к разрыву связи С-S
R S
H + H2
→ RH + H2S,
S
H + H2
→ RH + H2S,
RS - SR + 3Н2 → 2 RH + 2H2S,
R - S - R + 2H2 → RH + RH + H2S,
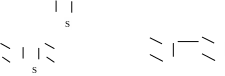
+ 4Н2 → С4Н10 + Н2S,
+ 4Н2 → Н2S +
В условиях промышленного проведения процесса могут протекать реакции гидрогенолиза связи С-C , связи С-N, связи C-O, приводящие к реакциям гидрокрекинга, гидродеазотирования и восстановления.
RCH2CH2R’ +H2 → RCH3 + R’CH3 ,
RNH2 + H2 → RCH3 +NH3,
ROH +H2 → RCH3 + Н2О.
Таким образом, в процессе гидроочистки органические соединения, содержащие серу, азот, кислород, превращаются в углеводороды с выделением сероводорода, воды и аммиака.
При гидрообессеривании происходит также гидрирование ненасыщенных соединений
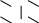
+ 5H2 →
Одновременно с реакциями присоединения водорода идут реакции гидрокрекинга с образованием небольшого количества легких бензиновых фракций и газов, реакции изомеризации парафиновых и нафтеновых углеводородов и т.п.
Реакция разложения сернистых и других органических соединений происходит на поверхности катализаторов гидроочистки.
Факторами, влияющими на ход процесса, являются:
к
 ачество
сырья;
ачество
сырья;активность катализатора;
удельная скорость;
соотношение водорода и сырья;
температура;
давление.
Качество сырья: скорость обессеривания уменьшается с увеличением плотности (молекулярного веса) сырья, так как с утяжелением фракционного состава увеличивается содержание тиофеновой серы.
Наличие смолистых соединений в сырье приводит к быстрому закоксовыванию катализатора и резкому снижению его активности. Содержание смолистых веществ в сырье косвенно характеризуется его цветом.
Активность катализатора: снижение активности катализатора происходит из-за отложений (кокс, окалина, металл и т.п.) на его поверхности. Образование коксовых отложений происходит за счёт окисления непредельных углеводородов кислородом, растворённым в сырье. Даже содержание кислорода 0,00001% в сырьё приводит к образованию смол с последующим коксообразованием. Коксоподобные вещества реагируют с сульфидами железа и отлагаются на поверхности катализатора, особенно на входном слое катализатора.
Удельная скорость: отношение объема сырья (м3/час) при 20 0С к объему катализатора ( подсчитанному по насыпному весу) в реакторе называется удельной скоростью. Чем тяжелее сырье, тем ниже должна быть удельная скорость. Увеличение удельной скорости приводит к уменьшению времени пребывания сырья в реакторе, а значит и к снижению степени обессеривания. С другой стороны снижение удельной скорости приводит к снижению производительности установки и удорожанию процесса. Увеличение удельной скорости в 2 раза требует повышения температуры гидрообессеривания примерно на 17 0С.
Соотношение водорода и сырья: при увеличении отношения водородосодержащий газ - сырье скорость процесса обессеривания увеличивается. Низкая степень обессеривания сырья при весьма малом отношении водородосодержащий газ - сырье объясняется недостаточным парциальным давлением водорода.
Кинетика реакций обессеривания имеет первый порядок по водороду и скорость обессеривания прямо пропорциональна парциальному давлению водорода. Парциальное давление водорода зависит:
о
 т
общего давления в реакторе,
т
общего давления в реакторе,от кратности ВСГ/сырье,
от концентрации водорода в ВСГ.
Заметное возрастание степени обессеривания происходит до определенного предела (700 нм3 циркуляционного газа на 1м3 сырья), так как при повышении расхода газа уменьшается время контакта. Для процесса гидроочистки дизельных фракций принята кратность циркуляции ВСГ 160-180 нм3/м3 из расчета на 100 %-ый водород.
Сероводород, образующийся при реакции, замедляет скорость реакции. При содержании H2S 0,3 % объемных в реакционной газовой смеси скорость реакции уменьшается на 5 %, поэтому необходимо производить очистку циркулирующего водорода от H2S. Скорость реакции также уменьшается при увеличении содержания ароматических углеводородов в дизельном топливе.
Температура: при повышении температуры скорость гидрирования сернистых соединений возрастает, достигая максимума при 400 0С. Для процесса гидроочистки дизельных фракций оптимальная температура 320-400 0С.
При температуре выше 400 0С развиваются процессы, вызывающие закоксовывание катализатора.
Давление: степень обессеривания увеличивается с возрастанием общего давления в системе, так как уменьшается объем газосырьевой смеси, увеличивается время контакта, увеличивается парциальное давление водорода. Повышенное давление ослабляет реакции дегидрирования углеводородов и уменьшает коксование катализатора. Повышенное давление в системе реакции ведет к увеличению насыщения непредельных и гидрогенизации ароматических углеводородов, что приводит к повышению расхода водорода.
Факторы влияющие на процесс очистки газов: очистка газов от сероводорода производится раствором МДЭА , который, контактируя с потоком циркуляционного газа, поглощает сероводород с образованием растворимого комплекса.
NСН3 (C2H4 OH)2 + H2S H2S ----- NСН3 (C2H4 OH)2
Регенерация раствора МДЭА основана на разложении образовавшегося комплекса.
H2S ----- NСН3 (C2H4 OH)2 NСН3 (C2H4 OH)2 + H2S
Разложение происходит при температуре 80-130 0С. Основными факторами, влияющими на процесс очистки газов, являются: температура, давление, концентрация МДЭА, расход раствора МДЭА .
О птимальная
температура абсорбции сероводорода –
30-40 0С. Повышение температуры
ухудшает поглощение сероводорода.
Важную роль играет соотношение температур
раствора МДЭА и газа, поступающего на
очистку. При высокой температуре газа
происходит охлаждение его раствором
МДЭА, с образованием жидкой фазы бензина.
Бензин при регенерации раствора МДЭА
испаряется и попадает в сероводородсодержащий
газ.
птимальная
температура абсорбции сероводорода –
30-40 0С. Повышение температуры
ухудшает поглощение сероводорода.
Важную роль играет соотношение температур
раствора МДЭА и газа, поступающего на
очистку. При высокой температуре газа
происходит охлаждение его раствором
МДЭА, с образованием жидкой фазы бензина.
Бензин при регенерации раствора МДЭА
испаряется и попадает в сероводородсодержащий
газ.
Повышение давления увеличивает степень поглощения сероводорода. Уменьшение концентрации МДЭА в растворе увеличивает энергетические затраты на регенерацию МДЭА , но уменьшает скорость коррозии оборудования. С увеличением расхода циркулирующего раствора МДЭА, степень очистки от сероводорода увеличивается.

 R
R